PROTOCOLO DE LA RM FETAL
Los estudios se deben realizar en Resonancias de alto campo (1.5T) con bobinas multicanales de gran resolución espacial.
Se realizan tres planos ortogonales a la madre y,
sobre éstos,
se planifican los cortes sagitales,
coronales y axiales del feto,
utilizando siempre como referencia la última secuencia utilizada para la planificación de la siguiente debido a los movimientos fetales.
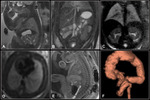
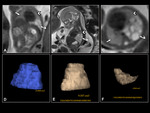
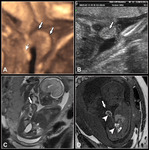
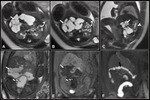
Las principales secuencias utilizadas son Fig. 1 :
- Secuencias potenciadas en T2 como Single Shot Fast Spin Echo T2 (SSFSE T2) y secuencias balanceadas como la secuencia Fast Imaging Employing Steady-State Acquisition (FIESTA) que presentan gran contraste tisular mostrando el líquido amniótico hiperintenso.
Ambas secuencias permiten el estudio de la vía aérea y del pulmón.
Todas estas estructuras presentan un comportamiento de señal hiperintenso en secuenciasT2.
La secuencia FIESTA nos permite además realizar estudios vasculares sin contraste intravenoso mostrando los vasos fetales hiperintensos (los vasos aparecen hipointensos en secuencias SSFSE T2 y T1).
- Secuencias potenciadas en T1 (3D gradiente doble eco,
2D FSPGR y 3D LAVA) tienen menor contraste tisular que las secuencias SS FSE T2 o FIESTA.
Se utilizan sobre todo para identificar la posición del hígado y de las asas intestinales con meconio que son visualizados como estructuras hiperintensas en el estudio de la hernia diafragmática congénita.
Estas secuencias son útiles para determinar la presencia de sangrado subagudo,
calcificaciones o lipomas (1).
- Secuencias de difusión: Sus aplicaciones están en desarrollo, utilizándose en el momento actual en el estudio de la madurez del parénquima pulmonar (2).
Parámetros de interés de las secuencias utilizadas:
Todos los estudios se han realizado utilizando una RM de 1.5 T (General Electric HDxt,
software 15),
utilizando los siguientes parámetros:
• Single Shot Fast Spin Echo T2 (SSFSE T2): TR =1088ms,
TE = mínimo (90 ms),
matriz = 256 x 256,
FOV = 34 cm,
ancho de banda = 20,83 KHz.
NEX = 0,5.
Espesor de corte = 3 mm,
distancia entre cortes = 0 mm.
• Secuencias balanceadas (FIESTA): TR = 3,9 ms,
TE = mínimo (1,7 ms),
matriz = 256 x 256,
FOV = 35 cm,
ancho de banda = 125 KHz.
NEX = 2 espesorde corte = 5,1 mm,
distancia entre cortes = 0 mm y ángulo = 45º.
• Secuencias potenciadas en T1 (3D gradiente doble eco ): TR = 8,5 ms,
TE = mínimo (2,4ms),
matriz =336 x 256,
FOV = 39 cm,
ancho de banda = 62,5KHz,
NEX = 0,69,
espesor de corte = 6 mm,
distancia entre cortes = 0 mm y ángulo = 12º.
• Secuencias de difusión: TR = 2500 ms,
TE = mínimo (69 ms),
matriz = 128x128,
FOV = 36 cm,
ancho de banda = 62-250 KHz,
NEX = 6,
espesor de corte = 4mm,
distancia entre cortes = 0 mm y b = 1000 s/mm2.
PATOLOGÍA TORÁCICA
• Desarrollo embrionario pulmonar
El desarrollo intrauterino pulmonar se divide clásicamente en cinco fases: embrionaria,
pseudoglandular,
canalicular,
sacular y alveolar.
En la fase embrionaria (3-6 semanas de gestación) el brote pulmonar se origina a partir de células epiteliales del endodermo del intestino primitivo anterior,
como un divertículo ventral alrededor del día 24-26 de gestación,
que penetra hacia el mesénquima circundante y crece por divisiones dicotómicas en dirección caudal,
para formar las estructuras proximales del árbol traqueobronquial.
Durante la fase pseudoglandular (6 - 16 semanas de gestación) continúan la ramificaficiones para formar los bronquiolos bronquíolos terminales.
En este período,
el árbol vascular se ramifica siguiendo a la vía aérea,
que actúa como un molde.
En la fase canalicular (16- 28 semanas de gestación) los bronquiolos terminales se dividen para formar los bronquiolos respiratorios y se empiezan a formar las estructuras acinares.
Se produce la angiogénesis del lecho capilar y en la semana 22-24 se aplana el epitelio acinar y empieza la diferenciación inicial de los neumocitos tipo II que producen surfantante y de los cuales derivarán los neumocitos tipo I.
La fase sacular está comprendida entre las 28 - 36 semana de gestación; en este período continúa la división de la vía aérea periférica con generación de ductos transitorios y los sáculos terminales.
De este modo aumenta el tamaño de la vía aérea periférica y crece la superficie para el intercambio gaseoso en la medida que la pared continúa adelgazándose (septos primarios).
La fase alveolar (36 semanas de gestación –final de gestación) se define por la aparición de pequeñas prominencias a ambos lados de las paredes saculares,
y forman los septos secundarios.
Estas crecen en forma perpendicular al espacio aéreo,
dividiendo los sáculos en forma incompleta en unidades menores,
los alvéolos (3).
• RM pulmonar
Los pulmones fetales ,
la tráquea y el árbol bronquial principal están compuestos fundamentalmente por agua y muestran alta señal en secuencias potenciadas T2 en comparación con las estructuras adyacentes,
permitiendo así una evaluación morfológica y volumétrica del pulmón.
La RM no sustituye al US como primera línea de cribado,
pero es útil en aquellos casos donde existen limitaciones en >US.
En el trabajo de Levine y colaboradores (4) se estudiaron por US 74 fetos con anomalías torácicas diagnosticados; la RM aportó información adicional en un 38% y modificó el manejo en el 8%.
Las anomalías congénitas torácicas más frecuentes estudiadas por RM incluyen: hernia diafragmática congénita (HDC),
malformación adenomatoidea quística (MAQ),
secuestro broncopulmonar (SBP) y quiste broncogénico congénito (QBC).
Hernia diafragmática congénita:
La hernia diafragmática congénita (HDC) es la principal indicación de RM fetal en patología torácica.
Su incidencia es 1/2500 -1/5000 los recién nacidos dependiendo si se incluyen o no los mortinatos (5); siendo el 85% izquierdas (hernia de Bochdalek),
13% derechas y 2% bilaterales (6).
Aproximadamente el 40% de los pacientes con HDC tienen otras malformaciones congénitas (sobre todo cardíacas y del sistema nervioso central),
anomalías cromosómicas (trisomía 21,18 y 13) y síndromes genéticos (Síndrome de Fryns,
síndrome de Lange o síndrome de Marfan) (7).
Las anomalías asociadas se consideran un factor independiente de supervivencia siendo la misma menor a 15% (8).
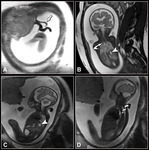
El grado de hipoplasia pulmonar y la herniación hepática son los principales factores pronósticos.
Para calcular el volumen pulmonar se utiliza en ecografía la razón LHR (área de pulmón contralateral/ circunferencia cefálica) medida en el segundo trimestre.
Si la ratioLHR es >1,6 la supervivencia es ≥ 83%; si la razón LHR es ≥1 y <1,6 la supervivencia es del 66%y con valores ≥ 0,8 y <1 supervivencia es del 16% (9).
En los fetos normales y aquellos con HDC (derecha o izquierda) la ratio LHR aumenta con la edad gestacional pero la ratio LHR observada en la ecografía con respecto a la LHR esperada para la edad gestacional (LHRo/LHRe) no cambian significativamente siendo ésta útil en la estimación del porcentaje de supervivencia supervivencia (10).
El estudio volumétrico pulmonar 3D por US para el cálculo del volumen pulmonar no es superior al LHR (11).
La RM permite medir el volumen pulmonar del pulmón ipsilateral a la hernia y el contralateral obteniendo un volumen pulmonar total observado (VPO).
Rypens y colaboradores (12) realizaron un estudio multicéntrico prospectivo en siete hospitales de Francia y Bruselas con RM 336 fetos que tenían sospecha de patología del sistema nervioso central para establecer la correlación del volumen pulmonar total con le edad gestacional.
El volumen pulmonar predictivo o esperado (VPE) es calculado por la ecuación VPE = 0.0033 x g 2.86
siendo g la edad gestacional en semanas.Coakley y colaboradores (13) en su estudio restrospectivo de 46 fetos de mujeres norteamericanas establecen una estrecha relación entre el volumen pulmonar total calculado por RM y el volumen hepático medido por RM,
el peso fetal estimado por la ecografía,
circunferencia cefálica medida por ecografía y la edad gestacional .
El VPE es calculado con la ecuación VPE = (0,47 x volumen hepático en ml) + (0,76 x diámetro biparietal en mm) - (0,39 x longitud del fémur en mm) -18,9.
Cannie y colaboradores (14) realizaron un estudio en 200 fetos sin anomalías en el Hospital Universitario de Gasthuisberg ( Bélgica) correlacionando el volumen pulmonar total con el volumen corporal fetal (VCF),
siendo superior a la correlación con el resto de variables biométricas.
El VPE es calculado por la ecuación VPE = (2.0 x 10 -9 x VCF 3) - (1,19 x 10 -5 x VCF 2) + (0,0508 x VCF) -1,79.
La relación VPO/VPE x 100 establece el volumen pulmonar relativo (VPR).
Se considera hipoplasia los valores inferiores al 80% (15).
Todos los fetos con valores <14,3 % presentan 100% de mortalidad,
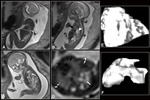
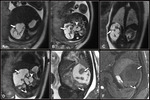
los valores > 32,8 tienen 100% de supervivencia y los valores > 44% no necesitaránoxigenación membranal extracorpórea( ECMO) (16) .Fig. 2 Fig. 3 Fig. 4
La RM permite también valorar la madurez pulmonar mediante intensidad pulmonar : Se ha correlacionado la madurez pulmonar con la hiperseñal que presenta el pulmón en secuencias T2 valorando el ratio de señal entre el pulmón/el liquido cefalorraquídeo (17),
pulmón/ líquido gástrico o pulmón/hígado (18).
La intensidad de señal aumenta con la gestación (19).
El grupo de Moore y colaboradores (20) han estudiado los pulmones fetales con secuencias de difusión y han demostrado que el ADC aumenta con la edad gestacional (a partir de la semana 18) probablemente reflejando el aumento de las secreciones alveolares y de la vascularización pulmonar (21,22).
La espectroscopía tiene un teórico potencial en la evaluación de la madurez pulmonar.
El surfactante está compuesto en un 90% por fosfolípidos,
básicamente por fosfatidilcolina (lecitina) en un 70%,
y en un 10% por proteinas.
La cantidad de colina,
el ratio colina creatina,
lecitina y lactato se podrían correlacionar con la cantidad de surfactante del pulmón (23 ,24).
Desgraciadamente esta técnica tiene varias limitaciones especialmente los artefactos de movimiento.
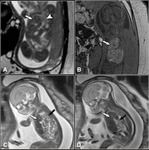
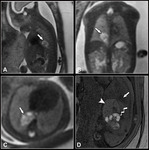
Los fetos con herniación hepática tienen una supervivencia del 50%.
La posición supradiafragmática hepática es difícil de visualizar por ecografía.
La RM permite identificar sobre todo en los planos sagital y coronal el defecto del diafragma (solución de continuidad de la banda hipointensa en secuencias T2) y la posición anómala del hígado que presenta una señal hiperintensa en secuencias T1 e hipointensa en secuencias T2.
Las estructuras que se hernian con mayor frecuencia en hernias diafragmáticas izquierdas son la grasa omental,
intestino delgado,
lóbulo hepático izquierdo y estómago.
Raramente se hernian el riñón o el páncreas.
En hernias diafragmáticas derechas el hígado es el órgano que se hernia con más frecuencia con herniación del lóbulo hepático derecho.
El tratamiento con balon de oclusion endotraqueal (FETO) está indicado en los casos de herniación hepática,
LHR< 1,
en la semana 26-29 y en la ausencia de alteraciones cromosómicas o de anomalías asociadas.
Es una terapia mínimamente invasiva donde se infla un balón endotraqueal durante 3-6 semanas.
La retención de fluidos en el pulmón acelera la maduración pulmonar y disminuye el riesgo de hipertensión pulmonar.
Debe ser realizado antes de la semana 29 para ser retirado posteriormente por fetoscopia tras punción del balón en la semana 34,
ex-utero-intraparto (EXIT) o de forma neonatal (traqueoscopia o punción percutánea).
El tratamiento con FETO realizado anterior a las 29 semanas produce importante expansión del pulmón por marcada producción de fluidos.
Cuando el balón es retirado existe un casi 50% de pérdida de VPR pero es un 40% superior al VPR previo del feto.
El tratamiento con FETO realizado posterior a la semana 29 no incrementa el VPR después de la retirada del balón (25).
En el trabajo de Jani JC y colaboradores (26) las principales complicaciones fueron: ruptura prematura de membranas (47%),
corioamnionitis o parto prematuro.
El tratamiento con FETO aumentó la supervivencia en HDC izquierdas de 24,1% a 49,1% y la supervivencia en HDC derechas de 0% a 35,3%. El 97% de los fetos tratados con FETO nacieron vivos y de ellos el 50% soportaron la cirugía y salieron vivos del hospital.
Ruano y colaboradores (27) estudiaron casos aislados de severa hernia diafragmática congénita (LHR < 1 y herniación hepática torácica).
Las HDC fueron 71% izquierdas y un 29% derechas.
De los 19 casos tratados con FETO entre la semana 26-30 de gestación el parto tuvo lugar en una edad gestacional media de 35.4 con una supervivencia global a los 6 meses de edad del 52,6%.
No existieron problemas técnicos en la introducción ni extracción del balón.
En los 19 casos de manejo conservador expectante la edad gestacional media del parto fue 37.5 semanas con una supervivencia del 5,3%.
Malformación adenomatoidea quística (MAQ) o malformación congénita de la vía aérea pulmonar:
Es la masa pulmonar fetal más común diagnosticada en periodo neonatal.
Consiste en hamartoma pulmonar con proliferación de bronquiolos terminales y ausencia de alveolos normales.
Son masas sólidas o quísticas con vascularización por la arteria pulmonar y drenaje a venas pulmonares.
La mayoría de las MAQ son unilaterales y afectan a un lóbulo entero. Existen lesiones híbridas asociadas a secuestros pulmonares con vascularización sistémica (28,
29).
Stocker y colaboradores (30) las clasificaron en tipo I (uno o más quistes> 2cm),
tipo II (múltiples quistes 2-0,5cm) y tipo III (gran lesión microquística <0,5cm).
Las MAQ son normalmente detectadas por ecografía en la semana 20 (31)y aparecen como masas pulmonares ecogénicas quísticas o sólidas.
Ocasionalmente las MAQ pueden diagnosticarse por ecografía como HDC o viceversa (32).
Las MAQ aisladas tienen buen pronóstico con una supervivencia del 97%,
independientemente del tipo histológico si se excluyen las MAQ con anomalías asociadas que supone un 3-12% (la mayoría corresponden a lesiones tipo 2 de Strocker).
Más del 50% se resuelven espontáneamente en el embarazo (31).
Las MAQ presentan un crecimiento rápido entre las 20-26 semanas y posteriormente se estabilizan no desarrollando complicaciones si no han aparecido con anterioridad (33).
Típicamente las MAQ con volumen < 57% del volumen pulmonar total tienen una resolución completa,
las MAQ con un volumen > 84% del pulmonar total muestran una resolución incompleta.
El factor pronóstico más importante es la presencia o ausencia de hidrops (34).
La MAQ puede comprimir el corazón y la vena cava inferior y secundariamente reducir la contractilidad cardiaca y disminuir el retorno venoso (35).
Si no se trata la MAQ con hidrops más del 90% de los fetos morirán antes de nacer (36).
Para estimar el desarrollo de hidrops se calcula por ecografía la razón CVR (volumen de la MAQ/circunferencia cefálica).
El volumen de la MAQ se calcula con las medidas ecográficas de las tres dimensiones de la masa.
Este volumen se divide por la circunferencia cefálica.
La circunferencia cefálica se calcula por ecografía (diámetro óseo fronto-occipital + diámetro óseo biparietal) x 1,57.
Si la CVR es >1,6 el feto desarrollará hidrops en un 75% de los casos,
si CVR es <1,6 se producirá hidrops en < 3% (37).
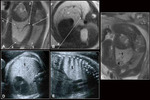
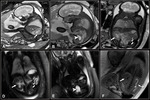
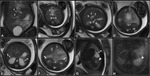
Los hallazgos en RM varían según el tipo de MAQ,
en el tipo I aparece como una lesión unilocular hiperintensa en secuenciasT2,
en el tipo II como lesión multilocular hiperintensa en secuenciasT2 y en el tipo III como masa sólida hiperintensa en secuenciasT2,
adyacente al pulmón normal que es más hipointenso.
Permite además calcular el volumen de la lesión y del parénquima pulmonar y así cuantificar y monitorizar el crecimiento o resolución de las lesiones (34) Fig. 5 Fig. 6 .Requieren cirugía postnatal pasado el mes de vida por el riesgo de infección y bajo riesgo de malignización con tasa anual del 3% (niños pequeños a blastoma pleuropulmonar,
rabdomiosarcoma o myxosarcoma y niños mayores o adultos a carcinoma bronquioalveolar (38).
Secuestro broncopulmonar:
Es la segunda lesión pulmonar más común en el diagnóstico prenatal.
Consiste en tejido broncopulmonar que no conecta con el árbol bronquial o arterias pulmonares y está irrigado por vascularización sistémica normalmente de la aorta torácica o abdominal y ocasionalmente del tronco celíaco,
arteria esplénica,
intercostal,
subclavia e incluso arterias coronarias (39).
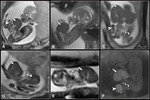
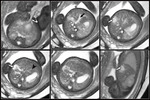
Su localización más frecuente es en el lóbulo inferior izquierdo (>2/3) (40) siendo un 90% supradiafragmáticos Fig. 7 y un <10% infradiafragmáticos (41) (Fig. 8 .
El secuestro tipo extralobar es el que está presente en el feto,
presentando revestimiento pleural propio y drenaje venoso sistémico a ázigos o vena cava inferior (25% a venas pulmonares) (42).
El secuestro extralobar puede estar asociado con otras malformaciones como la hernia diafragmática congénita,
hipoplasia pulmonar,quistes de duplicación intestinales o anomalías cardíacas.
(39).
El secuestro intralobar no tiene pleura propia y drena a venas pulmonares (43).
Los secuestros intralobares son raramente diagnosticados prenatalmente y suelen estar asociados a las MAQ tipo II (lesiones híbridas) (44).
Tienen un excelente pronóstico cuando es un hecho aislado y desaparecen intraútero más del 50% (31).Las lesiones de gran tamaño pueden comprimir el esófago y las venas torácicas causando hidrops siendo indicación de intervención fetal y parto precoz (45).
El tratamiento prenatal se realiza en casos de hidrotórax a tensión con shunt tóraco-amniótico.
En RM secuestro pulmonar aparece como una lesión sólida hiperintensa en secuencias T2 frecuentemente en el lóbulo inferior izquierdo en localización paraespinal,
muy similar a las MAQ tipo 3.
La identificación del aporte vascular sistémico facilita el diagnóstico sobre todo con las secuencias balanceadas.
En los casos de secuestro infradiafragmático,
el diagnóstico diferencial incluye el neuroblastoma y la hemorragia suprarrenal.
Los neuroblastomas son más frecuentes de localización derecha y son normalmente diagnosticados en el tercer trimestre.
Las lesiones híbridas muestran hallazgos radiológicos y patológicos del SBP y MAQ (normalmente MAQ tipo II).
La RM detecta lesiones de pequeño tamaño y anomalías asociadas.
En el periodo postnatal,
la mayoría son asintomáticos,
pudiendo presentar distress respiratorio o cianosis.
El tratamiento postnatal consiste en embolización del aporte vascular o/y resección quirúrgica debido al riesgo de infección,
hemorragia y cuestionable malignidad sobre todo en lesiones híbridas (45).
Quiste broncogénico:
El quiste broncogénico es la lesión quística solitaria más común encontrada en el tórax fetal.
La mayoría son únicos y tienen una localización mediastínica en la proximidad del esófago o/y tráquea (bifurcación traqueal o hilio pulmonar),
de predominio derecho; siendo menos frecuente la localización intrapulmonar,
pleura o diafragma (46).
En el diagnóstico diferencial debemos incluir los quistes de duplicación y los quiste neuroentéricos.
Los quistes de duplicación generalmente están localizados en mediastino medio o posterior y los quistes neuroentéricos en mediastino posterior con defectos vertebrales asociados en la región de comunicación del quiste con el conducto raquídeo (47).
El verdadero beneficio de la RM fetal es localizar el quiste y establecer sus relaciones anatómicas.
En RM aparece como un quiste de bordes bien definidos,
hiperintenso en secuencias potenciadas en T2,
comparado con el tejido pulmonar adyacente Fig. 9 .Ocasionalmente pueden presentar hiperseñal en secuencias potenciadas en T1 por la presencia de contenido mucoide o hemorrágico en el quiste.
Además la RM puede detectar obstrucción bronquial por efecto de masa de algunos quistes con hiperintensidad en secuenciasT2 del lóbulo obstruido (48).
El papel de la RM queda limitado a los casos que presenten obstrucción bronquial que se beneficiarían con EXIT con ECMO con resección de la lesión obstructiva seguida de reconstrucción de la vía aérea.
Otras indicaciones menos frecuentes :
Entre la patología torácica menos frecuente estudiada por RM se incluyen: obstrucción congénita de la vía aérea (por factores extrínsecos o malformación atrésicas o estenóticas traqueales y bronquiales),enfisema lobar congénito,
malformación arteriovenosa pulmonar,
linfangiectasia pulmonar congénita,
derrame pleural,
derrame pericárdico,
tumores pericárdicos (teratoma),
tumores mediastínicos (teratoma,
linfangioma),
tumores cardíacos (rabdomiomas) (49) o las obstrucciones bronquiales por tapón mucoso (50).
Las obtrucciones bronquiales por tapón mucoso de un bronquio principal o lobar produce una imagen similar a la MAQ tipo III o a un secuestro con masa intratorácica hiperintensa en T2 que puede desplazar el mediastino Fig. 10 .
Se puede resolver de forma espontánea intraútero o por broncoaspiración postnatal.
PATOLOGÍA ABDOMINAL
El número de trabajos publicados sobre la utilidad de la RM en patología abdominal es muy inferior a los publicados en RM torácica.
La mayoría de las ecografías son diagnósticas,
sin embargo,
existen limitaciones ecográficas que requieren una imagen alternativa.
DEFECTOS DE LA PARED ANTERIOR DEL ABDOMEN
Los defectos de la pared anterior del abdomen presentan una incidencia de 1 en 2.000 recién nacidos vivos (51),
siendo los más frecuentes,
la gastrosquisis y el onfalocele y poco frecuentes como la pentalogía de Cantrell (defecto de la pared abdominal en línea media,
hernia diafragmática anterior,
defecto del pericardio diafragmático,
defecto esternal inferior y anomalías cardiacas),
extrofia vesical y cloacal.
Onfalocele: Es un defecto de la pared abdominal en línea media con herniación de contenido abdominal ,
recubierto de peritoneo y amnios con inserción del cordón umbilical en el ápex del onfalocele.
El hígado,
estómago y asas de intestino delgado se hernian más frecuentemente y son fácilmente identificados por RM.
El onfalocele se asocia a otras malformaciones en 40-70%.
La incidencia de anomalías cromosómicas es de 10-40%,
incluidas trisomías 13,
14,15,
18 y 21 (52).
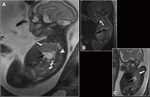
La presencia de hígado en los órganos herniados ha sido considerada como el elemento que diferencia un onfalocele grande de uno pequeño.
Los
onfaloceles grandes tienen una alta mortalidad ya que requieren varios procedimientos quirúrgicos para obtener el cierre del defecto y presentan como mayor limitación una cavidad torácica pequeña,
asociada a hipoplasia pulmonar y necesidad prolongada de ventilación mecánica Fig. 11 .
La RM diagnostica fácilmente la presencia del hígado en la herniación y puede establecer el grado de hipoplasia pulmonar.
Por otra parte los onfaloceles pequeños Fig. 12 muestran una mayor asociación con cromosomopatías (53).
Gastrosquisis: Es un defecto paraumbilical de la pared abdominal anterior.
típicamente derecho (54).
Las asas del intestino delgado se prolapsan con frecuencia y flotan en el líquido amniótico sin recubrimiento membranal.
El colon puede ser extracorporal en la gastrosquisis, pero no el recto ni el sigma. Con menos frecuencia existe prolapso hepático.
Su incidencia es mayor en madres que toman sustancias vasoactivas (cocaína,
nicotina,
decongestivos o aspirinas) y en madres menores de 25 años.
Generalmente no se asocian a otras malformaciones aunque pueden afectar en un 10-15% al tracto intestinal (atresias,
estenosis,
intestino corto),
debido probablemente a fenómenos isquémicos determinados por la obstrucción de las asas( 55).
Se asocia a oligoamnios y restricción del crecimiento intrauterino (RCI).
Si se acompaña de polihidramnios hay que descartar obstrucción o atresia intestinal.
La RM facilita la visualización en los casos de oligoamnios u obesidad materna así como las complicaciones intestinales asociadas.
En 4-5% se asocian malformaciones cardiacas (56). La incidencia de anomalías cromosómicas en gastrosquisis es inferior a 3% (57).
ANOMALÍAS GASTROINTESTINALES:
La base del estudio del tracto gastriointestinal en el feto es la presencia de un medio de contraste natural: el líquido amniótico deglutido que pasa al intestino y el meconio.
La deglución del líquido amniótico comienza en la semana 9-10 de gestación (58),
sin embargo hasta la semana 25 de gestación,
salvo en el estómago,
no existe una cantidad suficiente en el intestino que sirva de contraste.
En el feto a término el volumen de líquido amniótico deglutido es de unos 750 ml/día.
El meconio se empieza acumular en el recto a las18-20 semanas con relleno retrógrado del colon y asas de íleon distal.
La mayoría de las anomalías son diagnosticadas por ecografía y no necesitan un método diagnóstico complementario.
Las principales indicaciones de la RM en el estudio gastrointestinal son:
Identificar el nivel de las obstrucciones intestinales (atresias intestinales,
íleos meconiales y vólvulos intestinales),
descartar isquemia intestinal (engrosamiento de pared,
peritonitis meconial ) y malrotaciones intestinales.
Atresia esofágica: La más frecuente es la tipo A con atresia proximal y fístula traqueo-esofágica distal.
El diagnóstico se establece por polihidramnios,
estómago pequeño,
bolsón proximal esofágico y RCI en el 2o o3 o trimestre (59) Fig. 13 .
La fístula traqueoesofágica no puede ser detectada por RM.
Se asocia a trisomía 18 y si no presenta fístula es más común en trisomía 21.
Atresia o estenosis duodenal : Es diagnosticada por el signo de la doble burbuja del estómago y duodeno (hipointensas en secuencias T1 e hiperintensas en secuencias T2) (60) que incluye estenosis duodenal,
páncreas anular ,
bandas de Ladd y vólvulo.
La atresia duodenal asocia a otras anomalías y a trisomía 21(61).
Atresia o estenosis de intestino delgado: Existe dilatación de asas intestinales proximales a la obstrucción.
La RM proporciona información adicional dado que si la atresia o estenosis es yeyunal las asas dilatadas serán hipointensas en secuenciasT1 e hiperintensas en secuenciasT2 (con signo de triple burbuja y polihidramnios si afecta a yeyuno proximal) y en la atresia o estenosis ileal aparecerán asas dilatadas con forma de “ristra de salchichas” con meconio,
hiperintensas en secuencias T1 e iso-hipointensas en secuencias T2 (62 ).
Las atresias distales tienen más riesgo de perforación y peritonitis meconial.
Peritonitis meconial: Es una peritonitis química secundaria a la perforación de un asa intestinal que se diagnostica con el US por la presencia de calcificaciones peritoneales ,
ascitis y pseodoquistes (60 ).
La RM no identifica las calcificaciones pero permite identificar las asas dilatadas,
la ascitis,
polihidramnios y las masas quísticas (pseudoquistes meconiales) con facilidad.
Los pseudoquistes pueden tener septos en su interior y una señal: variableT1 y alta en T2 (63), hiperintenso en T1 e intermedio en T2 (64) o hiperintenso en T1 y muy baja en T2 (65).
Malrotaciones del colon: Se pueden diagnosticar a partir de la semana 25 de gestación por RM que muestra la posición anómala del colon utilizando secuencias ponderadas en T1 dado el contenido meconial (60).
Síndrome del megavejiga- microcolon- hipoperistaltismo:.
La ecografía y la RM diagnostican fácilmente el aumento de tamaño vesical que es el hallazgo más característico.
La RM identifica a partir de la semana 25 de gestación por la escasa cantidad de meconio generalmente presente en el recto.
Al final de la gestación se acumula más meconio y se puede visualizar el microcolon (60).
Atresias de intestino grueso: Afectan fundamentalmente al recto.
La atresia de colon transverso produce dilatación del colon proximal a la misma,
escaso meconio distal y dilatación de asas de delgado con ausencia de peristaltismo.
La atresia cecal produce dilatación del ciego y del íleon terminal con abundante meconio (66).
Enfermedad de Hirschsprung: Se observa dilatación rectal con señal invertida hipointensa en secuencias T1 e intermedia en secuencias T2 (67).
Atresia anal: Las formas pequeñas y aisladas pueden ser indetectables por RM.
Las asas en forma de U o V en pelvis sugieren el diagnóstico.
Frecuentemente asociada a fístula del tracto urinario que produce enterolitos (que se identifican mejor con ecografía) (68),
o forman parte del síndrome de VACTERL (anomalías vertebrales,
atresia anal,
anomalías cardíacas,
fístula traqueo-esofágica,
anomalías renales y malformaciones en los miembros).
ANOMALÍAS GENITOURINARIAS:
La orina fetal es la principal fuente de producción del líquido amniótico.
A partir de la décima semana de gestación los riñones fetales producen orina y durante la segunda mitad del embarazo produce el 90% del líquido amniótico.
La RM estaría solamente indicada cuando los resultados de la ecografía no son concluyentes,
especialmente en los casos de oligoamnnios o anhidramnios .
Las secuencias T2 2D y 3D con tiempo de repetición (TR) largo permiten obtener imágenes urográficas del sistema excretor sin el uso de contraste intravenoso que está contraindicado.
La secuencia de difusión sería útil en los casos de sospecha de infarto renal por trombosis venosa con disminución del coeficiente de difusión aparente (ADC) y en los síndromes de transfusión feto-fetal donde el valor de ADC del riñón de donante es superior al del receptor y se correlaciona con la severidad del síndrome.
La difusión facilita el diagnóstico de agenesia renal (uni o bilateral) ya que es una técnica muy sensible en la detección del parénquima renal (69,70).
La hidronefrosis es claramente visualizada en T2,
en el plano coronal podemos realizar imágenes urográficas visualizando todo el trayecto ureteral (71).
La estenosis de la unión pieloureteral es la causa más frecuente de hidronefrosis detectada prenatalmente (72) y cuando progresa puede producir un riñón displásico con múltiples quistes corticales y medulares.
La duplicidad del sistema pielocalicial es la malformación más frecuente (73).
La RM puede ayudar a establecer el diagnóstico de duplicidad completa o incompleta así como la desembocadura ectópica de un uréterocele asociado al uréter superior.
La RM permite el diagnóstico de agenesia renal bilateral ya que el severo oligoamnios o anhidramnios dificulta la valoración por US.
Se acompaña de cardiomiopatías congénitas y síndrome de Potter por el oligoamnios (facies característica,
contracturas articulares e hipoplasia pulmonar) (74).
La agenesia renal unilateral Fig. 14 generalmente es un hecho aislado con esperanza de vida normal aunque en ocasiones puede asociarse a síndrome de VACTERL.
Cuando un riñón no está localizado en la fosa renal la RM ayuda a identificar la situación del riñón ectópico.
La enfermedad renal poliquística autosómica recesiva presenta riñones grandes con alta intensidad uniforme en secuenciasT2 con pérdida de diferenciación córticomedular y no se identifica el sistema pielocalicial (75).
Los riñones displásicos multiquísticos Fig. 15 están aumentados de tamaño con múltiples quistes de diferentes tamaños en situación periférica y central con escaso parénquima renal entre los quistes (76).
Los quistes presentan hiperseñal en secuenciasT2 y están separados del sistema pielocalicial.
La extrofia vesical es una rara malformación con pared anterior vesical ausente y la pared posterior expuesta externamente.
La RM identifica una masa sólida extruida en situación infraumbilical,
con riñones y LA normales (77).
La malformación cloacal es una causa infrecuente de uropatía obstructiva secundaria al fallo en la división de la cloaca primitiva con comunicación entre tracto gastrointestinal,
tracto urinario y genitales con un solo orificio perineal.
Más frecuente en sexo femenino con hidronefrosis bilateral,
lesión quística en pelvis y dificultad para visualizar la vejiga por su pequeño tamaño Fig. 16 .
Se acompaña de calcificación del meconio en el tracto urinario y colon que se identifican mejor por ecografía (77-79).
Existe una variante menor,
el seno urogenital,
donde permanece una comunicación entre la vagina y el tracto urinario; lo cual existe normalmente durante el desarrollo embriológico.
Dicha comunicación ocurre en cualquier punto,
desde el meato uretral hasta la vejiga,
pero generalmente se da en la uretra media o distal.
Las dos estructuras se unen y desembocan en el periné como un único canal común (80).
El síndrome de Prune Belly o de Eagle-Barret es una rara malformación congénita con severa hidronefrosis,
deficiencia de la musculatura abdominal y criptorquidia.
La RM identifica la hidronefrosis y dilatación ureteral bilateral y dilatación de toda la uretra a diferencia de las valvas posteriores que dilata la uretra proximal,
genitales ausentes y se acompaña de oligoamnios (81).
MASAS ABDOMINALES
La mayoría de las masas abdominales son lesiones quísticas benignas:
Quiste de duplicación intestinal: Quiste unilocular con doble pared mucosa y muscular) más frecuente en el íleon distal.
Quiste del mesenterio: Se considera una malformación linfática.
Puede ser unilocular o más frecuente multilocular con múltiples septos Fig. 17 .
En ocasiones se extiende a retroperitoneo y extremidades inferiores.
Quiste del ovario: Es la masa abdominal femenina más frecuente,
en el tercer trimestre.
Los ligamentos del ovario son laxos y puede estar en cualquier localización.
Puede ser simple o complicado con torsión y sangrado
Quiste del uraco: Quiste unilocular en línea media entre la vejiga y la inserción del cordón.
Quiste del colédoco: Quiste unilocular en cuadrante superior derecho.
Pueden verse ductos biliares que entran en el quiste.
La RM permite la detección ,localización y caracterización de las lesiones quísticas benignas diferenciándolas de las asas intestinales (82,83).
La experiencia en RM en el diagnóstico de las masas hepáticas congénitas es muy limitada.
La mayoría son masas grandes y sólidas (hemangioendotelioma,
hepatoblastoma o metástasis de neuroblastoma) siendo menos frecuentes las lesiones quísticas (hamartoma mesenquimal) (84).
El nefroma mesobástico es la masa renal sólida más común,
es un tumor benigno con pronóstico excelente que se acompaña en un 70% de los casos de polihidramnios (85).
La RM delimita mejor su órgano-dependencia y se presenta como una masa sólida de señal uniforme,
levemente hiperintensa en secuenciasT2.
El neuroblastoma es el tumor maligno más frecuente en periodo neonatal(86).
La mayoría se originan de la médula adrenal y pueden presentarse como masas suprarrenales sólidas,
quísticas o sólido-quísticas (87) y las metástasis hepáticas son frecuentes (87).
Se debe establecer el diagnóstico diferencial con la hemorragia suprarrenal (la RM identifica hemorragia en los diferentes estadios) (88),
con el secuestro pulmonar infradiafragmático (la RM puede mostrar el aporte sistémico vascular) (89) y con teratomas retroperitoneales (90) Fig. 18 .
ESTUDIOS DE PATOLOGÍA VASCULAR
El uso de contraste intravenoso (gadolinio) no está aceptado ya que los quelatos de gadolinio pasan la barrera placentaria (91) y por el riesgo potencial de nefrotoxicidad del gadolinio (fibrosis sistémica nefrogénica) (92).
Las secuencias balanceadas (FIESTA) permiten realizar estudios vasculares torácicos y abdominales sin contraste (88),
sobre todo en los casos de secuestros intra o extralobares,
anomalías del desarrollo de la vena cava inferior Fig. 19 o de malformaciones vasculares como los shunt porto-sistémicos hepáticos Fig. 20 .