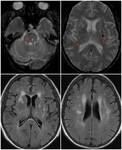
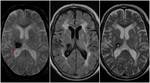
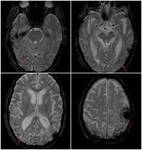
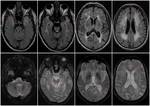
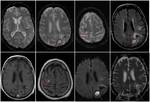
Dentro del grupo de secuencias para el estudio craneal mediante RM se encuentra la secuencia eco de gradiente potenciada en T2 (T2*).
Presenta una gran sensibilidad para la detección de lesiones hemorrágicas en el sistema nervioso central debido al efecto de susceptibilidad magnética generado por los productos de degradación de la hemoglobina.
También tiene gran sensibilidad para la detección de calcificaciones o aire intracraneal aunque pare ello la TC es superior.
Es una secuencia que no siempre se utiliza de rutina en los protocolos del estudio craneal.
En nuestro centro la utilizamos de rutina: bajo tiempo empleado en su adquisición (aproximadamente 3 minutos) y gran aportación de información.
Recientemente las nuevas secuencias de susceptibilidad magnética han demostrado una capacidad superior para la detección de restos hemáticos en el sistema nervioso central pero en nuestro centro aún no están disponibles.
En la secuencia T2* las hemorragias se van a manifestar como lesiones hipointensas y nuestro objetivo es presentar el diagnóstico diferencial cuando nos encontramos ante múltiples lesiones hipointensas de etiología hemorrágica en la secuencia T2* en el sistema nervioso central el cual se muestra en la siguiente tabla:
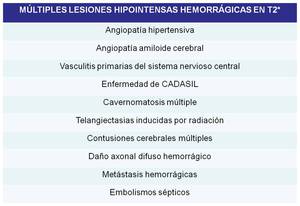
Table 2: Diagnóstico diferencial de múltiples lesiones intracraneales hipointensas en secuencia ecode gradiente T2.
Los hallazgos en esta secuencia no deben interpretarse por separado y en su análisis deben tenerse en cuenta otras consideraciones clínicas y radiológicas como son:
- Edad
- Contexto clínico (vascular,
demencia,
traumático,
tumoral o infeccioso)
- Aspecto y localización de las lesiones
- Hallazgos asociados
- Correlación con otras secuencias de resonancia
- Correlación con otras pruebas de imagen (tomografía computarizada)
Presentamos las claves diagnósticas de cada una de estas patologías principalmente en resonancia magnética,
con especial énfasis en el contexto clínico,
aspecto de las lesiones,
su localización y los posibles hallazgos asociados.
Angiopatía hipertensiva
Es el resultado de una hipertensión arterial mal controlada de larga evolución. Se produce lipohialinosis y necrosis fibrinoide de pequeñas arterias que da lugar a:
– Estenosis vasculares e infartos secundarios
– Hemorragias por rotura directa vascular o tras la formación de pequeños aneurismas (denominados de Charcot-Brouchard)
Las arterias principalmente afectadas son: lenticulo-estriadas,
ramas paramedianas de la arteria basilar y las arterias cerebelosas.
Por tanto nos vamos a encontrar hemorragias de localización central afectando a ganglios basales,
tálamo y al tronco,
asociándose o no a infartos lacunares o áreas de desmielinización periventricular isquémica.
Se van a producir dos tipos de hemorragias:
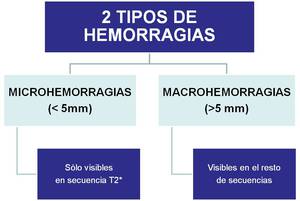
Table 3: Tipos de hemorragias hipertensivas.
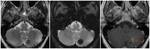
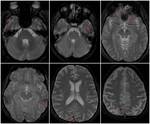
Las microhemorragias únicamente son visibles en la secuencia T2* y no son detectables en el resto de secuencias (Figura 1).
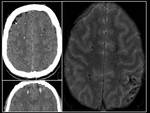
Las macrohemorragias son detectables en todas las secuencias (Figura 2).
Puntos clave:
• Edad media/avanzada.
• Historia de HTA de larga evolución.
• Micro/macrohemorragias de localización central en la protuberancia y ganglios basales.
• Asociación con patología isquémica de pequeño vaso.
Angiopatía Amiloide Cerebral
Se trata de una alteración vascular cerebral caracterizada por el depósito de proteína β-amiloide en la pared de vasos de pequeño y mediano tamaño. Existen dos variedades: una hereditaria que afecta a individuos de mediana edad y otra esporádica cuya prevalencia y severidad se incrementa con la edad.
Muchos pacientes se encuentran asintomáticos por lo que la prevalencia exacta no es bien conocida (se estiman cifras superiores al 75% en pacientes con más de 90 años).
El cuadro clínico típico es el de hemorragias intracraneales agudas,
accidentes isquémicos transitorios y demencia en pacientes sin historia de hipertensión arterial o coagulopatía.
El depósito de β-amiloide debilita la pared de los vasos y por tanto los predispone a su ruptura y consecuente hemorragia.
Además se producen estenosis de los mismos lo que aumenta el riesgo de eventos isquémicos.
Típicamente existe afectación de los vasos de la corteza cerebral,
área subcortical y de las leptomeninges,
respetando vasos de similar tamaño de la sustancia blanca profunda.
Por tanto las hemorragias van a ser de localización cortico-subcortical:
- Microhemorragias (< 5 mm): generalmente asintomáticas con predominio en lóbulos occipitales y parietales.
- Macrohemorragias (> 5mm): sintomáticas y que pueden asociarse a hemorragia subaracnoidea o subdural.
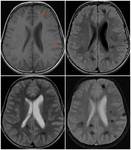
En estos pacientes también es típico encontrarse con áreas de desmielinización isquémica periventricular y atrofia cerebral secundaria (Figura 3).
Puntos clave:
• Edad avanzada.
• Hemorragias intracraneales de repetición sin historia de HTA o coagulopatía y con deterioro cognitivo asociado.
• Micro/macrohemorragias de localización cortico-subcortical con predilección por los lóbulos occipitales y parietales
• Signos de hemosiderosis superficial.
• Asociación con desmielinización isquémica y atrofia.
Vasculitis primarias del Sistema Nervioso Central
Son un grupo de enfermedades inflamatorias raras y de mal pronóstico aunque potencialmente tratables con inmunosupresores.
Presentan un amplio espectro clínico que va a depender del tipo de vaso afectado (grande-mediano vs pequeño) y la localización de las lesiones.
En las pruebas de imagen van a presentar lesiones isquémicas múltiples en distintos estadios pudiendo encontrarse pequeñas microhemorragias múltiples en la secuencia T2*.
También pueden asociarse a zonas irregulares de realce vascular en los estudios con gadolinio intravenoso que pondrían de manifiesto los vasos inflamados del sistema nervioso central.
La angiografía cerebral es la prueba diagnóstica de elección y puede demostrar un patrón típico vascular de zonas de estenosis y dilataciones alternantes.
En casos con alta sospecha diagnóstica clínica y arteriografías negativas puede ser necesario recurrir a la biopsia cerebral para confirmar el diagnóstico.
Enfermedad de CADASIL
Del inglés: Cerebral Autosomal Dominant Arteriopathy with Subcortical Infarcts and Leucoencephatopathy.
Es una enfermedad hereditaria autosómica dominante causada por una mutación en el gen NOTCH3 del cromosoma 19.
Se produce una degeneración progresiva de las células del músculo liso de las arterias de pequeño calibre con estenosis de las mismas y patología isquémica secundaria en sustancia blanca periventricular,
tronco y ganglios basales.
La edad de los pacientes suele ser menor que en los casos de isquemia de etiología arterioesclerótica (jóvenes y adultos de mediana edad).
En esta enfermedad es muy sensible y específica la afectación isquémica de la sustancia blanca anterior de los lóbulos temporales y la sustancia blanca frontal superior paramediana.
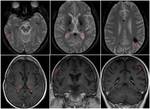
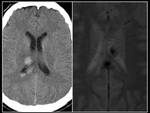
Pueden existir microhemorragias en secuencia T2* en el seno de las lesiones isquémicas (Figura 4).
En la actualidad no existe un tratamiento específico para esta enfermedad.
Puntos clave:
• Jóvenes y adultos de mediana edad.
• Afectación isquémica de la sustancia blanca anterior de los lóbulos temporales y región frontal superior paramediana.
• Pueden existir microhemorragias en secuencia T2* en el seno de las lesiones isquémicas.
Cavernomatosis múltiple
Los cavernomas representan junto con la MAV trombosada y la telangiectasia capilar,
el grupo de malformaciones vasculares cerebrales ocultas para la angiografía. Suelen debutar entre la 2ª-5ª década de la vida,
habitualmente con crisis y hemorragias.
Son lesiones dinámicas en las cuales se producen cambios a lo largo de su evolución (aparición de novo,
crecimiento,
reducción de tamaño).
Se han demostrado una serie de factores asociados a su formación de novo: irradiación previa,
infecciones virales,
hormonales (embarazo),
genética (casos familiares),
siembra a lo largo de un tracto de biopsia y asociación con anomalías del desarrollo venoso.
La asociación cavernomas con anomalías del desarrollo venoso (angiomas venosos) hay que buscarla pues se presenta con relativa frecuencia (hasta en el 20% según las series).
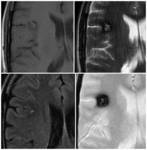
Existe una mejor visualización en los estudios con contraste intravenoso en los que el cavernoma permanece hipocaptante realzando el angioma venoso (Figura 5).
En caso de que el cirujano se plantee resecar el cavernoma debe preservar el angioma venoso o de lo contrario ocasionaría un infarto venoso.
Se ha propuesto una teoría para el desarrollo del cavernoma cuando existe una anomalía del desarrollo venoso subyacente:
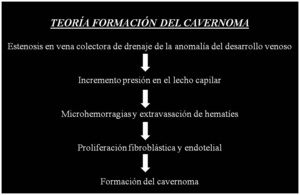
Table 4: Teoría para la formación de un cavernoma cuando existe una anomalía del desarrollo venoso.
Los cavernomas son lesiones hamartomatosas que se componen de restos hemáticos por tanto en RM los cavernomas van a tener una apariencia variable dependiendo del estadio de la hemorragia.
Su imagen más típica es conocida como “lesión en palomitas de maíz”: núcleo de señal heterogénea en secuencias potenciadas en T1 y T2 (resultante de trombosis,
hemorragia,
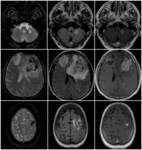
fibrosis y calcificación) rodeado por un anillo de hemosiderina completo en secuencias T2. La lesión “florece” en la secuencia T2* debido al efecto de susceptibilidad magnética generado por los productos de degradación de la hemoglobina (Figura 6).
No suele existir edema,
efecto de masa o realce tras la administración de contraste intravenoso.
Aproximadamente en un 15-20 % vamos a encontrar más de una lesión,
es lo que se conoce como cavernomatosis múltiple.
En tales casos habrá antecedentes familiares de cavernomas en más del 80% de los pacientes.
En estos pacientes existe mayor tendencia al sangrado,
por lo que suelen debutar a una edad más temprana. La localización de las lesiones va a ser aleatoria,
aunque de predominio supratentorial y en unión cortico-subcortical.
En los casos de cavernomas múltiples la secuencia T2* suele poner de manifiesto un mayor número de lesiones que el resto de secuencias,
debido al “florecimiento” de pequeñas lesiones en relación al efecto de susceptibilidad magnética condicionado por depósitos milimétricos de hemosiderina (Figura 7).
Puntos clave:
• Debut en infancia/adolescencia.
• Antecedentes familiares de cavernomas en más del 80% de los pacientes en los casos múltiples.
• Aspecto típico “en palomita de maíz” de las lesiones en secuencias T1 y T2.
• No suele existir edema o efecto de masa significativo para el tamaño de las lesiones.
Importancia de descartar anomalía del desarrollo venoso asociada administrando contraste intravenoso.
Telangiectasias inducidas por radiación
Dentro de los efectos secundarios tardíos de la radiación sobre el sistema nervioso central se encuentran: la atrofia cerebral,
necrosis de la sustancia blanca,
desmielinización,
gliosis reactiva,
inducción de neoplasias y el desarrollo de lesiones proliferativas vasculares.
Las lesiones proliferativas vasculares incluyen la telangiectasia capilar y los cavernomas y se postula que son el resultado de un daño en la microcirculación cerebral con incremento en la producción de factor de crecimiento del endotelio vascular tras la radiación.
Muchos autores consideran a ambas dentro del espectro de una misma patología.
En primer lugar se desarrollarían las telangiectasias capilares (entre 3 y 9 meses de media tras la radiación) y posteriormente los cavernomas (entre 1 y hasta 25 años tras la radiación).
El desarrollo de lesiones proliferativas vasculares en el sistema nervioso central es más común cuando los pacientes son radiados durante la infancia y habitualmente son múltiples.
Pueden asociarse además a otras lesiones inducidas por la radiación (Figura 8).
Puntos clave:
• Considerar a las telangiectasias capilares y los cavernomas en el diagnóstico diferencial de una lesión hemorrágica cerebral en cualquier paciente que haya recibido previamente irradiación sobre el sistema nervioso central.
• Especialmente considerarlo si la radiación se ha producido durante la infancia.
• Buscar otros efectos secundarios de la radioterapia.
Contusiones cerebrales múltiples
Siempre existirá antecedente de traumatismo cráneo-encefálico que provocará zonas de contusión cerebral cortical hemorrágicas debido al choque del parénquima cerebral contra la tabla interna craneal o la dura.
Se van a producir dos tipos de lesiones:
- Por golpe: zonas de impacto directo
- Por contragolpe: en las zonas opuestas al impacto directo
Las localizaciones típicas de las contusiones corticales son: los polos anteriores de los lóbulos temporales y las regiones frontobasales.
Mucho menos frecuentes son las contusiones cerebelosas.
En los casos agudos puede existir edema asociado y signos de hipertensión intracraneal,
siendo en estos casos de elección la TC.
En RM encontraremos restos hemáticos en secuencia T2* en las localizaciones típicas (Figura 9).
Pueden existir otras lesiones postraumáticas asociadas: daño axonal difuso,
hemorragia subaracnoidea,
hematomas epidurales y hematomas subdurales.
Puntos clave:
• Antecedente de traumatismo cráneo-encefálico.
• Localizaciones típicas en polos anteriores temporales y regiones frontobasales.
• Buscar lesiones por contragolpe.
Coexistencia de otras lesiones postraumáticas.
Daño axonal difuso hemorrágico
La lesión axonal difusa (LAD) o daño axonal difuso es la 2ª lesión intraparenquimatosa más frecuente tras TCE cerrado y es la causa más frecuente de coma post-traumático y de estado vegetativo persistente.
Se produce una disrupción inmediata e irreversible de haces axonales producidos por fuerzas de aceleración-deceleración y rotación cefálica rápida,
típicamente en los accidentes de tráfico.
Aunque las tasas de mortalidad exclusivamente por LAD son bajas existen elevadas tasas de morbilidad por sus graves secuelas neurológicas.
En el momento agudo tras el TCE la prueba de elección para su valoración es la TC,
aunque en ocasiones puede ser normal.
Después debe realizarse siempre RM.
Aunque tanto la TC como la RM infraestiman las lesiones encontradas en la anatomía patológica la RM es mucho más sensible para su detección.
En la LAD existen 2 tipos de lesiones:
- Hemorrágicas: secuencia T2* la más sensible en su detección. - No hemorrágicas (traducen áreas de edema): secuencia FLAIR la más sensible.
Estas lesiones se producen en unas localizaciones típicas y en ello se basa la clasificación de Gentry (Adams) la cual además tiene valor pronóstico:

Table 5: Clasificación de Gentry (Adams) del daño axonal difuso hemorrágico
Las lesiones que afectan a la interfase sustancia gris-blanca son las más frecuentes y a la vez las que conllevan un mejor pronóstico.
Tienen predominio en los lóbulos frontales y temporales,
una localización parasagital cuando afectan a los lóbulos frontales y una morfología ovoidea,
paralela al eje de los axones (Figura10).
Las lesiones del cuerpo calloso son más frecuentes en la zona del cuerpo y del esplenio.
Habitualmente son unilaterales,
excéntricas y suelen ir asociadas a lesiones en la interfase sustancia gris-blanca.
La lesión del cuerpo calloso puede extenderse por víaa transependimaria (posiblemente por laceración de venas ependimarias) al sistema ventricular asociándose por tanto a hemorragia intraventricular (Figura 11).
La LAD es la lesión traumática más frecuente del tronco del encéfalo y típicamente se localizan en el cuadrante dorsolateral del mesencéfalo.
Cuando se producen lesiones en el tronco en los pacientes con LAD indican un TCE severo,
son lesiones predominantemente hemorrágicas y casi siempre con lesiones supratentoriales asociadas (lesiones en la interfase sustancia gris-blanca y cuerpo calloso).
Son las lesiones que conllevan un peor pronóstico.
Otras localizaciones menos frecuentes son el brazo posterior de la cápsula interna,
la cápsula externa,
el tálamo o el núcleo lenticular por laceraciones de las arterias lenticulo – estriadas.
Lesiones en la línea media como el fórnix,
septum pelucidum y comisura anterior van muchas veces asociadas a lesiones del cuerpo calloso.
También pueden observarse lesiones en cerebelo.
Puntos clave:
• Antecedente de TCE grave con coma post-traumático.
• Localizaciones típicas en región cortico-subcortical de la convexidad (parasagitales y de morfología ovoidea),
en región posterior del cuerpo calloso (unilaterales y excéntricas) y región dorsolateral del mesencéfalo.
• Coexistencia de otras lesiones postraumáticas asociadas.
Metástasis hemorrágicas
Determinadas metástasis cerebrales muy vascularizadas tienen tendencia al sangrado,
siendo más común en las del coriocarcinoma,
melanoma,
pulmón,
riñón y tiroides.
También pueden existir hemorragias tras tratamiento con quimioterapia o radioterapia en metástasis que primariamente no lo eran.
En la mayoría de los casos suele existir neoplasia sistémica conocida.
Las lesiones van a ser múltiples en aproximadamente el 50% de los casos.
Suelen ser de predominio supratentorial y en la interfase cortico-subcortical.
Las lesiones hemorrágicas van a presentar hipointensidad de señal en secuencia T2* y habitualmente va a existir intensidad de señal heterogénea en el resto de secuencias así como importante edema vasogénico asociado.
El tipo de realce tras la administración de contraste intravenoso es variable (homogéneo,
heterogéneo,
anular) pudiendo asociarse a signos de carcinomatosis meníngea (Figura 12).
Generalmente no existe restricción en la secuencia de difusión,
aunque puede haberlo en metástasis densamente celulares.
Puntos clave:
• Suele existir neoplasia sistémica conocida.
• Más tendencia a la hemorragia en metástasis de coriocarcinoma,
melanoma,
pulmón,
riñón y tiroides.
• Señal heterogénea en otras secuencias,
importante edema vasogénico asociado y el tipo de realce es variable.
• Generalmente no existe restricción a la difusión (aunque puede haberlo en metástasis densamente celulares).
Embolismos sépticos
El cuadro clínico suele ser multisistémico asociado a menudo a complicaciones neurológicas.
El caso más común es el de un paciente con endocarditis infecciosa mitral generando embolismos de origen cardiogénico.
También pueden ocurrir embolismos sépticos cerebrales en los casos de infecciones de accesos venosos periféricos o de endocarditis derechas (con shunt intracardíacos o intrapulmonares),
lo que se conoce como embolismos paradójicos.
Existirá diseminación de los émbolos a los vasos del parénquima cerebral (produciendo abscesos cerebrales que aunque es raro pueden asociar áreas hemorrágicas) o a los vasos meníngeos (produciendo meningitis).
Puede producirse también patología isquémica por oclusión vascular o más raramente la formación de aneurismas micóticos.
Las lesiones suelen encontrarse en la unión cortico-subcortical,
con edema vasogénico asociado y con captación del contraste intravenoso de forma anular (fino y lineal),
pudiendo existir zonas de realce meníngeo asociadas.
Los abscesos cerebrales presentan típicamente un patrón de restricción a la difusión,
lo que es muy importante para el diagnóstico diferencial con otras patologías (Figura 13).
Puntos clave:
• Contexto infeccioso habitualmente de origen cardiológénico.
• Lesiones en unión cortico-subcortical con captación anular fina de contraste que asocian edema vasogénico y que típicamente presentan restricción a la difusión.
• Pueden existir zonas de realce meníngeo traduciendo meningitis asociada.