El amplio uso de las pruebas de imagen,
y los avances de las mismas,
han aumentado exponencialmente los hallazgos incidentales de masas renales en estudios realizados por otras razones.
Ante una masa renal el radiólogo tiene dos papeles fundamentales:
1- Analizar las características de la lesión para establecer el diagnóstico más probable.
2- Recomendar el manejo de la tumoración.
Las posibilidades son: Ignorar,
hacer un seguimiento,
recomendar otra prueba complementaria,
biopsia o cirugía.
La tomografía computarizada multidetector (TCMD) es una herramienta fundamental para la detección y caracterización de los tumores,
el estudio de extensión,
la planificación prequirúrgica y la valoración de la respuesta al tratamiento.
Para ello el radiólogo debe valorar el comportamiento de la lesión tras la administración de contraste y realizar reconstrucciones.
A.
CARACTERIZACIÓN DE LOS TUMORES RENALES
El hecho de que estén aumentando los hallazgos incidentales en pacientes asintomáticos,
conlleva que con mayor frecuencia las lesiones son de pequeño tamaño cuando se detectan.
Esto dificulta su caracterización y el diagnóstico diferencial.
Consideramos que es importante conocer los aspectos técnicos del TCMD y los protocolos de estudio de las masas renales para obtener su máximo rendimiento.
1) PROTOCOLO DE ESTUDIO DE LAS MASAS RENALES:
Consta de cuatro fases,
siendo la última optativa:
- Estudio basal sin contraste
- Fase córticomedular -> Se obtiene a los 25-70 segundos (sg) de la administración de contraste.
- Fase nefrográfica o parenquimatosa -> A los 80-120 sg.
- Fase excretora (optativa) -> A partir de 180 sg.
En nuestro hospital disponemos de un TCMD de 64 detectores y obtenemos la fase córticomedular a los 35 sg,
la fase nefrográfica a los 90 sg y la fase excretora a partir de los 180sg.
El algoritmo de reconstrucción es de 2 mm grosor de corte con 1 mm de intervalo,
permitiéndonos obtener reconstrucciones multiplanares (MPR) de alta calidad.
Se administran 100 ml (125 ml en obesos) de contraste yodado intravenoso (CIV),
con una concentración de 320 mg/ml y a una velocidad de infusión de 4ml/sg.
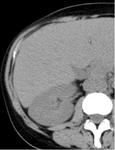
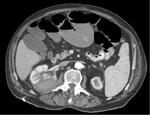
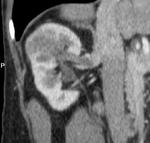
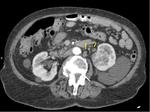
a) Estudio basal:
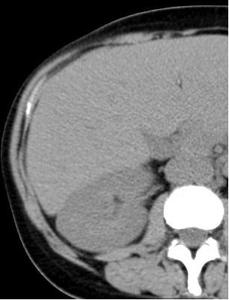
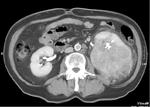
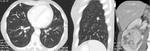
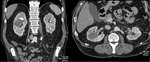
Fig. 1: Estudio basal sin contraste.
Esta fase es fundamental para poder cuantificar el realce de la lesión tras la administración de contraste IV.
Se detectan muy bien las calcificaciones.
Por sí sola esta fase no es muy útil para discriminar lesiones tumorales.
Ante una lesión homogénea y bien definida,
mediremos las unidades hunsfield y podremos deducir que:
- Si mide < 20 UH → Se trata de un quiste simple.
- > 20 UH → Puede ser un quiste denso o un carcinoma de células renales (CCR).
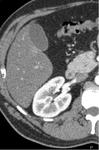
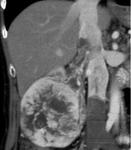
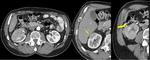
b) Fase córticomedular (25-70 sg):
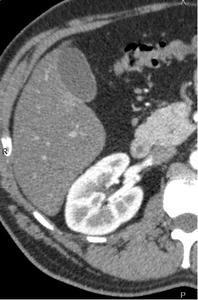
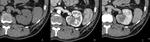
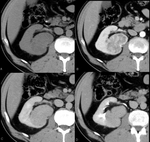
Fig. 2: Fase córticomedular obtenida a los 35 sg tras la administración de contraste iv.
En esta fase se realza la corteza renal.
VENTAJAS:
- Muy útil para valorar los vasos renales.
- Diagnóstico de variantes anatómicas ( Ej.
hipertrofias de las columnas de Bertin)
- Diagnóstico de metástasis.
Las metástasis hepáticas son hipervasculares y se pueden ver en esta fase.
En la fase siguiente pueden pasar desapercibidas.
DESVENTAJAS:
Puede no detectar:
- Pequeñas lesiones hipovasculares de la médula (por no realzar lo suficiente debido a la baja atenuación que presenta la médula en esta fase).
- Pequeñas lesiones hipervasculares de la corteza (por quedar enmascaradas debido a la alta atenuación que presenta la corteza en esta fase).
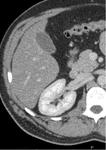
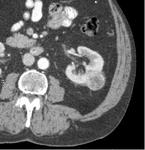
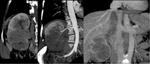
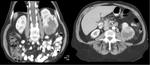
c) Fase nefrográfica o parenquimatosa (80-120 sg):
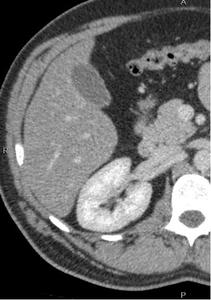
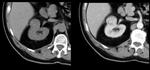
Fig. 3: Fase nefrográfica obtenida a los 90 sg de la administración de contraste.
El CIV produce un realce homogéneo de todo el parénquima renal
Es la fase mas eficaz para el estudio de las masas renales de pequeño tamaño.
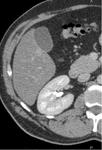
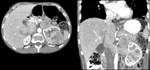
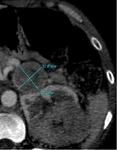
d) Fase excretora o pielográfica (a partir de 180sg):
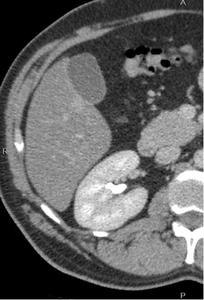
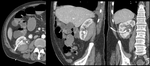
Fig. 4: Fase excretora obtenida a los 180 sg de la administración de contraste.
El CIV se localiza en la vía excretora.
Útil en caso de sospecha de invasión del aparato excretor.
No es necesaria en el protocolo habitual de estudio de la masa renal (optativa).
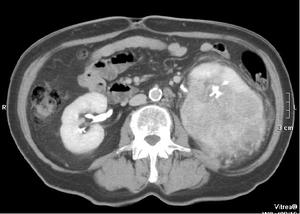
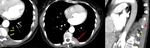
Fig. 5: Masa renal izquierda de 11 x 10 x 18 cms de ejes AP, transverso y craneocaudal respectivamente. Imagen en el plano axial obtenida en la fase excretora (>180 sg), donde se demuestra que la masa invade y distorsiona la pelvis renal, aunque no impide la excreción de contraste.
2) PATRÓN DE REALCE
Se considera realce el aumento de mas de 20 UH en la fase nefrográfica respecto al estudio basal.
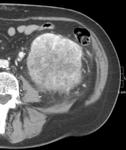
Las masas de gran tamaño suelen tener un realce heterogéneo con áreas de necrosis en su interior.
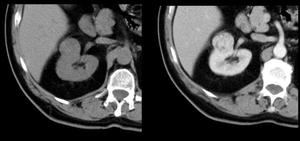
Fig. 6: Masa renal izquierda de 3 x 3 cms. Captación heterogénea de contraste con un realce en la fase nefrográfica superior a 20UH respecto al estudio basal
Sin embargo debemos ser conscientes que existen artefactos,
como el del endurecimiento del haz (pseudorealce)
Pseudorealce: Los quistes renales simples pueden mostrar un realce artificial superior a 10 UH en los estudios con contraste,
producido por los algoritmos de reconstrucción de la imagen en las TC helicoidales.
Este fenómeno es mas pronunciado en lesiones intrarrenales,
pequeñas (< 2cms)
Por lo tanto,
si existen dudas respecto al realce de una tumoración,
es preferible recomendar otra prueba diagnóstica (ecografia,
RM).
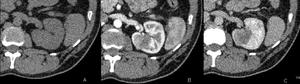
Fig. 7: Tumoración renal izquierda de 3 x 3 cms en región interpolar. Imágenes en el plano axial en fase basal sin contraste (A), fase córticomedular (B) y fase nefrográfica (C). Se observa un realce inferior a 20 UH en fase nefrográfica respecto al estudio basal.
3) PATRÓN DE LAVADO
El realce es un fenómeno transitorio y por tanto también es útil valorar la disminución de la atenuación en estudios tardíos
Si objetivamos un quiste denso en una TC con contraste IV realizada por otro motivo,
podemos hacer un estudio retardado a los 15 minutos,
midiendo de nuevo las UH:
- Pérdida de 10 UH o mas → Se trata de una masa sólida.
- Ausencia de variación → Se trata de un quiste denso.
4) CARCINOMA DE CÉLULAS RENALES.
SUBTIPOS HISTOLÓGICOS
El carcinoma de células renales (CCR) el el tumor primario maligno mas frecuente del riñón (90%).
Presenta diferentes tipos histológicos,
de los cuales el más frecuente es el carcinoma de células claras.
| SUBTIPO HISTOLÓGICO |
PREVALENCIA |
| Carcinoma de células claras |
70% |
| Carcinoma de células papilares |
10% |
| Carcinoma de células cromófobas |
5% |
| Síndromes de cáncer hereditario |
5% |
| Carcinoma quístico multilocular |
<1% |
| Carcinoma de conductos colectores |
<1% |
| Carcinoma medular |
<1% |
| Carcinoma mucinoso tubular |
<1% |
| Neuroblastoma asociado a CCR |
<1% |
| Xp11.2 translocación TFE-3 |
<1% |
| Lesiones inclasificables |
4% |
OMS 2004: CLASIFICACIÓN DEL CARCINOMA DE CÉLULAS RENALES
Aunque es muy difícil caracterizar el subtipo histológico mediante la TCMD,
sabemos el realce de la lesión es distinto en función del mismo:
C.
CÉLULAS CLARAS (70%): Masa con realce heterogéneo con o sin áreas necróticas o quísticas en su interior.
C.
CELS.
PAPILARES (10%): Hipovascular.
Menor realce y mas homogéneo
C.
CROMÓFOBO (5%): Realce homogéneo y moderado (intermedio entre los dos anteriores).
Este subtipo histológico es el que se suele confundir con el oncocitoma.
C.
MEDULAR (1%): Infiltrativo con epicentro en la médula condicionando dilatación calicial.
B.
DIAGNÓSTICO DIFERENCIAL DE LOS TUMORES RENALES
No todas las lesiones renales son tumores.
También nos podemos encontrar con:
1 - Parénquima hipertrófico junto a cicatriz *
2 - Congénitas: Columna de Bertin hipertrófica *
*El parénquima hipertrófico adyacente a una cicatriz y las alteraciones congénitas se caracterizan por realzar de forma idéntica al resto del parénquima renal (fase corticomedular y nefrogénica).
Los tumores renales,
suelen realzar menos que el resto del parénquima renal y el realce suele ser mas heterogéneo.
3 - Anomalías vasculares: Aneurismas,
malformaciones arteriovenosas
4 - Trauma,
infarto,
hemorragia e infección
Veamos algunos ejemplos:
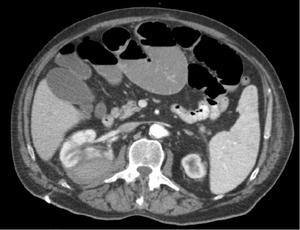
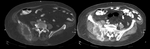
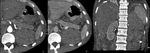
Fig. 8: Colección de alta densidad en riñón derecho de 5 x 4 cms, que deforma el parénquima renal. Riñón izquierdo atrófico.
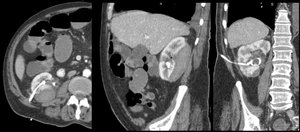
Fig. 9: Mismo caso de la figura anterior. Imagen axial obtenida 2cms por debajo e imágenes en sagital y coronal. Se aprecia el catéter de nefrostomía colocado en la pelvis renal. Se trataba de un hematoma agudo limitado por la cápsula renal tras colocación de nefrostomía. También se observan algunas burbujas de gas.
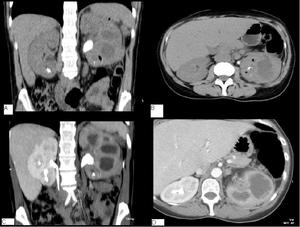
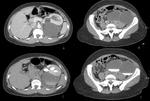
Fig. 10: A y B. Imágenes en coronal y axial de TC sin contraste IV. C y D. Imagenes en coronal y axial de TC con contraste IV en fase de eliminación (5 minutos). El riñón derecho presenta un cálculo en el grupo calicial inferior, con correcta eliminación de contraste a través del uréter. El riñón izquierdo presenta un cálculo coraliforme en la pelvis renal así como colecciones líquidas en la zona mesorrenal y en el polo inferior con burbujas de aire. Existe hidronefrosis izquierda y no se demuestra eliminación de contraste a través del uréter izquierdo. El diagnóstico fue de pielonefritis xantogranulomatosa. La paciente fue operada (nefrectomia radical) y la AP confirmó el diagnóstico
Lesiones quísticas
El 10% de los carcinomas de células renales son quísticos o predominantemente quísticos,
lo que implica que ante una lesión quística atípica,
hay que plantear el diagnóstico diferencial entre quiste complicado (por hemorragia,
infección o isquemia) y carcinoma quístico.
Para ello nos valemos de la clasificación de Bosniak.
CLASIFICACIÓN DE BOSNIAK
Bosniak distingue cinco categorías y en función de la posibilidad de malignización de cada grupo,
aconseja una actitud a seguir.
|
I
Quiste simple
Ausencia de tabiques,
calcificaciones o componentes sólidos
Ausencia de captación de contraste
Ignorar
|
|
II
Quiste mínimamente complicado
Tabiques finos (<1mm) o calcificaciones finas en la pared
Hiperdenso (>20 UH) menor de 3 cms sin realce
Ignorar
|
|
IIF
Masas quísticas moderadamente complicadas
Tabiques finos abundantes o engrosamiento liso o nodular de la pared
Calcificaciones groseras
Quistes hiperdensos de 3 cms o más sin realce
Seguimiento
|
|
III
Masas indeterminadas
Paredes o tabiques engrosados,
irregulares,
con realce medible
50% de posibilidad de malignizar
Resección y dx histológico
|
|
IV
Neoplasias quísticas
Cualquier categoría anterior pero con un componente sólido intraquístico que capta contraste
Tratamiento quirúrgico
|
| |
Las categorías IIF y III pueden ser difíciles de distinguir y están sujetas a variabilidad interobservador.
No obstante,
las decisiones terapeuticas dependen de la combinación de hallazgos de imagen,
factores clínicos y de las opciones terapéuticas disponibles.
Por ejemplo,
una lesión quística de categoría IIF en un paciente joven (que según la clasificación de Bosniak requeriría seguimiento) es probable que el cirujano decida tratarla con nefrectomía parcial laparoscópica.
Sin embargo una lesión de categoria III en un paciente mayor con factores de riesgo quirúrgico (que según la clasificación de Bosniak requeriría biopsia y extirpación),
es posible que se decida una actitud expectante y seguimiento.
C.
ESTADIFICACIÓN
Es fundamental realizar una correcta estadificación en el momento del diagnóstico para establecer el pronóstico y las posibilidades terapéuticas.
Tanto la TCMD como la RM son técnicas eficaces para el estudio de extensión.
Sin embargo la TCMD es mas rápida y tiene mayor disponibilidad,
por lo que sigue siendo la técnica de elección para la estadificación.
Actualmente el CCR se estadifica según la clasificación TNM.
Fue revisada por el American Joint Committee on Cancer en enero del 2010.
CARACTERISTICA TNM
No se puede valorar el tumor Tx
No hay evidencia de tumor primario T0
T.
confinado a la cápsula renal
< o = 4 cms T1a
> 4 cms – 7cms T1b
> 7cms T2
Invade suprarrenal o grasa perirrenal confinado a la f.
de Gerota T3a
Trombo venoso
V.
renal T3b
VCI infradiafragmática T3b
VCI supradiafragmática T3c
Ganglios linfáticos
No se pueden evaluar Nx
No se demuestran metástasis ganglionares regionales N0
Un ganglio linfático regional N1
Mas de un g.
linfático regional N2
Extensión local.
Atraviesa la fascia de Gerota T4
Metástasis
No valorables Mx
No hay metástasis a distancia M0
Hay metástasis a distancia M1
Los tumores de pequeño tamaño (estadios T1) pueden ser estatificados con TC abdominopélvico y Rx de tórax.
Para los tumores en estadío T2 o superior es recomendable realizar también TC torácica.
Solo se realizará la búsqueda activa de metástasis en otras localizaciones (ej cerebrales) en pacientes sintomáticos.
1) Tumor confinado a la cápsula renal
Es el que tiene mejor pronóstico (supervivencia 60-90% a los 5 años).
Si la localización y el tamaño lo permiten,
los cirujanos tienden a realizar tumorectomía (nefrectomía parcial).
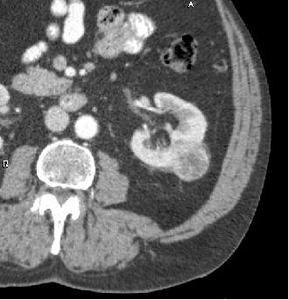
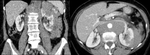
Fig. 11: Tumoración en la región posterior del riñón izquierdo de 4 cms de diámetro, que protuye en la cortical, sin afectación de la grasa perirrenal.
2) Diseminación perirrenal
Supone indicación de nefrectomía total.
El hallazgo mas específico es la presencia de un nódulo hipercaptante en el espacio perirrenal (T3a).
El mayor problema que existe con esta fase son los falsos negativos y positivos.
- Falso negativo (no detectar la diseminación perirrenal).
- Falso positivo (por infiltración grasa perirrenal por edema,
inflamación o uropatía obstructiva previa).
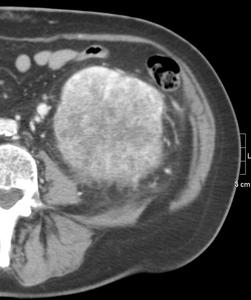
Fig. 12: Mismo caso de la figura 5. Masa renal izquierda de gran tamaño, con áreas de necrosis central y captacion heterogénea de contraste. Importante estriación de la grasa perirrenal.
3) Diseminación venosa tumoral
La tromobosis venosa se considera tumoral cuando se observa un defecto de repleción en el interior de la vena,
de captación heterogénea similar al tumor.
Tiene valor pronóstico de morbimortalidad perioperatoria
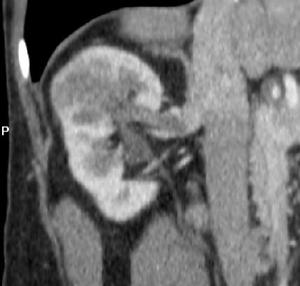
Fig. 13: Imagen obtenida en el plano coronal. La trombosis aislada de la v. renal no modifica el pronóstico pero hace necesaria una nefrectomía radical por cirugía abierta
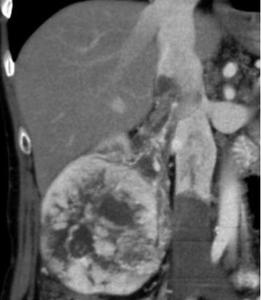
Fig. 14:
Reconstrucción en el plano coronal. Masa en el riñón derecho de 9 x 9 cms de ejes AP y craneocaudal, que presenta un realce heterogéneo, con trombosis de la vena renal que se extiende a la v. cava inferior sin alcanzar la porción intrahepática. Marcada circulación colateral. La nefrectomía radical se puede realizar por abordaje abdominal.
-
V.
cava inferior intrahepática subdiafragmática→ Cuando la trombosis tumoral se extiende hasta la porción intrahepática de la v.
Cava,
sin sobrepasar los diafragmas,
la cirugía precisa un abordaje toracoabdominal.
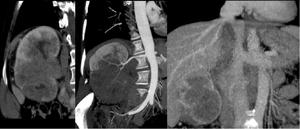
Fig. 15: Gran masa renal derecha de 8 x 11 cms de ejes AP y craneocaudal, de aspecto infiltrativo y con escaso realce. El aspecto radiológico no era muy sugestivo de carcinoma renal de células claras, ya que este suele presentarse como una masa con realce heterogéneo. Sin embargo el resultado de la AP fue de ca. de células claras. En la imagen de la derecha se aprecia la trombosis de la vena renal que se extiende a la v. cava inferior , afectando a la porción intrahepática sin sobrepasar el diafragma. La paciene precisó nefrectomía radical con abordaje toracoabdominal.
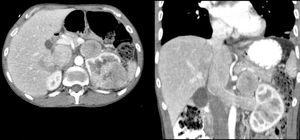
Fig. 16: Masa renal izquierda de 7,5 x 7,5 cms en ejes AP y craneocaudal con realce heterogéneo y adenopatías de gran tamaño. Trombosis tumoral de la v. renal que se extiende por toda la v. cava inferior hasta la aurícula derecha. El paciente precisó nefrectomía radical con abordaje toracoabdominal y trombectomia reno-cavo-auricular con apertura de la aurícula y circulación extracorpórea. AP: Carcinoma renal de células claras.
4) Diseminación ganglionar
- Se consideran metastásicos los ganglios > 1cm de diámetro menor e hipercaptantes.
- Suponen peor pronóstico (supervivencia 5-30% a los 5 años).
- Existen falsos positivos (adenopatías de origen inflamatorio).
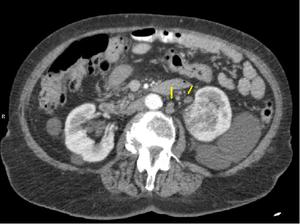
Fig. 17: Adenopatías perihiliares y paraaórticas, la mayor de 1,8 cms y masa renal izquierda de realce heterogéneo.
La paciente había ingresado por quistes hepáticos complicados que precisaron drenaje quirúrgico. Uno de los quistes, localizado en el segmento VI, es de gran tamaño y desplaza al riñón izquierdo hacia delante. La tumoración renal fue un hallazgo incidental.
5) Extensión local
Es difícil valorar la afectación de órganos vecinos.
El signo radiológico mas importante es el cambio de densidad de las estructuras adyacentes.
Son signos sugestivos: Márgenes irregulares entre ambas estructuras o pérdida de planos grasos (15% Falsos positivos).
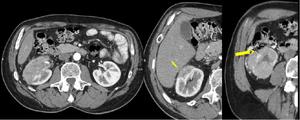
Fig. 18: Tumoración sólida de 6 x 8 cms de ejes AP y craneocaudal en región mesorrenal y polo inferior del riñón derecho. Se observa la afectación de la grasa perirrenal y la presencia de colaterales. Márgenes irregulares de separación entre la porción mas superior de la masa y el hígado y pérdida de planos grasos en su porción mas inferior estando en íntimo contacto con el colon (flechas). Se le realizó nefrectomía radical por cirugía abierta. AP: Ca renal de cels claras
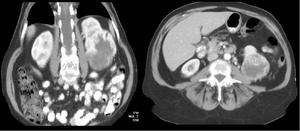
Fig. 19: Tumoración sólida de 6 x 8,5 cms de ejes AP y craneocaudal en región mesorrenal y polo inferior del riñón izquierdo. Afectación de la grasa perirrenal. Márgenes irregulares entre la porción mas inferior de la masa y el músculo psoas iliaco. Se le realizó nefrectomía radical por vía laparoscópica. AP: Ca renal de cels claras
6) Diseminación suprarrenal homolateral
Es mas frecuente en tumores con extensión local o localizados en el polo superior
Si la glándula no está afectada no se extirpa.
Si la glándula está aumentada de tamaño,
desplazada o no se visualiza → Nefrectomía ampliada.
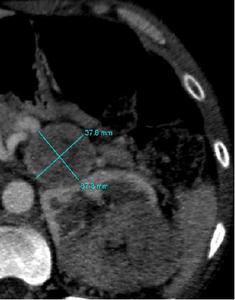
Fig. 20: Mismo caso de la figura 16. Adenopatía de gran tamaño que desplaza al riñón y la glándula suprarrenal izquierdos. La AP demostró que no existía afectación de la glándula.
7) Metástasis a distancia
Las mas frecuentes son a pulmón,
mediastino,
hueso e hígado (hipervasculares)
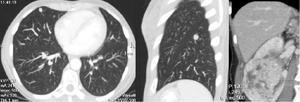
Fig. 21: Mismo caso de la fig 14. Se observan nódulos pulmonares en el segmento apical del lóbulo inferior izquierdo y en el lóbulo medio.
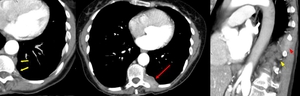
Fig. 22: Mismo caso de la fig 15. Metástasis mediastínicas: Masa de planos blandos en situación paraespinal izquierda, a la altura de T10, de 32 mm con afectación de músculos intercostales (flecha roja). Adenopatías en situación retroaórtica izquierda, adyacentes a la masa de planos blandos (flechas amarillas).
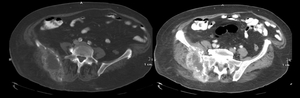
Fig. 23: Mismo caso de las figuras 5 y 12. Paciente con carcinoma de células renales en el riñón izquierdo en estadio T3a, que se trató con nefrectomía radical. AP: Ca. de células claras.
Ocho años después consultó por dolor en cadera derecha, objetivándose en la TC una extensa lesión lítica en la pala iliaca derecha con masa de planos blandos asociada.
La BAAG de la lesión fue positiva para adenocarcinoma de céls claras. La imagen reproducía las características histológicas de su biopsia previa y la inmunohistoquímica fue compatible con metástasis.
D.
OTROS TUMORES RENALES MALIGNOS
LINFOMA
TUMOR DE CÉLULAS TRANSICIONALES
METÁSTASIS
1- Linfoma
La afectación renal por un linfoma puede ser :
- Formando parte de un LNH diseminado.
- Que se trate de un linfoma primario extranodular.
Los linfocitos malignos alcanzan el riñón vía hematógena (invadiendo el hilio y extendiéndose al intersticio) o por contigüidad (invadiendo la corteza y extendiéndose a la médula renal)
En general se caracterizan por presentar escaso realce (son hipovasculares),
asociar adenopatías retroperitoneales de gran tamaño y por no producir trombosis venosa (tiende a rodear vasos más que a invadirlos).
Pueden ser unilaterales o bilaterales.
PATRONES DE PRESENTACIÓN:
a - Múltiples lesiones nodulares (50-60%).
Es la presentación mas frecuente.
b - Lesión nodular única.
c - Grandes adenopatias retroperitoneales e invasión del espacio perirrenal y riñón.
d - Patrón infiltrativo: Con pérdida de diferenciación córticomedular y aumento de tamaño de los riñones sin alteración de su silueta.
e - Afectación exclusiva del seno renal: A diferencia del carcinoma de células transicionales no suele producir hidronefrosis.
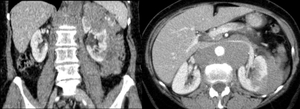
Fig. 24: Grandes bloques adenopáticos retroperitoneales que rodean y comprimen los vasos . Invasión de la grasa perirrenal y del polo superior del riñón izquierdo. Se trataba de un paciente con linfoma no Hodgkin
2- Tumor de células transicionales
Los uroteliomas de vias urinarias son relativamente infrecuentes.
Se presentan hasta en un 4% de pacientes con cáncer de vejiga.
Es mas frecuente la afectación de la pelvis renal que la de los uréteres.
Puede ser bilateral y multifocal
PATRONES DE PRESENTACIÓN:
- P.
de defecto de repleción.
- P.
de atrapamiento sinusal o periureteral (infiltrando el parénquima renal).
- P.
escirro (afectación desmoplástica).
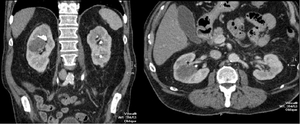
Fig. 25: TCMD con contraste IV en fase de eliminación. Reconstrucción en coronal e imagen axial. Paciente con urotelioma de alto grado vesical sometido a RTU en dos ocasiones. En la TCMD de control presenta una masa de 3 x 3 cms de ejes AP y craneocaudal respectivamente, situada en el tercio medio-superior del riñón derecho que condiciona una discreta dilatación del grupo calicial superior. Se le realizó nefroureterectomía derecha. La AP fue positiva a urotelioma.
3- Metástasis
Suelen ser lesiones sólidas,
múltiples y bilaterales.
Los tumores primarios mas frecuentes son:
- Mama
- Pulmón
- Melanoma
- Colon
E.
TUMORES RENALES BENIGNOS
- ANGIOMIOLIPOMA (frecuentes)
- ONCOCITOMA
- TUMOR YUXTAGLOMERULAR O RENINOMAS
- TUMOR FIBROSO
1- Angiomiolipomas:
Son tumores de origen mesenquimal formados por músculo,
grasa y vasos
Se diagnostican demostrando la presencia de grasa macroscópica dentro de una masa sólida
Cuando el componente graso es escaso,
puede ser preciso recurrir a la RM (secuencias eco de gradiente T1 en fase opuesta,
observándose la pérdida de señal en el interior de la lesión,
allí donde se localiza la grasa).
2- Oncocitoma
Son tumores benignos raros
Los de gran tamaño pueden presentar una cicatriz central característica,
aunque solo se presenta en un tercio de los casos.
Los de pequeño tamaño son muy difíciles de distinguir del carcinoma de células renales (especialmente del subtipo histológico cromófobo).
Kim JI et all (8) realizaron un estudio prospectivo con 98 pacientes,
demostrando que existe un patrón característico de realce en los oncocitomas de pequeño tamaño.
Se trata de un patrón segmentario con inversión en las fases corticomedular y nefrográfica en los oncocitomas de pequeño tamaño: El oncocitoma tiene dos componentes,
de tal forma que en la fase corticomedular uno es hiperdenso y el otro hipodenso.
Sin embargo,
en la fase nefrográfica dichos patrones se invierten (el primero se transforma en hipodenso y viceversa).
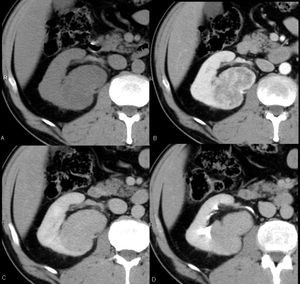
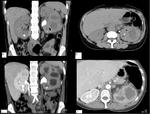
Fig. 26: Estudio basal (A), fase córticomedular (B), nefrográfica (C) y de excreción (D). Masa de 7 x 5 cms de ejs AP y transverso en el tercio medio del riñón derecho, que desplaza al hilio renal hacia delante sin infiltrarlo. Presenta moderado realce homogéneo en la fase nefrográfica, sin cicatriz central. Se le realizó nefrectomía radical laparoscópica. La AP fue de oncocitoma
F.
TRATAMIENTO QUIRÚRGICO
Es el tratamiento de elección.
Clásicamente se realizaba la nefrectomía radical en todos los carcinomas de células renales.
En la actualidad se tiende a la nefrectomía parcial,
siempre y cuando se asegure la escisión completa del tumor con un margen libre de 5 mm.
Opciones: - Cirugía abierta
- C.
laparoscópica
La decisión respecto a una u otra técnica dependerá de múltiples factores,
incluida la experiencia del cirujano.
Sin embargo,
es importante que le aportemos una serie de datos que le puede ayudar en su toma de decisiones.
Lo que el radiólogo debe valorar:
- TAMAÑO: Hasta 7 cms es posible realizar la nefrectomia parcial.
Hasta 15 cms se puede optar por la via laparoscópica.
- LOCALIZACIÓN: Polar,
interpolar,
anterior o posterior.
- NATURALEZA QUÍSTICA O SÓLIDA: Una lesion quística de gran tamaño excluye la cirugía laparoscópica por posibilidad de rotura y diseminación.
- PROFUNDIDAD: Si la lesión es pequeña y no protuye en la corteza se excluye la vía laparoscópica porque el cirujano no la va a poder ver.
- SITUACIÓN RESPECTO AL SISTEMA EXCRETOR: Si existe posibiliad de incisión en el mismo,
son muy probables las complicaciones postquirúrgicas como el urinoma y se prefiere la nefrectomía radical.
- SITUACIÓN RESPECTO AL HILIO RENAL: Puede dificultar un abordaje laparoscópico y preferirse una cirugía abierta o actitud expectante.
- ANATOMIA VASCULAR: Si existe una o mas a.renales,
arterias nutricias y origen de las mismas...
- EXISTENCIA DE TROMBOSIS VENOSA.
-CIRCULACIÓN COLATERAL: Si existe abundante colateralidad peritumoral puede determinar la elección de cirugía abierta frente a la laparoscópica.
Es importante valorar estos parámetros realizando reconstrucciones MPR,
que van a ayudar al cirujano a hacerse una mejor idea espacial de como es la tumoración y su relación respecto a los vasos y al resto de estructuras renales.
Complicaciones postquirúrgicas:
- C.
VASCULARES
- Infarto en nefrectomía parcial
- Sangrado activo
- C.
DEL SISTEMA EXCRETOR
- Fuga urinaria (urinoma)
- C.
INFECCIOSAS
- Abcesos/colecciones en la fosa renal o en la pared abdominal
- Pielonefritis
- C.
INTESTINALES
- Ileo paralítico/obstrucción
Hematoma postnefrectomía
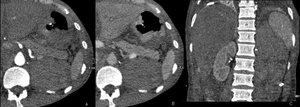
Fig. 27: Mismo caso de las figuras 16 y 20. Nefrectomía radical izquierda por carcinoma de células renales. A las 24h de la intervención, el paciente presenta cuadro de hipotensión y dolor abdominal. Se realiza angioTC de aorta abdominal.Imágenes obtenidas en el plano axial en la fase arterial (A) y venosa (B) y en el plano coronal (C). Se observa una masa hiperdensa y heterogénea en el lecho quirúrgico, compatible con hematoma de 6 x 7 x 13 cms de ejes AP, transverso y craneocaudal, sin evidencia de sangrado activo.
Urinoma
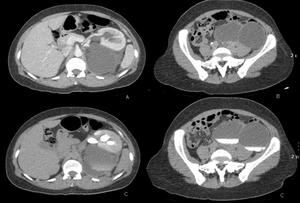
Fig. 28: A) y B) Imágenes en el plano axial de TC con contraste IV. Colección hipodensa retroperitoneal izquierda de 11 x 12 x 22 cms de ejes AP, transverso y craneocaudal respectivamente, que desplaza al riñón hacia delante y se extiende a la pelvis. El riñón presenta una adecuada captación de contraste. C) y D) Imágenes en el plano axial de TC en fase de eliminación de contraste (F. retardada) en la que se observa paso del contraste a la colección, por lo que se trata de un urinoma izquierdo.
Colecciones postquirúrgicas
La ausencia de aire en el interior de una colección no excluye el diagnóstico de abceso.
Por tanto si un paciente no evoluciona correctamente puede ser preciso drenar la colección o realizar PAAF para el análisis microbiológico.
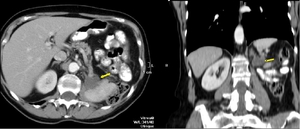
Fig. 29: Mismo caso de la fig 19. Tc realizado un mes después de nefrectomía izquierda. Lesión de 3 x 3 cms de ejes AP y transverso, de baja densidad en el lecho quirúrgico compatible con colección.
G.
TRATAMIENTOS ABLATIVOS: CRIOTERAPIA Y RADIOFRECUENCIA
Son técnicas relativamente recientes,
con buenos resultados en seguimiento a corto plazo,
demostrando ser eficaces y con mínimas complicaciones
Ventajas: Menor morbilidad,
tiempo postoperatorio,
estancia hospitalaria y coste.
Indicaciones:
- Tumores pequeños en pacientes con alto riesgo quirúrgico.
- RCC multicéntricos en pacientes con predisposición hereditaria.
- Monorrenos.
- Pacientes que rechazan cirugía.
- Mayores > 75 años.
RADIOFRECUENCIA.
Aplicación de corriente de alta energía en la lesión tumoral a través de un electrodo,
alcanzando una Tª > 60ºC para conseguir la muerte celular
COMPLICACIONES: Son raras.
La mas frecuente es el hematoma.
También están descritas: Lesión de vía urinaria,
quemadura de órganos adyacentes,
neumotórax y diseminación tumoral por el trayecto de la aguja (esta última es muy poco frecuente).
SEGUIMIENTO: TCMD control (sin y con contraste IV) a las 6 semanas y a los 6 meses durante 2 años.
Luego controles anuales.
Se considera ablación incompleta o recidiva si se objetiva un realce de 10 UH en la zona tratada.
Es frecuente observar la presencia de un halo graso encapsulado peritumoral (Signo del halo) por necrosis grasa o bien el borramiento de la grasa perirrenal.
Estos hallazgos no tienen significación patológica.