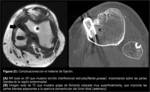
Las indicaciones de reconstrucción del LCP son: lesiones por avulsión ósea de la inserción del LCP,
lesiones agudas con laxitud significativa del LCP (grado 3+),
lesión combinada de múltiples ligamentos o laxitud crónica sintomática del LCP (1,
2,
4).
TÉCNICAS QUIRÚRGICAS
Las técnicas de reconstrucción del LCP han ganado mayor interés y se han desarrollado en los últimos años,
aunque no existe una técnica estándar y continúa siendo un tema controvertido (3,
5).
El objetivo de la cirugía es restaurar la función ligamentosa con un injerto que remede el ligamento nativo,
consiguiendo la isometría sin producir pinzamiento,
laxitud o sobretensionar la plastia (1,
6).
Se puede reparar en LCP de forma aislada o conjuntamente con otros ligamentos (LCA,
corner posteroexterno…) en las lesiones ligamentosas múltiples (3,
7).
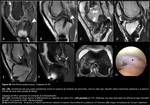
El LCP nativo consta de 2 fascículos,
anterolateral (AL) y posteromedial (PM),
aunque podría describirse como una continuidad de fibras que rotan durante el ciclo de flexoextensión de la rodilla (3).
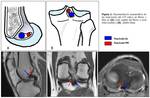
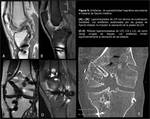
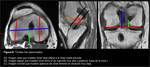
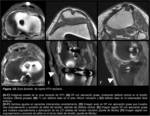
El conocimiento de los puntos de inserción del LCP nativo en fémur y tibia ayuda a posicionar los túneles en la reconstrucción del LCP (Fig. 1). Se acepta que el posicionamiento óptimo del injerto es el que se aproxime más al LCP nativo (6-8).
Varios estudios han demostrado que es más importante la posición del túnel femoral que la posición del túnel tibial,
cuya influencia sobre la laxitud de la plastia y el resultado clínico es menos clara (2,
5,
7,
8).
Las técnicas quirúrgicas varían según (3,
9,
10):
- La técnica de fijación tibial
- Uno o dos fascículos (y túneles) femorales
- El tipo de injerto tendinoso
- El material de fijación
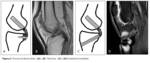
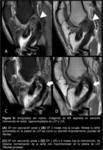
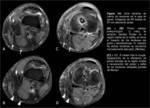
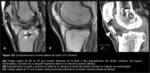
Hoy en día fundamentalmente se emplean 2 técnicas diferenciadas de fijación tibial (Fig. 2): la técnica de inlay tibial y la técnica de tunelización ósea transtibial.
En la técnica inlay de fjiación tibial directa el extremo de la plastia se fija directamente a la tibia (2,
6,
10).
Esta técnica debería evitar el desgaste del injerto que se produce en el denominado killer turn “giro de la muerte” (ver Fig. 17) que ocurre en las técnicas de tunelización transtibial a la salida del túnel,
aunque su superioridad no se ha demostrado (3,
9).
En la técnica de tunelización transtibial el túnel tibial se perfora desde anterior a posterior con visualización artroscópica de la inserción tibial del LCP nativo.
Tras tensionar adecuadamente el injerto y reducir el cajón posterior,
se fijan ambos extremos (2).
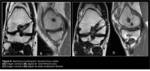
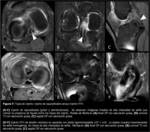
La elección de fascículo (y tunelización) femoral único o doble (Fig. 3) es controvertida.
La técnica con monotúnel femoral se ciñe a reconstruir el fascículo AL,
más potente,
pero se ha descrito que no limita la traslación posterior de la tibia en la flexión a 90º.
Hipotéticamente,
la técnica de doble tunelización con dos fascículos,
que se asemeja más al LCP nativo,
sería más eficaz en el control de la estabilidad posterior en todos los grados de flexión,
pero no hay consenso al respecto en la literatura,
y añade dificultad técnica (3,
5,
11).
En cuanto a la elección del tipo de injerto,
la técnica inlay se suele realizar con autoinjerto hueso-tendón rotuliano-hueso (HTH) o aloinjertos de distintas procedencias,
más frecuentemente tendón de Aquiles (1).
La técnica de tunelización transtibial suele realizarse empleando tendones de la pata de ganso (lo más habitual),
HTH o aloinjertos (1,
2,
10).
Los injertos HTH suelen ser de elección en atletas jóvenes,
ya que permiten la rápida reincorporación a la actividad física (1,
6).
La mayor desventaja de esta técnica es la frecuente aparición de complicaciones en la zona dadora (1).
El injerto tendinoso se obtiene del tercio central del tendón rotuliano junto con pequeños tapones óseos del polo inferior de la rótula y de la tuberosidad tibial anterior (1,
2,
6).
El uso de injerto de tendones isquiotibiales se ha extendido en los años recientes debido a la mejora de los sistemas de fijación (1).
Las ventajas de esta técnica incluyen la ausencia de complicaciones en la región anterior de la rodilla,
la pequeña incisión requerida en la zona donante y la regeneración de los tendones donantes hasta el 95% de su potencia prequirúrgica en un plazo de 3 años (1).
La desventaja es la posibilidad de expansión de túneles a largo plazo. Se obtienen fibras de 2 tendones,
generalmente grácil y semintendinoso,
extirpando fibras desde la inserción tibial hasta la unión miotendinosa,
obteniendo fibras largas que se pliegan sobre sí mismas y se suturan juntas,
resultando en un injerto compuesto de varios haces (1,
2).
Los tendones donantes quedan sin inserción distal (1).
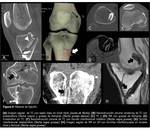
Existe una amplia gama de opciones y material de fijación (Fig. 4).
Se distinguen 2 categorías básicas de técnicas de fijación: fijación mediante bloqueo óseo y fijación de partes blandas.
El bloqueo óseo puede ser procedente de la zona dadora de injerto en los casos de HTH o ser un tapón obtenido del lecho óseo donde se realiza la tunelización transtibial.
Existen una gran variedad de dispositivos de fijación de partes blandas disponibles,
incluyendo grapas y tornillos metálicos,
cross-pins,
endobuttons y tornillos de material reabsorbible (1).
APARIENCIA POSTQUIRÚRGICA NORMAL
APARIENCIA POSTQUIRÚRGICA NORMAL DE LA PLASTIA DE LCP
La RM es la técnica de imagen que permite una valoración más global de la reconstrucción ligamentosa ya que permite la valoración del injerto ligamentoso,
los túneles y las potenciales complicaciones (8,
10,
12).
Los túneles y el estado del material de fijación pueden valorarse también mediante TC o incluso radiografías simples (RXS).
Los protocolos empleados de RM varían de unos centros a otros,
pero en general en una rodilla con una plastia ligamentosa conviene incluir una secuencia oblicua sagital que siga el trayecto de la plastia.
Según el tipo y la cantidad de material de fijación,
se producirán más o menos artefactos de susceptibilidad magnética (1) (Fig. 5).
En las reconstrucciones de LCP,
a diferencia de las ligamentoplastias de LCA,
los artefactos suelen dificultar más la valoración de la plastia debido a la localización más proximal de la fijación tibial,
sobre todo en la técnica inlay (1,
2).
A pesar de los artefactos se suele conseguir una valoración aceptable del trayecto intrarticular de la plastia (1,
2,
12) en las reconstrucciones aisladas de LCP,
aunque la valoración se complica cuando existe reconstrucción de múltiples ligamentos.
Dependiendo de la cantidad de artefactos de susceptibilidad magnética,
el empleo de secuencias con saturación grasa estará más o menos limitado.
En general,
las secuencias en eco de gradiente se desaconsejan por este motivo.
Hemos de valorar la apariencia del injerto ligamentoso,
la morfología y posición de los túneles y el estado del material de fijación.
INJERTO LIGAMENTOSO
La plastia ligamentosa en sí únicamente es valorable mediante RM,
si bien signos indirectos de su estado son valorables mediante otras técnicas.
La apariencia en RM de la plastia de LCP varía significativamente dependiendo del tipo de injerto empleado,
la técnica de fijación y el tiempo trascurrido desde la cirugía (1,
10).
La plastia se valora mejor en las secuencias potenciadas en T2 y la posición de túneles en las imágenes sagitales (1,
5).
La intensidad de señal en RM variará según la antigüedad del injerto,
es decir,
según el tiempo transcurrido desde la cirugía (1,
5,
10).
En los primeros 3-4 meses,
el injerto es avascular y muestra una señal similar a la del tendón donante,
hipointenso en todas las secuencias (1).
La mayoría de autores sostiene que en los 4-8 meses tras la intervención,
el injerto tendinoso sufre una remodelación y resinovialización,
proceso denominado ligamentización,
ya que se transforma morfológica e histológicamente en un tejido similar al LCP nativo (1,
2,
4,
10).
Durante la ligamentización puede aparecer un aumento de señal difuso o segmentario en secuencias T2 que no debe confundirse con una rotura.
La señal siempre debe ser menor que la del líquido (1),
y debe visualizarse continuidad de las fibras.
A partir de 1-2 años tras la cirugía el aspecto de la plastia debería ser similar al LCP nativo,
hipointenso en todas las secuencias (1,
2,
4,
10) (Fig. 6).
No obstante,
en los injertos de tendones isquiotibiales,
debido a la configuración interna en haces descrita previamente,
existe una diferencia notable con los injertos de HTH: pueden apreciarse imágenes lineales longitudinales de señal intermedia interpuestas entre los haces empleados para formar el injerto,
o incluso de alta intensidad de señal si se introduce líquido entre los haces,
constituyendo un hallazgo normal que sería claramente patológico en un injerto HTH formado por un único haz (Fig. 7) (1,
2,
4).
Las pequeñas colecciones laminares suelen reabsorberse en el primer o segundo año tras la cirugía y deben distinguirse de un ganglión (1).
La artrofibrosis es un hallazgo muy frecuente en las reconstrucciones de LCP,
mucho más que en las ligamentoplastias de LCA.
Incluso se cree que puede mejorar la estabilidad de la rodilla tras la reconstrucción por lo que cierto grado de artrofibrosis podría considerarse un hallazgo normal,
siempre que no limite la movilidad (1,
2,
13).
(ver Fig. 18)
TÚNELES
En contraste con las ligamentoplastias de LCA,
existen escasos estudios sobre la posición de túneles en las reconstrucciones de LCP (1,
2,
8).
La posición de los túneles puede evaluarse mediante distintas técnicas de imagen.La RXSquizá sea la más accesible,
pero la interpretación es más variable (6-8).La TCyla RMpermiten una valoración más precisa de los túneles,
aunque quizála TCofrezca la visión más exacta de los túneles óseos (5,
7,
8).
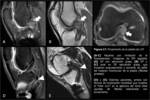
Mariani et al.
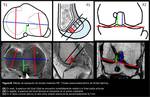
(8) publicaron un método de evaluación de túneles mediante RM (Fig. 8 y Fig. 9) para las técnicas de túnel femoral único.
Se emplean imágenes en axial,
sagital y coronal oblicuo.
La imagen axial,
obtenida a la altura del platillo tibial,
determina el punto T1 o punto de inserción tibial del LCP.
Se trazan líneas en los diámetros máximos AP de ambos platillos tibiales (interno y externo).
Se une el punto medio de cada línea creando otra línea.
Una perpendicular en el centro de esta línea indica la línea media articular.
El punto de inserción ideal se encuentra en ese punto o mínimamente medial al mismo.
La imagen sagital a nivel del punto de inserción femoral del LCP,
determina el punto F1,
punto de indica posición profunda o superficial de la inserción femoral del LCP.
Se divide la línea de Blumensaat en 4 partes I-IV.
La zona 1 es la posición óptima para la fijación y está menos asociada a laxitud posterior de la rodilla.
La imagen coronal oblicua,
perpendicular a la línea de Blumensaat,
determina el punto F2,
punto de inserción femoral en coronal del LCP.
Indica la altura baja o alta en la pared medial del intercóndilo.
Se realiza un ratio entre dos distancias a una línea que conecta las superficies articulares de ambos cóndilos,
desde el techo del intercóndilo y desde el centro de la inserción del LCP en el CFI.
Se debe colocar a aproximadamente 8,5 mm.
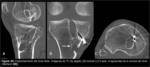
Gancel et al.
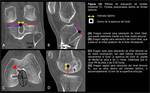
(7) describieron un método de valoración de túneles mediante TC (Fig. 10 y Fig. 11),
también para técnica monotúnel.
El punto de inserción tibial se mide en los planos coronal y sagital.
En el plano coronal se traza una línea que recorre el diámetro mediolateral completo del platillo tibial,
marcando un intervalo de 5 mm centrado en un punto a 48% desde el borde medial.
Se traza una línea desde el borde medial del platillo tibial hasta el punto medio de la apertura del túnel tibial,
que debe recaer en el intervalo marcado.
En el plano sagital se traza una línea siguiendo la superficie retroespinal,
marcando un intervalo de 5 mm en la mitad posterior.
Se traza otra línea desde el extremos posterior de la espina tibial hasta la apertura del túnel,
que debe recaer en el intervalo marcado.
El punto de inserción femoral se valora en los planos sagital y axial.
En la imagen sagital a nivel de CFI se mide la distancia desde el centro del túnel hasta la superficie articular,
que debe encontrarse en torno a 10 ± 2,5 mm.
En el plano axial,
se dibuja una cara de reloj en el intercóndilo con las 3 hrs y 9 hrs fijadas en la base del intercóndilo y eje paralelo al borde posterior del cóndilo.
Se considera adecuada una posición del túnel entre las 10:30 - 11:30 hrs para la rodilla izquierda y de 12:30-1:30 para la rodilla derecha.
Unificando ambos criterios y de acuerdo con otros trabajos publicados,
podemos simplificar la localización de los túneles de la siguiente manera: La localización del punto óptimo de la apertura articular del túnel femoral dependerá de si se trata de una técnica monotúnel o de doble túnel.
En la técnica monotúnel se sitúara la apertura próxima a la inserción femoral del fascículo AL,
en la mitad anterior de la inserción del LCP nativo a las 11 hrs o 1 hrs,
según sea la rodilla izquierda o derecha respectivamente,
y a unos 8-10 mm del margen articular (2,
5-7).
En las reconstrucciones con doble túnel femoral,
los puntos de apertura articular se deben colocar uno en el tercio anterior de la inserción de LCP nativo y otro en el tercio medio-distal de dicha inserción,
a la 1 y las 3 horas (rodilla derecha) y a las 11 y 9 horas (rodilla izquierda) (5,
11).
El punto de fijación tibial en ambas técnicas (inlay y tunelización transtibial) se sitúara en el centro de la mitad posterior de la superficie retroespinal,
inmediatamente medial a la línea media de la articulación,
8-15 mm distal a la superficie articular (2,
3, 6-8).
En general,
se permite una pequeña variabilidad en la posición de los túneles y no está claro qué grado de precisión se requiere para evitar rotura,
laxitud o pinzamiento (2,
3,
7,
8).
Se considera que un túnel está mal posicionado cuando 75% o más de la anchura de la apertura articular se sitúa fuera del punto isométrico (5).
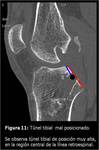
Los errores más habituales en la ubicación de los túneles suelen ser un túnel femoral de localización muy posterior y un túnel tibial de posición muy proximal,
que determina in injerto de posición muy vertical con capacidad limitada para resistir la traslación tibial posterior (5).
Debe valorarse la conservación del eje fémorotibial en las imágenes sagitales.
(ver Fig. 15 y Fig. 16)
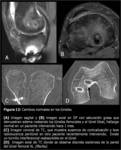
En el periodo postquirúrgico temprano y hasta 12 meses tras la intervención,
puede persistir edema óseo en grado variable alrededor de los túneles (1).
También puede aparecer una leve radiolucencia alrededor del injerto previa a su incorporación (6).
Con el tiempo,
no es infrecuente apreciar esclerosis de los túneles (6).
(Fig. 12)
FIJACIÓN:
Los dispositivos metálicos producen artefactos significativos que persisten indefinidamente,
mientras que los materiales reabsorbibles producen menos artefactos que tienden a disminuir con el tiempo,
permitiendo una mejor valoración de la plastia y los túneles óseos (1,
12).
(ver Fig. 4 y Fig. 7). También en las zonas de fijación puede existir un grado variable de edema óseo en el periodo postquirúrgico temprano (1).
APARIENCIA POSTQUIRÚRGICA NORMAL DE LAS ZONAS DONANTES
En la técnica HTH (Fig. 13) observaremos un defecto de aproximadamente5 mm de ancho en la zona central del tendón rotuliano y pequeños defectos óseos en el polo inferior de la rótula y en la tuberosidad tibial anterior.
Habitualmente el defecto se rellena en los primeros 2 años tras la cirugía,
por un tejido que en RM es indistinguible del tendón nativo,
es decir,
hipointenso en todas las secuencias.
Inicialmente,
el tendón rotuliano estará engrosado y mostrará señal aumentada en secuencias T1 y T2.
Si el engrosamiento > 10 mm o persiste la hiperseñal,
debe considerarse que existe tendinopatía rotuliana (1).
En los injertos a partir de tendones isquiotibiales (Fig. 14),
durante el primer mes es habitual visualizar láminas fluidas en las zonas dadoras siguiendo la teórica localización de los tendones empleados.
En estas zonas,
durante los siguientes 6-12 meses,
irán apareciendo signos de regeneración tendinosa,
con aspecto engrosado persistente,
hasta 1-2 cm de la inserción tibial,
que no suele llegar a recuperarse y mantendrá mal definida y con aumento de la señal.
A partir del primer año es difícil detectar los cambios postquirúrgicos en la zona dadora,
salvo a nivel de la inserción tibial de los tendones,
ni suele existir atrofia de los músculos correspondientes (1).
COMPLICACIONES
COMPLICACIONES DE LA PLASTIA DE LCP:
Pueden ocurrir diversas complicaciones tras la reconstrucción del LCP,
y las técnicas de imagen juegan un papel fundamental en la evaluación de pacientes sintomáticos tras la cirugía.
Distinguimos distintas complicaciones según la clínica:
- Rodilla inestable: pensaremos en fracaso del injerto por rotura o laxitud de la plastia.
- Limitación de la flexoextensión de la rodilla: puede ser secundaria a pinzamiento de la plastia,
artrofibrosis o presencia de cuerpos libres intraarticulares (1,
12).
- Dolor persistente,
que puede deberse a múltiples causas.
ROTURA DELA PLASTIA DE LCP
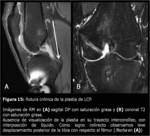
La rotura de la plastia de LCP (Fig. 15) puede ocurrir en cualquier momento tras la reconstrucción,
si bien el injerto es más vulnerable durante el periodo de ligamentización (1,
10).
Teóricamente,
el injerto se equipara al LCP nativo a partir del primer año postquirúrgico (1).
La rotura puede ser secundaria a nuevo traumatismo o ser el resultado de un pinzamiento crónico.
La ausencia de visualización de la plastia o la presencia de una solución de continuidad de espesor completo en las fibras con interposición de señal fluido son los signos más específicos de rotura de la plastia (1,
2,
10).
Se debe considerar el tiempo de evolución postquirúrgico,
recordando que el aumento de la señal en secuencias T2 es un hallazgo normal en la fase de ligamentización.
Un signo indirecto de rotura es el desplazamiento posterior de la tibia con respecto al fémur,
que equivale al signo del cajón posterior (1,
7,
10).
LAXITUD DEL INJERTO LIGAMENTOSO
Se debe considerar posible laxitud de la plastia de LCP (Fig. 16) si existe inestabilidad de rodilla y visualizamos integridad de las fibras del injerto enla RM.
Se puede apreciar acodamiento o abombamiento de la plastia.
La laxitud de la plastia se ha relacionado más con los injertos de isquiotibiales.
En la mayoría de los casos,
se requiere reintervención quirúrgica para recobrar la estabilidad,
que puede realizarse mediante retensado de la plastia (térmico o por radiofrecuencia)o mediante nueva reconstrucción (1).
Es importante diferenciar la laxitud de la plastia de una rotura si se considera la opción de retensado.
PINZAMIENTO DELA PLASTIA
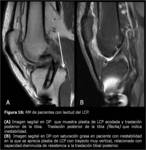
El pinzamiento de la plastia de LCP (Fig. 17) es una complicación trascendente,
ya que suele presentarse con limitación de la flexoextensión,
pero puede derivar en rotura del injerto.
Una localización errónea de los túneles o el killer turn en las plastias con tunelización transtibial,
deriva en una posición forzada de la plastia,ocurriendo roce con las estructuras óseas que deriva en desflecamiento,
fibrosis,
rotura de los haces del injerto y ulterior rotura completa (1).
En RM,
podemos observar engrosamiento y aumento de señal en secuencias T1 y T2 del trayecto intrarticular de la plastia (1,
10).
No debemos confundirlo con el aumento de señal normal puede durante el periodo de ligamentización,
que debe resolverse.
En los casos de pinzamiento la señal aumentada no se resuelve,
sino que persistirá o empeorará con el tiempo (1,
10).
Otro signo es el acodamiento de la plastia en las aperturas articulares de los túneles (1).
ARTROFIBROSIS
La artrofibrosis puede producir dolor y limitación a la flexoextensión de la rodilla,
sin embargo como se ha mencionado previamente,
en las reconstrucciones de LCP un leve grado de artrofibrosis puede considerarse un hallazgo normal (1,
2,
13).
Existen 2 formas de artrofibrosis (Fig. 18),
la forma focal y la forma difusa (1).
La artrofibrosis focal se conoce también como lesión cíclope por su apariencia artroscópica.
Consiste en un nódulo de tejido fibroso,
que suele localizarse rodeando la plastia de LCP o en la grasa de Hoffa (1,
2),
y se delimita mejor en las imágenes sagitales.
Debido a su composición,
suele aparecer hipointenso en todas las secuencias aunque puede presentar en señal variable en T2 (1,
2,
10).
La forma difusa se presenta generalmente como una masa espiculada mal definida de baja intensidad de señal (1).
La artrofibrosis sintomática requiere resección artroscópica (1,
10).
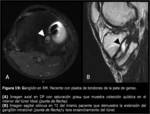
FORMACIÓN DE GANGLIONES
La formación de un ganglión quístico (Fig. 19) puede derivar de la degeneración o rotura parcial de la plastia (1,
10).
Se han relacionado más frecuentemente con las plastias de tendones isquiotibiales y aloinjertos (1,
5).
Existen controversias en cuanto a su relación con el fracaso de la plastia (1,
10).
Generalmente,
los quistes se forman en el interior del túnel tibial,
y a medida que van creciendo,
pueden protruir proximalmente en la articulación o hacia las partes blandas distales adyacentes a la apertura extraarticular del túnel (1).
Se asocian con ensanchamiento de los túneles (10).
Pueden ser asintomáticos o producir dolor,
limitación de la flexoextensión o masa palpable (1).
En el TC se observan como una masa de densidad líquido,
o con ensanchamiento de los túneles con remodelado de las paredes o pérdida de definición de la cortical.
Enla RMse muestran como estructuras quísticas lobuladas de señal líquido (1).
Se deben diferenciar de las pequeñas colecciones laminares intratúnel normales descritas previamente en los injerto de isquiotibiales.
ENSANCHAMIENTO DE LOS TÚNELES
El ensanchamiento de los túneles (Fig. 20) se puede ocasionar por incorporación incompleta de la plastia en el túnel o por el efecto de un ganglión (10).
Se considera significativo si existe un aumento de más del 50 % en el área del túnel (5).
Si es significativo,
puede producir un movimiento del injerto en el interior del túnel denominado “efecto limpiaparabrisas” (10),
que no suele tener consecuencias significativas.
COMPLICACIONES RELACIONADAS CON EL MATERIAL DE FIJACIÓN.
El material de fijación puede movilizarse o romperse (Fig. 21) (6).
Ambas complicaciones se valoran mejor en RXS o TC.
Si el material impronta las partes blandas periarticulares,
puede producir dolor,
cambios inflamatorios,
formación de colecciones,
etc… En el caso del material reabsorbible,
la sinovitis reactiva en los primeros meses no es un hallazgo inusual.
COMPLICACIONES EN LAS ZONAS DONANTES:
Las complicaciones en las zonas donantes son más frecuentes en la técnica HTH (Fig. 22) (1,
10).
En esta técnica,
las potenciales complicaciones son dolor en la región anterior de la rodilla y degeneración del tendón rotuliano,
frecuentes,
y la patela baja residual,
rotura del tendón rotuliano y fractura rotuliana infrecuentes (1,
6,
10).
La tendinosis rotuliana es un hallazgo se manifiesta en RM con engrosamiento y aumento de señal del tendón,
que no debe confundirse con los hallazgos postquirúrgicos normales (10).
En la zona donante de tendones isquiotibiales,
puede existir pérdida de fuerza o dolor persistente.
La atrofia muscular es poco frecuente.
La rotura del tendón nativo,
generalmente por sobretoma de injerto,
es excepcional (1,
14).
OTRAS COMPLICACIONES
El éxito de la técnica depende en gran medida del posicionamiento de los túneles,
pero existen otros factores que pueden contribuir al fracaso de la reconstrucción.
La deficiencia no corregida de otros ligamentos como el LCA o las estructuras del corner posterolateral producirían inestabilidad que derivaría en el fracaso de la reconstrucción y progresión de los cambios osteoartrósicos (5).
Una alineación en varo también puede contribuir al fracaso de la plastia (5).
La presencia de cuerpos libre articulares por lesión condral o fragmentos meniscales puede limitar también la flexoextensión de la rodilla y producir bloqueos.
Obviamente,
la reconstrucción del LCP se puede complicar también con complicaciones genéricas propias de cualquier cirugía articular (6): sinovitis reactiva,
artritis séptica,
trombosis venosa profunda,
etc… que no son el objeto de este trabajo.