Se seleccionaron 31 pacientes cirróticos con CHC tratados con RFA como primer tratamiento durante el periodo comprendido entre el 3- diciembre de 2007 y el 19 de diciembre de 2011.
Se excluyeron aquellos pacientes tratados con RFA en combinación con otras técnicas como inyección percutánea de etanol,
resección quirúrgica o quimioembolización (TACE).
En total,
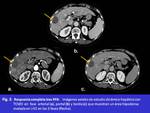
se estudiaron 36 nódulos con un tamaño medio de 21.7 mm (18.8-24.5 IC 95%)( Fig. 1 ).
De los 31 pacientes,
23 eran hombres,
con una media de edad de 68 años,
un estadio Child-Pugh A 5 (29% alcohol,
42% hepatitis C,
29% otros) y un valor medio de AFP de 6.7 ng/ml (rango 2.9-26).
Del total de pacientes,
13 tenían un nódulo ≤ 20mm (BCLC-0,
42%) 13 un nódulo > 20mm y 5 pacientes,
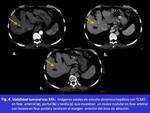
dos nódulos.( Fig. 2 ).
El diagnostico se realizó mediante programa de cribado en 24 pacientes.
En 5 casos fue necesario realizar estudio histológico para confirmar el diagnóstico de CHC ya que los nódulos presentaban un patrón de realce atípico en los estudios de imagen.
En total,
se realizaron 37 sesiones de RFA,
34 vía percutánea.
Se realizó un seguimiento prospectivo: un estudio inicial mediante un TCMD al mes del procedimiento para comprobar la ablación completa del nódulo y posteriormente,
seguimientos mediante TCMD o RM cada 4 meses.
Para valorar la respuesta al tratamiento se utilizaron los criterios mRECIST (JM Llovet,et al,
J Natl Cancer Inst 2008).
Todos los casos fueron valorados por un equipo multidisciplinar compuesto por Cirujanos,
Radiólogos y Hepatólogos.
Los procedimientos percutáneos fueron realizados por Radiólogos previa sedación y analgesia y los casos de RFA vía laparoscópica por Cirujanos y Radiólogos bajo anestesia general.
Los pacientes se colocaron en decúbito supino o lateral,
dependiendo de la localización de la lesión y de la posición óptima para la introducción de la aguja.
Previa inyección de anestesia local con lidocaína al 1% a lo largo del trayecto del electrodo desde la piel hasta el peritoneo,
se realiza una pequeña incisión cutánea y se introduce la aguja del electrodo bajo control ecográfico.
Se utilizó un generador de 480 kHz,
con una potencia máxima de 200 W (CC1; Radionics,
Burlington,
Mass) a través de una ajuga 16G monopolar con una punta activa de 3 cm guiada por ecografía con una sonda de 3.5 a 5 mHz.
Una vez colocada la punta de la aguja dentro de la lesión,
se activó el generador de radiofrecuencia a la potencia necesaria para alcanzar una temperatura mínima de 60º.
La duración media de cada sesión fue de 10 minutos.
Cada ablación produce una lesión térmica de aproximadamente 3 cm.
Los nódulos de menos de 3 cm fueron tratados con una o dos ablaciones.
Los nódulos de mayor tamaño,
se trataron con varias ablaciones,
reposicionando la ajuga en diferentes partes del tumor. El tratamiento se consideró satisfactorio cuando se observaba un área hiperecogenica en la localización inicial del tumor.
Después del procedimiento,
los pacientes permanecieron en observación durante 24 horas,
realizándose controles de función hepática y hemograma.
En todos los controles realizados al mes de la RFA y en la mayoría de los seguimientos posteriores,
se llevó a cabo estudio dinámico trifásico hepático mediante TCMD 64 (Toshiba Aquilion),
después de la inyección de 125ml de contraste no iónico ( Ioversol,
Optiray Ultrayet® 320 mg/ml) a un flujo de 4ml/s.
Los parámetros técnicos fueron: voltaje del tubo de 120kV,
intensidad de 180-400 mA con modulación de dosis,
grosor de corte de 1mm,
intervalo 0,5mm.
El estudio dinámico hepático consistió en la realización de tres fases,
de acuerdo con el protocolo estándar de nuestro hospital: arterial,
portal y de equilibrio (a los 25-28seg,
70 seg y 240 seg aproximadamente tras el inicio de la inyección del contraste).
En un pequeño porcentaje de pacientes,
los seguimientos se realizaron mediante estudio de RM con un equipo de 1.5-T (Signa LX; GE Medical Systems).
Todas las imágenes fueron adquiridas con una antena de cuerpo multicanal.
El protocolo de imagen incluyó secuencias ponderadas en T1 y T2 y estudio dinámico con supresión grasa en varias fases antes y después de la administración de contraste.
Se adquirieron imágenes en fase arterial,
venosa portal,
tardía y fase hepatobiliar a los 20,
60,
120 y 20 minutos respectivamente después de la inyección de Gd-BT-DO3A (Gadovist®,
Bayer Schering Pharma AG) 1 mmol/ml.
0,1ml/kg,
a un flujo de 1ml/seg.
Todos los pacientes tenían estudio de imagen con TCMD o RM previo al procedimiento de RFA.
Las imágenes fueron analizadas independientemente por dos radiólogos en una estación de trabajo Toshiba (Vitrea® 2 versión 4.1.2.0) con ajuste óptimo de ventana en cada caso,
en cortes axiales y reconstrucciones multiplanares mediante MIP (Maximum Intensity Projection) y VR (Volume Rendering).
Las variables evaluadas fueron:
- patrón de realce de los nódulos tras la RFA
- hiperemia reactiva
- hematoma intralesional
- presencia de burbujas de aire dentro de la lesión tras RFA
- tamaño de los nódulos tratados (diámetro mayor)
- volumen del área de RFA
El patrón de realce fue clasificado:
- Un área de baja densidad que no realza tras la administración de contraste en las tres fases del estudio dinámico,
se consideró tejido necrótico y por lo tanto,
compatible con respuesta completa (Fig. 3).
- Un área de realce en fase arterial: de tipo nodular,
cuando se observaba un área focal de realce en el margen interno o externo de la lesión tratada (Fig. 4 ) o tipo halo,
cuando el área de realce presenta una morfología en semiluna en el margen externo de la lesión tratada.
Todos los focos de realce en fase arterial (nodulares o en semiluna) con lavado en fase portal e hipodensos en fase de equilibrio,
representan viabilidad tumoral.
Las áreas de realce que no presentaban este patrón,
se consideraron tumor viable cuando se observaba un aumento progresivo de tamaño en los estudios de seguimiento.
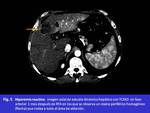
Hiperemia reactiva: definida como un realce periférico anular, de grosor fino y homogéneo que rodea a la lesión tratada,
en fase arterial de los estudios TCMD y RM.
Generalmente es isodenso en fases tardías aunque puede observarse un realce persistente en esta fase en estudios de RM.
( Fig. 5).
Hematoma intralesional: área central hiperdensa en la lesión tratada y en el trayecto de la aguja de radiofrecuencia ( Fig. 6 ).
Volumen del área tras RFA,
evaluada en cada estudio de seguimiento con TCMD o RM.
Se evaluó en la fase portal, utilizando inicialmente una herramienta de medida del área en cada corte y posteriormente una técnica de sumación de dichas áreas.
Las variables continuas se analizaron utilizando medias y desviaciones típicas.
Las variables nominales se describieron mediante frecuencias absolutas y relativas.
Para valorar la relación entre variables nominales se utilizó el test de Fisher.
La diferencia se consideró significativa cuando p<0.05.