CIRUGIA DE CITORREDUCCIÓN ( DEBULKING)
El tratamiento de elección del cáncer de ovario es la citorreducción quirúrgica primaria seguida de quimioterapia.
Sin embargo sólo se ha demostrado que este tratamiento aumente la supervivencia si se logra lo que se denomina una resección óptima (1),
que consiste en lograr una resección completa sin evidencia de tumor macroscópico,
o que este sea inferior a 1 cm de diámetro.
Las tasas de obtención de citorreducción óptima varían entre las instituciones.
Los resultados dependen de la experiencia del equipo quirúrgico,
la técnica,
esfuerzo,
protocolo y política institucional. Se estima que cirujanos expertos consiguen citorreducciones optimas en al menos el 75% de los casos (1),
siendo menor este porcentaje con ginecólogos no especialistas en cirugía oncológica.
Los procedimientos quirúrgicos que se realizan en la citorreducción incluyen la disección pélvica radical,
omentectomía,
resección intestinal,
raspado diafragmático y/o resección hepática y esplenectomía .
En la práctica clínica habitual,
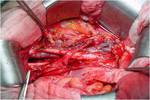
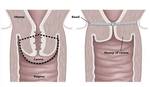
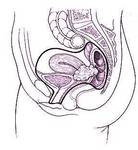
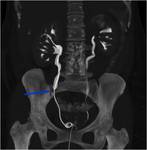
de inicio se realiza una estadificación quirúrgica completa,
donde se realizan biopsias aleatorias o dirigidas a las áreas sospechosas para demostrar el origen tumoral.
Una vez diagnosticada,
en el mismo acto quirúrgico se estima la posibilidad de alcanzar una citorreducción óptima,
y si ésta no es posible,
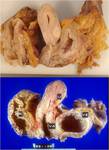
se resecan los ovarios,
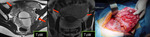
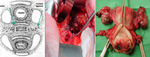
y el omento para comprobar el origen del tumor (1) Fig. 4
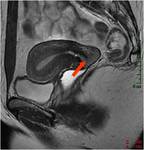
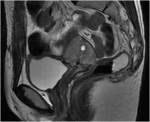
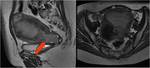
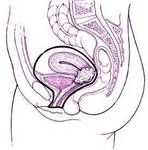
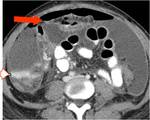
Omentectomía:
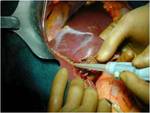
La omentectomía se realiza de forma sistemática en todas las pacientes intervenidas con fines diagnósticos o terapéuticos.
La resección del omento fundamentalmente cuando está invadido por múltiples metástasis (omental cake) se realiza siempre aunque no se vaya a obtener una reducción óptima con el fin de disminuir la masa tumoral y evitar la formación de ascitis postoperatoria Fig. 5
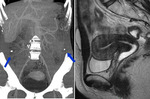
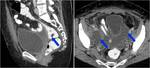
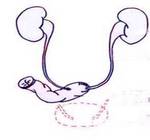
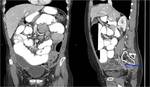
Resección intestinal:
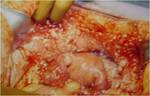
La resección intestinal se reserva para cirugías extensas con intención curativa o en casos de obstrucción intestinal .El rectosigma y el fondo de saco de Douglas suele ser un santuario tumoral,
foco de múltiples recurrencias ,
siendo prácticamente obligatoria la resección en cirugía citorreductor con fines curativos .Lo más habitual en estos casos es la realización de una exenteración posterior modificada, que consiste en resección en bloque del peritoneo pélvico,
útero,
ovarios y rectosigma Fig. 6
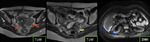
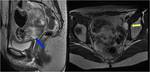
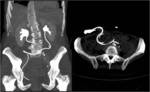
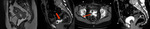
Linfadenectomía :
La toma de biopsias de adenopatías pélvicas y paraaórticas debe de realizarse incluso en enfermedad en estadio precoz Fig. 7 Fig. 7 Fig. 8 .Existe controversia en cuanto a la realización de linfadenectomía sistemática pélvica y paraaórtica versus la resección dirigida a las adenopatías en rango patológico.
Dos ensayos randomizados respecto a este asunto no mostraron aumento significativo de la supervivencia con linfadenectomía sistemática ,
aunque sí mayor morbilidad (1).
Esplenectomía:
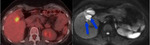
La esplenectomía está justificada en el caso de afectación del hilio esplénico Fig. 9
Enfermedad diafragmática y hepática.
Al contrario de lo que se pueda pensar,
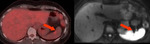
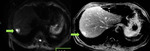
las metástasis parenquimatosas hepáticas ( estadio IV) no son necesariamente una contraindicación para la obtención de citorreducción optima Fig. 10 Fig. 11 pudiéndose realizar metastasectomía o hepatectomía parcial en casos seleccionados.
La cirugía reductora agresiva incluye la resección de la enfermedad diafragmática.
Normalmente la enfermedad diafragmática puede ser tratada mediante rapado de la superficie peritoneal,
si bien en casos avanzados el hígado puede ser parcialmente retraído,
el ligamento hepático dividido ,
con resección de la porción del diafragma membranoso afectado usando disección por ultrasonidos,
electro cauterización o laser de argón.
La principal complicación es la apertura a la cavidad pleural que se trata mediante toracocentesis con tubo de tórax.
PAPEL PREQUIRUGICO DE LA IMAGEN
Como se puede deducir,
las técnicas de imagen permiten predecir la posibilidad de cirugía óptima.
Además hay varios ensayos que demuestran que en casos seleccionados de cáncer de ovario avanzado,
el tratamiento con quimioterapia neo adyuvante seguido de citorreducción de intervalo muestra igual o incluso mejor pronóstico (1) .Esta opción además de permitir una posibilidad curativa a estas paciente,
tiene como otra ventaja potencial evitar una cirugía agresiva en mujeres con enfermedad quimio-resistente con mal pronóstico independientemente del tratamiento.
En la práctica clínica,
la citorreducción de intervalo se reserva para pacientes con enfermedad muy extensa no resecable al diagnóstico.
Especialmente en estos casos es cuando el papel de la imagen del juega una papel fundamental para la predicción de citorreducción subóptima (2).
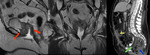
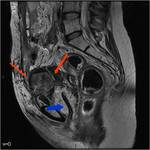
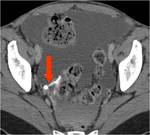
Los criterios de imagen que indican irresecabilidad de inicio son:
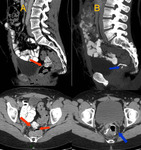
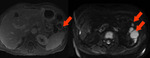
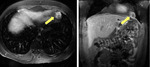
- Ascitis de gran volumen (> 1000 ml) Fig. 12
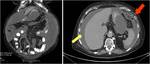
- Afectación mesentérica extensa Fig. 13
- Masa bulky en abdomen superior (>1 cm - 2 cm) Fig. 14
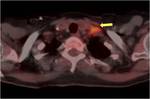
- Enfermedad extra abdominal Fig. 15
- Adenopatías suprarrenales.
- Extensa enfermedad parenquimatosa hepática o diafragmática.
PAPEL POSTQUIRUGICO DE LA IMAGEN
Como se ha comentado previamente,
la experiencia clínica y la agresividad quirúrgicas son los principales determinantes para una resección quirúrgica optima.
Sin embargo,
la valoración postoperatoria de la enfermedad residual no resecada es realizada por el cirujano,
presentado un alto componente sugestivo (1).
Para evitar este sesgo,
ensayos clínicos prospectivos suelen requerir un estudio de imagen postquirúrgico (RM o CT) antes de iniciar la quimioterapia; si bien en este campo aún no se ha validado la exactitud de la imagen .
Posibles causas que justificarían la mala correlación entre la estimación del cirujano de la enfermedad residual y la imagen postquirúrgica podrían deberse a la subvaloración subjetiva de la enfermedad residual,
el rápido de crecimiento del tumor tras la cirugía,
o cambios y complicaciones postquirúrgicas.
Las pacientes con cáncer de ovario tratado suelen ser seguidas mediante mediciones periódicas de CA-125 y pruebas de imagen ( CT,
RM).
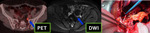
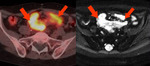
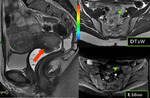
La incorporación de técnicas de imagen funcional (PET- TAC y DWI) han permitido el abandono de la laparotomía de second-look ,
diagnosticando recurrencias que miden5 mm o menos (3) Fig. 16 ,si bien aún no ha sido adecuadamente establecida la importancia clínica del diagnostico de enfermedad microscópica.
De forma similar al tumor primario,
la mayoría de la recurrencias de cáncer de ovario son intraabdominales y potencialmente subsidiarias de citorreducción secundaria. Sin embargo el beneficio de la citorreducción secundaria es aún poco claro debido a la ausencia de ensayos randomizados.
Basándose en los datos actuales,
se considera la realización de citorreducción secundaria en (4):
- Progresión libre de enfermedad de al menos 12 meses.
- Respuesta a la primera línea de terapia.
- Buen estado clínico.
- Enfermedad recurrente local.
- Enfermedad extensa subsidiaria de citorreducción óptima
Al igual que con el tratamiento primario,
el principal factor pronóstico es el tratamiento óptimo.
La supervivencia de pacientes con cáncer de ovario recurrente tratados con citorreducción secundaria optima es de 16 a 61 meses (versus de 8 a 27 meses cuando la citorredccuíon secundaria es subóptima)(4)
HISTERECTOMÍA.
La histerectomía es la intervención quirúrgica ginecológica más realizada.
Histerectomía radical se refiere a escisión del útero en bloque con parametrios (ligamentos redondo,
ancho,
cardinal y útero sacros) y del tercio superior de la vagina (5) Fig. 17 .Asocia normalmente linfadenectomía pélvica.
La resección de los ovarios es opcional,
preservándolos si se considera clínicamente apropiado.
INDICACIONES.
La histerectomía radical se realiza como tratamiento primario para (5):
- cáncer de cérvix estadio IB o IIA Fig. 18
- pacientes seleccionados con adenocarcinoma de endometrio estadio II Fig. 24 Fig. 25
- carcinoma de la vagina superior,
sarcomas uterinos o cervicales y canceres poco frecuentes confinados al área de cérvix,
útero o vagina superior.
- Como opción de tratamiento curativo a la exenteración en mujeres con cáncer de cérvix con recurrencia central previamente tratadas con radioterapia.
HISTERECTOMÍA EN EL CÁNCER DE CÉRVIX.
La indicación más frecuente de histerectomía radical y linfadenectomía pélvica es el cáncer de cérvix en estadio precoz (FIGO IB o IIA sin invasión parametrial Fig. 18 Fig. 19 .
La cirugía está contraindicada si el tumor invade el parametrio (IIB) o se extiende a la pared pélvica,
al tercio inferior de la vagina,
recto o vejiga.
En estos casos el tratamiento de elección es la radioterapia.
Las tasas de supervivencia a 5 años y el intervalo libre de enfermedad son similares con ambos tratamientos (83% del tratamiento quirúrgico primario versus 74% de la radioterapia) (5).
La presencia de enfermedad metastásica en ganglios linfáticos (15% de las mujeres en estadio IB y en el 25% de las pacientes con un estadio IIA) disminuye la supervivencia (5).
En estos casos se opta por tratamiento de elección con radioterapia Fig. 20 Fig. 21
TRAQUELECTOMÍA
La traquelectomía se define como una resección quirúrgica del cérvix y parametrio,
manteniendo el cuerpo uterino (6,7) .
La traquelectomía radical con linfadenectomía pélvica se trata de un tratamiento quirúrgico conservador pero radical y curativo del carcinoma de cérvix en estadio precoz (estadio IB1 o inferior),
que combina una cirugía local radical con conservación de la fertilidad en mujeres jóvenes( aproximadamente el 30% de las mujeres con cáncer de cérvix son menores de 35 años).
La traquelectomía radical muestra una menor mortalidad y morbilidad,
con tasas similares de curación que la histerectomía tradicional radical.
El procedimiento quirúrgico Fig. 22 Fig. 23 consiste en la resección del cérvix y bóveda vaginal.
El cuerpo uterino restante se anastomosa al remanente vaginal mediante una sutura de cerclaje que se coloca alrededor del cuerpo uterino.
Esta sutura mantiene la competencia del útero para posteriores embarazos.
EXENTERACIÓN PELVICA
Procedimiento quirúrgico ultraradical que consiste en la resección en bloque de estructuras pélvicas incluido el útero,
cérvix,
vagina,
vejiga y recto,
en un mayor o menor grado (8) Fig. 26
En siempre un procedimiento curativo,
ofrecido como última opción quirúrgica en pacientes con cáncer uterino,
vulvar o vaginal recurrente.
Las indicaciones son muy seleccionadas,
tratándose de tumores ginecológicos recurrentes en localización central con ausencia de diseminación linfática,
peritoneal o a distancia.
Los cánceres de ovario o de endometrio no suelen ser candidatos a la exenteración pélvica debido a su alta tendencia a la diseminación peritoneal más allá de la pelvis.
La mayoría de las indicaciones de exenteración son pacientes diagnosticadas de cáncer de cérvix con recurrencia central previamente tratado con radioterapia con o sin cirugía.
La supervivencia a 5 años es de aproximadamente el 50% y la mortalidad operatoria es del 3-5% (8)
INDICACIONES.
- Recurrencia central de cáncer de cervix postradioterapia (cúpula vaginal o pelvis sin afectación de la pared) siempre y cuando el estudio de extensión descarte diseminación metastásica (9) Fig. 27
- Cáncer de vulva: Aunque no suele realizarse exenteración en mujeres con cáncer de vulva avanzado,
podría realizarse en caso seleccionados de recurrencia tumoral central con amplia destrucción tumoral de uretra,
vejiga o ano
- Cáncer de ovario y endometrio: Debido a la tendencia a diseminación peritoneal de estos tumores más allá de la pelvis,
no son candidatos de exenteración pélvica
- Otros cánceres: Se realiza exenteración en casos seleccionados de carcinoma vaginal,
rabdomiosarcoma y otros tumores poco frecuentes.
También puede realizarse esta alteración en caso de radionecrosis severa, hoy día infrecuente gracias a la tecnología moderna.
CONTRAINDICACIONES (8).
ABSOLUTAS.
- Metástasis peritoneales
- Extensión a las paredes pélvicas Fig. 30
- Metástasis intestinales a distancia.
- Diseminación hematógena pulmonar o hepática Fig. 29
RELATIVAS.
- Adenopatía retroperitoneales
- Invasión directa tumoral de las asas intestinales Fig. 28 Fig. 28 adyacentes.
- Recidiva en menos de un año o persistencia de enfermedad tras finalizar el tratamiento con radioterapia.
- Ureterohidronefrosis
TIPOS(8).
- TOTAL Fig. 31 Fig. 37 extirpación de útero,
trompas,
ovarios,
parametrios,
vejiga,
recto,
vagina,
uretra,
y musculatura elevadora del ano.
Puede incluirse fase perineal, con resección del ano,
uretra,
y vulva.
- ANTERIOR Fig. 32 Fig. 32 Fig. 38 : En la exenteración anterior,
se preserva el recto.
- POSTERIOR Fig. 6 : En la exenteración posterior,
la uretra y vejiga son respetadas.
.
La exenteración posterior raramente se realiza de forma aislada,
realizándose como parte de cirugía de citorreducción del cáncer de ovario.
TÉCNICAS DE RECONSTRUCCIÓN.
1. Anastomosis intestinal:
La elección de realizar colostomía sigmoidea o anastomosis rectal baja se basa en el nivel de resección,
la longitud del muñón rectal,
y la coexistencia de procesos concomitantes.
2. Flap omental (hamaca epiploica)
En flap omental rellena la cavidad y sirve del pegamento de las superficies peritoneales expuestas tras la exenteración
El omento se libera de la flexura hepática,
creándose una banda de omento libre anclada a la flexura esplénica que se coloca a lo largo de la gotiera paracólica izquierda y pelvis,
creando una hamaca que sostiene el intestino delgado,
manteniéndolo alejado del defecto pélvico Fig. 33
3. Derivación urinaria.
La elección de derivación urinaria continente o no continente depende de las características del paciente y la posibilidad de utilizar el ilion terminal,
colon derecho y válvula ileocecal para crear un sistema competente.
La técnica masa empleada es derivación urinaria tipo Bricker,
o urétero- enterostomía modificada Fig. 34 Fig. 35 .
Se trata de una derivación no continente,
con creación de un conducto urinario ileal donde se implantan los uréteres de un una manera antiperistáltica con posterior anclaje a la superficie cutánea mediante una estoma
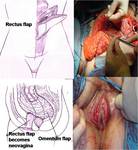
4. Reconstrucción vaginal y pélvica.
Se han descrito varios métodos para la reconstrucción vaginal y pélvica:
- Injerto cutáneo
- Injerto omental.
- Injerto miocutáneo usando los músculos recto abdominal (VRAM)o gracillis
- Intestinal.
La reconstrucción mediante injertos cutáneos no es recomendable debido a la mala vascularización y falta de soporte pélvico.
Los injertos miocutáneos son de elección ya que están ampliamente vascularizados,
lo que reduce la probabilidad de necrosis y desarrollo de síndrome de pelvis vacía.
El más utilizado es el injerto miocutaneo vertical de recto abdominal( VRAM) (10) Fig. 36
COMPLICACIONES QUIRÚRGICAS TRAS CIRUGÍA ONCOLÓGICA GINECOLÓGICA.
La cirugía ginecológica oncológica es normalmente muy extensa,
requiriendo una disección meticulosa de las lesiones tumorales que afectan a estructuras como la vejiga,
recto,
uréteres y grandes vasos de la pelvis.
La mayoría de las complicaciones se originan en resecciones extensas especialmente cuando existe fibrosis por cirugía previoa y sobre todo por radioterapia.
Las principales complicaciones son hemorragia,
infección y lesiones viscerales(intestinal,
del tracto urinario,
fístulas).
COMPLICACIONES TRAS EXENTERACIÓN PÉLVICA (8).
Prácticamente todos los paciente desarrollan al menos una complicación tras una excentración pélvica,
y aproximadamente de 40-50% sufren complicaciones mayores,
que requieren reintervención quirúrgica.
La mortalidad operatoria es del 2-5%.
COMPLICACIONES DEL TRACTO URINARIO.
Existe mayor incidencia de lesiones del tracto urinario tras la realización de histerectomía radical y linfadenectomía que tras la realización de histerectomía abdominal total por patología benigna (11).
La laceración vesical es la complicación postquirugica más habitual y es normalmente reconocida y corregida en el mismo acto quirúrgico.
La lesión ureteral puede ser consecuencia de trauma directo quirúrgico,
o por isquemia debido a raspado de la fascia periureteral Fig. 40
La mayoría de las lesiones vesicales o ureterales suelen curar sin si bien pueden desarrollar urinomas,
estenosis ureterales o fístula ureterovaginales o vesícocaginales Fig. 44
COMPLICACIONES DEL TRACTO DIGESTIVO.
En la cirugía ginecológica pueden dañarse tanto el intestino delgado como el colon rectosigmoideo.
La prevalencia de lesiones intestinales es mayor en pacientes con adherencias por cirugías previas,
radioterapia o enfermedad inflamatoria pélvica .
Las complicaciones más habituales incluyen perforación,
peritonitis,
formación de abscesos,
obstrucción intestinal o fístulas Fig. 42 Fig. 43
BIBLIOGRAFÍA
- William J Mann,
Jr,
MD,
Eva Chalas,
MD,
Fidel A Valea.
Epithelial ovarian cancer: Initial surgical management.
Retrieved October 4,
2010 from UpToDate online textbook: http://www.uptodate.com
- Qayyum A,
Coakley FV,
Westphalen AC,
et al.
Role of CT and MR imaging in predicting optimal cytoreduction of newly diagnosed primary epithelial ovarian cancer.
Gynecol Oncol 2005;96 :301–6.
- William J Mann,
Jr,
MD,
Eva Chalas,
MD,
Fidel A Valea.
Epithelial ovarian cancer: Second look surgery.
Retrieved September 18,
2010 from UpToDate online textbook: http://www.uptodate.com
- William J Mann,
Jr,
MD,
Eva Chalas,
MD,
Fidel A Valea.
Surgery for recurrent epithelial ovarian cancer.
Retrieved October 18,
2010 from UpToDate online textbook: http://www.uptodate.com
- William J Mann,
Jr,
MD .
Radical hysterectomy.
Retrieved March 15,
2011 from UpToDate online textbook: http://www.uptodate.com
- Marie Plante,
MD Fertility sparing surgery for invasive cervical cancer.
Retrieved September 7,
2011 from UpToDate online textbook: http://www.uptodate.com
- Sahdev A,
Jones J,
Shepherd JH,
Reznek RH.
MR imaging appearances of the female pelvis after trachelectomy.
Radiographics.
2005 Jan-Feb;25(1):41-52.
- Ken D Hatch,
MD,
William J Mann,
Jr,
MD.
Exenteration for gynecologic cancer.
Retrieved April 21,
2011 from UpToDate online textbook: http://www.uptodate.com
- Ungar L,
Palfalvi L,
Novak Z.
Primary pelvic exenteration in cervical cancer patients.
Gynecol Oncol 2008; 111:S9.
- O’Connell,Mirhashemi,
Kassira,
Lambrou,
McDonald.
Formation of Functional Neovagina With Vertical Rectus Abdominis Musculocutaneous (VRAM) Flap After Total Pelvic Exenteration Ann Plast Surg 2005;55: 470–473
- Paspulati RM,
Dalal TA.Imaging of Complications Following Gynecologic Surgery.
Radiographics.
2010 May;30(3):625-42