Beckwith et al.2 revisaron el complejo nefroblastomatosis proponiendo una nueva terminología y clasificación.
Definen el concepto de resto nefrogénico como un foco de células nefrogénicas anormalmente persistentes (más allá de la 36 semana de gestación) que pueden ser inducidas a la formación de un nefroblastoma.
Los restos nefrogénicos se han encontrado en el 1% de las autopsias de los recién nacidos.
La nefroblastomatosis es definida como la presencia difusa o multifocal de restos nefrogénicos hiperplásicos.
Además,
los clasifica según su relación con la topografía lobar renal en perilobares o intralobares.
Beckwith refiere una asociación del 41% entre tumor de Wilms y los restos nefrogénicos. Los restos intralobares (menos frecuentes) implican un transtorno en una etapa más temprana del desarrollo y tienen más posibilidades de transformación en nefroblastoma,
existiendo un riesgo aumentado de tumor metacrónico contralateral en los casos de restos intralobares asociados a Wilms.
En el tumor de Wilms bilateral sincrónico existe una incidencia cercana al 99% de restos nefrogénicos,
siendo la incidencia de los restos perilobares el doble que los intralobares.
Estos restos se pueden encontrar en diferentes estados dinámicos.
Algunos desaparecen,
otros regresan y se esclerosan,
mientras que otros tienen un crecimiento hiperplásico y pueden malignizarse.
La patogenesis del tumor de Wilms es compleja y multifactorial.
Aunque los restos nefrogénicos son una condición predisponente para el desarrollo del tumor de Wilms,
no todos los riñones con restos nefrogénicos desarrollarán el tumor.
Por ejemplo,
hasta el 40% de los riñones resecados por tumor de Wilms,
llegan a presentar focos nefrogénicos en áreas diferentes a las del tumor.
Aspectos genéticos.
Síndromes que predisponen al Tumor de Wilms.
Los modelos actuales de desarrollo del tumor de Wilms proponen que una mutación genética predispone a los restos nefrogénicos.
Como hemos comentado anteriormente estos restos pueden ser intralobares,
perilobares o distribuirse de forma difusa.
Los restos nefrogénicos intralobares (lesiones en el lóbulo renal,
en el seno renal,
o en las paredes de los cálices) se asocian con el Síndrome de WAGR y el síndrome de Denys-Drash (DDS).
Los restos nefrogénicos perilobulares (lesiones múltiples en la periferia del lóbulo renal) se asocian con el síndrome de Beckwith-Wiedemann (SBW) y la hemihipertrofia.
Sin embargo, la asociación entre el tipo de resto nefrogénico y el síndrome de predisposición no es absoluta.
Causas.
1.
Mutaciones germinales del gen WT1 ocasionan alrededor del 10% -15% de los tumores de Wilms.
- Estas mutaciones del gen WT1 pueden dar lugar al tumor de Wilms aislado (es decir,
tumor de Wilms sin evidencia de un síndrome subyacente).
- Dentro del síndrome de WAGR,
o del Denys-Drash (DDS) o del el síndrome de Frasier.
2.
Alteraciones epigenéticas y genéticas del cromosoma 11p15 dan lugar al síndrome de Beckwith-Wiedemann (SBW).
3.
Otros genes de predisposición al tumor de Wilms familiar.
A.
Causas sindrómicas por defectos en WT1.
- El síndrome de WAGR (tumor de Wilms,
aniridia,
anomalías congénitas,
retraso) es causada por la deleción en el cromosoma 11p13 que incluyen tanto PAX6 y WT1.
La aniridia se debe a la eliminación de PAX6,
que se encuentra a unos 0,6 Mb de WT1.
Delante de un individuo con aniridia aislada es obligado descartar el riesgo de tumor de Wilms,
si en el estudio genético hay integridad del gen WT, el riesgo es el mismo que para la población general.
En el WAGR se observará una presentación más temprana,
siendo más frecuente que sea bilateral.
Alta incidencia de restos nefrogénicos intralobares y tumores con una histología favorable.
- El síndrome de Denys-Drash (DDS). La mayoría de las personas van a tener una mutación en el exón 8 o 9 del gen WT1, lo cual provoca en individuos con cariotipo 46,XY la presencia de genitales externos poco masculinizados (de ambiguos a aparentemente femeninos),
esclerosis difusa mesengial que conduce a fallo renal y a tumor de Wilms,
cuyo riesgo es del 90%.
- El síndrome de Frasier. Se debe a mutaciones puntuales en el intron 9 del gen en el gen WT1, provoca en individuos con cariotipo 46,XY la presencia de genitales externos poco masculinizados,
glomeruloesclerosis segmentaria y focal,
y gonadoblastoma.
Aunque el síndrome de Frasier (FS) no se asocia típicamente con el tumor de Wilms,
varios casos han sido reportados.
Esto,
además de informes de casos de gonadoblastoma en las personas con DDS,
ha llevado a la sugerencia de que el DDS y el FS representan dos extremos de un espectro fenotípico.
- Anomalías genitourinarias sin fallo renal. Otras mutaciones en WT1 dan lugar a anomalías genitourinarias y Tumor de Wilms.
B.
Causas sindrómicas por defectos en 11p15.
- Síndrome de Beckwith-Wiedemann y hemihipertrofia. En el síndrome de Beckwith-Wiedemann el riesgo de desarrollar un tumor de Wilms es de aproximadamente un 5%.
La UPD (disomia uniparental paterna) de 11p15 o el aumento de la metilación en IC1 se asocia con mayor riesgo de tumor de Wilms y hepatoblastoma.
En más del 80% de las personas con SBWS,
la prueba genética molecular es capaz de detectar una de las cinco alteraciones:
- La pérdida de metilación del IC2 en el cromosoma materno.
- Aumento de la metilación de IC1 en el cromosoma materno.
- La mutación del alelo materno CDKN1C.
- Disomía uniparental paterna del cromosoma 11p15.5.
- Duplicación,
inversión o desplazamiento que implica la banda p15.5 del cromosoma 11.
C.
Otros síndromes asociados con tumor de Wilms.
- Trastornos autosómicos dominantes;
Síndrome de Li-Fraumeni.
Síndrome de Sotos.
Síndrome de hiperparatiroidismo-tumor mandíbula (gen CDC73).
Neurofibromatosis tipo 1,
- Trastornos autosómicos recesivos;
La anemia de Fanconi.
El síndrome de Bloom.
- Ligada al cromosoma X;
Síndrome de Simpson-Golabi-Behmel.
- Síndrome de Perlman.
- Trisomía 18.
Hallazgos radiológicos.
Clásicamente los restos nefrogénicos permanecen ocultos hasta que son descubiertos de forma incidental por las pruebas de imagen (RM,
TAC o ecografía) o aparecen en conjunción con el tumor de Wilms en la cirugía.
La nefroblastomatosis difusa se puede manifestar como masas palpables unilaterales o bilaterales y generalmente son descubiertos en la exploración antes del año de vida.
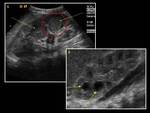
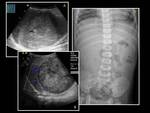
La apariencia ecográfica (Fig.
1) de la nefroblastomatosis es variable: se puede observar desde agrandamiento difuso de ambos riñones,
con áreas de cambios sutiles en la ecogenicidad y ecoestructura que alteran la diferenciación córtico-medular,
en algunos casos con pequeño efecto de masa,
que en ocasiones son difíciles de visualizar,
hasta masas hipo,
iso o hiperecoicas rodeando ambos riñones,
como ocurre típicamente en la nefroblastomatosis perilobar.
En la TC y en la urografía excretora,
el tejido anormal presenta un leve realce homogéneo (comparado con el gran realce del parénquima renal normal).
La nefroblastomatosis difusa puede ser indistinguible de la enfermedad poliquística renal autosómica recesiva,
leucemia o linfoma.
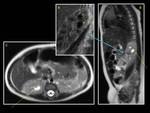
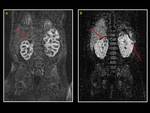
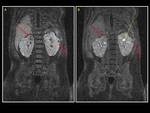
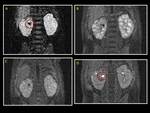
En la RM (Fig.
3,
Fig.
4,
Fig.
5),
estas lesiones típicamente muestran una baja señal relativa a la corteza renal en las secuencias con potenciadas en T1 y son de iso a ligeramente hiperintensas en las secuencias con potenciadas en T2,
con un realce leve con el medio de contraste; pequeñas placas superficiales de nefroblastomatosis pueden ser imperceptibles,
y la diferenciación del linfoma renal puede ser difícil.
Nótese en que la descripción de la tabla,
es la clasificación comúnmente aceptada y expone como se visualizan dependiendo de la técnica escogida los restos nefrogénicos (tabla 1,
tabla 2),
pero aun así,
y en base a nuestra experiencia hemos visto que pueden existir restos perilobares en niños con síndrome de WAGR (en los cuales es más común la presencia de restos intralobares) y a su vez asociarse a alteraciones renales como los divertículos calicilares (Fig.
1,
Fig.
2,
Fig.
5) que pueden ser un primer indicador de la existencia de alteraciones renales parenquimatosas concomitantes que no son visualizadas de entrada en los estudios ecográficos,
por ejemplo.
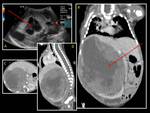
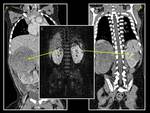
Este paciente desarrollo un tumor de Wilms a los 18 meses (Fig.
6,
Fig.
7,
Fig.
8).
En nuestro caso,
tanto los restos nefrogénicos perilobares y la presencia de divertículos calicilares,
son hallazgos no descritos en el síndrome de WARG.
Estos hallazgos ponen de manifiesto,
como comentamos anteriormente que la asociación entre el tipo de resto nefrogénico y el síndrome de predisposición no es absoluta y por ello se deberían de explorar detalladamente todas las regiones independientemente del síndrome presente.
Por lo que respecta al manejo radiológico de la nefroblastomatosis,
un esquema comúnmente aceptado es el de realizar un control ecográfico cada 3-4 meses hasta los 7 años (ya que por encima de esta edad no se ha descrito ningún caso de transformación maligna)4,
y en caso de visualizarse cambios en el seguimiento,
como crecimiento o aumento del número de lesiones,
plantearse la realización de estudios RM y/o TC.
De todas las técnicas de imagen,
la resonancia,
es que la que ha aportado mayor sensibilidad a la hora de visualizar focos de nefroblastomatosis,
y es por eso que en pacientes con síndromes en los cuales el riesgo sea muy alto,
como el síndrome de WARG o el Drash,
se debería plantear la opción de realizar un estudio RM de entrada.
Tratamiento.
El tratamientode la nefroblastomatosis es controvertido.
El riesgo de transformación a tumor de Wilms es algo mayor en la nefroblastomatosis debido al mayor número de células con riesgo a malignizarse.
Como regla general,
el tratamiento ha de individualizarse siendo muy útil la realización periódica de pruebas de imagen para planificar una estrategia de tratamiento adecuada,
debiendo evitar la exéresis innecesaria de restos benignos.
Controvertido es asimismo el uso de la QMTpreoperatoria6 y los detractores se basan en que:
La QMT trata un proceso benigno,
que suele regresar espontáneamente (70% aprox.);
Incertidumbre sobre el resultado final obtenido ya que la QMT no previene totalmente el desarrollo neoplásico;
Daño potencial a células sanas ya que puede ser más activa contra células sanas,
que contra los nódulos de NB;
Resultado transitorio,
las lesiones pueden disminuir de tamaño,
pero no desaparecer "permaneciendo aletargadas".