INTRODUCCIÓN
La patología aórtica aguda es una situación clínica crítica cuyo pronóstico depende de un diagnóstico rápido y certero,
así como de la instauración temprana de su tratamiento.
La angiografía por tomografía computerizada (Angio-TC) es una técnica que aporta una información diagnóstica exacta y rápida (sensibilidad y especificidad cercana al 100%) suficiente para decidir el traslado urgente del paciente a un centro de referencia con radiología intervencionista y/o cirugía cardiovascular.
Es importante disponer de herramientas de telerradiología para poder intercambiar la información del centro de referencia para valoración conjunta pre y postquirúrgica.
La aorta debido a una exposición continua a la presión pulsátil y fuerzas de cizallamiento está predispuesta a sufrir lesiones de su pared, aparición de dilataciones aneurismáticas y un mayor riesgo de rotura.
Revisamos la patología aórtica más frecuente mediante casos atendidos en urgencias de nuestro hospital: la rotura del aneurisma aórtico,
la disección aórtica,
las lesiones postraumáticas y las complicaciones en pacientes ya tratados.
En cuanto al protocolo de los estudios realizados en algunos casos la patología aórtica es un hallazgo incidental al realizar TC de tórax y/o abdomen con contraste.
En los casos en los que la sospecha clínica es de patología aórtica se programa un estudio completo de aorta, incluyendo aorta ascendente hasta su bifurcación,
sin y con contraste en fase arterial (con técnica "bolus tracking").
ROTURA DE ANEURISMA AÓRTICO
El diámetro máximo de la aorta en adultos corresponde a 3 cm en su origen y va disminuyendo a 2,5 cm en aorta descendente torácica hasta 1,8 a 2 cm en la aorta abdominal.
Se considera que la aorta presenta una dilatación aneurismática torácica cuando supera los 5 cm en aorta ascendente y los 4 cm en aorta descendente. El aneurisma de aorta abdominal (AAA) se define cuando es mayor de 3 a 3,5 cm de diámetro transverso.
La incidencia aumenta con la edad,
entre 2% en mayores de 65 años y 12 % en mayores de 75 años con una relación entre hombres y mujeres de 6:1.
Los factores de riesgo para el desarrollo del aneurisma de aorta son: edad mayor de 65 años,
sexo masculino,
familiar de primer grado con historia de AAA,
hipertensión arterial,
tabaquismo,
enfermedad arterial periférica,
EPOC y enfermedad de tejido conectivo.
La presentación clínica típica de la rotura del aneurisma consiste en dolor torácico o abdominal agudo que puede irradiarse a tórax,
zona inguinal,
escroto,
muslo y pierna,
se puede plantear como diagnóstico diferencial: cólico renal,
diverticulitis,
pancreatitis,
infarto agudo de miocardio,
isquemia mesentérica.
La Angio-TC es la técnica más precisa para medir el diámetro del aneurisma y aporta información adicional como el lugar de sangrado,
complicaciones isquémicas y patología arterial asociada,
se obtiene una descripción de las arterias renales,
mesentéricas e ilíacas y es parte importante en la evaluación preoperatoria.
Los hallazgos radiológicos son:
TC sin contraste:
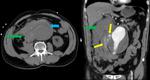
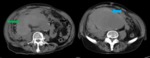
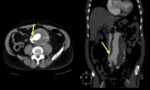
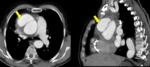
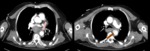
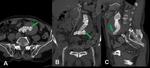
- Semiluna de alta atenuación: se identifica un aumento de densidad en el interior de la zona trombosada del aneurisma compatible con hematoma intramural agudo.
(Fig. 1,
Fig. 2)
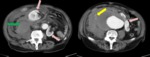
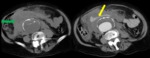
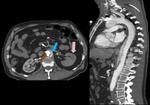
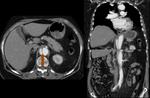
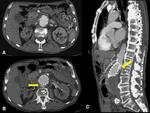
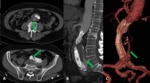
- Colecciones hiperdensas alrededor del aneurisma que indican hematoma por extensión del sangrado.
(Fig. 1 ,
Fig. 2, Fig. 3 y Fig. 4)
- Discontinuidad de la calcificación intimal del aneurisma.
TC con contraste:
La rotura aguda de un AAA tiene una elevada mortalidad,
del 77 al 94 %,
el riesgo de rotura es directamente proporcional al diámetro del aneurisma,
la rotura se produce hacia el espacio retroperitoneal (71%),
intraperitoneal (25%),
tracto gastrointestinal (2,5%) y vena cava inferior Fig. 5 (3,5%).
DISECCIÓN AÓRTICA
La pared vascular está formada por: a) Íntima,
compuesta de endotelio,
lámina basal y capa subendotelial de tejido conjuntivo laxo; b) Túnica media,
formada por capas concéntricas de células musculares lisas y matriz extracelular; c) Adventicia formada fundamentalmente por tejido conectivo,
que engloba los vasa vasorum y la inervación del vaso.
Los factores predisponentes de disección aórtica son la hipertensión arterial,
anomalías congénitas de la válvula aórtica,
trastornos hereditarios del sistema conectivo y traumatismos.
La disección aórtica comienza con la formación de un desgarro en la íntima de la aorta,
que expone la capa media subyacente al flujo sanguíneo pulsátil.
Éste penetra en dicha capa media,
disecándola y extendiéndose en longitud variable,
creando una falsa luz,
la distensión de la falsa luz puede llegar a estenosar y distorsionar la luz aórtica verdadera.
La localización del desgarro intimal primario más frecuente es en la aorta ascendente,
entre 1-5 cm por encima del seno de Valsalva derecho en el 65% de los casos,
en la aorta descendente proximal debajo de la subclavia izquierda en el 20%,
en el arco aórtico transverso en 10% y en aorta distal toracoabdominal en el 5%.
El síntoma más frecuente es el dolor severo súbito,
de carácter desgarrante,
de tipo pulsátil,
migratorio siguiendo el sentido de la disección,
localizado en la cara anterior del tórax,
cuello y mandíbula cuando la disección es en la aorta proximal,
o localizado en la zona interescapular y el abdomen si la disección es distal.
Según la clasificación de Stanford existen dos tipos: Tipo A,
la disección en la aorta ascendente con o sin afectación del cayado o de la aorta descendente. Tipo B, afecta a cualquier segmento de la aorta torácica descendente sin afectar a la ascendente ni al cayado.
En los centros de segundo nivel la Angio TC es la ténica de elección debido a su exactitud diagnóstica,
su amplia disponibilidad y a la facilidad y rapidez de la exploración.
Los hallazgos en la disección aórtica pueden ser:
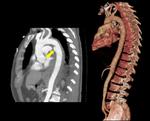
- Desplazamiento interno de la calcificación de la íntima en el estudio sin contraste.
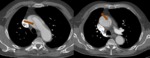
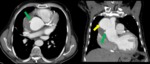
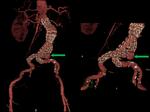
- El colgajo de la íntima se visualiza como una estructura lineal que separa dos luces,
la luz verdadera de la falsa.
Fig. 6,
Fig. 7,
Fig. 8,
Fig. 9, Fig. 10,
Fig. 11 y Fig. 12
- La luz verdadera puede distinguirse de la luz falsa por su temprana e intensa opacificación al administrar contraste,
su área con frecuencia es menor.
- Realce tardío de la falsa luz debido al flujo más lento.
- Trombosis de la luz falsa.
- Extensión de la disección hacia las ramas de la aorta.
Fig. 7,
Fig. 8 y Fig. 9
- Isquemia o infarto de los órganos vascularizados por las ramas de la aorta ocluidas por el colgajo de la íntima.
Fig. 9
LESIÓN AÓRTICA POSTRAUMÁTICA
En el 90% de los casos,
la rotura se encuentra en el istmo aórtico distal al origen de la arteria subclavia izquierda, en el 10% restante se encuentra en otras localizaciones como la raíz aórtica o aorta ascendente.
Tiene una mortalidad sin tratamiento de un 85 a un 90%,
requiere tratamiento en las primeras 24h,
puede realizarse mediante cirugía abierta convencional o reparación endovascular torácica; esta última ha evolucionado en los últimos años por lo que actualmente se considera de elección.
Se clasifican en:
- Tipo I: defecto intimal
- Tipo II: hematoma intramural
- Tipo III: pseudoaneurisma
- Tipo IV: rotura con sangrado activo
Los hallazgos en la TC son:
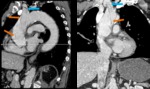
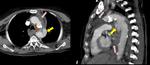
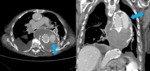
- Hematoma mediastínico.
Fig. 13
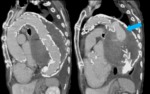
- Rotura intimal.
Fig. 13 y Fig. 14
- Pseudoaneurisma.
Fig. 15
- Cambios en el contorno de la aorta.
- Hematoma intramural.
- Extravasación de contraste.
COMPLICACIONES TRAS TRATAMIENTO ENDOVASCULAR
Las complicaciones de las técnicas endovasculares en el tratamiento de la patología aórtica pueden ser endofugas,
cambios estructurales de los dispositivos por fatiga del material,
migración de la endoprótesis,
disecciones aórticas tardías,
infecciones del dispositivo,
fistulización en órganos vecinos y expansión y rotura del aneurisma tratado.
Las endofugas son la complicación principal,
consisten en la persistencia de flujo sanguíneo en la luz del aneurisma, suele provocar un crecimiento continuado del aneurisma que,
en caso de no ser tratado,
puede provocar su rotura.
Se manifiestan como la presencia de contraste fuera de la endoprótesis y dentro del saco del aneurisma.
Se clasifican en cinco tipos:
- Tipo I: Deficiente sellado entre la prótesis y la pared del vaso.
Fig. 16
- Tipo II: Flujo retrógrado por colaterales. Fig. 17
- Tipo III: Alteración estructural de la prótesis. Fig. 18,
Fig. 19,
Fig. 20 y Fig. 21
- Tipo IV: Filtración a través de la prótesis,
por porosidad en el recubrimiento.
- Tipo V: Endotensión con crecimiento del aneurisma sin fuga demostrable.
La incidencia de fugas periprotésicas postimplantación se estima entre el 7 y el 52% de los casos; sin embargo,
entre el 40 y el 88% de ellas se resuelve de forma espontánea,
sobre todo las fugas tipo II,
de modo que en este tipo de fugas se realiza un control periódico mediante TC y si son persistentes o producen el crecimiento del aneurisma,
se debe intentar la embolización de la arteria responsable de la endofuga.