1.
INTRODUCCIÓN.
El Síndrome de Budd Chiari es una entidad rara que se caracteriza por la obstrucción parcial o completa del flujo venoso de las venas suprahepáticas.
Algunos autores consideran también parte de este síndrome a la obstrucción de la vena cava inferior.
Es una enfermedad muy poco frecuente con una incidencia de 1/100.000.
Usualmente afecta a personas jóvenes o de mediana edad con una larga esperanza de vida por lo que es importante su diagnóstico precoz.
Las formas agudas son poco frecuentes y se presentan característicamente con dolor abdominal,
hepatomegalia dolorosa y ascitis.
Las formas crónicas y subagudas suelen presentarse de forma inespecífica y el diagnóstico puede resultar más difícil.
Requiere de un alto índice de sospecha para su diagnóstico, ya que frecuentemente pasa inadvertido y se diagnostica en fases tardías evolucionadas.
2.
ANATOMÍA DE LAS VENAS SUPRAHEPÁTICAS.
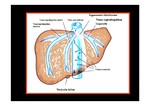
Existen tres venas suprahepáticas principales: derecha,
media e izquierda.
La vena suprahepática izquierda drena separada en la vena cava inferior, pero las venas suprahepáticas media y derecha suelen fusionarse y formar un tronco común en el 65-85% de los casos.
Existen pequeñas venas accesorias que drenan directamente en la vena cava inferior y usualmente recogen la sangre de la parte posterior del lóbulo hepático derecho y del caudado (Fig. 1).
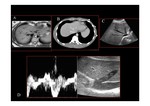
Las venas suprahepáticas principales son intersegmentarias,
sus ángulos de ramificación son verticales y su calibre aumenta en dirección craneal a medida que nos aproximamos a la vena cava inferior (Fig. 2).
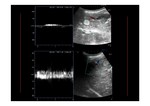
Las venas suprahepáticas presentan un registro pulsátil trifásico con dos pulsos anterógrados y uno retrógrado.
Se deben obtener al final de la espiración normal por ecografía (Imagen D de Fig. 2).
3.
EPIDEMIOLOGÍA Y ETIOLOGÍA.
Como se había comentado anteriormente,
este síndrome es poco frecuente con una incidencia de 1/100.000.
Puede ocurrir a cualquier edad,
pero es más común en personas de mediana edad y en mujeres.
Se conocen numerosas causas del síndrome pudiéndose dividir en causas primarias y secundarias,
siendo las causas primarias las más frecuentes.
Causas primarias (más del 75%):
- Estados de hipercoagulabilidad (Policitemia Vera,
Deficiencia de proteína C y S,
trombocitosis esencial y Síndrome Antifosfolípido).
- Oclusión por membranas,
frecuente en Asia.
Causas secundarias:
- Compresión extrínseca.
- Invasión tumoral (carcinoma hepatocelular,
carcinoma de células renales y el carcinoma suprarrenal).
- Toma de anticonceptivos orales como forma de estado de hipercoagulabilidad secundario.
En la Fig. 3 se exponen detalladamente las diferentes causas de este síndrome agrupadas en causas trombóticas y no trombóticas.
4.
FISIOPATOLOGÍA.
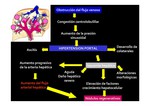
La obstrucción del flujo venoso del hígado da lugar a una grave congestión venosa centrolobulillar con un aumento de la presión sinusoidal que ocasiona un flujo venoso portal retardado o invertido.
Se producen a su vez cambios morfológicos en la circulación y daño hepático,
dando como resultado ascitis,
desarrollo de colaterales,
aumento del flujo arterial hepático y nódulos regenerativos.
Todos estos cambios se representan en Fig. 4.
5.
PRESENTACIÓN CLÍNICA.
Las presentaciones clínicas se pueden dividir en agudas,
subagudas y crónicas.
Las formas agudas son las menos frecuentes (< 5%) y se caracterizan por:
- Obstrucción venosa en un periodo menor de 2 semanas.
- Intensa necrosis hepática.
- Clínica de dolor abdominal,
vómitos,
hepatomegalia brusca,
hipertransaminasemia,
ictericia,
ascitis,
signos de insuficiencia hepática aguda,
fallo renal e incluso éxitus.
Las formas subagudas suponen la presentación más frecuente y se identifican por:
- Una instauración entre 2 semanas y 6 meses.
- Clínica inespecífica: dolor abdominal,
ascitis,
hepatomegalia,
hipertransaminasemia,
aumento de bilirrubina y descenso de tiempo de protombina.
Las formas crónicas corresponden a las cirrosis inexplicables y presentan:
- Una evolución de más de 6 meses.
- Una clínica indistinguible de otros tipos de cirrosis con hipertensión portal,
ascitis rica en proteínas (20-30 g/l) de difícil tratamiento y pruebas hepáticas normales.
6.
HALLAZGOS EN LAS PRUEBAS DE IMAGEN.
A) ECOGRAFÍA.
La ecografía es frecuentemente la primera prueba que se realiza en estos pacientes y presenta las siguientes ventajas y desventajas:
Ventajas:
- Es la técnica de elección en el cribado.
Tiene una alta sensibilidad (> 85 %).
- Las imágenes doppler permiten evaluar la presencia y la dirección del flujo venoso hepático.
- Se pueden visualizar cambios en parénquima hepático.
- Permite evaluar la vena porta,
el bazo y la presencia de colaterales.
- No es invasiva.
Desventajas:
- La técnica está limitada por el hábito corporal del paciente (menos útil en obesos) y es dependiente del operador.
- Subestima la presencia de trombosis o membranas.
En cuanto a los hallazgos ecográficos del Síndrome de Budd-Chiari se pueden dividir en tres categorías,
que son las siguientes:
Categoría 1.
Signos directos.
Suponen menos del 20% de los casos.
- Ausencia de visualización de las venas suprahepáticas.
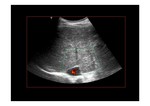
- Identificación de trombos en el interior de las venas o visualización de un cordón fibroso en su localización (Fig. 5).
- Alteraciones del flujo en el interior de las venas suprahepáticas (ausente,
invertido,
turbulento o continuo).
Categoría 2.
Signos de circulación colateral intrahepática.
Son más sensibles para el diagnóstico y están presentes en más del 80% de los casos.
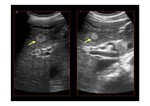
- Colaterales intrahepáticas vena-vena: En patrón de tela de araña (spiderwebs),
colaterales drenando a la vena cava y venas subcapsulares (Fig. 6).
- Colaterales intrahepáticas portocavas.
- La vena caudada de 3 mm de diámetro en el contexto clínico apropiado es diagnóstica.
Se aprecia en el 50 % de los casos y se explica porque al ser la única vía de drenaje recibe sangre no solamente del lóbulo caudado sino de otras partes del hígado a través de vasos colaterales.
Se mide en el corte epigástrico longitudinal.
Se debe descartar que el paciente presente insuficiencia cardiaca congestiva.
Categoría 3.
Otros hallazgos inespecíficos.
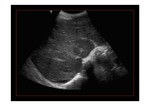
- Nódulos regenerativos (Fig. 7).
- Parénquima hepático heterogéneo e hipertrofia del lóbulo caudado (Fig. 8).
- Trombosis portal.
- Reecanalización de venas umbilicales.
- Ascitis.
- Esplenomegalia.
B) TC.
La ventaja del estudio con TC es que permite la visualización de cambios en el parénquima,
sobre todo en pacientes en los que no hay una buena visualización de éste por ecografía.
Las venas suprahepáticas se pueden visualizar en algunos pacientes en TC abdominales en fase portal,
aunque en ocasiones esta técnica presenta una baja sensibilidad para estudiar las venas suprahepáticas.
Como desventajas estarían la radiación y la nefrotoxicidad por los contrastes yodados.
Entre los hallazgos por TC que podemos apreciar en el Síndrome de Budd Chiari se encuentran los siguientes:
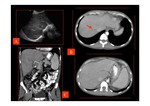
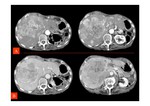
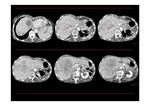
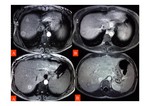
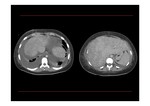
- En las formas agudas en la TC sin contraste puede visualizarse una hepatomegalia global con hipoatenuación hepática difusa por congestión hepática y suele haber ascitis que puede llegar a ser severa.
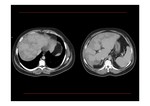
- Trombos en las venas suprahepáticas o no visualización de éstas (Imagen izquierda de Fig. 9).
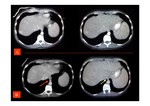
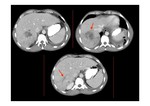
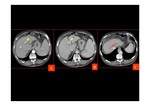
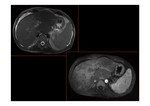
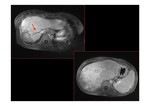
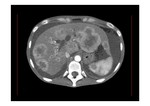
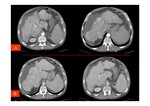
- Captación de contraste parcheada del parénquima hepático,
con hipodensidad de las zonas periféricas y captación normal de las áreas centrales del hígado que típicamente están respetadas (Fig. 9 y Fig. 10).
- El contorno hepático puede ser liso o lobulado pero no tan irregular como en la cirrosis hepática.
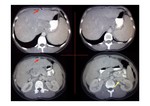
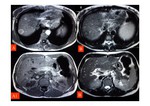
- Puede haber nódulos regenerativos que suelen ser múltiples y pueden estar presentes al diagnóstico,
pero habitualmente se observan durante el seguimiento (fases subagudas o crónicas).
Se suelen observar en el 80 % de los casos y son de 0,5-4 cm de tamaño.
Se visualizan iso o hiperatenuantes en TC sin contraste,
con hiperatenuación homogénea y marcada en fase arterial,
que permanecen con ligero realce en fase portal.
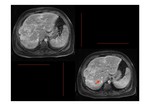
En algunos casos se puede identificar un anillo perinodular hipoatenuante que se debe al tejido atrófico en la periferia de la lesión (Fig. 11 y Fig. 12).
- Trombosis concomitante de la porta hasta en un 20% de los casos.
- Infartos hepáticos periféricos en forma de cuña que no captan contraste.
- Esplenomegalia.
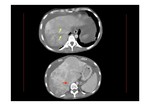
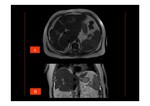
- Hipertrofia del lóbulo caudado con compresión de la vena cava inferior,
sobre todo en fases crónicas.
El lóbulo caudado se hipertrofia porque sigue manteniendo su drenaje conservado directamente a la vena cava inferior (Fig. 13).
- Puede verse la vena cava inferior estrechada u ocluida.
- Circulación colateral intrahepática o portosistémica.
- Hipertrofia de la arteria hepática en estadios avanzados.
- En los casos secundarios,
además de los hallazgos descritos,
se puede identificar la causa que ha provocado el Síndrome (Fig. 14,
Fig. 15,
Fig. 16 y Fig. 17).
C) RESONANCIA MAGNÉTICA.
Presenta una alta sensibilidad y especificidad para el diagnóstico de éste Síndrome.
La mayoría de los hallazgos son superponibles a los descritos en TC.
Esta técnica suele ser muy útil para estudiar las colaterales venosas y la vena cava inferior,
siendo muy útiles las secuencias T2 gradiente para demostrar la ausencia de flujo en las venas hepáticas y en la vena cava inferior.
Se pueden apreciar los siguientes hallazgos:
o Las imágenes en T1 muestran una menor intensidad de señal en la periferia del hígado que suponen las áreas afectadas,
con una intensidad más normal en el lóbulo caudado (área respetada).
o En T2 se observa un incremento de señal heterogéneo en la región periférica hepática con un señal homogénea normal en el lóbulo caudado.
o Las imágenes con gadolinio muestran una captación heterogénea con una captación precoz en el lóbulo caudado y en la región central.
Este patrón puede persistir en las imágenes más tardías e incluso puede invertirse.
- Se pueden identificar fácilmente los trombos en las venas suprahepáticas o en la vena cava inferior ,
así como las vías de circulación colateral intrahepáticas o portosistémicas .
Se suelen visualizar las venas ácigos y hemiácigos dilatadas en aproximadamente un tercio de los pacientes.
- Asocian en un 20 % trombosis portal.
- En las fases crónicas es común solamente visualizar un parénquima heterogéneo.
- Pueden visualizarse nódulos regenerativos múltiples,
menores de 4 cm.
Son hipo/hiperintensos en T1 sin contraste e isointensos o hipointensos en secuencias T2.
En fase precoz captan de forma homogénea (ver comentarios de Fig. 22 y Fig. 23).
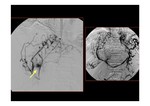
D) FLEBOGRAFÍA.
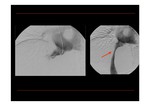
Es la prueba que más diagnóstica este Síndrome junto a la biopsia hepática.
La incapacidad para canular la vena suprahepática no puede ser considerado como diagnóstico por sí mismo,
pero en manos experimentadas es de alta sospecha (Fig. 24 y Fig. 25).
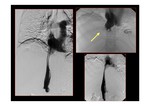
La flebografía es la prueba de oro para delimitar el nivel de la obstrucción y mostrar las colaterales hepáticas o el típico patrón en tela de araña (spiderweb) Fig. 26.
Se recomienda siempre su realización previamente a realizar maniobras terapéuticas percutáneas.
Es necesario realizar la biopsia hepática acoplada a la flebografía por vía transyugular ya que la realización de una biopsia transcapsular percutánea imposibilita la realización posterior de tratamiento trombolítico.
7.
MANEJO DIAGNÓSTICO.
Para el diagnóstico de este síndrome es necesario una alta sospecha clínica,
prestando especial atención a los pacientes con hepatopatía crónica con leve alteración de la función hepática pero con ascitis intratable,
fallo hepático agudo con hepatomegalia y alteración analítica hepática en paciente con enfermedad protrombótica (más detalles en Fig. 27).
Las pruebas de imagen deben realizarse para confirmar la obstrucción venosa hepática.
La ecografía suele ser la técnica de elección para el estudio inicial (técnica barata,
rápida y accesible).
La TC y la RM se realizarían en un segundo tiempo,
si la ecografía no es diagnóstica o hay dudas,
porque suelen ser técnicas que presentan un mayor porcentaje de diagnósticos de este síndrome.
También se utilizan para determinar algunas de las causas secundarias.
La técnica de confirmación última serían la flebografía para intentar canalizar y visualizar las venas suprahepáticas,
asociada a la biopsia hepática.
En la Fig. 28 se representan el porcentaje de diagnósticos de cada una de las pruebas de imagen.
8.
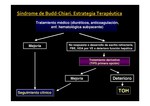
TRATAMIENTO.
Cuando hemos establecido el diagnóstico de este síndrome se realiza un tratamiento médico (diuréticos,
anticoagulación y tratamiento de enfermedad hematológica subyacente si la hay).
Si el paciente presenta mejoría clínica con este tratamiento,
se realizarán controles clínicos posteriores solamente.
Por el contrario,
si el paciente no mejora o presenta ascitis refractaria,
hemorragia digestiva alta por varices esofágicas o deterioro de la función hepática se procede a realizar un tratamiento derivativo con TIPS (Transyugular Intrahepatic Portosistemic Shunt) como primera opción.
Si con este tipo de tratamiento el paciente mejora se realizará seguimiento clínico.
Si no es así,
el paciente puede requerir como última opción un transplante hepático.
En la Fig. 29 se resume el algoritmo del tratamiento.
7.
EVOLUCIÓN Y PRONÓSTICO.
La historia natural de este síndrome no es bien conocida,
siendo su evolución extremadamente variable dependiendo del paciente.
La mortalidad al año es del 60% en los pacientes no tratados,
aunque actualmente la supervivencia a los 10 años en centros especializados suele ser entorno al 75 %.
La mayor tasa de mortalidad se da en los primeros 12-14 meses después del debut.
Los factores pronósticos mejor identificados son la gravedad de la afectación hepática en el momento de la presentación (Clasificación Child-Pugh).
La existencia de trombosis portal asociada también empeora el pronóstico.
8.
DIAGNÓSTICO DIFERENCIAL.
El diagnóstico diferencial de este síndrome se haría con todas aquellas patologías que presentan una estructura heterogénea del parénquima hepático principalmente,
pero la mayoría de los diagnósticos diferenciales se descartan porque se visualizan las venas suprahepáticas permeables.
Algunos de los diagnósticos diferenciales que tendríamos en cuenta tanto por clínica como por hallazgos en imagen serían los que exponemos a continuación:
- Insuficiencia cardiaca congestiva: Entre los hallazgos comunes estarían una hepatomegalia dolorosa y ascitis.
También podría haber heterogenicidad hepática,
pero las venas suprahepáticas y la vena cava inferior suelen visualizarse aumentadas de calibre (Fig. 30).
- Hígado isquémico: Entre los hallazgos comunes estarían una elevación de las transaminasas que volverían a sus valores normales en un corto periodo de tiempo.
No suele haber ascitis ni hepatomegalia.
Se puede visualizar la vena cava inferior y las suprahepáticas permeables y los pacientes suelen tener antecedentes de insuficiencia circulatoria.
- Metástasis hepáticas difusas: Suelen tener en común que se presentan con hepatomegalia dolorosa,
ascitis,
alteración de la analítica hepática y un hígado heterogéneo.
Las venas suprahepáticas y la vena cava inferior suelen estar permeables (Fig. 31).
- Enfermedad hepática avanzada: Suelen tener en común que presenta una heterogenicidad hepática,
pueden haber ascitis si está descompensada,
las venas suprahepáticas pueden ser irregulares y no visibles.
Los pacientes cirróticos evolucionados tendrían un contorno irregular hepático,
mientras que en el Síndrome de Budd-Chiari el contorno suele ser liso.
Los pacientes cirróticos también podrían tener nódulos de regeneración y circulación colateral.
En ocasiones sería difícil distinguir entre las dos entidades siendo la biopsia hepática la que daría el diagnóstico (Fig. 32).
- Síndrome de obtrucción sinusoidal: Tienen en común que podrían presentarse con hepatomegalia,
ascitis y alteración de las pruebas hepáticas.
Las venas suprahepáticas y la vena cava inferior suelen estar permeables y los pacientes presentan historia reciente de quimioterapia o radioterapia.