INTRODUCCIÓN
La endometriosis se define como la presencia de de tejido endometrial hormono-dependiente fuera de la cavidad endometrial y miometrio.
Este tejido ectópico puede consistir desde implantes microscópicos hasta grandes quistes con contenido hemático (endometriomas).
Debido a su hormono-dependencia origina sangrado,
inflamación,
fibrosis y formación de adherencias,
ocasionando dolor pélvico e infertilidad.
La prevalencia de la endometriosis es difícil de determinar de forma precisa,
si bien se estima que afecta al 5-10% de la población femenina,
con o sin sintomatología (1).
La prevalencia es mayor en mujeres con infertilidad o dolor pélvico.
Entre la mujeres con endometriosis el porcentaje de de endometriosis profunda presenta un rango muy amplio que va desde el 5 al 25%(2).
A efectos prácticos,
la endometriosis se clasifica en tres categorías en cuanto a sintomatología,
manejo y evolución: la endometriosis ovárica,
la endometriosis peritoneal y la endometriosis profunda( infiltrante).
La endometriosis pélvica profunda se define por la presencia de lesiones endometriósicas penetrantes en el espacio retroperitoneal o pared de órganos vecinos a una profundidad de al menos 5 mm bajo la superficie peritoneal(3).
En la práctica clínica suelen usarse indistintamente endometriosis pélvica profunda y endometriosis infiltrante,
aunque de forma rigurosa,
debería reservarse el termino endometriosis profunda únicamente a las lesiones que afectan a tejidos retroperitoneales(3)( denominada por otros autores endometriosis subperitoneal o extraperitoneal)(4) y endometriosis infiltrante a aquellas lesiones que afectan estructuras viscerales como intestino,
uréteres y vejiga.
Los implantes peritoneales de la endometriosis se describe clásicamente como lesiones en "quemaduras de pólvora" de color gris-azulado en la inspección visual.
El color se atribuye a la sangre menstrual que se encapsula por tejido fibrótico y es posteriormente hemolizada (3).
El endometrio ectópico también puede aparecer como lesiones vesiculares no pigmentadas,
placas blancas o petequias rojizas
Microscópicamente,
tanto las lesiones endometriósicas superficiales típicas como las profundas contienen glándulas y estroma y pueden acompañarse de hemorragia o fibrosis adyacente.
Sin embargo, las lesiones endometriosicas infiltrantes y profundas se caracterizan por generar clásicamente hiperplasia fibromuscular rodenado al foco de endometriosis dando lugar a la típica formación de nódulos sólidos ( endometriosis infiltrante sólida) .En la endometriosis infiltrante visceral,
los implantes se adhieren a la superficie serosa visceral y pueden invadir las capas musculares,
provocando proliferación del músculo liso ,
con consecuente estenosis y obstrucción .
La causa de la endometriosis es controvertida.
Se han propuesto diferentes teorías,
como la implantación metastásica por menstruación retrógrada,
o la teoría de la diferenciación metaplasica de la superficie serosa del peritoneo o de remanente de conductos de Müller.
Otra teoría alternativa,
la teoría de la inducción,
propone que el endometrio ectópico induce la diferenciación del mesénquima indiferenciado en tejido endometrial(1).
Alternativamente,
algunos expertos sugieren que la endometriosis rectovaginal representa nódulos adenomioticos originados de restos mullerianos por un proceso de metaplasia(2).
El tratamiento de la endometriosis,
sobre todo la profunda,
es complejo.
Aunque los tratamientos médicos inducen una quiescencia temporal de algunas lesiones activas profundas,
no actúan con la fibrosis y adherencias,
por lo que le tratamiento quirúrgico es normalmente la solución final.
El diagnóstico prequirúrgico en estos pacientes resulta crucial para establecer una distribución precisa de lesiones infiltrantes profundas,
que pueden pasar desapercibidas en la cirugía,
con el fin planificar correctamente el acto quirúrgico e intentar asegurar una extirpación completa,
que es de lo que depende el éxito del tratamiento(3).
ANATOMÍA
Tras los ovarios y peritoneo pélvico,
en orden descendente de frecuencia,
las lesiones endometriósicas profundas se localizan en el espacio pélvico subperitoneal,
el aparato digestivo y el sistema urológico.
Entre las localizaciones más frecuentemente de endometriosis pélvica profunda son,
en orden descendente,
ovarios,
torus uterino y ligamentos uterosacros,
espacio de Douglas,
trompas uterinas,
vagina,
colon rectosigmoideo y vejiga .La frecuencia de afectación del saco de Douglas ha sido descrita según series hasta en un 54-56% (5)
La endometriosis pélvica profunda se clasifica según su distribución anatómica en compartimento anterior y posterior.
Para mejor valoración de la endoemtriosis intestinal véase el poster de este mismo congreso “Valoración prequirúrgica de la endometriosis intestinal por RM” del doctor Luis Herraiz
COMPARTIMENTO ANTERIOR
El compartimento anterior de la pelvis incluye la vejiga urinaria,
uréteres distales,
ligamentos redondos y uretra.
Estas estructuras se encuentran en la pelvis menor,
anterior al útero y vagina y posterior a la sínfisis del pubis.
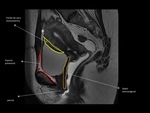
Los planos grasos entre estas estructuras se denominan septo vesicovaginal ( más caudal) y espacio prevesical (craneal) Fig. 1 (4).
La cúpula vesical está cubierta de peritoneo,
creando un pliegue anterior con la pared pélvica,
que es el espacio prevesical,
y un pliegue posterior con el útero,
conocido cono fondo de saco anterior o vesicouterino,
siendo esta última una localización habitual de endometriosis infiltrante profunda .
Las lesiones suelen estar confinadas a la superfice serosa,
sin embargo pueden infiltrar el detrusor,
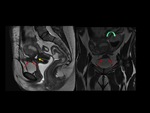
generando nódulos sólidos murales que se proyectan en la luz vesical Fig. 2 Fig. 17
La endometriosis vesical suele presentar clínica de presión suprapúbica,
urgencia y disuria .
La hematuria mestrual se ve en 20-30% de los pacientes
En la cirugía,
el útero suele estar en anteflexión y el fondo de saco anterior obliterado por extensas adherencias peritoneales entre la cúpula vesical y el útero.
La infiltración del detrusor suele ser nodular,
quedando adherido al cuerpo uterino anterior,
bien a nivel de itsmo,
trígono o septo vesicovaginal.
COMPARTIMENTO POSTERIOR
El compartimento posterior está dominado por el recto y los tejidos conectivos que lo rodean.
La demarcación morfológica de este compartimento está formada por la fascia rectal, que es visible en RM como una fina estructura hipointensa que bordea el compartimento perirrectal (4).
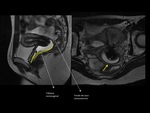
El septo rectovaginal Fig. 3 es una fina membrana que contiene grasa,
y se localiza entre la pared vaginal posterior y la pared rectal anterior,
extendiéndose desde la porción más profunda del fondo de saco de Douglas al techo del periné.
En ausencia de esta grasa,
las paredes rectal y vaginal son indistinguibles .La distensión vaginal con gel permite una mejor valoración de la pared,
con un grosor de 3 mm(4)
Los pliegues rectouterinos contienen abundante tejido fibroso y fibras musculares no estriadas que se anclan al sacro constituyendo los ligamentos uterosacros .
Estas estructuras se ven en RM como finas líneas hipointensas,
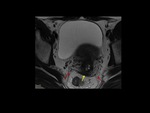
que se originan del margen lateral del cérvix uterino y bóveda vaginal y se dirigen dorso cranealmente al sacro .El torus uterino Fig. 4 es un pequeño engrosamiento transverso que une la inserción original de los ligamentos uterosacros,
detrás del cérvix posterior,
si bien es una estructura que no suele verse en condiciones normales en RM,
a menos que esté engrosado (4)
El espacio retrocervical es un espacio virtual extraperitoneal detrás del cérvix,
situado en el mismo plano que el fondo de saco Douglas y craneal al septo rectovaginal.
Los fórnices vaginales son las porciones más profundas de la vagina que se extiende mediante recesos creados por la extensión del cérvix al espacio vaginal.
El receso mayor es el fórnix vaginal posterior y está localizado posterior al cérvix vaginal.
El fondo de saco rectovaginal-rectouterino o fondo de saco de Douglas Fig. 3 se trata de un saco peritoneal profundo situado entre ambos pliegues rectouterinos.
Es la porción más inferior de la cavidad peritoneal,
cubriendo parte de la vagina y recto,
siendo su base el límite superior del tabique rectovaginal.
En el 93% de las mujeres se extiende al tercio medio de la vagina(4),
aunque no puede verse en condiciones normales en RM,
salvo que haya líquido peritoneal.
Las lesiones endometriosicas del compartimento posterior incluye lesiones peritoneales localizadas en la porción más dependiente del fondo de saco de Douglas ,
lo que genera adherencias ente las superficies peritoneales de la pared rectal anterior y posterior Fig. 5 ,
con la posible infiltración de las capas musculares de estas estructuras.
Esto podría justificar que lesiones endometriosicas del tabique rectovaginal tengan origen en enfermedad masiva de la parte más profunda del fondo de saco de Douglas,
con posterior exclusión de la pelvis restante por adherencias ( 2)
2)
Otro posible origen sugerido por muchos autores de las lesiones endometriosiscas del tabique rectovaginal sería la metaplasia de los remanente müllerianos que persisten en esta localización extraperitoneal.
La lesiones del tabique rectovaginal se han clasificado según su localización en lesiones del septo rectovaginal( tipo I),
fórnix vaginal posterior ( tipo II) y lesiones en reloj de arena ( tipo III)(3).
- Las lesiones del septo rectovaginal Fig. 6 Fig. 8 se observa en 10% de los casos y suelen ser de pequeño tamaño.
Se localizan en el septo rectovaginal,
entre la pared posterior de la mucosa vaginal y la muscular de la pared rectal anterior.
Estas lesiones no están relacionadas con el cérvix uterino y se sitúan en localización extraperioneal,
por debajo del pliegue peritoneal del fondo de Saco de Douglas(3).
- Las lesiones del fórnix vaginal posterior Fig. 7 Fig. 8 Fig. 14 se observan en el 65% de los casos.
Estas lesiones suelen ser pequeñas,
y no suelen extenderse al septo recto vaginal o pared rectal,
aunque si pueden originar fibrosis de la grasa y fascia mesorrectal.
- Las lesiones en reloj de arena se observan en un 25% de los casos Fig. 9 ,
y ocurre cuando las lesiones del cérvix posterior se extienden cranealmente a la pared rectal anterior.
Suelen ser de mayor tamaños(más de 3 cm),con invasión de la pared rectal de forma sistemática(3)
La afectación endometriosica intestinal suele verse en rectosigma Fig. 9 Fig. 16 ,
pero puede afectar en orden decreciente a apéndice,
ciego e ileon distal Fig. 17 Fig. 18 Fig. 20 (Para mejor valoración de la endoemtriosis intestinal véase el poster de este mismo congreso “Valoración prequirúrgica de la endometriosis intestinal por RM” del doctor Luis Herraiz) .
Se estima que ocurre en el 12-37% de los pacientes con endometriosis.(1).
Los implantes suelen ser serosos,
pero pueden erosionar e infiltrar capas subserosas,
con engrosamiento y fibrosis de la muscular propia (hiperplasia fibromuscular).Por RM se comportan como formaciones nodulares retractiles adheridas a la pared hipointensas en secuencias potenciadas en T2 .
Los implantes superficiales serosos o síndromes adherenciales pueden únicamente presentarse como distorsión o angulación parietal,
mientras que los implantes infiltrantes podrán ocasionar un engrosamiento parietal focal o circunferencial,
erosiones mucosas,
llegando a producir estenosis,
procesos suboclusivos u obstructivos francos,
e incluso la formación de raros endometriomas intestinales.En una revisión sistemática la extensión microscópica de la afectación mural en paciente sometidas a resección intestinal por endometriosis colorrectal,
el 95% mostraban invasión de la serosa,
el 95%de la muscular propia,
38% penetraba hasta la submucosa y sólo el 6% afectación mucosa(2).
DIAGNÓSTICO
La laparoscopia es el método diagnóstico de referencia de la endometriosis(1).
Las lesiones típicas consisten en nódulos o placas marrones o negras en la superfice peritoneal y son patognomónicas.
La clasificación de la Sociedad Americana de Fertilidad ( 1975) es la más empleada para la estadificación de la endometriosis (1).
Este sistema usa 3 componentes : la evaluación de los implantes ( localización ,
tamaño y profundidad de penetración),
grado de obliteración del fondo de saco de Douglas y la evaluación de adherencias( apariencia y área afectada) .Según la puntuación asignada por este sistema,
se clasifica a las pacientes en 4 tipos : mínimo,
leve,
moderado o severo Este sistema de estadificación permite cierto grado de estandarización para un mejor manejo con fines pronósticos y terapéuticos.
La laparoscopia sin embargo muestra limitaciones en los casos atípicos fundamentalmente en la valoración de la endometriosis profunda extraperitoneal,
muchas veces oculta por las adherencias adyacentes.
En el acto quirúrgico requiere palpación y apertura del espacio subperitoneal para confirmar y evaluar la extensión de las lesiones,
por lo que un correcto estudio por imagen facilita la elección de la estrategia quirúrgica.
La ecografía es la primera y más utilizada técnica diagnostica la para la evaluación de pacientes con dolor pélvico e infertilidad.
La técnica más empleada es la ecografía endovaginal.
Se trata de una técnica útil para la valoración de endometriomas ováricos y endometriosis de la vejiga,
pero es de escaso valor en la evaluación de la endometriosis peritoneal,
adherencias y endometriosis profunda.
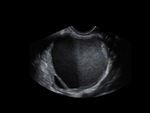
La apariencia ecográfica clásica de un endometrioma suele ser una lesión bien definida,
con contenido homogéneo moderadamente ecogénico Fig. 10 (1) .
La ecografía endoscópica rectal con sonda de alta frecuencia ha sido recomendado para la detección de la endometriosis rectovaginal,
ligamentos uterosacros,
y visceral en recto y colon sigmoide.
Su principal ventaja es que proporciona un medio fiable para valorar el grado de infiltración de la pared intestinal.
Los resultados preliminares muestran que la ecografía endoscópica rectal es mejor que la RM para el diagnóstico de la infiltración de la pared intestinal.
(6)
RM
Por su capacidad multiplanar,
alta sensibilidad en la detección de productos de degradación de la sangre y habilidad para identificar enfermedad oculta por adherencias ,
la RM es la técnica no invasiva de elección en la detección y estadificación e la endometriosis .Además proporciona una tremenda ventaja respecto a otros métodos diagnósticos debido a la posibilidad de realizar una valoración panorámica completa de los compartimentos anterior y posterior de la pelvis en un mismo tiempo.
En un estudio por Togashi et al.
(1;7) la RM alcanza una sensibilidad,
especificad,
y precisión de 90%,
98%,
y 96%,
respectivamente,
para el diagnóstico de endometriomas.
Sin embargo su valor en la demostración de endometriosis en vejiga,
lesiones superficiales y focos ováricos es controvertida y algunos autores han resaltado las limitaciones de la RM en la definición de pequeñas lesiones en estas localizaciones a pesar de que recientes estudios han demostrado buena sensibilidad en la detección de pequeños implantes peritoneales(6) .Teniendo en cuenta todas las localizaciones en su conjunto,
la RM tiene una sensibilidad superior al 90% (6;8) Sin embargo la valoración radiológica puede ser dificultosa,
fundamentalmente en casos de obliteración del receso rectovaginal o en los casos de afectación de vagina o del tabique rectovaginal donde la sensibilidad de la RM según algunos autores puede caer entre el 70 y 80% (6).
Clásicamente,
la endometriosis se diagnosticaba con RM mediante la detección de quistes endometriosicos ováricos (endometriomas ) e implantes con contenido hemático .Estas lesiones presentan un comportamiento hiperintenso en T1 con supresión grasa,
permitiendo además su diferenciación con lesiones con contenido graso.
Un signo patognomónico de endometrioma es el signo del “oscurecimiento”, que consiste en la perdida de señal en T2 de lesiones con comportamiento hiperintenso en T1 .
Este oscurecimiento refleja la naturaleza crónica del endometrioma a consecuencia de episodios repetidos de hemorragia crónica,
que acumula altas concentraciones de hierro,
proteínas y metahemoglobina intracelular.
Un 30% asocia alteraciones tubáricas como hematosalpinx.
(1) Fig. 11 Fig. 12
En el caso de la endometriosis pélvica profunda,
existe una amplia variedad de lesiones,
pudiendo encontrar lesiones del tabique rectovaginal, pequeños implantes infiltrantes,
lesiones ligamentosas sólidas pélvicas profundas y adherencias (generalmente localizadas en el saco de Douglas,
afectando a los ligamentos uterosacros o torus uterino) o la endometriosis infiltrante visceral sólida (afectando a la vejiga o pared rectal) .
Los hallazgos de imagen representan directamente el predominio del componente fibrótico o glandular.
Así podemos encontrar lesiones fibróticas,
glandulares,
fibroglandulares o fibromusculares,
acompañadas o no por la presencia de contenido hemorrágico. En implantes con infiltración profunda,
la RM sólo en ocasiones demuestra focos puntiformes hemorrágicos,
no siendo imprescindible su identificación para el diagnóstico de endometriosis.
El componente fibrótico predominante y ubicuo y las adherencias,
se presenta con hipointensidad de señal franca en imágenes T2 (difícil de diferenciar de la pared vaginal y rectal) Fig. 12 . En ausencia de componente inflamatorio asociado estas lesiones fibróticas no demuestran realce post-contraste.
Algunas masas endometriósicas,
localizadas en ligamentos redondos Fig. 13 ,
uterosacros ,
fórnix vaginal posterior o saco de Douglas,
pueden estar compuestas por una gran proporción de material glandular con escasa reacción fibrótica,
resultando en elevada hiperseñal en T2 (4) y demostrar los focos puntiformes de elevada intensidad de señal en secuencias ponderadas en T1,
representativas de hemorragias petequiales.
Este material glandular sólido suele realzar intensamente y de forma precoz tras la administración de contraste intravenoso.
La afectación de de los ligamentos uterinos,
especialmente los uterosacros,
con nódulos endometriosicos generan un engrosamiento de los mismos,
y en estadios avanzados,
fibrosis y adherencias con obliteración del fondo de saco de Douglas .En RM las adherencias son normalmente de baja señal,
oscurecido las interfases entre los órganos pélvicos.
Signos indirectos que sugieren la presencia de adherencias son desplazamiento de ovarios,
retroflexión uterina,
angulación de la asas ,
elevación del fórnix vaginal posterior o la presencia de líquido loculado Fig. 14 Fig. 15 (1).
Las lesiones viscerales sólidas corresponden a implantes fibroglandulares o fibromiomatosos y presentan una intensidad de señal baja o intermedia con focos puntiformes de alta señal en secuencias ponderadas en T1,
demostrando una señal uniforme y baja en imágenes ponderadas en T2.
Tras la administración de contraste intravenoso se ha descrito realce correspondiente a abundante cantidad de tejido fibrótico localizado en estas lesiones en el análisis histológico ,
si bien en nuestra experiencia estos implantes profundos fibróticos así como los implantes infiltrantes viscerales fibromusculares (por proliferación del músculo liso) se comportan en el estudio dinámico como hipocaptantes respecto a la pared intestinal en fases precoces con realce progresivo e intenso en fases tardías Fig. 16 Fig. 17
PROTOCOLO DE RM
- En nuestra institución realizamos RM pélvica de alta resolución en un equipo de 3T con antena torso-array de 8 canales,
sin preparación previa.
Las imágenes anatómicas de alta resolución las hemos obtenido con secuencias FRSET2 en incidencias axial,
sagital y coronal.
- Es obligatoria la realización de secuencias T1,
(SET1) para mejorar la conspicuidad de lesiones con contenido hemático,
que es una característica cardinal de implantes endometriosicos
- Por protocolo realizamos estudio dinámico tras la administración de contraste 3DLAVA en incidencias axial y sagital.
Se ha descrito la utilidad del contraste intravenoso para definir la extensión de procesos inflamatorios activos asociados con la endometriosis (1). El realce de la superficie peritoneal puede demostrar la localización de implantes subyacentes localizados o difusos en el caso de reacción inflamatoria provocada por los implantes profundos en reflexiones peritoneales sobre los ligamentos uterosacros y en el saco de Douglas.
El uso de secuencias post-contraste se ha recomendado también para identificar nódulos sólidos captantes en quistes endometriósicos cuando se sospecha transformación maligna (1) Fig. 19
- La RM se realiza independientemente del momento del ciclo menstrual de la paciente ya que no hay evidencia de que la RM realizada en el periodo menstrual tengan mayor precisión diagnostica.
No obstante se documenta la fecha de la última regla.
- Para mejor valoración de la endometriosis rectovaginal obtenemos imágenes con distensión vaginal y,
según sospecha,
también rectal mediante gel ecográfico estéril o enema rectal con suero templado( figura 9) (4).
La opacificación de la vagina y el recto con gel de ultrasonido mejora de forma significativa la sensibilidad de la RM para la detección de endometriosis pélvica profunda por la distensión de las cavidades vaginal y rectal,
delimitando mejor las estructuras pélvicas (El gel ecográfico estéril tiene una intensidad de señal similar al agua con hiperintensidad de señal franca en secuencias ponderadas en T2,
lo que contrasta con la hiposeñal relativa de la pared vaginal y rectal.
).Además dada su naturaleza viscosa se evita la perdida durante la realización de la prueba .Es por ello,
especialmente eficaz para detección de las lesiones localizadas en la vagina y tabique rectovaginal
- Aunque no es necesaria la preparación intestinal,
se pide ayunas de las pacientes 6 horas antes de la prueba.
En ocasiones se administra un fármaco antiespasmódico con el fin de reducir los artefactos intestinales causados por la peristalsis y las contracciones uterinas.
Se administra 20 mg de N-butil-escopolamina (Buscopan) IV inmediatamente antes del inicio de la prueba.
- Se procura que la vejiga se encuentre a media repleción,
ya que una vejiga vacía o muy replecionada oblitera los recesos adyacentes,
impidiendo la adecuada valoración de pequeñas lesiones.
- En caso de sospechar afectación intestinal,
se realiza enteroRM( 9),
que pueden realizarse en un solo tiempo de estudio o en dos sesiones separadas .Se realiza en RM de 1.5T con antena de superficie que permite el estudio de todo el abdomen y pelvis en la misma exploración.
En ella se incluye secuencias FIESTA axial y coronal,
RM fluoroscópico o multifase SSFSE (modo cine) y SSFSE FATSAT en axial y coronal,
y estudio dinámico LAVA tras la administración de gadolinio en axial o coronal.Además en la misma explración se puede estudiar el tracto urinario,
gracias a las secuencias coronales FIESTA,
las secuencias dinámicas cine (permitiendo valorar la dinámica de ambos uréteres) y el estudio de uroRM postcontraste Fig. 20 (Para mejor valoración de la endometriosis intestinal véase el poster de este mismo congreso “Valoración prequirúrgica de la endometriosis intestinal por RM” del doctor Luis Herraiz)
BIBLIOGRAFÍA
- Choudhary S,
Fasih N,
Papadatos D,
Surabhi VR.
Unusual imaging appearances of endometriosis.
AJR Am J Roentgenol 2009 Jun;192(6):1632-44.
- Berlanda N,
Vercellini P,
Fedele L.
Rectovaginal or bowel endometriosis. 10-6-2011.
Ref Type: Online Source
- Del FC,
Girometti R,
Pittino M,
Del FG,
Bazzocchi M,
Zuiani C.
Deep retroperitoneal pelvic endometriosis: MR imaging appearance with laparoscopic correlation.
Radiographics 2006 Nov;26(6):1705-18.
- Coutinho A,
Jr.,
Bittencourt LK,
Pires CE,
Junqueira F,
Lima CM,
Coutinho E,
et al.
MR imaging in deep pelvic endometriosis: a pictorial essay.
Radiographics 2011 Mar;31(2):549-67.
- Hottat N,
Larrousse C,
Anaf V,
Noel JC,
Matos C,
Absil J,
et al.
Endometriosis: contribution of 3.0-T pelvic MR imaging in preoperative assessment--initial results.
Radiology 2009 Oct;253(1):126-34.
- Bazot M,
Darai E,
Hourani R,
Thomassin I,
Cortez A,
Uzan S,
et al.
Deep pelvic endometriosis: MR imaging for diagnosis and prediction of extension of disease.
Radiology 2004 Aug;232(2):379-89.
- Togashi K,
Nishimura K,
Kimura I,
Tsuda Y,
Yamashita K,
Shibata T,
et al.
Endometrial cysts: diagnosis with MR imaging.
Radiology 1991 Jul;180(1):73-8.
- Chassang M,
Novellas S,
Bloch-Marcotte C,
Delotte J,
Toullalan O,
Bongain A,
et al.
Utility of vaginal and rectal contrast medium in MRI for the detection of deep pelvic endometriosis.
Eur Radiol 2010 Apr;20(4):1003-10.
- Herraiz Hidalgo L,
Alvarez Moreno E,
Carrascoso Arranz J,
Cano Alonso R,
et al.
Entero-resonancia magnética: revisión de la técnica para el estudio de la enfermedad de Crohn.
Radiología.
2011;53(5):421-433