CARDIO RM DE ESTRÉS:
La evaluación del paciente con síntomas sospechosos de isquemia coronaria es hoy en día uno de los escenarios clínicos más frecuente.
Durante las últimas tres décadas se han producido grandes avances en el manejo terapeútico del paciente con Síndrome Coronario Agudo (SCA),
con una reducción significativa de las complicaciones y de la mortalidad en los 30 primeros días tras el evento.
A pesar de ello,
hay que tener en cuenta que más del 50% de los fallecimientos secundarios a un infarto,
se producen antes de su llegada al hospital.
De esto deriva la importancia de estratificar el riesgo para el desarrollo de eventos coronarios.
Existen varios índices clínicos de riesgo (presencia y tipo de dolor torácico,
edad,
diabetes,…),
mientras que las técnicas de imagen tienen como objetivo incrementar el valor pronóstico.
Las técnicas no invasivas para evaluar la presencia de isquemia comprenden:
- SPECT (limitaciones por baja resolución y artefactos).
- Ecocardiografía de estrés (limitaciones técnicas como mala ventana; peores resultados en pacientes con anomalías de la contractilidad y/ó disfunción sistólica)
- Dobutamina.
- Fármaco vasodilatador: Dipiridamol ó Adenosina.
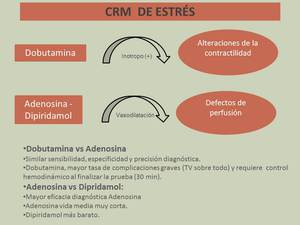
Fig. 1
La RM es hoy en día la técnica de referencia para la valoración estructural y funcional cardiaca.
En los últimos años,
la caracterización tisular mediante esta técnica ha demostrado una buena correlación con el pronóstico del paciente.
Además,
la evaluación de la isquemia mediante cardio-RM de estrés ha experimentado un desarrollo progresivo siendo hoy en día una técnica segura,
cada vez más disponible y potencialmente rentable,
con una alta precisión diagnóstica.
Su objetivo consiste en poner de manifiesto defectos de perfusión miocárdicos en situación de estrés inducido.
La hipoperfusión traduce isquemia,
generalmente por estenosis coronaria significativa.
Esta técnica ha demostrado un alto valor predictivo negativo,
del 99,2% en 3 años para eventos coronarios.
LA RM de estrés también tiene sus limitaciones:
- Inherentes a la técnica (dispositivos metálicos,...).
- Contraindicación para la adenosina (asma,
bloqueo A-V de 2º grado ó mayor,
bradicardia).
- Fibrosis nefrogénica sistémica.
Complicación rara descrita en pacientes con insuficiencia renal avanzada.
Nuestro objetivo es revisar los factores técnicos que van a determinar la calidad de la exploración,
así como repasar los algoritmos diagnósticos clásicos y aquellas situaciones especiales que nos podemos encontrar a la hora de interpretar los estudios.
FÁRMACO VASODILATADOR: ADENOSINA
Es un fármaco agonista de receptores A2A que actúa sobre las fibras musculares lisas de las arterias,
generando un efecto vasodilatador.
A nivel coronario aumenta 3-4 veces el flujo debido a la caída de resistencias.
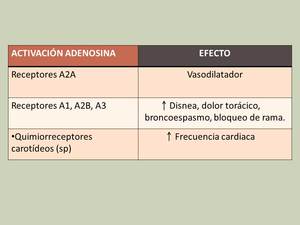
Fig. 2
En presencia de una estenosis significativa,
la arteria coronaria reacciona de forma compensatoria con una dilatación máxima en reposo.
La administración del fármaco provoca un efecto vasodilatador en el resto de territorio coronario,
que generará una reducción de la perfusión en el territorio irrigado por la arteria estenótica,
donde se generará isquemia (fenómeno de “Robo coronario”).
La adenosina tiene una vida media inferior a 10 segundos,
por lo que su efecto es inmediato tras el comienzo de la infusión y desaparece rápidamente tras la interrupción.
Además su efecto puede ser bloqueado de forma inmediata administrando aminofilina.
Se administra a una dosis estándar de 140 microgr/kg/min durante 4-6 minutos.
Aunque la mayoría de los pacientes consigue una correcta respuesta hemodinámica a esta dosis de adenosina,
en ocasiones se puede requerir una estimulación a altas dosis,
con un máximo descrito de 210 microgr/ kg/ min.
En nuestra experiencia no ha sido necesario aumentar la dosis en ningún caso.
En ocasiones,
cuando se genera una respuesta rápida y estable al fármaco (controlado por la taquicardización),
se puede reducir el tiempo de infusión.
La literatura refiere que entre el 28-65% de los pacientes muestran sintomatología secundaria,
generalmente leve,
mientras que en el 2-8% se debe interrumpir la prueba.
Tras revisar nuestros casos,
el 60 % presentaron sintomatología,
siendo el dolor torácico el síntoma más frecuente.
Únicamente se tuvo que interrumpir la prueba en 2 pacientes,
uno por bloqueo A-V (requirió administración de atropina) y otro por dolor torácico intenso.
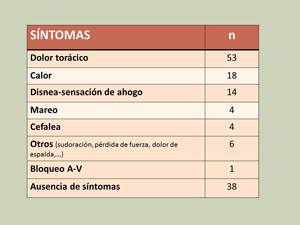
Fig. 3
La tensión arterial tiende a disminuir,
generalmente de forma no significativa,
aunque en ocasiones hemos tenido que administrar suero fisiológico al interrumpir la adenosina para remontarla.
Esto se ha relacionado con la caída de las resistencias vasculares y con el aumento de la frecuencia cardiaca.
Por último,
hay que tener en cuenta al programar la secuencia que debido al aumento de la frecuencia cardiaca se va a reducir la duración del ciclo cardiaco hasta un 16%,
lo cual va a requerir un ajuste personalizado de los parámetros para cada paciente,
ya que puede reducirse el número de cortes adquiridos por ciclo.
CONTRASTE:
El medio de contraste actúa generando una alteración del campo magnético local que provocará un aumento de la tasa de relajación tisular (protones de agua).
El tiempo de relajación T1 y T2 de estos protones es inversamente proporcional a la concentración local de Gadolinio (Gd).
Así,
áreas bien perfundidas tendrán un T1 corto y aparecerán hiperintensas,
mientras que las zonas hipoperfundidas poseerán un T1 más largo.
La literatura describe la posibilidad de utilizar agentes de contraste extracelular e intravascular,
ambos con una precisión diagnóstica similar.
En todo caso la mayoría de las revisiones se basan en el estudio de primer paso de un bolus de contraste Gd-DTPA (extracelular).
En cuanto a la dosis,
se debe administrar la mínima cantidad de Gd necesaria para conseguir un adecuado contraste,
ya que la concentración del bolus se ha asociado con la aparición del artefacto en anillo subendocárdico.
Así,
la literatura describe la administración de 0.05-0.1 mmol/kg a 3-6 ml/seg.
En nuestra experiencia,
comenzamos administrando un bolus de Gd-DTPA de 0.05mmol/ kg a 5 ml/seg.
Dado que el paso de contraste por las cavidades era excesivamente rápido (lo ideal es que tarde 15-20 segundos en pasar por las cámaras cardiacas),
aumentamos la dosis y disminuimos la velocidad.
Actualmente,
de forma estándar administramos 0.07mmol/kg a 4 ml/seg,
seguido de 30 cc de suero fisiológico a la misma velocidad,
siempre supeditado a las características del paciente.
EQUIPO Y PROTOCOLO:
Para la realización de los estudios de perfusión miocárdica se requiere:
- Equipo de alto campo.
- Gradientes rápidos y potentes.
- Bobinas de superficie multicanal (utilización de técnicas en paralelo).
- Sincronización cardiaca.
- Secuencias,
software y postprocesado específico.
La utilización de equipos de 3T,
al aumentar la relación de la señal y del contraste /ruido mejora la imagen de perfusión, permitiendo una mejor diferenciación entre miocardio perfundido - no perfundido.
A pesar de ello, la presencia de inhomogeneidades de campo, mayor efecto T2* y susceptibilidad a artefactos,
limitan actualmente su utilización.
Todos nuestros estudios se han realizado en un equipo de 1.5 T (Magnetom Avanto),
utilizando bobina de superficie multicanal y sincronización cardiaca.
El paciente permanece monitorizado durante toda la prueba ( ECG,
frecuencia cardiaca,
TA y PO2).
El protocolo utilizado:
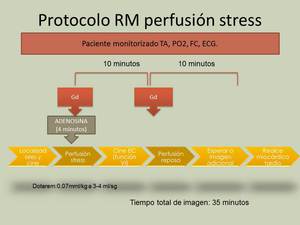
Fig. 4
SECUENCIAS
La imagen de perfusión cardiaca ha experimentado un desarrollo significativo desde sus inicios hace más de 20 años.
La secuencia utilizada tendrá repercusión en el contraste de la imagen, la resolución y la cobertura.
Además influirá en la presencia de artefactos.
Su objetivo es estudiar la distribución del agente de contraste en el miocardio durante el primer paso tras la administración del bolus.
Para ello,
los requisitos básicos de la secuencia de perfusión miocárdica serán:

Fig. 5
El grosor de corte de la secuencia es típicamente de 5-10 mm,
con una resolución en plano de 1.5 a 3 mm.
En función de la resolución,
del FOV y del uso de factor de aceleración, el tiempo de adquisición de cada corte varía entre 50 y 200 ms.
Para ello se requieren secuencias ultra-rápidas: SR-GRE,
SR-EPI ó SSFP (TrueFISP).
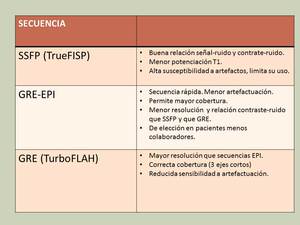
Fig. 6
La secuencia SSFP permite una mejor relación señal/ruido que las GRE pero es más susceptible a artefactos,
por lo que los actualmente las secuencias GRE son la base de la mayoría de protocolos (aunque no existe un claro consenso en cuanto a la secuencia a utilizar).
En nuestra Unidad,
de forma estándar utilizamos la secuencia GRE,
limitando el uso de la EPI a aquellos pacientes poco colaboradores.
ARTEFACTO EN ANILLO SUBENDOCÁRDICO:
La presencia de artefactos en la imagen de perfusión miocárdica es un factor limitador para la aceptación clínica.
Aunque existen otros propios de este tipo de exploraciones, de particular relevancia es el denominado anillo subendocárdico.
Consiste en la aparición de un anillo hipointenso transitorio a nivel subendocárdico en algunos pacientes,
que puede simular un área hipoperfundida.
Su origen no está aclarado siendo varios los mecanismos involucrados:
- Movimiento cardiaco.
- Concentración del bolus de contrate.
- Anillo de Gibbs
- Falta de uniformidad del espacio K
- Cancelación por volumen parcial entre miocardio – sangre
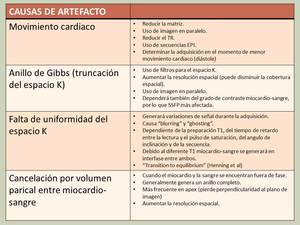
Fig. 7
VER CINE,
Artefacto en anillo subendocárdico de predominio basal.
Fila superior perfusión de estrés,
fila inferior perfusión en reposo.
Fig. 8
ANÁLISIS - INTERPRETACIÓN DE LOS ESTUDIOS:
Existen diferentes métodos para el análisis de la perfusión miocárdica:
- Cuantitativo.
- Semicuantitativo.
- Cualitativo.
Todos ellos han demostrado en estudios previos una buena y similar correlación con la coronariografía (técnica considerada patrón oro).
Nos centramos en el método cualitativo,
por ser el más ampliamente referido en la literatura,
y el utilizado en nuestra Unidad.
Algoritmo clásico:
En 2006,
Klem estableció un algoritmo diagnóstico consistente en realizar una correlación visual entre el realce tardío (RT) - perfusión de estrés - perfusión de reposo.
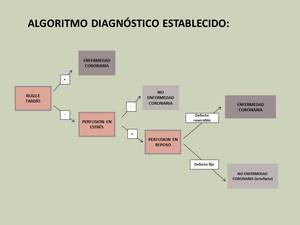
Fig. 9
References: klem et al, JACC 2006
Así,
siguendo el algoritmo:
- Un estudio positivo para isquemia mostrará las siguientes características:
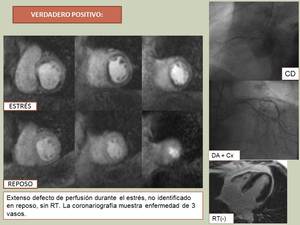
Fig. 10
VER CINE,
fila superior perfusión estrés,
fila inferior reposo,
cortes basal-medio-apical.
Fig. 11
- Un estudio negativo no mostrará defecto de perfusión en estrés ni reposo.
- El artefacto se visualizará como un defecto fijo,
en estrés y reposo.
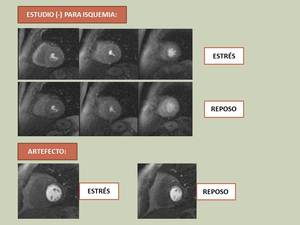
Fig. 12
En nuestra experiencia,
la principal limitación de este algoritmo radica en la interpretación de los artefactos.
El artefacto en anillo subendocárdico es más patente durante la perfusión en estrés que durante el reposo,
visualizándose en ocasiones únicamente en el estrés,
por lo que puede simular un defecto de perfusión isquémico.
Este hallazgo ha sido previamente descrito en la literatura y se ha relacionado al incremento de la frecuencia cardiaca que provoca la adenosina,
ya que generará mayor artefacto de movimiento y una mayor concentración del bolus de contraste.
Además en la perfusión de reposo,
el contraste miocardio- sangre es menor,
debido a la existencia de contraste residual del 1º bolus.
Esto conlleva la necesidad de seguir una curva de aprendizaje basada en la utilización de unos criterios de lectura sistemáticos,
en la concordancia interobservador y en la correlación con la coronariografía.
Los criterios de lectura propuestos por la literatura:

Fig. 13
De éstos,
el más útil en la práctica sería la duración del defecto.
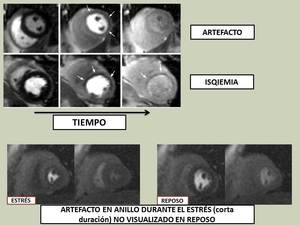
Fig. 14
Infarto-Cardiopatía isquémica:
El comportamiento del infarto de miocardio en los estudios de perfusión es variable.
Esto posiblemente sea debido a diferentes factores,
como pueden ser la revacularización y los diferentes estadíos en maduración del tejido cicatricial.
Según los algoritmos clásicos,
el infarto se puede comportar como un defecto de perfusión fijo con realce en el estudio de viabilidad o bien sin traducción en el estudio de perfusión miocárdica con posterior realce en la viabiliadad.
En nuestra experiencia,
con el protocolo previamente descrito (1º perfusión de estrés,
2º de reposo) el patrón más frecuentemente objetivado consiste en un defecto de perfusión “reversible”, con realce en el estudio de viabilidad.
Este fenómeno de “reversibilidad" es debido a la difusión del contraste del 1º bolus hacia el espacio intersticial del segmento infartado,
que dificulta la visualización del defecto en reposo.
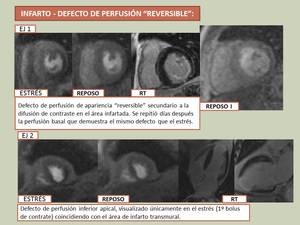
Fig. 15
Se ha planteado la posibilidad de cambiar el protocolo realizando la perfusión en reposo antes que el estrés.
EL problema en estos casos radicaría en que el contraste residual del 1º bolus podría dificultar la visualización de pequeños focos de isquemia durante el estrés.
En pacientes con cardiopatía isquémica (definida como un descenso de la FE -<50%- en presencia de enfermedad coronaria severa,
y englobando fisopatológicamente un amplio espectro,
desde el miocardio hibernado hasta la cicatriz miocárdica irreversible),
el valor de la detección de isquemia es controvertido,
ya que de momento no hay datos concluyentes de hasta que punto la presencia de ésta tiene valor predictivo.
Existen diversos estudios con conclusiones dispares,
hallazgo explicable por el pequeño tamaño de las muestras en estos estudios y la utilización de diferentes métodos de imagen (PET,
Eco,..) para su estudio.
Sí queda establecido que en pacientes con cardiopatía isquémica,
con enfermedad coronaria estable sintomática y FE preservada,
la revascularización parece beneficiosa únicamente si existe isquemia significativa.
Así la perfusión en estos casos podría identificar a aquellos pacientes con alto riesgo infarto/fallo cardiaco / muerte cardiaca.
La isquemia puede aparecer en contigüidad a un área infartada (isquemia peri-infarto) ó en otro territorio vascular.
Isquemia peri-infarto:
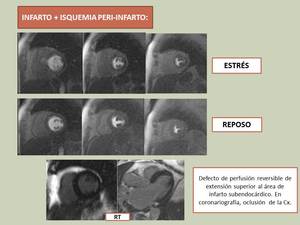
Fig. 16
VER CINE,
fila superior estrés,
fila inferior reposo.
Fig. 17
Infarto e isquemia en otro territorio:
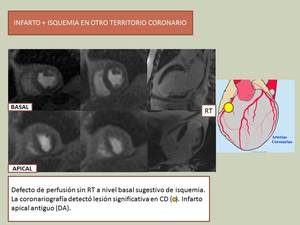
Fig. 18
Cardiopatía hipertrófica:
Los estudios de perfusión tienen un papel establecido en la cardiopatía hipertrófica (CMH).
Ésta es la enfermedad genética cardiaca más frecuente,
con una prevalencia de 1:500,
que se caracteriza por una gran heterogeneidad en la expresión fenotípica y evolución clínica.
Es la causa más frecuente de muerte súbita en gente joven y una causa mayor de fallo cardiaco a cualquier edad.
La isquemia miocárdica es un hallazgo establecido en la MCH.
Se ha demostrado una disminución del flujo coronario (reserva coronaria) en estos pacientes,
de predominio subendocárdico con respecto al epicardio y correlacionado con el grosor mural.
Su presencia parece asociada con la aparición de complicaciones,
incluyendo el remodelado adverso y disfunción sistólica.
Las causas de isquemia en esta patología son múltiples:
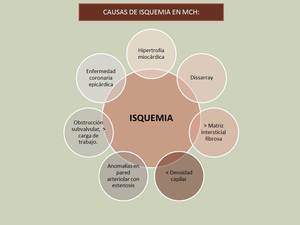
Fig. 19
La enfermedad coronaria epicárdica es uno de los posibles mecanismos de isquemia en pacientes con CMH,
por lo que puede ser difícil determinar así cual es su causa (lesión coronaria ó disminución del flujo coronario por lesión microvascular).
En estos casos puede resultar de ayuda el TC coronario dentro de la valoración no invasiva.
La RM permite detectar defectos de perfusión,
además de hipertrofia y fibrosis (Realce Tardío).
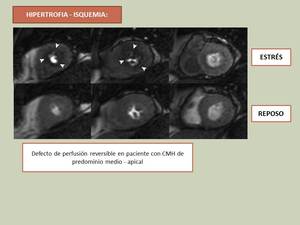
Fig. 20
References: Chun et al , Radiographics 2010
Es estos casos es necesaria una valoración conjunta de la perfusión con el resto de secuencias,
especialmente con el realce tardío ya que, áreas de inflamación/fibrosis miocárdica se pueden comportar como un defecto de perfusión durante el estrés que,
por difusión del contraste del 1º bolus hacia el espacio intersticial del segmento afecto,
no se visualiza en la perfusión en reposo y puede simular isquemia (similar a lo descrito en el infarto).
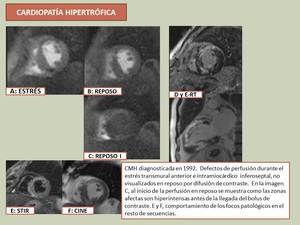
Fig. 21
VER CINE, Fila superior estrés,
fila media reposo,
inferior cine,
basal-medio-apical.
Fig. 22
Falsos (+) de la CRM estrés vs Falsos (-) de la coronariografía:
Se han descrito diversas situaciones en las que puede existir defecto de perfusión sin enfermedad coronaria.
Síndorme X:
La definición más aceptada de este síndrome incluye dolor torácico de características coronarias,
prueba de esfuerzo positiva (descenso típico del segmento ST) y arterias coronarias angiográficamente normales.
Además,
se deben excluir causas extracardíacas de dolor torácico,
espasmo coronario,
hipertensión arterial (HTA) e hipertrofia ventricular.
Su fisiopatología abarca diferentes mecanismos que parecen variar de paciente a paciente.
- Disfunción endotelial microvascular - isquemia
- Alteración de la percepción del dolor cardíaco
- Alteraciones metabólicas del músculo cardíaco
- Hiperfuncionamiento de la bomba Na+/H+
- Aumento del tono simpático
Generalmente afecta a mujeres y aunque previamente se consideraba que era una entidad benigna,
actualmente se considera que la disfunción microvascular tiene mal pronóstico.
El patrón característico en el estudio de perfusión en estrés consiste en un defecto de perfusión en forma de anillo subendocárdico,
sin respetar territorios coronarios.
Enfermedades sistémicas:
Se han descrito anomalías de perfusión miocárdica en el 40% de las mujeres afectas de lupus eritematoso sistémico,
con coronarias normales y sin disfunción ventricular,
secundarios a lesión microvascular.
En la esclerodermia también se ha descrito su presencia por la misma causa.
En estos casos,
el defecto tampoco respeta territorios coronarios,
pudiendo incluso ser circunferencial.
Arterias coronarias de pequeño calibre:
Se han descrito asimismo defectos de perfusión miocárdica en pacientes con arterias coronarias de pequeño calibre ,
siendo así una posible causa de “falso” (+).
En estos casos el defecto de perfusión se suele localizar en la cara diafragmática,
ya que la irrigación coronaria en la superficie costoesternal cardiaca suele ser constante.
























