Las miocardiopatías son un conjunto de enfermedades cuyo denominador común en la disfunción del músculo miocárdico por causas que le afectan directamente.
Han sido clasificadas atendiendo a sus características clínicas,
morfológicas e histológicas.
Desde el punto de vista de la imagen la clasificación morfofenotípica de de la European Society of Cardiology (ESC) es la más práctica.
Aunque la ecocardiografía es la técnica inicial de estudio,
el protagonismo que está adquiriendo la cardioRM y la angioTCMD de arterias coronarias en la valoración de las mismas hacen imprescindibles su conocimiento por parte de los radiólogos.
En primer lugar describiremos nuestras herramientas: las secuencias de cardioRM,
reseñando su aportación y valor en el estudio cardiaco.
En segundo lugar,
se realiza una breve descripción de las características epidemiológicas y clínicas de las distintas miocardiopatías,
se expone con amplia iconografía los hallazgos más relevantes para el diagnóstico y,
por último,
se destaca el valor diagnóstico de las distintas secuencias de cardioRM en el estudio de las mismas.
NUESTRAS HERRAMIENTAS: LAS SECUENCIAS DE CARDIO-RM.
Secuencias cineSSFP (secuencias de cine tipo precesión libre en estado estacionario:FIESTA,
Balanced-FFE,
TrueFISP según casa comercial).
En planos cardiacos habituales (2C,
4C,
Eje Corto) para el estudio funcional del corazón.
Secuencias STIR (short tau inversión recovery) sangre negra y FSE T1,
T2. Recomendables ante alteraciones segmentarias de la contractilidad o ante la sospecha de afectación infiltrativa,
inflamatoria o isquémica aguda,
para detectar el edema miocárdico (área hiperintensa).
Secuencias en “sangre negra” (SE) y “sangre blanca” (eco-gradiente), en planos ortogonales del tórax para el examen anatómico.
Mapas de flujo (con codificación de velocidad o de contraste de fase). Para el estudio funcional de las válvulas cardiacas tanto en el plano valvular como a través de plano.
También permite la valoración de estenosis vasculares ó curvas de flujo en cualquier vaso,
así como en las cámaras cardiacas.
Estudio de perfusión miocárdica. Tras administración de un bolo de contraste intravenoso,
mediante una secuencias de inversión-recuperación.
Secuencia que valora la presencia de defectos de perfusión,
sobre todo en el contexto isquémico,
aunque no exclusivamente.
(vídeo 1).
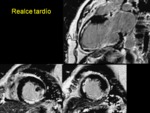
Realce tardío del miocardio. Se basa en el uso de contraste de gadolinio,
que difunde rápidamente al espacio intersticial pero no al intracelular.
En el miocardio sano el espacio intersticial es muy pequeño por la gran compactación de los sarcómeros.
En cambio,
existe una gran concentración de gadolinio tanto en el IAM agudo por la pérdida de integridad de las membranas,
como en el IAM crónico o en cualquier patología en que exista fibrosis infiltrativa por la presencia de tejido fibrótico,
menos compacto que el miocardio.
Además,
existe una cinética de lavado del contraste más lenta en las zonas necróticas (figura 2).
Antes de lanzar la secuencia se espera un tiempo entre 5-10 minutos para permitir el acúmulo de gadolinio en el miocardio dañado.
Para la técnica de realce tardío se usa una secuencia de eco de gradiente potenciada en T1 y con una preparación de la magnetización (pulso 180º para suprimir la señal del miocardio sano).
Para información más detallada recomendamos la presentación electrónica “Optimización en la adquisición de estudios de cardioRM: protocolo gráfico”.
NUESTRO OBJETIVO DE ESTUDIO: LA MIOCARDIOPATÍAS.
Hemos estudiado los siguientes procesos:
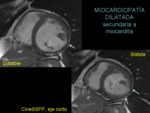
MIOCARDIOPATÍA DILATADA (MCD)
La miocardiopatía dilatada (MCD) se caracteriza por una dilatación biventricular progresiva con pérdida de la función contráctil (figura 3,
figura 4).
Es fundamental establecer la causa subyacente de esta disfunción ventricular (tabla 5).
Algunas causas pueden identificarse a partir de la historia clínica y pruebas de laboratorio.
Debe diferenciarse la MCD idiopática de la secundaria a enfermedad coronaria,
de peor pronóstico y que puede beneficiarse de técnicas de revascularización.
La ecografía permite su diagnóstico y monitorización,
pero no puede establecer su etiología.
La cardioRM,
además de dar información exacta y reproducible sobre la morfología y función cardiaca,
permite: (1) diagnosticar la existencia de una etiología isquémica y diferenciarla de otras causas secundarias (inflamatorias) según el patrón de realce tardío,
(2) en pacientes sin un patrón de realce tardío isquémico hace innecesario el estudio de las arterias coronarias,
(3) es un examen eficaz para el seguimiento y la valoración de la respuesta al tratamiento y (4) el tipo de realce tardío es un factor pronóstico.
Así,
se ha descrito la presencia de un realce mesomiocárdico en segmentos medios del VI en el 30% de estos pacientes en relación a fibrosis miocárdica y mal pronótico.
Miocardiopatía dilatada idiopática frente a miocardiopatía isquémica.
Ante un paciente con disfunción ventricular siempre se plantea la posibilidad de que sea de origen isquémico.
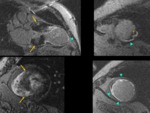
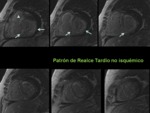
La secuencia de realce tardío del miocardio tras administración de gadolinio permite diferenciar el patrón isquémico (realce subendocárdico o transmural que sigue un territorio coronario y defectos de perfusión en la misma localización) de los pacientes con patología coronaria frente al patrón no isquémico (realce con distintos patrones como el mesocárdico,
subepicárdico,… que no siguen un territorio vascular y estudio de perfusión miocárdica normal) que puede verse en pacientes con disfunción ventricular y coronarias sanas (figura 6).
Asimismo,
el estudio de perfusión miocárdica es normal en pacientes con MCD no isquémica mientras que muestra defectos de perfusión en la misma localización que el realce subendocárdico en las de origen isquémico.
Además,
ante la sospecha de una miocardiopatía dilatada destacaremos que las secuencias morfológicas FSE T1,
T2 y STIR (short tau inversión recovery) son recomendables en el caso de que se identifiquen alteraciones segmentarias de la contractilidad o que se sospeche afectación infiltrativa o inflamatoria,
para detectar el edema miocárdico (zona hiperintensa) (figura 7).
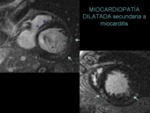
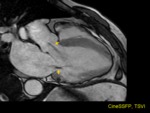
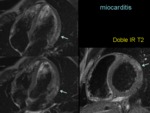
MIOCARDITIS
Proceso inflamatorio del miocardio con múltiples agentes causales (ver tabla).
Suele ser asintomática o presentarse habitualmente por síntomas menores.
Aunque la mayoría de los casos se resuelve de forma espontánea,
un 5-10% evolucionan a miocardiopatía dilatada.
Dada la escasa sensibilidad de la biopsia endomiocárdica –técnica de referencia- por la distribución focal de la enfermedad,
el diagnóstico se realiza en base a alteraciones electrocardiográficas,
ecocardiográficas (disfunción del VI) y séricas (aumento de la creatincinasa o de la troponina T).
Se emplea la cardio-RM para el dtco y seguimiento de esta patología dado que permite cuantificar la disfunción del VI y detecta el edema y la fibrosis miocárdica.
Las secuencias potenciadas en T2 o STIR permiten detectar la hiperintensidad de señal del edema miocárdico: único parámetro que se correlaciona con los parámetros séricos y que desaparece con la curación (figura 8).
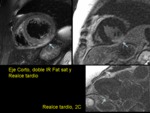
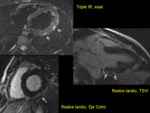
Las secuencias de realce tardío permiten la detección de áreas de daño miocárdico irreversible que muestran un patrón no isquémico que afecta típicamente la porción subepicárdica de la cara lateral del VI de forma multifocal (figura 9).
Este realce focal en la fase aguda,
se hace difuso y menos intenso en un período de semanas o meses,
pudiendo persistir áreas de realce tardío en la fase crónica que representan áreas de fibrosis.
Esta secuencia sirve de guía para la biopsia.
MIOCARDIOPATÍA RESTRICTIVA (MCR)
Patología poco frecuente,
casi siempre idiopática,
aunque puede tener un origen genético o ser secundaria a enfermedades sistémicas (tabla 10).
Algunas causas son tratables cuando su diagnóstico es precoz.
Se caracteriza por un llenado ventricular restringido (disfunción diastólica) (video 11) con ventrículos pequeños o normales con función sistólica preservada.
Existe una dilatación de las dos aurículas con presencia de trombos de forma frecuente e insuficiencia de las válvulas auriculoventriculares.
El ventrículo izquierdo de tamaño y función sistólica normal,
puede mostrar un aumento del grosor miocárdico y de la masa ventricular.
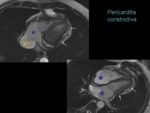
El principal diagnóstico diferencial es con la pericarditis constrictiva (figura 12).
La ecografía permite su estudio de forma global mientras que la cardioRM es superior en el diagnóstico diferencial con la pericarditis constrictiva y ayuda a caracterizar las enfermedades por depósito que pueden condicionar un patrón restrictivo.
Algunos patrones característicos:
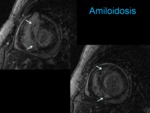
Amiloidosis
Es una causa frecuente de miocardiopatía restrictiva.
La infiltración miocárdica por proteína fibrilar produce una pérdida de la distensibilidad con alteración de la función diastólica y posteriormente sistólica que puede producir la muerte poco tiempo después de la aparición de insuficiencia cardiaca.
La ecografía muestra un patrón en “cristal molido”.
La cardioRM al igual que la ecografía muestra las alteraciones morfológicas y funcionales propias de esta entidad: el engrosamiento miocárdico difuso,
la pérdida de la función sistólica,
el engrosamiento del tabique interauricular y de las tres valvas auriculoventriculares (vídeo 13).
Además,
se observa un patrón de realce difuso leve que no sigue ningún territorio coronario,
que puede ser transmural,
parcheado o difuso “en cebra” (figura 14).
Este patrón de realce se acompaña de una cinética de gadolinio anormal que dificulta encontrar el tiempo de inversión adecuado en las secuencias de realce tardío de miocardio.
Ante la sospecha de amiloidosis cardiaca se recomienda valorar la viabilidad miocárdica a los tres minutos de la administración del contraste en lugar de a los 5-10 minutos habituales.
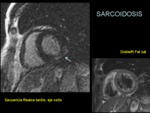
Sarcoidosis
Aunque la afectación cardiaca en la sarcoidosis no es muy frecuente,
la muerte súbita puede ser la forma de presentación y por ello,
es importante el diagnóstico precoz.
La ecocardiografía puede demostrar el patrón restrictivo típico,
pero no los granulomas sarcoideos que tienen una distribución parcheada.
La cardioRM puede detectarlos,
determinar su evolución temporal y servir como guía de la biopsia (figura 15).
En la fase inflamatoria los granulomas son hiperintensos en T2 y muestran realce tardío,
siendo la pared libre del VI y el septo interventricular las localizaciones más frecuentes.
En las fases inactivas son hipointensos en todas las secuencias debido a la fibrosis.
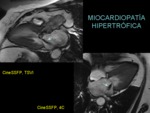
MIOCARDIOPATÍA HIPERTRÓFICA (MCH)
La miocardiopatía hipertrófica es una enfermedad familiar de penetrancia variable con una prevalencia de 1/500 en adultos (tabla 16).
En la mayoría de los casos suele desarrollarse durante la pubertad y presenta una distribución asimétrica con afectación predominante del septo interventricular.
La mayoría de los pacientes permanecen asintomáticos y sin complicaciones.
En una baja proporción de pacientes la primera manifestación de la enfermedad es la muerte súbita secundaria a arritmia ventricular por la presencia de fibrosis y desorganización miofibrilar.
En otros casos existe una rápida evolución a insuficiencia cardiaca severa.
Se han descrito varios marcadores clínicos de mal pronóstico.
La técnica de primera elección en el estudio de un paciente con sospecha de MCH es la ecografía-Doppler que confirma o descarta la sospecha y determina la severidad y la distribución de la hipertrofia.
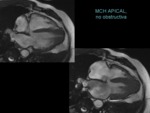
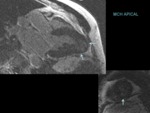
La cardioRM es superior a la ecografía en la identificación del patrón de distribución de la hipertrofia del VI visualizando regiones que a veces no son visibles ecográficamente como el ápex (figura 17 y figura 18).
Actualmente está aceptada como patrón de referencia en la cuantificación de la masa del miocardio del VI y es la técnica de elección en la monitorización de los ensayos clínicos por la escasa variabilidad intra- e interobservador.
Además,
la secuencia de realce tardío miocárdico permite la detección de la cicatriz miocárdica.
Por último,
las secuencias de cineSSFP identifican flujos turbulentos que permiten diagnosticar la obstrucción al flujo en el tracto de salida del VI (vídeo 19).
Un gradiente de presión > 30 mmHg en el tracto de salida del VI también se ha asociado a un mayor riesgo de muerte cardiaca: las secuencias de contraste de fase pueden calcular este gradiente.
Detección de fibrosis miocárdica: realce tardío del miocardio.
El 50-80% de los pacientes con MCH muestran algún tipo de realce tardío del miocardio.
Existen distintos patrones de distribución.
Uno de los más frecuentes es una distribución parcheada en los segmentos medios del VI con una afectación característica de las zonas de unión del ventrículo derecho con el izquierdo.
Algunos autores identifican como de buen pronóstico.
Por otro lado,
la presencia de una extensa fibrosis con un patrón multifocal o difuso parece indicar una mala evolución (figura 20 y figura 21).
Otra de las aplicaciones de la valoración de la viabilidad miocárdica es el control del resultado de la ablación septal,
al identificarse el área exacta donde se ha producido la necrosis por dicho tratamiento.
Diagnóstico diferencial en la MCH
El hallazgo de una hipertrofia ventricular obliga a descartar posibles causas,
algunas potencialmente tratables.
Las secuencias de cineSSFP y las de mapa de velocidades permiten descartar una valvulopatía aórtica.
Además la cardioRM es la técnica de elección en el estudio de la coartación de aorta gracias al cálculo de la circulación colateral aplicando secuencias de mapa de velocidad en la aorta descendente.
Por último,
la valoración del patrón del realce tardío miocárdico permite el diagnóstico de algunas enfermedades por depósito que muestran un patrón de distribución característico (captación tardía difusa de predominio subendocárdico en la amiloidosis (figura 22),
típico realce tardío no subendocárdico en la cara lateral inferobasal en la enfermedad de Anderson-Fabry,...)
Por todo ello,
la cardioRM es indicación clase I en la MCH apical y clase II en los demás fenotipos de miocardiopatía hipertrófica.
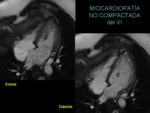
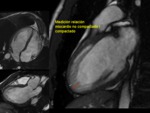
MIOCARDIOPATÍA NO COMPACTADA del VI (MCNC)
La miocardiopatía no compactada es un defecto de la embriogénesis que causa una detención del proceso de compactación miocárdica.
Ello condiciona una morfología muy característica,
diferenciándose dos capas: una delgada subepicárdica (compactada) y una gruesa subendocárdica (no compactada,
con múltiples recesos y trabeculaciones).
La mayor parte de los pacientes asocia un mal pronóstico evolucionando a insuficiencia cardiaca severa,
tromboembolismos y/o arritmias malignas.
El diagnóstico de esta entidad se base en criterios morfológicos: miocardio grueso donde se distinguen dos capas y una proporción entre la capa no compactada / compactada > 2.3 en la telediástole (figura 23),
asociado a (1) apariencia similar en paciente de primer grado,
y/o (2) complicaciones relacionadas con esta enfermedad (embolismo sistémico,
anomalías de la contractilidad segmentaria,…)
Las secuencias cine-SSFP dan imágenes con alta resolución espacial con alto contraste entre la sangre y el miocardio,
permitiendo distinguir la zona compactada de la no compactada con sus recesos y trabeculaciones (figura 24).
Además la cardioRM permite detectar las áreas de fibrosis miocárdica (realce tardío) y la presencia de isquemia subendocárdica (estudio de perfusión miocárdica).
La cardioRM es el método de elección para el dtco de la miocardiopatía no compactada del VI.
Permite un correcto estudio morfológico,
el cálculo de volúmenes,
fracción de eyección y valorar fibrosis miocárdica.
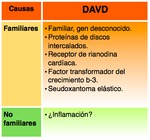
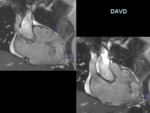
DISPLASIA ARRITMOGÉNICA DEL VENTRÍCULO DERECHO (DAVD)
Miocardiopatía hereditaria rara (incidencia 1:5000 individuos),
difícil de diagnosticar,
que es una causa frecuente de muerte súbita en jóvenes (tabla 25).
La DAVD muestra una afectación específica del miocardio del ventrículo derecho (VD) con atrofia de éste que es reemplazado por tejido adiposo o fibroadiposo causante de las arritmias ventriculares e insuficiencia cardiaca derecha progresiva.
Puede debutar con palpitaciones,
síncope,
arritmias o parada cardiaca.
El diagnóstico debe realizarse mediante análisis genético molecular que es caro y poco extendido.
Por ello,
la ESC propuso unos criterios diagnósticos (tabla 26) que se han mostrado insuficientes en la detección de las formas iniciales o leves de la enfermedad.
Las técnicas de imagen son esenciales para el reconocimiento de las alteraciones estructurales de la DAVD,
siendo la cardioRM la técnica de elección ya que permite detectar la grasa y la fibrosis parietal,
así como las alteraciones estructurales y funcionales.
Además,
parece más sensible que los criterios de la Task Force de la ESC en el diagnóstico de las fases iniciales.
Alteraciones estructurales y disfunción global y/o regional
El ventrículo derecho (VD) se encuentra dilatado de forma global o segmentaria (dilatación del tracto de salida del VD) y muestra una hipocinesia regional con buena relación con las áreas de reemplazo fibrograso.
Hay un incremento de los volúmenes telediastólico y telesistólico del VD por la dilatación ventricular y disminución de la fracción de eyección del VD (85% de los casos).
Evaluación fiable y reproducible mediante secuencias cineSSFP (vídeo 27).
Se detectan aneurismas del VD y trabeculaciones prominentes de localización típica en el “triángulo de la displasia” (región infundibular,
pared posteroinferior o área subtricuspídea y pared anteroapical o ápex del VD).
Indicador específico de fallo sistólico (FEVI < 40%) (figura 28).
Puede haber adelgazamiento del grosor miocárdico de la pared libre del VD (67% de los casos).
La detección de este hallazgo tiene una gran variabilidad por el escaso grosor de la pared libre del VD.
Por ello,
se recomienda el uso de secuencias "sangre negra" doble-IR con alta resolución espacial. Algunos autores recomiendan la valoración parietal durante la sístole a pesar de los artefactos por el latido.
Alteraciones tisulares
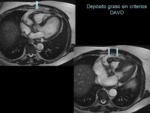
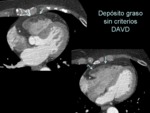
El hallazgo más característico es la hiperintensidad miocárdica de la pared libre del VD que indica la presencia de tejido adiposo.
Este hallazgo tiene varias limitaciones: (1) es difícil caracterizar la infiltración patológica cuando está localizada en áreas donde suele estar presenta la grasa epipericárdica (ej.
surco auriculoventricular),
(2) una importante infiltración grasa del VD ocurre en ancianos y en sujetos con obesidad mórbidad (“síndrome de disociación grasa” con escasa arritmogenicidad) (figura 29 y figura 30) y,
(3) la detección de cambios grasos es muy dependiente de la calidad de la imagen. Las secuencias con saturación grasa o triple-IR pueden ayudar a la detección de la grasa parietal.
También se puede detectar fibrosis miocárdica como áreas de realce tardío.
Existe una clara relación entre la localización y severidad de la disfunción ventricular y la extensión del realce miocárdico.
SÍNDROME DE TAKO TSUBO (MIOCARDIOPATÍA DE STRESS)
Disfunción sistólica,
regional y transitoria,
del ápex o de los segmentos medios del VI en ausencia de miocardiopatía isquémica.
Suele afectar a mujeres posmenopáusicas que presentan un cuadro (clínico,
electrocardiográfico y enzimático) similar a la angina o al IAM precedido por un importante estrés emocional o físico.
Este cuadro se normaliza en días o semanas y no suele recurrir.
El diagnóstico se realiza en urgencias con ecocardiografía y angiografía invasiva.
La cardioRM es útil en el seguimiento y suele mostrar la dilatación transitoria del ápex con hipercontractilidad basal (secuencias cineSSFP) (vídeo 31).
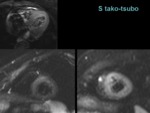
En la fase aguda,
las secuencias sangre negra potenciadas en T2 detectan el edema miocárdico: áreas hiperintensas en los segmentos con alteración de la contractilidad (figura 32).
Este edema se relaciona con el grado de disfunción sistólica.
La ausencia de áreas de realce tardío ayuda a diferenciarla de la miocarditis y de la miocardiopatía isquémica.