En la búsqueda bibliográfica del tema encontramos únicamente series cortas ó case report.
El potente servicio de oncohematología de nuestro hospital nos ha permitido recoger una casuística de 14 casos hasta la fecha de manifestaciones inusuales de este tipo de patologías,
que exponemos,
junto con una revisión bibliográfica de cada una de ellas.
| GRUPOS DE PATOLOGÍAS: |
|
1.
NEOPLASIAS DE CÉLULAS PLASMÁTICAS:
- Mieloma extraóseo
- Leucemia de células plasmáticas
- Plasmocitoma extramedular
2. LINFOMA NO HODGKIN (LNH):
- LNH intravascular con afectación pulmonar
- LNH yeyunal
- Linfoma linfoplasmocítico o Macroglobulinemia de Waldenstrom
- Linfoma no Hodgkin con afectación de glándulas de cabeza y cuello
- Linfoma tiroideo con diseminación pleural
3. LINFOMA DE HODGKIN (LH)
4.
LEUCEMIA AGUDA:
- Leucemia aguda linfoide T (LAL T)
- leucemia aguda mieloide (LAM)
5.
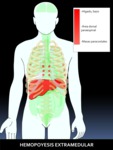
HEMATOPOYESIS EXTRAMEDULAR
6.
HISTIOCITOSIS:
- ENFERMEDAD DE ERDHEIM-CHESTER
- HISTIOCITOSIS DE CÉLULAS DE LANGERHANS (HCL)
|
GRUPO 1: NEOPLASIA DE CÉLULAS PLASMÁTICAS.
Este grupo representa un espectro de enfermedades formado por el mieloma múltiple (MM),
el plasmocitoma solitario óseo,
el plasmocitoma extramedular (PEM) y la leucemia de células plasmáticas (1). Se originan en las células B y son consideradas manifestaciones diferentes de la misma enfermedad.
Sus manifestaciones se solapan y no existen unos límites claramente establecidos entre ellas.
El MM está mayoritariamente confinado la médula ósea y sus manifestaciones clínicas están relacionadas principalmente con la infiltración medular y la destrucción ósea.
Sin embargo,
la afectación extramedular (sin continuidad ósea) en el MM es frecuente.
El plasmocitoma extramedular difiere de otras formas de mieloma en que las lesiones primarias surgen fuera de la médula ósea.
MIELOMA MÚLTIPLE (MM).
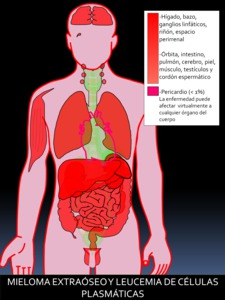
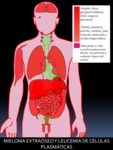
Fig. 1: Figura 1. Grado de afectación de órganos extraóseos en el MIELOMA EXTRAÓSEO Y EN LA LEUCEMIA DE CÉLULAS PLASTMÁTICAS, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
El diagnóstico se realiza ante la presencia de más de un 10% de células plasmáticas en la médula ósea ó de un plasmocitoma probado por biopsia,
o bien,
en presencia de uno de esos criterios junto con paraproteína en suero u orina,
lesiones óseas radiolucentes u osteoporosis generalizada.
MM CON EXTENSIÓN EXTRAÓSEA Y HALLAZGOS RADIOLÓGICOS:
En las series de autopsias del MM,
la afectación extraósea a distancia del hueso fue encontrada en el 60-70% de los pacientes (1,2) pero la detección clínica o radiológica de las manifestaciones extraóseas se da en aproximadamente el 10-16% de los casos,
habiendo aumentado el porcentaje de detección en las últimas décadas gracias a la mejora de los métodos de imagen y al incremento de la supervivencia de los pacientes con MM.
La extensión extraósea se asocia con un peor pronóstico (acortamiento de la supervivencia global y de la supervicencia libre de progresión) (2).
Por ello,
es importante la detección precoz de la afectación extraósea en el seguimiento de estos pacientes,
para lo cual las técnicas de imagen juegan un importante papel.
Varios investigadores han comprobado índices más altos de recaída extraósea de la enfermedad después de un transplante de médula ósea,
como en nuestro caso,
siendo más frecuente en pacientes jóvenes y en subtipos agresivos de MM,
lo que sugiere que esas localizaciones extraóseas sirven como “santurario” de la enfermedad activa (2).
La extensión extraósea puede afectar virtualmente a cualquier órgano,
y los hallazgos de imagen son inespecíficos y pueden simular otras patologías.
Radiológicamente suelen manifestarse como masas de partes blandas con densidad homogénea en el TC,
carentes de necrosis ni de calcificación,
con baja señal en secuencias potenciadas en T2 en RM por su alta celularidad e hipercaptantes en el FDG PET.
MANIFESTACIONES ATÍPICAS EN NUESTRA CASUÍSTICA: MM con extensión extraósea,
usual e inusual:
- nódulos circunscritos hipervasculares en el espacios perirrenal y senos renales(figuras 2,
3 ,4 y 5).
- masa paravertebral en un foramen intervertebral dorsal (figuras 2 y 3).
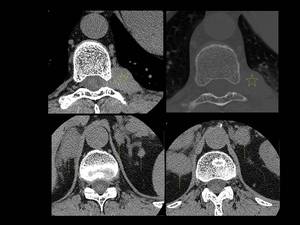
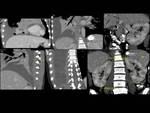
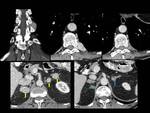
Fig. 2: Figura 2. Hombre, 54 años. Mieloma múltiple en remisión completa.
TC de columna dorsal:
Masas foraminal y paravetebral(estrellas) yperirrenal (flechas) detectadas incidentalmente en el TC de columna dorsal, sin afectación ósea asocida, que fueron estudidadas posteriormente mediante TC con contraste iv (ver figura 2).
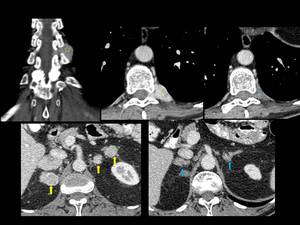
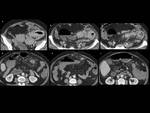
Fig. 3: Figura 3. Hombre, 54 años. Mieloma múltiple en remisión completa.
TC abdominal: nódulos hipervasculares circunscitos situados en el espacio perirrenal (flechas amarillas) y en los senos renales (flechas vacías) y masas foraminales y paravertebrales (estrellas amarillas). La afectación mejoró tras el tratamiento (flecha azul y estrella azul).
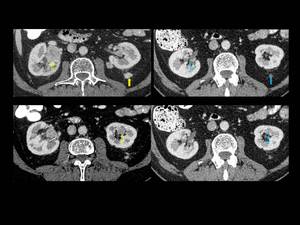
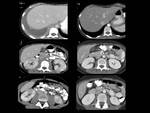
Fig. 4: Figura 4. Hombre, 54 años. Mieloma múltiple en remisión completa.
TC abdominal: nódulos hipervasculares circunscitos situados en el espacio perirrenal (flechas amarillas) y en los senos renales (flechas vacías) y masas foraminales y paravertebrales (estrellas amarillas). La afectación mejoró tras el tratamiento (flecha azul y estrella azul).
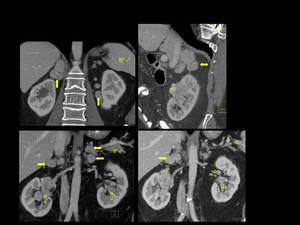
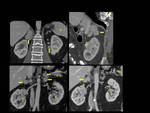
Fig. 5: Figura 5. Hombre, 54 años. Mieloma múltiple en remisión completa.
TC abdominal con reconstrucciones sagital y coronal: masas perirrenales (flechas amarillas), en el seno renal (flechas vacías) e hidronefrosis (flecha blanca vacía) secundaria a una de las masas del seno renal.
Los lugares más frecuentes de afectación extraósea son el sistema retículo endotelial y el riñón:
-Sistema retículo endotelial: hígado (lesiones hipodensas,
hipocaptantes e hipoecogénicas,
únicas o múltiples o,
más frecuentemente,
afectación difusa),
bazo (aisladamente o coexistente con la afectación hepática) y ganglios linfáticos (masas nodales grandes y homogéneas; generalmente están afectadas varias estaciones ganglionares) (2).
-Riñón: afectación difusa (más frecuente (1,2)) o masas renales focales y/o masas perirrenales,
como en nuestro caso.
La afectación perirrenal,
frecuente también en el linfoma y en la hematopoyesis extramedular,
puede deberse a la actividad de células angiohematopoyéticas primitivas en esa localización,
"santuario" de enfermedad activa.
El diagnóstico diferencial incluye también metástasis (melanoma,
etc) y carcinoma de células transicionales (3).
-Otras posibles estructuras abdominales afectadas:
- masas omentales,
mesentéricas y retroperitoneales.
- intestino: masas murales o intraluminales generalmente homogéneas,
lobuladas y excéntricas.
- páncreas: afectación focal o multifocal.
-Afectación torácica: pulmón (nódulos/masas parenquimatosas ó infiltración intersticial) o pleura (simula metástasis pleurales o mesotelioma).
-SNC y afectación de cabeza y cuello: extensión leptomeníngea,
epidural o plasmocitomas en las partes blandas con predilección por la cavidad nasal y la nasofaringe.
-Miscelánea: tejido celular subcutáneo,
músculos,
testículos y cordón espermático.
LEUCEMIA DE CÉLULAS PLASMÁTICAS (LCP). (Fig. 1).
La leucemia de células plasmática puede ser diagnosticada en pacientes con MM (el MM con evolución a LCP supone el 40% de los casos de LCP (4) ó en pacientes sin los criterios diagnósticos de MM sistémico (5).
La LCP es la neoplasia de células plasmáticas más infrecuente y supone sólo el 2-3% del grupo de MM.
Tiene un curso agresivo,
pobre respuesta al tratamiento y supervivencia corta.
Existe extensión extramedular en el 10% de los casos (4).
La afectación ganglionar es frecuente.
La LCP puede ser difícil de distinguir de otras neoplasias y de la proliferación reactiva de células plasmáticas.
MANIFESTACIONES EXTRAÓSEAS Y HALLAZGOS RADIOLÓGICOS:
En series cortas de casos de MM con evolución a LCP (5),
las masas de células plasmáticas fueron localizadas en pelvis,
tórax,
cuello y en columna lumbar.
La literatura al respecto de esta entidad es escasa.
MANIFESTACIONES ATÍPICAS EN NUESTRA CASUÍSTICA: MM con progresión a LCP,
con afectación de (la afectación fue similar al MM con extensión extraósea,
descrita previamente):
- Plasmocitoma orbitario: plasmocitomas intraconales bilaterales y extraconal derecho,
con erosión ósea.
Estas masas son bien definidas,
pueden ser lobuladas,
moderadamente hiperdensas en el TC comparándolas con el parénquima cerebral e hipercaptantes,
pudiendo dar lugar a erosión ósea (3) como en nuestro caso:
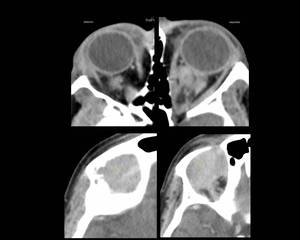
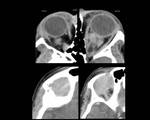
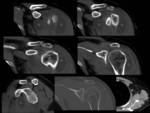
Fig. 6: Figura 6. Mujer, 49 años. MM con evolución a leucemia de células plasmáticas.
TC de órbitas: masas densamente hipercaptantes bilaterales intraconales (estrellas negras) y derecha extraconal (con erosión ósea (estrellas amarillas), correspondientes a plasmocitomas.
- Adenopatías mediastínicas:

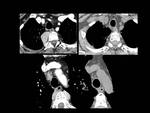
Fig. 7: Figura 7. Mujer, 49 años. MM con evolución a leucemia de células plasmáticas.
TC de tórax: masas paravertebrales (flecha amarilla) y adenopatías mediastínicas (estrella amarilla) de nueva aparición, que mejoraron tras el tratamiento (flecha azul).
3.
Masas paravertebrales hipervasculares (ver también la Fig. 7):
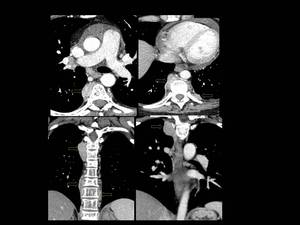
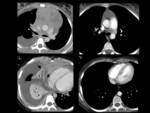
Fig. 8: Figura 8. Mujer, 49 años. MM con evolución a leucemia de células plasmáticas.
TC de tórax: masas paravertebrales (flechas amarillas) y derrame pericárdico (triángulo blanco). Reconstrucciones coronales (imágenes inferiores).
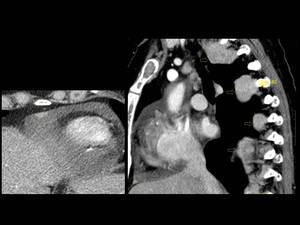
Fig. 9: Figura 9. Mujer, 49 años. MM con evolución a leucemia de células plasmáticas.
TC de tórax: realce pericárdico focal (círculo amarillo), derrame pericárdico (triángulo blanco) y masas hipervasculares paravertebrales (flechas amarillas).
4.
Afectación pericárdica ( Fig. 9 ).
5.
Afectación perirrenal:
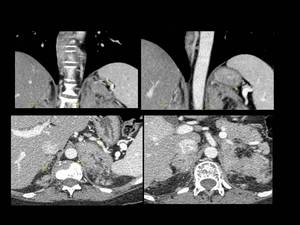
Fig. 10: Figura 10. Mujer, 49 años. MM con evolución a leucemia de células plasmáticas.
TC de tórax: afectación perirrenal (flechas amarillas) en imágenes coronales (superiores) y axiales (inferiores). El paciente también tenía derrame pleural (no mostrado).
6.
Masa hipervascular en el hilio hepático.
Se han reportado masas hepáticas con realce periférico o con relleno gradual hacia el centro de la lesión (1).
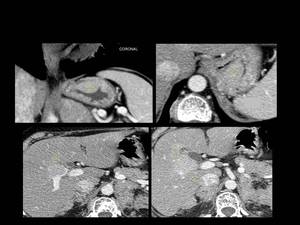
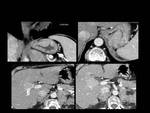
Fig. 11: Figura 11. Mujer, 49 años. MM con evolución a leucemia de células plasmáticas.
TC de tórax: masa sólida gástrica intramural (estrella amarilla) en planos coronal y axial (imágenes superiores) y masa hipervascular (flecha amarilla) en el hilio hepático (imágenes inferiores).
7.
Masa sólida intramural gástrica ( Fig. 11 ).
PLASMOCITOMA EXTRAMEDULAR (PEM).
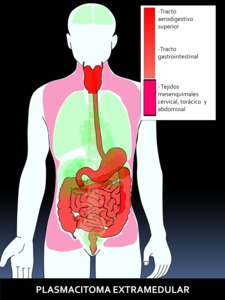
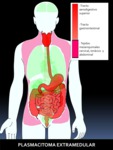
Fig. 12: Figura 12. Grado de afectación de órganos extraóseos en el PLASMOCITOMA EXTRAMEDULAR, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
El plasmocitoma primario,
óseo o extraóseo,
requiere la exclusión del MM (ausencia de hipercalcemia,
insuficiencia renal y anemia,
normalidad en el estudio de la serie ósea,
ausencia de plasmocitosis en la médula ósea y niveles de paraproteína en suero y orina menor a 2 g/dl) (1,3).
Representan aproximadamente el 3-4 % del grupo de las neoplasias de células plasmáticas (1,3).
Se dan en la 6ª-7ª década de vida y predominan en varones.
El PEM puede ser solitario o múltiple.
El plasmocitoma solitario tiene buen pronóstico (3),
mejor que el del MM.
La detección de plasmocitomas múltiples,
recurrentes o de lesiones de nueva aparición pueden influenciar el manejo del PEM,
pues pueden implicar la necesidad de asociar quimioterapia sistémica o transplante autólogo de progenitores hematopoyéticos (3).
Por todo ello es importante detectar y diferenciar el PEM (solitario o múltiple) del mieloma extraóseo.
LOCALIZACIÓN EXTRAÓSEA Y HALLAZGOS RADIOLÓGICOS:
Aproximadamente el 80% del PEM se da en el tracto gastrointestinal (GI) superior (1,3) con predilección por cabeza y cuello.
Sin embargo,
pueden darse en cualquier órgano,
incluyendo ganglios linfáticos,
piel,
mediastino,
pulmón,
corazón,
mama (3),
peritoneo,
tracto gastrointestinal,
vejiga,
páncreas,
adrenales,
riñones,
afectación perirrenal o periureteral (6) y vagina (1,3).
El tracto GI es la estructura abdominal más frecuentemente afectada,
manifestándose generalmente como una masa focal,
isointensa al músculo (3) con moderado o marcado realce,
homogéneo (1) o heterogéneo (3).
Se asocia generalmente con destrucción o infiltración de estructuras adyacentes (3).
MANIFESTACIONES ATÍPICAS EN NUESTRO CASO:
Plasmocitoma extramedular con localización y hallazgos radiológicos muy inusuales.
Nuestro paciente acude al hospital por masa cervical.
La rareza de esta infrecuente entidad es aun mayor en nuestro caso,
existiendo infiltración difusa del tejido mesenquimal a nivel cervical (ver figura 13 y 14),
pleural - extrapleural (figura 15 y 16),
retroperitoneal y pélvico (ver figura 17 y 18).
Los antecedentes personales del paciente son para la clave para el diagnóstico (neoplasia de células plasmáticas) y el diagnostico final fue de plasmocitoma extramedular,
con una biopsia de médula ósea negativa.
No hemos encontrado esta manifestación de enfermedad en la literatura actual,
como tal.
Entre los 11 casos de una serie corta (1),
existe únicamente un caso de plasmocitoma extramedular que se manifiesta como una masa infiltrativa retroperitoneal simulando linfoma y entre los 21 casos de otra corta (3),
existe un solo caso con infiltración pleural secundariamente desde un plasmocitoma pulmonar.
La infiltración retroperitoneal y periureteral se ha reportado pero los hallazgos radiológicos fueron masas de partes blandas hipercaptantes inespecíficas en el TC y la RM (6),
manifestación radiológica diferente a la de nuestro caso.
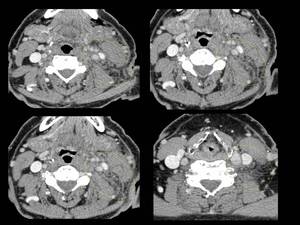
Fig. 13: Figura 13. Hombre, 67 años. Masa cervical a estudio.
TC cervical: infiltración difusa con efecto de masa de la grasa cervical alrededor de los vasos carotídeos y del espacio cervical posterior izquierdo (círculos amarillos) con afectación de la fascia cervical superficial y del múculo platisma del cuello.
Biopsia de la infiltración cervical, pleural y pélvica: presencia de células plasmáticas monotípicas kappa; ausencia de tejido amiloide; biopsia de la médula ósea: muy escasas y reactivas células plásmáticas, sin criterios de invasión neoplásica; proteinuria en orina: 0,09 g/dl; pruebas de medicina nuclear: ausencia de captación ósea; captación en las regiones del cuello afectadas en el TC. Diagnóstico final: plasmocitoma extramedular.
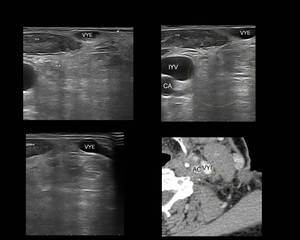
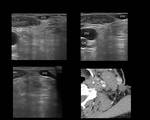
Fig. 14: Figura 14. Hombre, 67 años. Masa cervical a estudio.
Ecografía cervical: alteración estructural de la grasa del espacio cervical posterior con atenuación acústica posterior (área entre cursores) y correlación con el TC cervical (círculo amarillo)
“ECM”: músculo esternocleidomastoideo; “AC”: arteria carótida; “VYI”: vena yugular interna; “VYE”: vena yugular externa.
Biopsia de la infiltración cervical, pleural y pélvica: presencia de células plasmáticas monotípicas kappa; ausencia de tejido amiloide; biopsia de la médula ósea: muy escasas y reactivas células plásmáticas, sin criterios de invasión neoplásica; proteinuria en orina: 0,09 g/dl; pruebas de medicina nuclear: ausencia de captación ósea; captación en las regiones del cuello afectadas en el TC. Diagnóstico final: plasmocitoma extramedular.
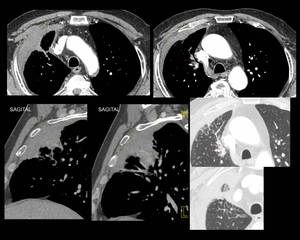
Fig. 15: Figura 15. Hombre, 67 años. Masa cervical a estudio.
TC de tórax: engrosamiento pleural/extrapleural con extensión al segmento anterior del LSD; engrosamiento del intersticio axial y del intersticio periférico adyacente.
Biopsia de la infiltración cervical, pleural y pélvica: presencia de células plasmáticas monotípicas kappa; ausencia de tejido amiloide; biopsia de la médula ósea: muy escasas y reactivas células plásmáticas, sin criterios de invasión neoplásica; proteinuria en orina: 0,09 g/dl; pruebas de medicina nuclear: ausencia de captación ósea; captación en las regiones del cuello afectadas en el TC. Diagnóstico final: plasmocitoma extramedular.
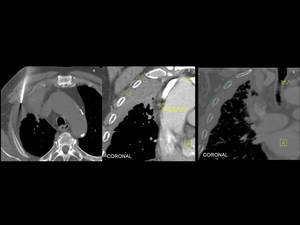
Fig. 16: Figura 16. Hombre, 67 años. Masa cervical a estudio.
TC de tórax: biopsia de la lesión torácica (a). Reconstrucciones coronales (b y c): engrosamiento pleural/extrapelural (flechas amarillas) no originado en el hueso, que no está afectado (flechas azules en la imagen c).
Biopsia de la infiltración cervical, pleural y pélvica: presencia de células plasmáticas monotípicas kappa; ausencia de tejido amiloide; biopsia de la médula ósea: muy escasas y reactivas células plásmáticas, sin criterios de invasión neoplásica; proteinuria en orina: 0,09 g/dl; pruebas de medicina nuclear: ausencia de captación ósea; captación en las regiones del cuello afectadas en el TC. Diagnóstico final: plasmocitoma extramedular.
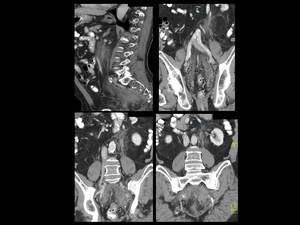
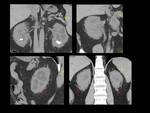
Fig. 17: Figura 17. Hombre, 67 años. Masa cervical a estudio.
TC abdominal con reconstrucciones sagitales(imágenes superiores) y coronales (imágenes inferiores): infiltración difusa con efecto de masa de la grasa perirrenal izda, fascia renal, grasa retroperitoneal ipsilateral (flechas azules), espacios presacro y mesorrectal y fascia mesorrectal (flechas blancas).
Biopsia de la infiltración cervical, pleural y pélvica: presencia de células plasmáticas monotípicas kappa; ausencia de tejido amiloide; biopsia de la médula ósea: muy escasas y reactivas células plásmáticas, sin criterios de invasión neoplásica; proteinuria en orina: 0,09 g/dl; pruebas de medicina nuclear: ausencia de captación ósea; captación en las regiones del cuello afectadas en el TC. Diagnóstico final: plasmocitoma extramedular.
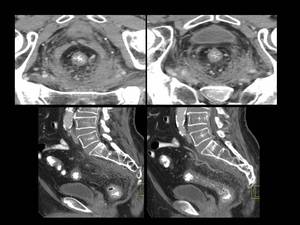
Fig. 18: Figura 18. Hombre, 67 años. Masa cervical a estudio.
TC abdominal axial (imágenes superiores) y reconstrucciones sagitales (imágenes inferiores): infiltración difusa con importante efecto de masa de los espacios presacro, mesorrectal y de la fascia mesorrectal (flechas blancas).
Biopsia de la infiltración cervical, pleural y pélvica: presencia de células plasmáticas monotípicas kappa; ausencia de tejido amiloide; biopsia de la médula ósea: muy escasas y reactivas células plásmáticas, sin criterios de invasión neoplásica; proteinuria en orina: 0,09 g/dl; pruebas de medicina nuclear: ausencia de captación ósea; captación en las regiones del cuello afectadas en el TC. Diagnóstico final: plasmocitoma extramedular.
MORALEJA en la neoplasia de células plasmáticas: en pacientes con neoplasia conocida de células plasmáticas,
una masa de partes blandas focal o una infiltración difusa,
incluso existiendo solapamiento con manifestaciones de otras enfermedades,
debería considerarse sospechosa de mieloma con manifestación extraósea (en particular en el pacientes con trasplante de médula ósea).
Además,
ante manifestaciones radiológicas atípicas en cualquier paciente,
hemos de investigar acerca de posibles antecedentes personales de neoplasias de estas características.
Grupo 2.
Linfoma no Hodgkin.
Existe una mayor incidencia de enfermedad extranodal y de afectación de la médula ósea en el linfoma no Hodgkin que en el linfoma de Hodgkin.
Las localizaciones extranodales que pueden afectarse son hueso,
sistema nervioso central,
leptomeninges,
glándulas parótidas,
tiroides,
hígado (lesiones focales,
aumento de tamaño del hígado),
tracto gastrointestinal,
páncreas,
tracto genitourinario,
retroperitoneo,
mesenterio,
pulmón,
pleura (masas pleurales sólidas,
derrame pleural primario),
pared torácica y mama (7,8,9).
Son afectados más frecuentemente en pacientes inmunodeprimidos (7).
El tracto gastrointestinal es la localización extranodal frecuente (20% los casos).
Es más frecuente en pacientes VIH positivo.
Tanto el linfoma primario como el sistémico con afectación del tracto gastrointestinal afectan al estómago en un gran porcentaje casos (50%).
Las masas linfomatosas en el TC son lesiones hiperdensas sin contraste ( debido a la hipercelularidad) y homogéneas e hipodensas con contraste intravenoso.
MANIFESTACIONES ATÍPICAS EN NUESTROS CASOS: afectación de órganos inusuales y por variantes inusuales de LNH:
- Linfoma no Hodgkin intravascular (angiotrópico).
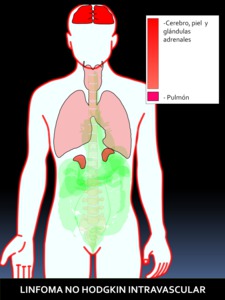
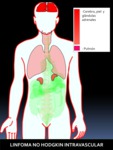
Fig. 19: Figura 19. Grado de afectación de órganos extraóseos en el LINFOMA NO HODGKIN INTRAVASCULAR, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
Supone menos de 1% en todos los linfomas no Hodgkin.
Se caracteriza una proliferación intravascular (pequeños vasos) de células linfomatosas B.
Tiene mal pronóstico.
El orden afectación de órganos es cerebro,
piel,
adrenales y,
a veces,
pulmón (10),
pero esto último es raro.
Hallazgos radiológicos de afectación pulmonar (10) (figuras 20 y 21):
- engrosamiento intersticial interlobulillar e intralobulillar: es el hallazgo predominante.
- opacidades extensas en vidrio deslustrado,
a veces de distribución peribronquial (11).
Se deben también a engrosamiento intersticial.
Esta manifestación puede solapase con manifestaciones como hemorragia,
edema o infarto asociadas a émbolos pulmonares,
aunque se ha visto que los espacios alveolares están prácticamente intactos en series autópsicas de linfoma intravascular pulmonar.
- nódulos centrilobulillares con atenuación en vidrio deslustrado
- estenosis de venas pulmonares.
- escasas adenopatías asociadas.
- normal: tanto la radiografía de tórax como el TC pueden no mostrar anomalías (12).
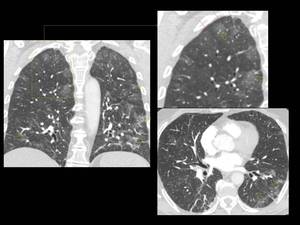
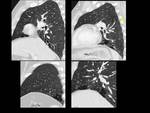
Fig. 20: Figura 20. Hombre de 70 años, con disnea y fiebre.
TC de tórax: engrosamiento intersticial interlobulillar (flechas rojas) y extensas opacidades parcheadas en vidrio deslustrado (flechas amarillas) algunas de las cuales tienen una distribución peribroncovascular (imagen sagital).
Biopsia de la piel, transbronquial, de médula ósea y hepática: LNH B de célula grande intravascular.
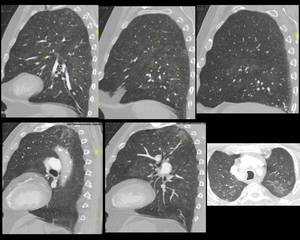
Fig. 21: Figura 21. Hombre de 81 años, con disnea de un mes de evolución.
TC de tórax: extensas opacidades parcheadas bilaterales en vidrio deslustrado (flechas amarillas) con nódulos de aspecto centroacinar en vidrio deslustrado a nivel de LLSS (flechas rojas).
Biopsia transbronquial: LNH intravascular.
2.
Linfoma no Hodgkin yeyunal en paciente VIH negativo.
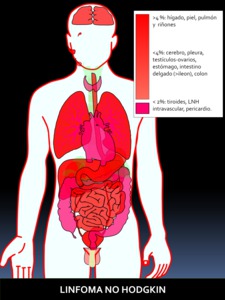
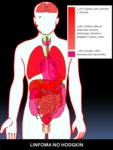
Fig. 22: Figura 22. Grado de afectación de órganos extraóseos en el LINFOMA NO HODGKIN, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
Los linfomas primarios del tracto gastro intestinal son menos comunes pero tienen mejor pronóstico que la enfermedad sistémica con afectación gastrointestinal.
El linfoma gastrointestinal primario afecta al tracto gastrointestinal y a las adenopatías confinadas al área de drenaje del tumor primario (ver figura 23),
sin afectación esplénica ni hepática,
ni adenopatías palpables ,
con radiografía de tórax normal y recuento de células blancas normal (9).
Suponen el 0,9% de todos los tumores del tracto gastrointestinal (9).
En raras ocasiones,
ciertos tipos de linfoma que generalmente se presenta como enfermedad sistémica (foliculary linfocítico B de célula grande,
como en su caso) puede aparecer como un linfoma primario del tracto gastrointestinal,
los cuales se dan principalmente en el intestino delgado distal,
especialmente en el íleon terminal.
Hallazgos radiológicos en el TC (figura 23):
Área segmentaria de engrosamiento circunferencial y asimétrico excéntrico de la pared del intestino,
con atenuación homogénea tanto sin como con contraste ,
sin rarefacción de de la grasa adyacente (13).
Los patrones descritos de infiltración en el linfoma B de célula grande,
son el polipoideo (nódulos único o múltiples),
el infiltrante (engrosamiento marcado,
homogéneo y circunferencial de la pared y dilatación aneurismática),
el endoexoentérico (ulceración y fístulización) y la forma invasiva mesentérica.
La forma endoexoentérica (figura 23),
como en nuestro caso,
puede causar engrosamiento intestinal y ulceraciones,
pudiendo fistulizar a otras vísceras o formar tractos sinusales hacia el mesenterio,
con formación de abscesos estériles.
El TC puede mostrar extensión extraluminal del contraste oral dentro de la cavidad,
la cual a menudo contiene líquido y debris.
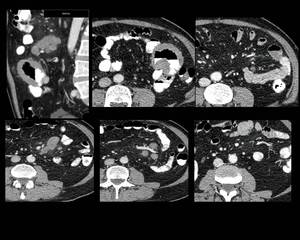
Fig. 23: Figura 23. Hombre de 70 años. Anemia ferropénica. VIH negativo. Ausencia de hepatoesplenomegalia.
Reconstrucciones sagitales e imágenes axiales de TC abdominal: engrosamiento mural segmentario ulcerado yeyunal (forma endoexocéntrica de linfoma) (flechas blancas), con adenopatías adyacentes (círculos blancos). Ambos hallazgos mejoraron tras el tratamiento (flecha y círculo azul respectivamente).
Biopsia intestinal (yeyunal): LNH B de célula grande. Biopsia de médula ósea: normocelular.
El diagnóstico diferencial incluye el GIST cavitado o las metástasis (9),
especialmente de melanoma.
3.
Linfoma linfoplasmocítico o Macroglobulinemia de Waldenstrom, con afectación renal,
perirrenal y retroperitoneal al diagnóstico (Fig. 22):
La Macroglobulinemia de Waldenstrom es un linfoma de bajo grado compuesto de linfocitos plasmocitoides maduros que produce IgM monoclonal e infiltración de la médula ósea.
Representa sólo el 1,5-2% de los linfomas no Hodgkin.
La afectación retroperitoneal es muy rara en la macroglobulinemia de Waldenstrom (6).
El tracto genitourinario esta raramente afectado en la presentación en el LNH (7),
afectándose más frecuentemente en el LNH avanzado (14).
Hallazgos radiológicos: patrones de afectación renal en el linfoma (figura 24):
- infiltración renal difusa
- masas renales múltiples
- invasión renal desde la afectación retroperitoneal contigua (probable patrón de afectación en nuestro caso): frecuentemente se produce por extensión a través de la cápsula renal o a través del seno renal.
Las adenopatías retroperitoneales están invariablemente presentes,
dando lugar en ocasiones a hidronefrosis obstructiva (14).
- masas solitarias
- infiltración perirrenal.
La infiltración perirrenal o capsular está a menudo asociada con masas linfomatosas retroperitoneales ,
como nuestro caso.
El diagnóstico diferencial incluye el hematoma perirrenal.
Las arterias y venas renales permanecen patentes a pesar de estar englobadas por el tumor siendo este un hallazgo característico de linfoma,
como en nuestro caso.
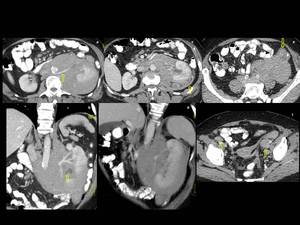
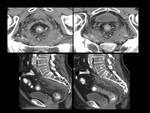
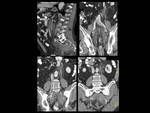
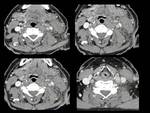
Fig. 24: Figura 24. Mujer, 73 años. Adenopatías cervicales e infiltración de múltiples glándulas de cabeza y cuello, a estudio. VIH negativo.
Invasión renal a partir del conglomerado adenopático retroperitoneal; vena renal no obliterada, a pesar de la estar rodeada por tumor (flecha en a); hidronefrosis obstructiva secundaria (flecha en b); afectación perirrenal (flecha en c); extensión a través del mesocolon izdo (flecha en e); adenopatías pélvicas (flechas en f).
Biopsia de médula ósea: normocelular. Linfoma linfoplasmocítico (Macroglobulinemia de Waldenstrom).
4.
Linfoma no Hodgkin con afectación de glándulas de cabeza y cuello (Fig. 22):
El LNH se presenta con adenopatías cervicales con enfermedad extranodal en aproximadamente el 23-30% de las cadenas.
La única estructura extranodal con mayor frecuencia de afectación que las estructuras de cabeza y cuello es el tracto gastrointestinal.
La afectación extranodal más común en la cabeza y cuello en el anillo de Waldeyer,
con afectación hasta en la mitad los casos.
Las siguientes localizaciones extra nodales por orden de frecuencia son los senos paranasales,
la cavidad nasal,
la laringe,
la cavidad oral,
las glándulas salivares,
el tiroides y la órbita.
El LNH con afectación de cabeza y cuello se da típicamente en pacientes entre 50 y 60 años de edad con una predominancia masculina,
excepto la afectación de glándulas salivares,
órbita y tiroides que es mas frecuente en mujeres (como en nuestro caso de afectación submandibular y tiroidea).
- LNH con supuesta afectación de glándula submandibular (mismo caso del linfoma retroperitoneal y renal) (figura 25).
El linfoma de glándulas salivares es raro,
representando el 2-5% de la neoplasias de glándulas salivales.
La afectación más frecuente es en la glándula parótida (70%),
y la más infrecuente es la de la glándula submandibular (15).
El síndrome de Sjöegren aumenta el riesgo de linfoma de glándula salivar (15).
Hallazgos radiológicos en nuestro caso (figura 25):
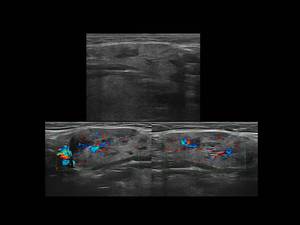
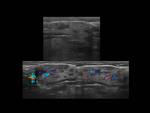
Fig. 25: Figura 25. Mujer, 73 años. Adenopatías cervicales e infiltración de múltiples glándulas de cabeza y cuello, con palpación rígida de glándulas submandibulares y parotídeas, a estudio. VIH negativo.
Ecografía cervical: estructura ecográfica heterogénea de las glándulas submandibulares (y de las parótidas-no mostradas-) con múltiples nódulos hipoecogénicos, sin hiperemia; adenopatías cervicales asociadas (no mostradas).
Biopsia de médula ósea: normocelular. Linfoma linfoplasmocítico (Macroglobulinemia de Waldenstrom).
-LNH con supuesta afectación de glándulas lacrimales (mismo caso del linfoma retroperitoneal y renal).El linfoma con afectación de los anejos oculares es la neoplasia orbitaria más frecuente en adultos mayores de 60 años.
El linfoma orbitario puede afectar la glándula lacrimal,
los músculos extraoculares,
la grasa orbitaria,
los párpados y la conjuntiva.
La localización más común es en el espacio extraconal anterior centrado en el cuadrante supero-temporal,
como en nuestro caso.
La afectación orbitaria se produce en más del 5% de todos los LNH sistémicos.
Hallazgos radiológicos en TC y RM en la afectación orbitaria por el LNH (figura 26): masa de partes blandas que se amolda a las estructuras adyacentes (16),
generalmente con intensidad de señal intermedia en secuencias T1 y T2,
homogénea y con realce moderado,
como nuestro caso.
La erosión ósea en el TC es rara,
siendo sugestiva de linfoma de alto grado cuando está presente (15).
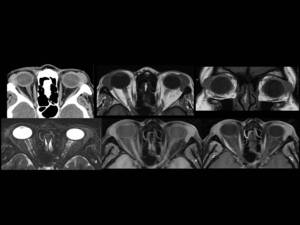
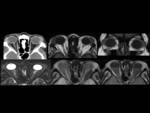
Fig. 26: Figura 26. Mujer, 73 años. Adenopatías cervicales e infiltración de múltiples glándulas de cabeza y cuello, con tumor orbitario izquierdo de crecimiento rápido, a estudio. VIH negativo.
-TC orbitario (a): aumento de tamaño de las glándulas lacrimales (flechas), predominantemente la izquierda, sin erosión ósea.
-RM orbitaria: aumento de tamaño de las glándulas lacrimales (flechas) con intensidad de señal intermedia en T1 (T1 axial en b y T1 coronal en c) y T2 (T2 axial en d) y con mínimo realce (T1 axial sin –e- y con contraste iv-f-).
Biopsia de médula ósea: normocelular. Linfoma linfoplasmocítico (Macroglobulinemia de Waldenstrom).
5.
Linfoma tiroideo con diseminación pleural ( Fig. 22 ).
El linfoma tiroideo primario es una entidad rara que puede ser confundida radiológicamente con el carcinoma tiroideo anaplásico y,
en el pasado,
incluso anatomopatológicamente.
Clínicamente se presenta como una masa cervical a la que puede asociarse disfagia y dificultad respiratoria,
como en nuestro caso.
Se manifiesta como un nódulo tiroideo frío en la gammagrafía.
Es más común mujeres,
entre 70 y 80 años.
Casi el 80% de casos de linfoma tiroideo se asocian con tiroiditis linfocítica crónica (Hashimoto).
Existen dos tipos distintos,
con clínica y pronóstico diferente:
- linfoma asociado al tejido mucoso (MALT) (6-27% los casos): enfermedad linfoproliferativa de bajo grado,
indolente.
- linfoma difuso de célula B grande (70%): curso clínico más agresivo,
mostrando casi en el 60% de los casos,
enfermedad diseminada al diagnóstico,
como en nuestro caso.
Hallazgos radiológicos (figura 27):
- masa con crecimiento rápido,
solitaria,
que simula un carcinoma anaplásico u otro tipo de carcinoma agresivo,
e incluso puede simular un bocio multinodular.
Esta es la manifestación mas frecuente.
El linfoma tiroideo es más homogéneo que el carcinoma tiroideo,
siendo raras las áreas la calcificación y de degeneración quística,
lo que lo distingue del bocio.
- el linfoma raramente se asocia con invasión traqueal,
aunque puede existir un estrechamiento significativo de la vía aérea (15).
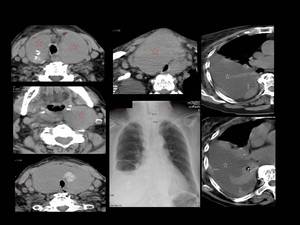
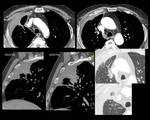
Fig. 27: Figura 27. Mujer de 85 años; no fiebre ni sudoración. Rápido aumento de tamaño del cuello, disfonía y dificultad para respirar. Gran bocio pétreo a la palpación.
TC cervical y torácico sin contraste iv: gran masa hipodensa homogénea (estrellas rojas) con calcificación (probablemente nódulos tiroideos calcificados englobados por la masa actual) y significativo estrechamiento de la vía aérea (flechas negras), con áreas focales derechas de engrosamiento pleural (flechas blancas) y gran derrame pleural derecho (estrellas blancas). Adenopatías cervicales asociadas (círculo).
Análisis anatomopatológico tiroideo tras la cirugía: LNH tiroideo.
MORALEJA en el LNH: a la afectación extranodal por el LNH puede afectar casi a cualquier estructura,
solapándose con múltiples patologías de otro origen.
GRUPO 3: LINFOMA DE HODGKIN (LH) :
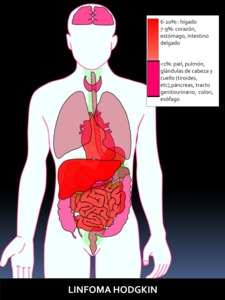
Fig. 28: Figura 28. Grado de afectación de órganos extraóseos en el LINFOMA DE HODGKIN, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
Representa aproximadamente en el 25% de todos los linfomas.
La afectación extranodal es extremadamente rara,
siendo mucho menos común que en el LNH (14,8).
MANIFESTACIONES ATÍPICAS EN NUESTRO CASO: afectación de estructuras muy inusualmente afectadas: LH colónico primario con afectación multisegmentaria,
tipo celularidad mixta.
La mayor parte de los casos de LH con afectación gastrointestinal se dan de forma concurrente con enfermedad generalizada (9,17).
El tracto gastrointestinal es la localización más común de afectación extranodal por el LH,
aunque los casos reportados con afectación gastrointestinal son del 0,5% de la totalidad de LH.
De todos los linfomas gastrointestinales,
solo del 1-1,7% de los casos corresponden a LH.
Otros lugares de afectación extranodal son pulmón,
tiroides,
piel,
sistema nervioso central y tracto genitourinario (17).
El subtipo LH tipo celularidad mixta es el que da lugar más frecuentemente a afectación colónica.
El pronóstico de LH localizado es favorable tras resección quirúrgica (17).
Se han reportado múltiples casos de asociación entre el LH y la enfermedad inflamatoria intestinal (9,17,18,21),
habiendo sido enmascarado el linfoma por la enfermedad de Crohn en la mayoría de los casos reportados (9,17,18,0,20,22,23,2425,26),
como en el nuestro, puesto que ambos tienen similares sintomatología,
hallazgos radiológicos y características endoscópicas,
siendo difícil el diagnóstico histológico del LH (18,21),
requiriendo un análisis inmunofenotípico y genotípico riguroso (21).
Hallazgos radiológicos (figura 29 y figura 30):
Los patrones radiológicos en los pocos casos reportados de LH colónico incluyen masas,
lesiones ulceradas,
engrosamiento de pliegues,
patrón infiltrativo desmoplásico (9) y la asociación con infiltración mesentérica adyacente (17),
como nuestro caso.
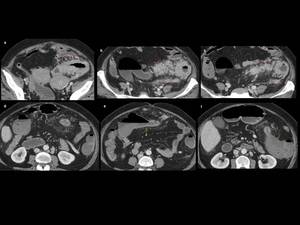
Fig. 29: Figura 29. Mujer, 57 años. Enfermedad de Crohn refractaria al tratamiento con varias recaídas en los últimos meses.
TC de abdomen: engrosamiento segmentario de la pared del colon a nivel de sigma (donde es predominante, con grosor de la pared de 16 mm (flechas blancas en a, b y c), flexura esplénica (flechas blancas en f) y colon transverso (fechas blancas en d) con relativa dilatación colónica entre esos segmentos (flechas amarillas). Se asocia a una extensa infiltración mesentérica, adyacente al sigma (flechas rojas) y adenopatías retroperitoneales (flechas azules). Masa anexial izquierda (estrella).
Análisis anatomopatológico colónico tras la cirugía (hemicolectomía izquierda): L. Hodgkin tipo celularidad mixta con afectación del ovario izdo; infiltración de todas las adenopatías adyacentes resecadas y de una adenopatía pericística.
Biopsia hepática: linfoma de Hodgkin.
Biopsia de médula ósea: ausencia de infiltración.
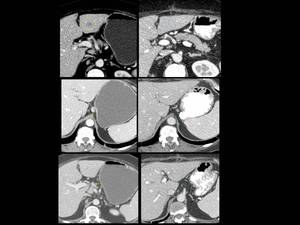
Fig. 30: Figura 30. Mujer, 57 años. Enfermedad de Crohn refractaria al tratamiento con varias recaídas en los últimos meses.
TC abdominal al diagnóstico (izquierda) y tras tres ciclos de QT (derecha): lesión hipodensa focal hepática (círculo amarillo) y adenopatías en el hilio hepático y el ligamento gastrohepático (flechas amarillas); todos esos hallazgos mejoraron tras el tratamiento (círculo y flechas azules).
Análisis anatomopatológico colónico tras la cirugía (hemicolectomía izquierda): L. Hodgkin tipo celularidad mixta con afectación del ovario izdo; infiltración de todas las adenopatías adyacentes resecadas y de una adenopatía pericística.
Biopsia hepática: linfoma de Hodgkin.
Biopsia de médula ósea: ausencia de infiltración.
MORALEJA en el LH: se ha reportado una asociación entre la enfermedad inflamatoria intestinal y el linfoma de Hodgkin colónico,
existiendo un solapamiento entre síntomas,
hallazgos radiológicos y características endoscópicas, así como una dificultad histológica para su detección.
Ante una enfermedad inflamatoria intestinal que no mejora con tratamiento debemos tener en mente esta asociación.
Se requiere un alto nivel de sospecha para llegar a confirmar el diagnóstico de linfoma de Hodgkin concurrente.
GRUPO 4.
LEUCEMIA AGUDA (HALLAZGOS AL DIAGNÓSTICO):
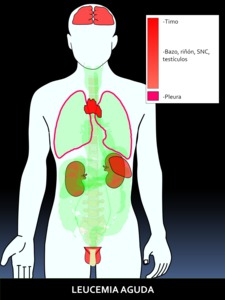
Fig. 31: Figura 31. Grado de afectación de órganos extraóseos en la LEUCEMIA AGUDA, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
La leucemia aguda se clasifica en el leucemia aguda linfoblástica (LAL) y leucemia aguda mieloblástica (LAM).
La leucemia aguda linfoblástica o linfoide y la leucemia aguda mieloblástica o mieloide representan tres cuartos y 1/5 de los casos de leucemias en adolescentes,
respectivamente (27).
La infiltración leucémica de vísceras sólidas,
especialmente del bazo y del timo es común,
y se manifiestan como organomegalia por infiltración difusa o como masas focales.
La infiltración difusa del timo es característica de la leucemia aguda linfoide de células T.
La nefromegalia en la presentación está causada generalmente por infiltración celular leucémica,
pero también puede deberse a trombosis venosa renal por leucostasis intravascular.
Las masas leucémicas renales focales al diagnóstico son generalmente multifocales,
bilaterales,
hipodensas en el TC e hipoecogénicas en la ecografía,
y deben ser diferenciadas del linfoma,
la nefroblastomatosis y la infección.
La infiltración renal se observa más frecuentemente en la leucemia aguda linfoide de células T y en los subtipos M4 y M5 de la leucemia aguda mieloide,
y se acompaña de afectación extramedular en otras localizaciones.
El engrosamiento pleural es frecuente en otros tipos de leucemia,
especialmente en la leucemia mielomonocítica juvenil.
La leucemia extramedular,
también conocida como sarcoma granulocítico o cloroma se define como una masa de células leucémicas fuera de la médula ósea.
Los lugares más frecuentemente afectados son la piel,
órbitas,
SNC y columna,
siendo comúnmente asociada con la leucemia aguda mieloide.
Leucemia aguda linfoide T (LAL T).
La LAL se subclasifica,
según la OMS y en función de su inmunofenotipo,
en LAL B (80-85%) o LAL T (12%).
La LAL T se da en pacientes de mayor edad,
hombres,
con leucocitosis y con presencia de una masa mediastínica (27) (nuestra paciente era una mujer de 14 años).
MANIFESTACIONES ATÍPICAS EN NUESTRO CASO: subtipo inusual de leucemia (LAL T) con afectación pleural (además de tímica y renal):
- afectación pleural al diagnóstico (figura 32,33 y 34): ha sido descrita en escasas ocasiones en el TC,
aunque es encontrada en la biopsia en un significativo porcentaje de los casos (27%) (28,29,30).
Tiene una apariencia inespecífica (28).
El derrame pleural debe ser diferenciado de un proceso infeccioso,
diseminación tumoral de otro origen o de complicaciones por el tratamiento.
Si la manifestación consiste en engrosamiento pleural en forma de placas,
pueden simular mesotelioma o exposición al asbesto.
- afectación mediastínica (timo) con adenopatías (figura 32 y 34).
- afectación renal bilateral (figuras 33 y 34).
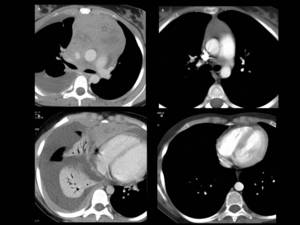
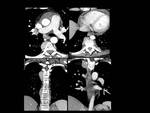
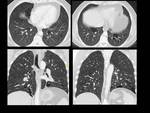
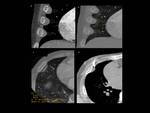
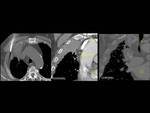
Fig. 32: Figura 32. Mujer, 14 años, diagnóstico de LAL-T.
TC abdominal (parte visible del tórax): gran masa mediastínica anterior, sugestiva de masa tímica (estrella en a), engrosamiento pleural difuso derecho (flechas en b) y derrame pleural derecho en b. Todos los hallazgos mejoraron tra el tratamiento (c y d).
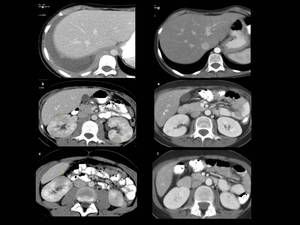
Fig. 33: Figura 33. Mujer, 14 años, diagnóstico de LAL-T.
TC abdominal: engrosamiento pleural difuso (flecha negra en a) y derrame pleural derecho en a. Nefromegalia y masas renales bilaterales multifocales con baja atenuación (flechas amarillas en b y c). Todos los hallazgos mejoraron tras el tto (d-f).
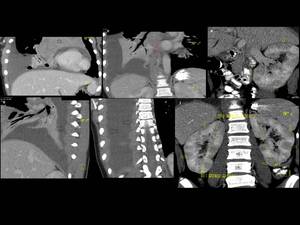
Fig. 34: Figura 34. Mujer, 14 años, diagnóstico de LAL-T.
TC abdominal con reconstrucciones coronal (a, c y d) y sagital (b y e): gran masa mediastínica anterior, sugestiva de masa tímica (estrella); engrosamiento pleural difuso derecho (flechas negras), adenopatías subcarinales (flechas rojas), nefromegalia (f) y masas renales bilaterales multifocales de baja atenuación (flechas amarillas en e y f).
Leucemia aguda mieloide.
MANIFESTACIONES ATÍPICAS EN NUESTRO CASO: afectación extensa difusa pulmonar,
presumiblemente infiltración leucémica,
detectable en la radiografía de tórax.
La infiltración leucémica se detecta en el pulmón en el 24-62% de autopsias de los pacientes fallecidos por leucemia.
Menos del 5% de estos pacientes muestran infiltración leucémica en la radiografía de tórax (31).
El diagnóstico de infiltración leucémica pulmonar causante de fallo respiratorio agudo se basa en estudios histológicos y citológicos así como en la negatividad de hallazgos que apoyen el resto de causas más comunes del esta manifestación clínica.
La presencia de más de un 40% de células blásticas en sangre periférica ha sido sugerido como criterio de sospecha de infiltración leucémica pulmonar (32) (nuestra paciente tenía un 71% de células blásticas).
La confirmación puede realizarse por efectividad inmediata de la quimioterapia en la mejoría de la función respiratoria,
después de un frecuente deterioro inicial secundario a una neumopatía aguda por lisis tumoral (32),
como ocurrió en nuestra paciente,
quien sufrió un síndrome de distrés respiratorio al inicio del tratamiento,
con una mejoría posterior.
Ha sido reportado un aumento de la incidencia de complicaciones pulmonares en pacientes con leucemia aguda mielomonocítica (LAMM) con inversión del cromosoma [inv(16)],
independientemente de la presencia de hiperleucocitosis (33),
inversión presente nuestro caso.
Hallazgos radiológicos en la infiltración leucémica pulmonar y en la leucostasis (probablemente debidos a obstrucción del lecho vascular por células blásticas (31,34,
35).
(Figuras 35,36,37 y 38):
- engrosamiento bilateral del intesticio peribroncovascular (suave o nodular) y del intersticio interlobular (suave,
nodular,
ambos).
Es el hallazgo dominante.
La afectación de los septos interlobulillares estaba presente de todos los casos en una serie de 10 pacientes con esta patología (31).
Este hallazgo se correlaciona con los estudios anatomopatológicos que describen una propensión de las células leucémicas a infiltrar el tejido conectivo peribronquial y peribronquiolar,
y los linfáticos del intersticio peribroncovascular,
septal y pleural (34).
Posteriormente las células pasan las paredes alveolares.
- nódulos parenquimatosos: peribroncovasculares (cuya fisiopatología es la misma que la del engrosamiento intersticial) y centrilobulares.
Presentes entre todos los pacientes,
aunque escasos en número y pequeños.
- áreas de atenuación en vidrio deslustrado y consolidaciones: por confluencia de nódulos centrilobulares mal definidos,
resultando en áreas de consolidación de distribución peribronquial,
probablemente por infiltración por células leucémicas de los espacios aéreos adyacentes.
- placas pleurales leucémicas,
asociadas con derrame pleural.
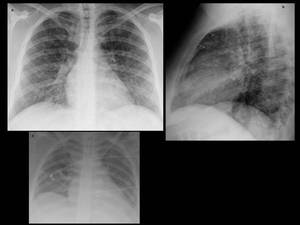
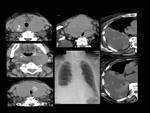
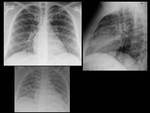
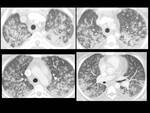
Fig. 35: Figura 35. Mujer, 26 años. Fiebre y hemoptisis.
-Rx de tórax PA y lateral (a-b): opacidades en vidrio deslustrado extensas, bilaterales y nódulos mal definidos de aspecto centroacinar.
-Rx de tórax AP (c) unos días más tarde: mejoría de la afectación parenquimatosa.
LAM con presunta infiltración pulmonar.
-Las técnicas citológicas, citoquímicas e inmunofenotípicas fueron sugestivas de LAM M4Eo.
-Leucocitos:76.4 (18 %N, 16 %L, 67 %M, 0 %E). Blastosis en sangre periférica (70%) y en el aspirado de médula ósea (70%)
-La afectación pulmonar estaba presente al diagnóstico y mejoró tras el tratamiento de la leucemia.
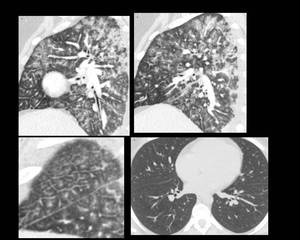
Fig. 36: Figura 36. Mujer, 26 años. Fiebre y hemoptisis.
TC de tórax:
-Engrosamiento suave bilateral del intersticio peribroncovascular (flechas negras) e interlobular (flechas rojas).
-Extensas opacidades en vidrio deslustrado y consolidaciones de distribución peribronquial (probablemente por la confluencia de nódulos centrilobulares mal definidos) (círculo verde).
-Mejoría tras la quimioterapia (d).
LAM con presunta infiltración pulmonar.
-Las técnicas citológicas, citoquímicas e inmunofenotípicas fueron sugestivas de LAM M4Eo.
-Leucocitos:76.4 (18 %N, 16 %L, 67 %M, 0 %E). Blastosis en sangre periférica (70%) y en el aspirado de médula ósea (70%)
-La afectación pulmonar estaba presente al diagnóstico y mejoró tras el tratamiento de la leucemia.

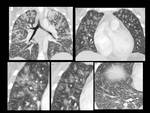
Fig. 37: Figura 37. Mujer, 26 años. Fiebre y hemoptisis.
TC de tórax:
Engrosamento septal interlobular suave bilateral (flechas rojas).
Opacidades nodulares parenquimatosas de distribución centrilobular (flechas amarillas).
Extensas consolidaciones y opacidades en vidrio deslustrado bilaterales (a-b).
LAM con presunta infiltración pulmonar.
-Las técnicas citológicas, citoquímicas e inmunofenotípicas fueron sugestivas de LAM M4Eo.
-Leucocitos:76.4 (18 %N, 16 %L, 67 %M, 0 %E). Blastosis en sangre periférica (70%) y en el aspirado de médula ósea (70%)
-La afectación pulmonar estaba presente al diagnóstico y mejoró tras el tratamiento de la leucemia.
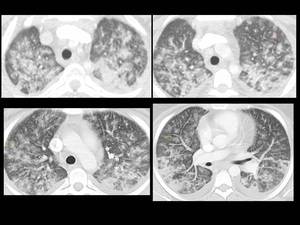
Fig. 38: Figura 38. Mujer, 26 años. Fiebre y hemoptisis.
Engrosamento septal interlobular suave (flecha rojas).
Opacidades nodulares parenquimatosas de distribución centrilobular (flechas amarillas).
Extensas consolidaciones y opacidades en vidrio deslustrado bilaterales.
LAM con presunta infiltración pulmonar.
-Las técnicas citológicas, citoquímicas e inmunofenotípicas fueron sugestivas de LAM M4Eo.
-Leucocitos:76.4 (18 %N, 16 %L, 67 %M, 0 %E). Blastosis en sangre periférica (70%) y en el aspirado de médula ósea (70%)
-La afectación pulmonar estaba presente al diagnóstico y mejoró tras el tratamiento de la leucemia.
Diagnóstico diferencial: toxicidad a drogas,
edema pulmonar,
hemorragia e infección,
las cuales pueden tener apariencias similares.
MORALEJA en la leucemia aguda: la posibilidad de infiltración leucémica debería ser considerada cuando el TC,
entre otros hallazgos,
muestra engrosamiento intersticial en pacientes con leucemia (31).
GRUPO 5.
HEMATOPOYESIS EXTRAMEDULAR :
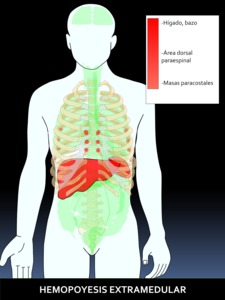
Fig. 39: Figura 39. Grado de afectación de órganos extraóseos en la HEMATOPOYESIS EXTRAMEDULAR, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación.
La hematoyesis es la formación y maduración de elementos sanguíneos.
Cuando los lugares primarios de hematopoyesis (huesos largos,
costillas y vértebras) fallan en el adulto,
como ocurre en las hemoglobinopatías (especialmente en la talasemia,
como en nuestro caso,
y en la anemia de células falciformes),
tejidos extramedulares adquieren esta función,
siendo más frecuente en ciertos órganos como el hígado,
el bazo y las regiones paraespinales del tórax.
Sin embargo,
este proceso puede afectar virtualmente a cualquier tejido (36).
MANIFESTACIONES ATÍPICAS EN NUESTRO CASO: localización inusual: masas paracostales en un caso de beta-talasemia.
Hallazgos radiológicos:
-Hallazgos frecuentes: masas paraespinales (frecuentemente encontradas caudalmente a la 6ª vértebra torácica),
a veces asociadas con masas subpleurales paracostales (descritas en paciente con anemia de células falciformes,
talasemia y enfermedad de Paget).
Los hallazgos radiológicos en el TC (figura 40) son masas bien definidas,
homogéneas,
de bordes suaves y circunscritas; en los casos de afectación costal,
existe un ensanchamiento costal por expansión medular,
expansión y/o elevación perióstica y adelgazamiento cortical,
asociados a la masa adyacente (37).
-Hallazgos infrecuentes: afectación de los espacios pleural y pericárdico y del intersticio pulmonar (36).
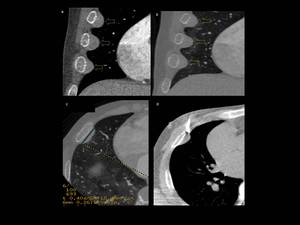
Fig. 40: Figura 40. Hombre, 47 años. Beta-talasemia conocida.
TC cardíaco: hallazgo incidental de masas subcostales bilaterales, bien definidas, homogéneas (flechas en a y en b).
El resultado del estudio anatomopatólógico, tras la biopsia guiada por TC (d), fue de hematopoyesis extramedular.
GRUPO 6.
HISTIOCITOSIS:
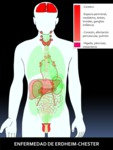
ENFERMEDAD DE ERDHEIM-CHESTER:
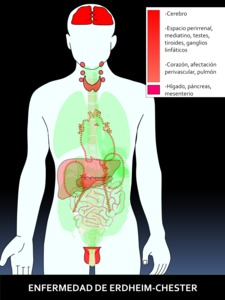
Fig. 41: Figura 41. Grado de afectación de órganos extraóseos en la ENFERMEDAD DE ERDHEIM-CHESTER, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
Es un tipo de histocitosis de células no Langerhans (xantogranulomatosis),
rara y multisistémica, de causa desconocida (38).
La afectación ósea es casi constante,
afectando clásicamente al esqueleto apendicular (osteoesclerosis simétrica parcheada medular y engrosamiento cortical de los huesos tubulares largos,
predominando en las metáfisis y las diáfisis de los miembros inferiores (38,39)).
La afectación del esqueleto axial es rara.
La apariencia clásica y patognomónica es una intensa captación en la gammagrafía,
bilateral y simétrica,
a nivel diáfisometafisario (como ocurría en nuestro caso) (38).
La afectación extraósea se da en SNC (lo más frecuente),
riñón,
mediastino,
testículo,
tiroides,
ganglios linfáticos,
pulmonar y cardíaca (siendo ésta la principal causa de muerte) (38) y los espacios perivasculares (rodeando la aorta y sus ramas,
las arterias pulmonares y la VCS).
La afectación del hígado,
páncreas y mesenterio es extremadamente rara (39,40). Puede ser muy grave.
MANIFESTACONES ATÍPICAS EN NUESTRO CASO: la propia enfermedad,
con infiltración perirrenal,
periureteral y mesentérica:
-Infiltración renal y perirrenal: se da en aproximadamente el 29% de los pacientes afectados,
pudiendo asociarse con afectación periureteral,
excepto a nivel del uréter pélvico que siempre está respetado,
ocasionando obstrucción del tracto urinario (6),
como en nuestro caso.
Esta afectación a menudo es asintomática,
pero puede dar lugar a fallo renal crónico y al resto de complicaciones asociadas a la hidronefrosis obstructiva (38).
-Infiltración peritoneal (extremadamente rara) (40).
Hallazgos radiológicos:
-Infiltración tisular perirrenal bilateral,
simétrica,
hipodensa y homogénea,
con mínima captación de contraste (“riñón peludo”),
hallazgo que es altamente sugestivo de esta entidad (6).Puede extenderse a la grasa de los espacios pararrenal anterior y posterior y a las glándulas adrenales (39).
(Figuras 42 y 43).
-La infiltración mesentérica da lugar a una imagen similar a la de la paniculitis mesentérica (Figura 42).
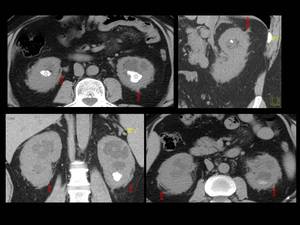
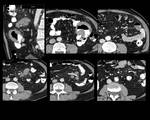
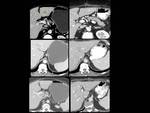
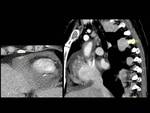
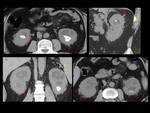
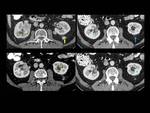
Fig. 42: Figura 42. Hombre, 45 años, dolor en ambas rodillas y lesiones blásticas óseas en la radiografía simple, a estudio.
TC abdominal con reconstrucciones sagitales:
-infiltración homogénea, hipodensa, simétrica, bilateral, con mínima captación de contraste perirrenal (“riñó peludo”) (flechas rojas) y periureteral (flechas amarillas). Hidronefrosis bilateral (estrellas blancas) y nefrolitiasis bilaterales (estrellas negras).
-afectación mesentérica similar a la paniculitis mesentérica (flechas blancas).
Gammagrafía: intensa captación de distribución bilateral y simétrica diametafisaria, compatible con histiocitosis , posiblemente enfermedad de Erdheim Chester
Biopsia de médula ósea compatible con enfermedad de Erdheim Chester
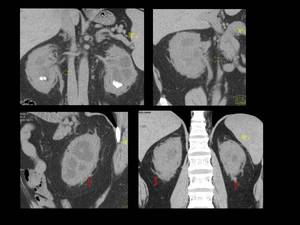
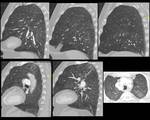
Fig. 43: Figura 43. Hombre, 45 años, dolor en ambas rodillas y lesiones blásticas óseas en la radiografía simple, a estudio.
TC abdominal con reconstrucciones sagitales:
-infiltración homogénea, hipodensa, simétrica, bilateral, con mínima captación de contraste, perirrenal (“riñó peludo”) (flechas rojas) y periureteral (flechas amarillas). Hidronefrosis bilateral (estrellas blancas) y nefrolitiasis bilaterales (estrellas negras).
-afectación mesentérica similar a la paniculitis mesentérica (flechas blancas).
Gammagrafía: intensa captación de distribución bilateral y simétrica diametafisaria, compatible con histiocitosis , posiblemente enfermedad de Erdheim Chester
Biopsia de médula ósea compatible con enfermedad de Erdheim Chester
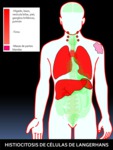
HISTIOCITOSIS DE CÉLULAS DE LANGERHANS (HCL):
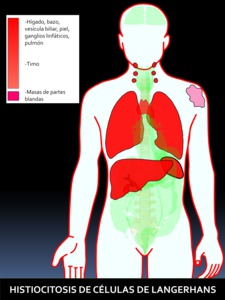
Fig. 44: Figura 44. Grado de afectación de órganos extraóseos en la HISTIOCITOSIS DE CÉLULAS DE LANGERHANS -Hand Schüller-Christian Disease-, de mayor (color rojo intenso) a menor frecuencia (color rojo suave) de afectación. Los órganos coloreados en rosa se encuentran afectados en un porcentaje muy bajo.
Puede manifestarse como una lesión solitaria, como múltiples lesiones en un solo órgano,
siendo el hueso el lugar más frecuentemente afectado,
o bien como enfermedad diseminada (42).
MANIFESTACIONES ATÍPICAS EN NUESTRO CASO: manifestación inusual en órganos comúnmente afectados y afectación inusual de estructuras:
- lesiones quísticas pulmonares en el LM y LLII,
con afectación de la región pulmonar de los ángulos cardiofrénicos (figuras 45 y 46).
El hallazgo inicial en la afectación pulmonar es la presencia de nódulos que pueden cavitar posteriormente y formar lesiones quísticas de pared gruesa ó fina,
que representan luces alveolares aumentadas de tamaño.
Frecuentemente coexisten nódulos y quistes.
Los quistes pueden ser redondeados pero a menudo son irregulares,
bilobulados,
en forma de trébol o con formas bizarras.
La forma irregular de los quistes,
la coexistencia con nódulos y la predominancia en los campos superiores con respeto de los ángulos costofrénicos son las características que distinguen a esta entidad de otras enfermedades quísticas pulmonares,
por ejemplo,
de la linfangioleiomiomatosis (43).
Pero estas características típicas no eran las de nuestro caso.
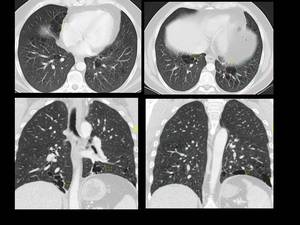
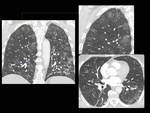
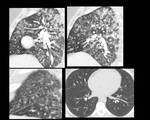
Fig. 45: Figure 45. Hombre, 35 años con diabetes insípida central y masa en el hombro izdo.
TC de tórax:
Lesioens quísticas pulmonares irregulares en el LM y LLII, con afectación de lo ángulos costofrénicos (flechas amarillas) y enfisema (círculo verde).
Biopsia de masa de partes blandas del hombro izdo: histiocitosis de células de Langerhans.
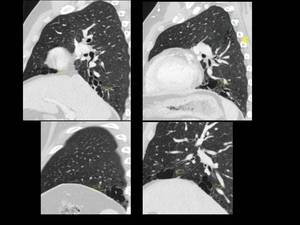
Fig. 46: Figure 46. Hombre, 35 años con diabetes insípida central y masa en el hombro izdo.
TC de tórax:
Lesioens quísticas pulmonares irregulares en el LM y LLII, con afectación de lo ángulos costofrénicos (flechas amarillas) y enfisema (círculo verde).
Biopsia de masa de partes blandas del hombro izdo: histiocitosis de células de Langerhans.
- masa de partes blandas unilateral extraósea,
en el hombro,
con adenopatías adyacentes (figura 47).
La afectación ganglionar puede darse como componente de la forma sistémica o representar la manifestación inicial y a veces es la única manifestación de la enfermedad.
En las partes blandas superficiales,
la histiocitosis de células de Langerhans principalmente afecta a la dermis (42),
siendo muy inusual la manifestación de nuestro caso.

Fig. 47: Figure 47. Hombre, 35 años con diabetes insípida central y masa en el hombro izdo.
TC de tórax: masa extraósea de partes blandas, unilateral, en el hombro izquierdo que respeta la dermis (estrellas) con adenopatías adyacentes (flecha blanca).
Biopsia de masa de partes blandas del hombro izdo: histiocitosis de células de Langerhans.