En la actualidad,
el seguimiento de los tumores primarios del SNC tratados,
ya sea con cirugía,
quimioterapia (con o sin inhibidores de la angiogénesis) o radioterapia (holocraneal,
estereotáxica o fraccionada) puede realizarse mediante múltiples métodos de imagen,
que permiten una visión multidisciplinar e integral de la patología.
A día de hoy,
la Resonancia Magnética ha demostrado ser la técnica de imagen “estructural” por excelencia en su seguimiento,
si bien las técnicas de imagen basadas en la IRM que podríamos denominar funcionales están incrementando de manera notable su potencia diagnóstica.
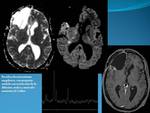
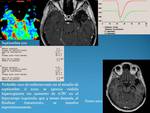
En primer lugar la difusión: Desde la introducción de las secuencias EPI para la evaluación de la difusión microscópica del agua en los tejidos, las secuencias de Difusión se han utilizado para evaluar diferentes patologías sobre todo a nivel cerebral,
especialmente en el campo de la patología isquémica, pero también en el estudio de integridad de fibras de sustancia blanca y para la diferenciación de tumores cerebrales según su grado de celularidad.
Se ha demostrado que los tumores muestran una relación inversamente proporcional entre los valores de ADC y su grado de celularidad.
En el estudio de RM difusión se recomienda utilizar una secuencia SS EPI con saturación espectral de la grasa y valores b de 0 y 1000 s/mm2, con adquisición de valores B en tres direcciones del espacio.
Las zonas con mayor hipercelularidad presentarán aumento de señal en las secuencias de difusión,
con hipointensidad en los mapas ADC.
Este hallazgo se correlaciona tanto con recidiva,
como con mayor grado histológico en tumores mixtos y que puedan progresar.
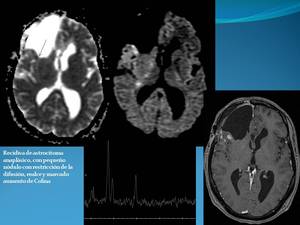
Fig. 1
En un segundo paso,
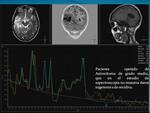
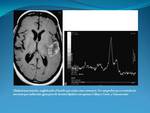
la espectroscopia por RM,
con técnicas mono o multivóxel,
permite detectar áreas de mayor recambio de membrana en virtud de la concentración relativa de metabolitos.
(

Fig. 2
References: Falini, ECNR, Roma, 2011
Fig. 2 )Un incremento relativo de la Colina,
con caída de la Creatina y el NAA,
con ratios Cho/Cr superiores al 2.43 para tumores gliales de alto grado y de 1.75 para gliomas de bajo grado,
son altamente sospechosos de incremento del recambio de membranas y,
por lo tanto,
de aumento de la división celular.
Los metabolitos más relevantes: Colina: integridad de membrana celular,
si se destruye,
aumenta; (3.2 ppm aprox) Creatinina: sistema reserva energía (3.0 ppm aprox); Naa: marcador específico función neuronal,
se produce en las mitocondrias neuronales (1.9 ppm aprox); Lactato: marcador de necrosis típico de procesos tumorales de alto grado.
( Fig. 3)
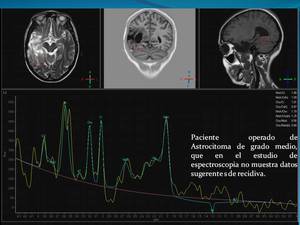
Fig. 3
.
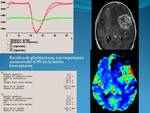
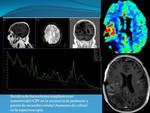
La RM perfusión,
de manera más extendida la basada en T2 gradiente,
también permite conocer las zonas con mayor angiogénesis y vascularización,
otorgando una herramienta extraordinaria más allá de la simple captación de contraste.
Se basa en la susceptibilidad en T2 * al paso de contraste,
y permiten conocer el grado de vascularización de una región de parénquima.
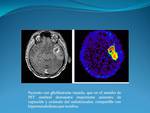
Va a permitir obtener mapas de CBV (volumen sanguíneo cerebral,
denominado Negative Index o Integral de realce negativo en la mayoría de los postprocesos),
así como de FSC (flujo sanguíneo cerebral),
TTP (tiempo al pico) y MTT (tiempo de tránsito medio).
Se ha propuesto como valor de corte aproximado una ratio de rCBV (Volumen sanguíneo cerebral relativo) de 1.75 para tumores de bajo grado,
siendo las ratios medias aproximadas para tumores de alto grado de aproximadamente 5.1.
( Fig. 4)
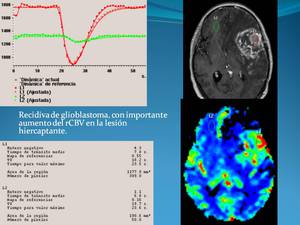
Fig. 4
Por otra parte,
las técnicas de medicina nuclear,
fundamentalmente el PET-TC con 18-F-deoxy-Glucosa y el SPECT con Talio o Metionina,
también han demostrado ser de utilidad en el seguimiento de estas patologías.
El Spect Talio se basa en la acumulación en el interior de la célula del anión Tl-201,
el cual es captado por la bomba de sodio-Potasio,
siendo un marcador indirecto de hipermetabolismo.
(
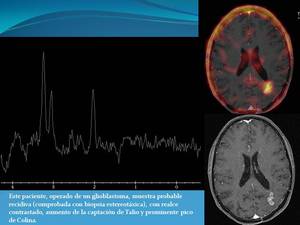
Fig. 5
) En cambio,
la Metionina es una amino ácido para el cual numerosos tumores del SNC sobre expresan transportadores,
por lo que presenta mayor grado de especificidad en la detección de su hipermetabolismo El PET-TC,
con una base fisiológica similar a la del resto del organismo,
Fig. 6 y aunque presente un alto grado de hipermetabolismo con SUV’s incrementados,
se considera de menor utilidad que los anteriores dado el gran consumo de fondo de glucosa en el parénquima cerebral.
La pseudoprogresión es en la actualidad uno de los principales problemas en el seguimiento de los tumores del SNC tratados con radio y quimioterapia,
especialmente en aquellos con temodal.
Se ha observado que durante el tratamiento (hasta 3 meses) estas lesiones experimentan un incremento del tamaño así como de la captación de contraste,
que no obstante cesan al acabar el tratamiento.
( Fig. 7)
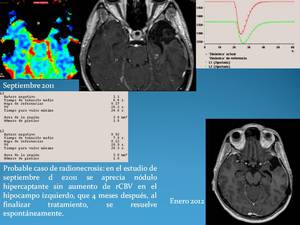
Fig. 7
Estos cambios no suelen presentar alteraciones en los estudios de espectroscopia ni SPECT Talio,
aunque a veces pueden condicionar alteraciones en los estudios de RM perfusión o PET.
La radionecrosis es el principal diagnóstico diferencial con la recidiva en los tumores del SNC tratados con radioterapia,
produciéndose del 5 al 24 % de los casos,
según las series. Se basa en un daño radioinducido sobre todo en el endotelio vascular,
que condiciona extravasación del contraste y un depósito inflamatorio con gliosis.
Puede producirse desde 2-6 meses tras el tratamiento,
si bien ha llegado a describirse hasta ¡¡ 23 ¡! Años tras el tratamiento.
La lesión presenta aumento del volumen,
con áreas mal definidas de contraste que se alternan con áreas necróticas.
Puede ser multifocal,
e incluso darse a distancia de la lesión originaria tratada.
En los estudios de Espectroscopia encontraremos disminución de Naa,
por daño neuronal,
si bien NO apreciaremos significativo aumento de la colina.
( Fig. 8 ) En los estudios de PET-glucosa SPECT Talio no habrá captación significativa,
y en la RM perfusión se aprecia un aparente aumento rCBV,
pero la curva presenta una característica persistencia de la caída de señal,
secundaria a la extravasación del contraste (Leakage),
que al corregir adecuadamente podremos comprobar cómo en realidad no existe verdadero aumento del rCBV.
Así,
ante una alta sospecha de recidiva,
es frecuente que encontremos lesiones con efecto de masa y realce contrastado,
áreas con restricción focal de la difusión (es importante diferenciar de artefactos por restos hemáticos),
aumento del rCBV,
patrón hipermetabólico en espectroscopia con aumento del cociente Cho/Cr,
e hipercaptación en los estudios metabólicos con radioisótopos.
( Fig. 9
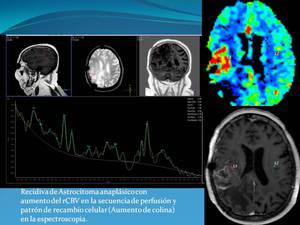
Fig. 9
.)