Introducción
El rabdomiosarcoma (RMS) es el sarcoma de partes blandas más frecuente en la infancia,
representando aproximadamente el 5% de todas las neoplasias pediátricas (1,
2) Deriva de las mismas células mesenquimales que dan origen al músculo estriado normal.
Su etiología es desconocida,
habiéndose asociado a algunos síndromes familiares como la neurofibromatosis y el síndrome de Li-Fraumeni (3)
Su presentación clínica es variable,
dependiendo de la localización del tumor,
aunque por lo general son síntomas indolentes en sus fases iniciales,
siendo difícil un diagnóstico clínico de sospecha (2)
Existen tres subtipos histológicos de rabdomiosarcoma: embrionario,
alveolar y pleomórfico.
En la práctica,
estos tres subtipos pueden reducirse a dos en el paciente pediátrico,
ya que el pleomórfico es casi exclusivo de adultos.
El subtipo embrionario es el más frecuente,
suponiendo hasta el 80% de rabdomiosarcomas en la edad pediátrica (3). El pronóstico es peor en el subtipo alveolar,
aunque afortunadamente son menos frecuentes.
Las localizaciones más habituales son cabeza y cuello (35-40%),
sistema genitourinario y extremidades (4). Dentro de los localizados en cabeza y cuello,
podemos subdividirlos en orbitarios,
parameníngeos (nasofaringe,
senos paranasales y oído medio) y no orbitario – no parameníngeo. Es importante recalcar la posibilidad del RMS de afectar a numerosos órganos y tejidos aun en ausencia de músculo estriado (5)
Presentación del caso
Paciente de 2 años,
varón,
sin antecedentes patológicos de interés salvo estudio en neurología por retraso en el inicio del lenguaje.
Acude al servicio de urgencias pediátricas con clínica de dolor abdominal de 3 días de evolución y fiebre de 39°C.
No leucocitosis y sedimento urinario normal.
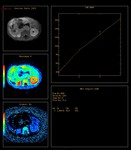
Ante la sospecha de foco séptico de origen urinario se solicitó estudio ecográfico urgente,
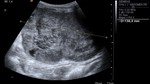
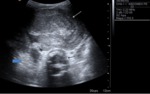
apreciándose la existencia de una gran masa abdominal de ecogenicidad heterogénea con áreas hipoecogénicas quístico / necróticas en su interior,
así como otros focos sólidos hiperecogénicos sin sombra acústica posterior.
Dicha masa presentaba aparente localización intraperitoneal,
produciendo desplazamiento de asas intestinales y debido a sus dimensiones (14 x 12 cm) ligera ectasia renal bilateral.
No se apreció con este estudio organodependencia.
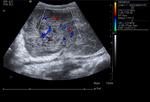
En el estudio Doppler color no se evidenciaron signos de trombosis vasculares,
existiendo evidente vascularización de la masa.
(Fig.
1,
Fig.
2 y Fig.
3)
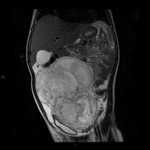
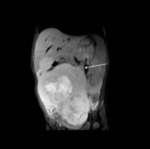
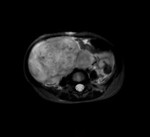
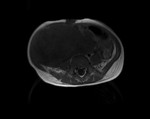
Se completó el estudio con RM abdominopélvica sin contraste intravenoso con secuencias coronales potenciadas en T2 FSE sin y con supresión grasa; sagitales potenciadas en SSFSE y T1 FSE; axiales potenciadas T1 FSE,
T2 FSE sin y con supresión grasa.
Tras contraste intravenoso paramagnético se realizó estudio dinámico mediante secuencias axial potenciada en T1 SPGR con supresión grasa y axial T1 FSE en fase tardía.
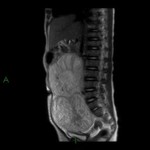
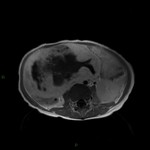
El estudio de RM abdominopélvica: (Fig 4-10)
- Confirmó la existencia de una voluminosa masa centroabdominal de 15 x 12 x 7.5 cm,
que ocupaba gran parte de hemiabdomen y hemipelvis derechos. Dicha masa estaba constituida por varias nodulaciones adoptando una morfología lobulada,
aparentemente bien definida por una cápsula o pseudocápsula,
no existiendo signos infiltrativos evidentes.
Su localización era intraperitoneal descartando totalmente un origen retroperitoneal.
No apreciamos organodependencia visceral,
exitiendo un probable origen mesentérico.
-
El contenido de la masa era heterogéneo,
con áreas marcadamente hiperintensas T2,
sugerentes de focos quísticos y otras de menor intensidad T2 e isointensas al músculo en T1 compatible con componente sólido de la masa.
No se apreció la existencia de grasa o sangrado en la tumoración.
-
El estudio dinámico tras contraste mostró una cinética de realce progresivo en la periferia de la masa.
-
En el resto del abdomen no se apreciaron otros hallazgos significativos ,
salvo la discreta ectasia renal bilateral ya descrita en estudio ecográfico.
No existía ascitis.
Se incluyó en el diagnóstico diferencial lesiones benignas como el hemangioma (sobre todo por la cinética de captación),
leiomioma y mesotelioma peritoneal quístico benigno y lesiones malignas como leiomiosarcoma y rabdomiosarcoma.
El paciente fue intervenido mediante laparotomía media,
extirpándose una gran masa peritoneal solidoquística multilobulada mesentérica.
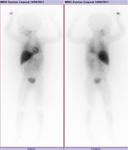
Se realizó una gammagrafía postquirúrgica con 3 milicurios de 123I-MIBG con rastreo a las 4 y 24 horas,
ya que clínicamente aún persistía la sospecha de neuroblastoma,
no apreciándose hallazgos significativos.
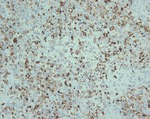
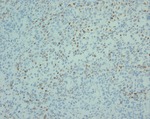
El resultado anatomopatológico de la pieza quirúrgica fue de Rabdomiosarcoma embrionario (subtipo no especificado) de localización abdominal con nódulos en mesenterio (15 x 12.5 x 6 cm y 2 x 1.5 x 1.5 cm),
con el siguiente perfil inmunohistoquímico: Vimentina (+),
Desmina (+); Actina sarcomérica (+/-); Miogenina (+); WT (+) citoplasmático; Ki 67 (+50%); Actina (-); GFAP (-); CD 34 (-); Enolasa (-);Neurofilamentos (-); S-100 (-); Cromogranina (-); Sinaptofisina (-); AE 1,
AE 3 (-); EMA (-); CD 99 (-).Se observan signos de anaplasia focal,
necrosis en el 10% y presencia de mitosis + (10/10 C.G.A.) Todos los nódulos se encuentran aparentemente encapsulados y sin signos de extensión a tejidos vecinos.
Todos los ganglios aislados se encuentran libres de infiltración.
No se ha observado invasión venosa o linfática.
(Fig 12-15)
Discusión
El RMS es una neoplasia poco frecuente,
a tener siempre en cuenta en el paciente pediátrico.
En nuestro conocimiento,
sólo existen siete referencias bibliográficas acerca de casos de RMS mesentéricos y/o peritoneales (6,7,8,9,10,11,12).
De todos ellos, sólo uno de los casos se trató de un paciente pediátrico (6).
No existen apenas referencias sobre los hallazgos radiológicos del RMS mesentérico,
tan sólo Oto et al. (7) describieron los hallazgos en TC de un caso de RMS intraperitoneal.
Sí son conocidos,
aunque inespecíficos los hallazgos del RMS en otras localizaciones (2,
13,
14,
15).
Se suele presentar como una masa sólida de localización variable,
heterogénea,
de contornos por lo general bien definidos,
a veces con algún componente quístico y focos necróticos.
En estudios tras contraste intravenoso muestra importante realce en sus porciones sólidas.
Su intensidad de señal en RM es homogénea e iso / hipointensa al músculo en secuencias potenciadas en T1,
mientras que en secuencias potenciadas en T2 generalmente son hiperintensos y más heterogéneos que en T1.
Tras la administración de gadolinio su captación es intensa y heterogénea,
a menudo con áreas centrales no captantes sugerentes de necrosis.
Nuestro caso mostró unos hallazgos en imagen similares a los del RMS en otras localizaciones,
aunque cabe recordar que estos hallazgos son totalmente inespecíficos y muy parecidos a los de otras masas de partes blandas pediátricas (2,14).
No hemos identificado ningún signo patognomónico o peculiaridad que permita realizar su diagnóstico radiológico de certeza,
debiendo hacer un diagnóstico diferencial con tumores como hemangiomas,
otros sarcomas de partes blandas,
fibrosarcoma infantil,
fibromatosis agresiva,
tumores neuroectodérmicos periféricos (PNET),
tumores rabdoides e incluso el sarcoma de Ewing no óseo.
Es importante en el diagnóstico diferencial recordar que el RMS es un tumor “relativamente frecuente” en el niño,
siendo la tercera causa de neoplasia extracraneal tras el tumor de Wilms y el neuroblastoma.
Incluso en localizaciones atípicas extremadamente raras como puede ser el tracto intestinal,
el corazón o el mesenterio,
debemos incluirlas en el diagnóstico diferencial ante una masa con las características radiológicas descritas en un paciente pediátrico.
Según nuestra experiencia y la literatura revisada,
el verdadero papel de las técnicas de imagen radiológicas,
aparte de acotar el diagnóstico diferencial,
es establecer la localización precisa de la lesión,
la afectación de estructuras adyacentes de cara a un tratamiento quirúrgico y sobre todo en la estadificación y pronóstico.
El pronóstico y tratamiento del RMS mesentérico,
al igual que el resto de RMS pediátricos, está bien establecido según el European Pediatric Soft Tissue Sarcoma (EpSSG) del año 2005 con el objetivo de dar un tratamiento homogéneo a nivel europeo,
a los pacientes pediátricos con sarcomas de partes blandas.
Entre los factores pronósticos se encuentran la variedad histológica,
estado postquirúrgico,
localización,
afectación ganglionar,
tamaño mayor o menor a 5 cm y edad (desfavorable en más de 10 años)