Durante los últimos años han aumentado los tratamientos mediante endoprótesis y con ello el número de estudios de control,
éstos buscan descartar complicaciones como el crecimiento del saco,
fugas,
movilización,
trombosis o infección.
El TC es el método habitual por su disponibilidad y resolución espacial,
si bien existen múltiples descripciones de controles mediante ecografía doppler o con contraste o por RM.
También se han descrito estudios TC sin contraste con estimación volumétrica del saco,
considerándose normal un aumento máximo de 2% del volumen.
Los intervalos recomendados de estudio son: 1er mes,
3er mes y 6to mes,
si no se detectan alteraciones,
se continúa con exploraciones anuales,
pero,
si existen fugas se pueden hacer exploraciones cada 6 meses hasta los dos años,
a menos que se demuestre necesidad de tratar.
En nuestro centro el protocolo consta de un estudio simple y en fase arterial,
en TC de 64 cortes (Philips,
Amsterdam The Netherlands) con 120Kv,
250-300mA/s,
con técnica de detección del bolo,
con umbral de 150UH,
una velocidad de giro de 0.5sec,
pitch 0.983,
con protocolo de reconstrucción de 2mm con avances de mesa de 1mm.
Los estudios se realizan con 70-80ml de Iomeprol 400mg/ml (Iomeron®,
Rovi,
Madrid España) con técnica de bolo de seguimiento de solución salina de 50mL mediante inyector eléctrico.
En este primer estudio deben identificarse las posiciones de los distintos componentes y la existencia de nuevas imágenes que pueden considerarse como normales o patológicas.
Imágenes habituales postratamiento,
no patológicas:
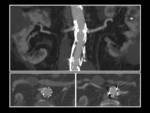
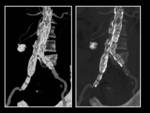
1.- La zona proximal de anclaje de la prótesis,
se encuentra sobre el origen de las arterias renales: es un hallazgo relativamente frecuente y no acarrea complicaciones a largo plazo.
Fig. 1
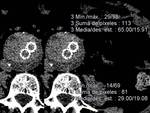
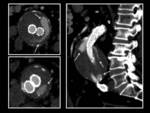
2.- Hiperdensidad periprotésica difusa (entre la prótesis y el trombo mural del saco aneurismático),
debe estar presente también en el estudio precontraste,
parece deberse a trombosis aguda de la luz periprotésica.
Fig. 2
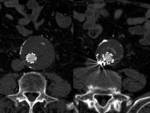
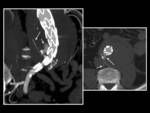
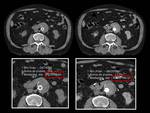
3.- Aparición de imágenes de alta densidad dentro del trombo mural,
puede deberse a placas que se han desplazado durante el tratamiento.
Es importante comparar con el estudio basal (sin contraste),
y así diferenciarlas de las fugas.
Fig. 3
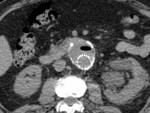
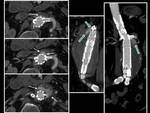
4.- Gas en el saco aneurismático periprotésico,
puede ser un hallazgo y no condiciona morbilidad alguna.
Fig. 4
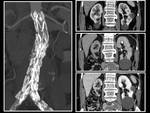
5.- Es imprescindible familiarizarse con el tipo de endoprótesis que porta el paciente,
ya que las distintas referencias radiológicas o la estructura puede hacer pensar,
que existen fracturas o un inadecuado acoplamiento entre las partes,
es importante recordar que la parte recubierta de la prótesis suele tener marcas que la delimitan,
ya que dicho material no es radio-opaco.
Fig. 5
Las fugas o endofugas se llama a la evidencia de contraste por fuera de la prótesis.
Son 5 tipos:
- Tipo I: pueden ser proximales (Tipo Ia) o distales (tipo Ib) son aquellas que se dan secundariamente a un inadecuado anclaje de la prótesis a las paredes del cuello o a las ramas ilíacas.
Suelen producir aumento del saco aneurismático y requerir tratamiento precoz.
Suele hacerse con plastia con balón o extensión de la prótesis.
Fig. 6
En prótesis aorto-unilíacas,
con bypass femoro-femoral y oclusión proximal de la ilíaca no utilizada,
la permeabilidad de ésta,
se considera una fuga tipo Ic,
también se recomienda tratar con prontitud.
- Tipo II: son aquellas que se deben al llenado retrogrado desde arterias cubiertas por la endoprótesis (típicas de la mesentérica inferior o de ramas aorticas lumbares.
Son de bajo riesgo y suelen seguirse para evaluar si hacen crecer el saco (raro) o si cierran de forma espontánea (común).
Es importante verificar que no aumenta el diámetro del aneurisma.
Fig. 7
- Tipo III: Son las que se deben a un fallo del acomplamiento de las partes de la endoprótesis,
en los casos en que la prótesis es aorto-bilíaca,
puede suceder entre la extensión en pantalón y la prótesis ilíaca.
También pueden deberse a manipulación inadecuada de la prótesis,
fractura o a un fallo primario de la misma.
Requieren también de tratamiento precoz,
ya que suponen riesgo de crecimiento del aneurisma.
Fig. 8
- Tipo IV: Por porosidad,
se describen como un aspecto de teñido nuboso o neblinoso clásico en la arteriografía intraoperatoria,
clásico de materiales no presentes en las nuevas prótesis y que en la actualidad son raras,
igualmente requieren de tratamiento precoz.
- Tipo V: Endotensión: Son aquellas en las que la única evidencia de fallo del tratamiento,
es el aumento del tamaño del saco aneurismático de forma significativa,
en controles sucesivos.
Deben evaluarse mediante otras pruebas incluyendo la arteriografía o la ultrasonografía con contraste (USCC) o la RM,
ya que agregan un componente dinámico a la evaluación,
en RM y US,
sin radiaciones ionizantes y así identificar,
posibles falsos negativos del angio-TC.
Fig. 9
Entre las otras complicaciones que pueden presentarse,
se encuentran:
1.- Reducción del tamaño renal,
aunque raro,
puede darse el caso de producirse una estenosis significativa de alguna arteria renal,
lo que a veces sólo es demostrable con la progresiva atrofia del parénquima renal.
Fig. 10
2.- Trombosis de la protésis: del cuerpo o de las ramas de la prótesis,
debe diferenciarse de aquellos casos,
en lo que el oclusor de una prótesis aorto-uniliaca pueda perecerse a un stent.
3.- Oclusión/trombosis hipogástrica bilateral: Puede producirse en paciente con anatomía muy tortuosa o con lesiones subyacentes avanzadas,
siempre que exista debe informarse y deben buscarse signos de patología visceral abdominal (principalmente colitis izquierda).
También se han descrito casos de colitis isquémica en pacientes con oclusión de arterias mesentéricas inferiores (AMI) de tamaño aumentado,
lo que podría ser un signo de derivación de flujo a través de ésta,
desde una estenosis en otra localización (tronco celíaco o arteria mesentérica superior o hipogástricas),
condicionando isquemia colónica con la oclusión de la AMI por la prótesis.
La identificación de este tipo de complicaciones,
pueden dar paso a la intervención de revisión o reparación,
que permitan reinstaurar o prolongar la utilidad y funcionalidad de la endoprótesis.
Una situación poco frecuente pero con grave morbi-mortalidad asociada es la infección protésica,
se pueden clasificar como:
- tempranas (antes de los 4 meses desde la cirugía) clínicamente suele ser la como un cuadro infeccioso agudo,
fiebre alta,
afectación sistémica,
leucocitosis y aumento de los reactantes de fase aguda (los hemocultivos son de utilidad limitada).
- tardías (más de 4 meses postoperatorios) se describen casos en los que el diagnóstico,
se ha realizado entre 7 días y 10 años.
La situación clínica suele caracterizarse por pseudoaneurismas,
sangrado digestivo asociado a fístulas aorto-entéricas,
hidronefrosis,
fibrosis periaórtica u osteomielitis,
habitualmente en ausencia de fiebre.
Debemos sospechar la existencia de una infección cuando existan alteraciones de los tejidos periaórticos,
con pérdida de planos de clivaje con los tejidos circundantes,
si se identifica tejido de partes blandas,
colección o gas periaórtico que muestra progresión,
o cuando se producen modificaciones del saco,
de rápida evolución en pruebas sucesivas por imagen.
Si bien estos hallazgos pueden ser sugerentes,
tradicionalmente se han utilizado la gammagrafía con leucocitos marcados con Tc99-hexametazima,
Indio-111 o galio,
así como la punción aspiración pre-antibiótica diagnóstica y más recientemente,
EL PET-TC para establecer su origen inflamatorio.