INTRODUCCIÓN
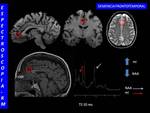
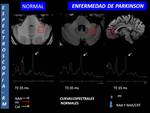
Las enfermedades neurodegenerativas (Fig. 1 ),
entendidas como una desestructuración cerebral progresiva y sin posibilidad de remisión,
son un reto para los servicios de neurología,
neurorradiología y de medicina nuclear.
Para los neurólogos es fundamental clasificar adecuadamente a estos pacientes para introducirlos en los diferentes programas y ensayos clínicos de las nuevas terapias que pretenden estabilizar o frenar la enfermedad, o bien al menos mejorar su calidad de vida.
A menudo la clínica de estos pacientes se solapa entre las diferentes entidades y el diagnóstico debe apoyarse en la información de la neuroimagen.
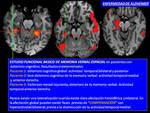
La neuroimagen puede ser decisiva para corroborar el diagnóstico clínico de sospecha cuando existen hallazgos en la imagen estructural o en los últimos años en la imagen funcional,
especialmente en el tensor de difusión la RM funcional,
la espectroscopía y el PET.
Estos hallazgos son insuficientes,
considerados aisladamente,
para establecer un diagnóstico precoz y de certeza,
pero muy útiles junto a los datos clínicos.
En este trabajo revisamos los hallazgos morfológicos de las secuencias convencionales en RM de 3T en las enfermedades neurodegenerativas más frecuentes encontradas en la práctica diaria y describimos los posibles hallazgos de la imagen avanzada funcional en estas patologías.
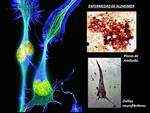
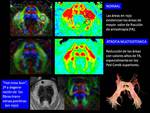
ENFERMEDAD DE ALZHEIMER (EA)
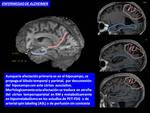
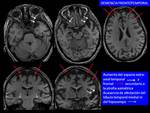
Enfermedad neurodegenerativa progresiva debido a la acumulación anómala de la proteína tau (Fig. 2 ),
que presenta un papel crucial en la disfunción neuronal / glial y muerte celular.
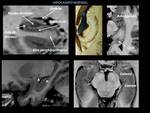
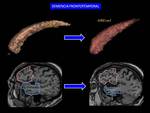
El proceso degenerativo comienza en la parte medial del lóbulo temporal,
en el hipocampo (Fig. 3 ) con extensión al espacio parahipocampal y resto del cortex frontotemporal.
La afectación motora y visual es la más tardía.
No existe aún prueba de imagen definitiva para el diagnóstico de certeza de la EA,
pero la imagen puede junto con los datos clínicos establecer un diagnóstico de sospecha.
El estudio estructural de RM generalmente se utiliza para excluir otras causas de demencia e identificar casos precoces que puedan incluirse en nuevos protocolos de tratamiento.
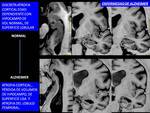
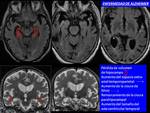
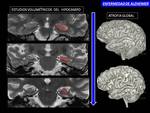
Los hallazgos morfológicos son tardíos (Fig. 4 ): a)atrofia temporal de predominio hipocampal con alisamiento de su superficie y en ocasiones discreta hiperseñal; b) ampliación del espacio extraaxial de la cisura parahipocampal; c) ampliación de la cisura de Silvio y aumento de tamaño del sistema ventricular temporal y d)mayor o menor grado de atrofia cortical parietotemporal (Fig. 5 ).
Los estudios de volumetría cortical son útiles para el seguimiento de la enfermedad objetivándose una pérdida progresiva del volumen del hipocampo y del lóbulo temporal (Fig. 6,
Fig. 7 ).
La principal limitación de la valoración volumétrica es que en muchos casos, es operador-dependiente ,
pero afortunadamente se están desarrollando cada vez más programas de segmentación y obtención volumétrica automática,
reproducibles y no operador-dependientes.
Los estudios de imagen funcional , aportan más información que la imagen convencional,
ya que identifica anomalías en áreas morfológicamente normales
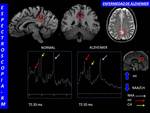
La espectroscopía -RM con técnica single voxel o multivoxel a TE corto (35 ms) localizada en el cíngulo posterior puede corroborar la sospecha clínica de EA.
Es un hecho que en los pacientes con EA se identifica un claro incremento del marcador glial myo-inositol (mI)( localizado a 3,56 ppm) en el cíngulo posterior,
con reducción por tanto,
del cociente NAA/mI.
(Fig. 8 ) Esta ratio es la de mayor capacidad discriminatoria entre EA y resto de patologías,
aunque no es exclusiva de EA.
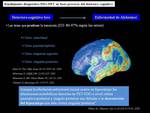
Por otro lado parece tener relevancia la ratio NAA/Cr <1,61 que podría predecir en 3 años la transformación del deterioro cognitivo leve(DCL) a EA.
La degeneración walleriana de la sustancia blanca secundaria al daño neuroaxonal en la EA es el mecanismo fundamental de afectación de la sustancia blanca del córtex asociativo temporo-frontoparietal en la EA .
Uno de los hallazgos en la EA es la reducción de volumen del stem temporal,
por donde pasan haces de conexión intrahemisferica frontotemporal ( el fascículo uncinado) ,
conexión frontooccipital (fascículo frontooccipital inferior) y el asa de Meyer ( conexión del núcleo geniculado lateral con la cisura calcarina).
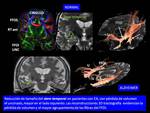
Los haces subcorticales más afectados en la EA son fascículos implicados en funciones cognitivas superiores como el fascículo uncinado de predominio izquierdo (memoria),
y el haz frontooccipital inferior (lenguaje) (Fig. 9 ),
estando preservados haces implicados en funciones primarias ( motora y visual) como el loop de Meyer y el haz corticoespinal ( REF Radiology y ajnr).
Estas alteraciones son difíciles de cuantificar en los estudios de tensor de difusión,
no existiendo valores absolutos de corte que permitan diferenciar entre normal y anormal,
pero es de gran utilidad la evidencia en muchos casos de asimetrías derecha-izquierda,
tanto en los valores de fracción de anisotropía como en coeficiente de difusión aparente y en ocasiones asimetrías en el volumen total de los haces de sustancia blanca,
siendo más llamativo en el fascículo uncinado.
Con la RM funcional de activación se han descrito en la literatura disminución de áreas de activación de cortex temporal medial en pacientes con EA,
al realizar paradigmas de memoria.
En nuestra experiencia,
los paradigmas de memoria son difícilmente reproducibles incluso en pacientes sin déficit cognitivo,
por lo que su aplicación en la práctica rutinaria del radiólogo es bastante difícil,
siendo los resultados contradictorios (Fig. 10 ).
En la EA,
los estudios de SPECT evidenciaban áreas de hipoperfusión cerebral parietotemporales (Fig. 11 ),
pero la correlación con la imagen anatómica era difícil.
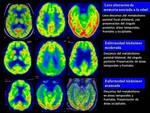
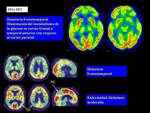
En la actualidad el estudio de PET-FDG (18F-deoxiglucosa) cerebral puede medir la cuantía y distribución del metabolismo de la glucosa y de ahí deducir la capacidad funcional de las zonas cerebrales,
ya que la glucosa se consume en las uniones neuronales.
En la EA el patrón clásico es el menor metabolismo en las áreas de asociación parieto-temporales (Fig. 12 )(Silverman y cols.
2002).
Existe una asociación significativa entre PET cerebral anormal y deterioro cognitivo posterior.
En el deterioro cognitivo leve (DCL) hay casi 5 veces más riesgo de aparecer EA si la PET muestra el patrón anormal adecuado (Kerholz y cols.
1999).
Las estructuras cerebrales que antes se alteran en la PET de la EA son: la corteza llamada entorrinal,
el giro hipocámpico,
y la corteza cingulada posterior,
que están íntimamente relacionadas con los procesos de memoria inmediata.
Este patrón puede diferenciar la EA con otros tipos de demencia como la demencia por cuerpos de Lewy (hipometaboliso occipital) y la demencia vascular(alteraciones focales parcheadas),
con áreas hipometabólicas claramente diferentes.
Estos hallazgos se ven por PET uno a dos años antes de que haya síntomas (Fig. 13 ) (Alexander y cols.
2002; Desgranges y cols.
2002).
En el futuro inmediato las imágenes PET con β-amiloide pueden potencialmente ayudar en el diagnóstico precoz y preciso de la enfermedad de Alzheimer.
Florbetaben (18F) es un prometedor 18F- marcado β-amiloide trazador PET en desarrollo clínico
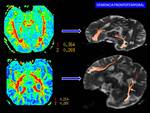
DEMENCIA FRONTOTEMPORAL (DFT)
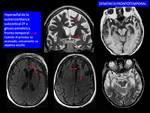
Demencia ocasionada por atrofia lobar frontal y /o temporal.
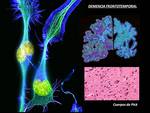
Antes llamada enfermedad de Pick,
término en la actualidad restringido a el hallazgo anatomopatológico de la presencia de cuerpos de Pick en un lóbulo cerebral atrófico (Fig. 14 ).
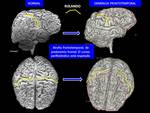
La atrofia suele afectar a la parte anterior del lóbulo frontal y temporal ,
respetando el margen posterior del giro temporal superior y al córtex peri-Rolándico.
El lóbulo parietal y occipital están también respetados.
Suele existir una asimetría derecha- izquierda,
con mayor afectación del hemisferio dominante.
La RM estructural demuestra los cambios secundarios a la atrofia cortical con (Fig. 15,
) a)remarcamiento de surcos corticales en los lóbulos frontales y temporales; b) hiperseñal de la sustancia blanca subcortical frontotemporal secundaria a gliosis (Fig. 16 ); c) asimetría izquierda.
Se han descrito también disminuciones de volumen significativas Los estudios de volumetría han evidenciado no solamente atrofia progresiva frontotemporal ,
sino también reducción de volumen en la comisura anterior y cingulo anterior del volumen del núcleo caudado ( cabeza y cuerpo) con respecto a sanos y a pacientes con EA (Fig. 17,Fig. 18 ). La DFT se caracteriza por alteraciones emocionales y cognitivas secundarias a la disfunción cognitiva frontal ocasionada por la atrofia,
en la que están implicadas los circuitos frontoestriatales.
La reducción de “inputs” al caudado ocasiona está pérdida de volumen que a su vez está relacionada con el grado de alteración cognitiva.
En los estudios de imagen funcional,
la espectroscopia con secuencias single voxel o multivoxel puede evidenciar reducciones del pico de NAA e incrementos de mI en el lóbulo frontal o en el cíngulo anterior (Fig. 19 ),
con curvas espectrales normales en el cíngulo posterior,
que permiten el diagnóstico diferencial con la EA.
La imagen con tensor de difusión ofrece hallazgos muy interesantes.
Obviamente el fascículo uncinado (Fig. 20 ) presenta una clara disminución de volumen al ser un haz de conexión frontotemporal implicado en los procesos de memoria. La reducción progresiva del valor de FA podría incluso servir de marcador evolutivo del estado clínico del paciente.
Por otro lado es también interesante la pérdida de volumen del cíngulo anterior,
implicado en los procesos de motivación e iniciación, y la reducción del valor de la FA con respecto a sanos del fascículo longitudinal inferior ( Fig. 20 ),
implicado en las afasias semánticas relacionadas con la memoria visual,
objetivadas en los pacientes con DFT.
La imagen con PET-Glucosa es muy útil en la diferenciación con otras demencias como la EA,
al presentar marcado hipometabolismo en el córtex fronto temporal,
cíngulo anterior con preservación del córtex parietal y occipital (Fig. 21 )
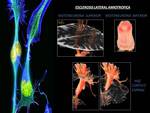
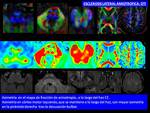
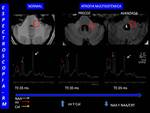
ESCLEROSIS LATERAL AMIOTROFICA (ELA)
También llamada enfermedad de Lou Gehring o enfermedad de motoneurona o enfermedad de Charcot.
Es la degeneración de las neuronas motoras del tronco-médula espinal ( enfermedad de motoneurona inferior),
neuronas del cortex primario motor( enfermedad de motoneurona superior) y pérdida eventual de fibras del haz corticoespinal (Fig. 22 )
Clinicamente puede presentar síntomas de motoneurona superior y / o inferior o bien presentar un predominio de síntomas bulbares,
que generalmente cursan con un deterioro clínico mayor y más rápidamente progresivo.
La RM estructural se realiza exclusivamente en estos pacientes,
siguiendo los criterios de El Escorial y la World Federation of Neurology Research Group on Motor Neuron Diseases,
para excluir otras posibilidades diagnósticas,
especialmente cuando la clínica es de predominio bulbar.
Hay que recordar que estos criterios no están basados en criterios radiológicos de RM de alto campo y los radiólogos que trabajamos con la RM de 3T sabemos que ésta puede identificar hallazgos morfológicos sutiles precoces que unidos a la sospecha clínica,
faciliten el diagnóstico.
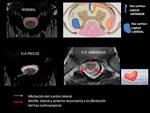
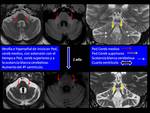
Los hallazgos morfológicos de RM más determinantes y especificos en la ELA es la hiperseñal en la secuencia potenciada en T2 de los cordones anterolaterales de la médula espinal.
Suele ir acompañado de alteración de la convexidad normal anterior del parénquima medular,
incluso en fases precoces (Fig. 23 ).
Cuando aparece este hallazgo en el adecuado contexto clínico el diagnóstico de ELA es altamente probable y generalmente estos pacientes suelen ser más jóvenes y con una progresión más rápida.
Tardíamente se identifica una marcada atrofia del cordón medular que adquiere una morfología en corazón,
por la atrofia anterior y lateral del tracto corticoespinal.
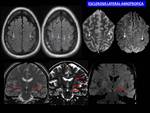
Los hallazgos intracerebrales en la ELA son menos específicos,
pero sí ayudan a a corroborar el diagnóstico clínico de presunción.
Se han descrito (Fig. 24 ) a) hiperseñal en secuencias FLAIR y potenciadas en T2,
en el cortex peri-Rolándico bilateral,
especialmente en el giro central b) Hiposeñal en las secuencias potenciadas en T2 en el cortex periRolándico bilateral,
relacionadas con depósito de hierro en estas localizaciones (posible factor etiopatogénico en enfermedades neurodegenerativas); c) hiperseñal en secuencias FLAIR y potenciadas en T2 a lo largo del trayecto intracraneal del haz corticoespinal,
hallazgo indeterminado ya que se puede identificar en otras patologías como las adrenomieloneuropatías,
enfermedad de Krabbe o enfermedad de Charcot-Marie Tooth,
e incluso en pacientes sanos cuando la hiperseñal aparece en el brazo posterior de la cápsula interna.
De hecho este hallazgo no se correlaciona con la discapacidad funcional de los pacientes.
Habrá que considerar este hallazgo como patológico cuando la hiperseñal se extiende más allá de la cápsula interna o cuando existe una progresión en el tiempo de la extensión de la hiperseñal del haz corticoespinal en FLAIR o en secuencias potenciadas en T2 (Fig. 25 ).
Los estudios volumétricos seriados pueden mostrar una leve pérdida progresiva y global de volumen cerebral en los pacientes con ELA,
generalmente insuficiente para el seguimiento de estos pacientes.
Unicamente hay destacar que existe una variante que ELA que asocia una demencia similar clínica e histológicamente con la demencia frontotemporal,
en las que se identifica una marcada atrofia frontotemporal e hiperseñal subcortical en dichas localizaciones.
Existen también trabajos del control volumétrico seriado del parénquima medular cervicodorsal,
aunque estos estudios necesitan de programas sofisticados que generalmente escapan a las posibilidades del radiólogo en el ejercicio de su práctica diaria
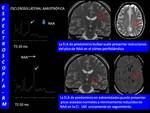
Los estudios de imagen funcional en la ELA aportan una información indirecta de la afectación del haz corticoespinal,
siendo las más útiles la espectroscopía-RM y el tensor de difusión.
Los estudios de espectroscopía-RM son bastante explícitos,
aunque no específicos,
evidenciando una reducción de la ratio NAA/Col y NAA/Crt secundaria a la pérdida neuronal y especialmente de la ratio NAA/ mI en el cortex peri-Rolándico,
secundario a la gliosis (Fig. 26 ).
Estas alteraciones en los metabolitos cerebrales ocurren especialmente en el cortex motor y en la corona radiada,
más pronunciados en la forma bulbar de la ELA.
Debido a la superposición de los valores de estas ratios con los de pacientes normales,
estas proporciones son útiles no para el diagnóstico sino en el seguimiento de estos pacientes,
correlacionándose con la severidad de los síntomas clínicos.
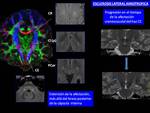
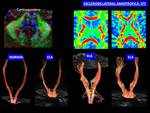
La imagen con tensor de difusión es una de las técnicas más prometedoras en la valoración de los haces de sustancia blanca y en este caso del haz corticoespinal.
Se ha objetivado reducciones significativas de la fracción de anisotropía (FA) especialmente en el brazo posterior de la cápsula interna con respecto a controles sanos.
En nuestra experiencia la reducción del conjunto de valores de FA a lo largo del haz corticoespinal desde el brazo posterior de cápsula interna,
pasando por el pedúnculo cerebral,
protuberancia hasta la pirámide presenta mayor especificidad diagnóstica que un valor aislado y probablemente se convierta en un marcador de evolución clínica.
En las reconstrucciones 3D de tractografía pueden evidenciarse pérdidas de volumen del haz CE con respecto a controles sanos,
especialmente cuando existe una alteración severa en los mapas de fracción de anisotropía (Fig. 27,Fig. 28 ).
No obstante es difícil establecer unos niveles de corte de valores de FA debido a la gran variabilidad entre los pacientes y entre los diferentes equipos de RM,
de ahí que esta técnica este aún en desarrollo,
no estando incluida aún en los protocolos de seguimiento de la ELA.
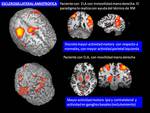
Los estudio funcionales de activación realizados en pacientes con ELA nos muestran alteraciones en el patrón de actividad motora “normal” con respecto a controles,
con mayor actividad en áreas motoras no primarias ( motora suplementaria,
cortex sensorial,
cortex parietal inferior,
cerebelo) tras paradigmas sencillos como el “finger-tapping”.
En ocasiones la dificultad de movimientos con la extremidad superior obliga al técnico de resonancia a realizar él mismo el movimiento de pinza del paciente,
objetivándose igualmente mayores áreas de activación ( en menor medida que sí el paciente realiza el paradigma) con respecto al patrón normal (Fig. 29 ) En definitiva,
no existe un patrón de actividad motora sugestiva de ELA y los hallazgos dependerán del mayor o menor grado de afectación de la motoneurona superior o inferior.
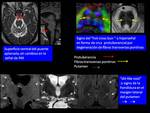
ATROFIA MULTISISTEMICA (AMS)
Desorden degenerativo esporádico de aparición en la edad adulta de etiología incierta,
con alteraciones cerebelosas,
afectación piramidal,
extrapiramidal y síntomas autonómicos.
También conocida como atrofia olivopontocerebelosa esporádica (OPCA)(Fig. 30 (cuando el cerebelo,
los pedúnculos cerebelosos,
la oliva inferior y la protuberancia están más afectados),
enfermedad estriadonigral (cuando predomina la afectación en el putamen y en la base de la protuberancia y se considera como una variante de la enfermedad de Parkinson) o enfermedad de Shy-Drager (sin diferencias morfológicas con la OPCA pero con predominio de síntomas autonómicos).
Estructuralmente la RM presenta hallazgos muy característicos,
aunque como en casos anteriores,
indeterminados.
Hallazgos radiológicos frecuentes en las secuencias convencionales son (Fig. 31 ) a)la marcada atrofia de los pedúnculos cerebelosos con > o < hiperseñal en secuencias potenciadas en T2; b) variable grado de atrofia de la sustancia blanca hemisférica cerebelosa (generalmente menor que la atrofia peduncular) con o sin hiperseñal en las secuencias potenciadas en T2; c) aumento del tamaño del cuarto ventrículo;d) la superficie ventral de la protuberancia aplanada,
sin cambios en la señal de RM; e) el signo del ”hot cross bun “(Fig. 32 ) o hiperseñal en forma de cruz en el puente en las imágenes axiales potenciadas en T2 o T2FLAIR por degeneración de fibras transversas pontinas; f) aumento de la señal en secuencias potenciadas en T1 o descenso de la señal en imágenes potenciadas en T2 (ref) en el margen lateral e inferior del putamen,
por depósito de hierro (más frecuente en la degeneración estriadonigral); g) “slit-like void” o signo de la hendidura en el margen lateral del putamen,
secundario a atrofia y aumento del espacio ente la cápsula externa y el putamen (Fig. 32 ).
Aparece como una línea hipointensa en secuencias potenciadas en T1 e hiperintensa en T2,
aunque este signo radiológico aisladamente es inespecífico,
especialmente en la imagen obtenida en imanes de 3T.
Los estudios volumétricos longitudinales aunque escasamente utilizados en esta patología,
pueden evidenciar moderada atrofia cortical progresiva especialmente frontoparietal.
Los estudios de imagen avanzada en la AMS son especialmente útiles en corroborar la sospecha clínica,
especialmente la espectroscopía-RM y el tensor de difusión.
La espectroscopía-RM presenta anomalías en las curvas espectrales en el cerebelo y en la protuberancia comparativamente con sujetos sanos de edades similares y con voxels en otras localizaciones cerebrales supratentoriales,
identificando en fases precoces incremento del pico de myo-inositol y de Colina y tardíamente,
descenso del pico de NAA,
con leve incremento del mI (Fig. 33 ).
La reducción de la ratio NAA/Crt se ha relacionado con la discapacidad de estos pacientes.
El tensor de difusión en la AMS permite diferenciar entre la AMS y otras entidades clinicamente similares como la enfermedad estriadonigral o enfermedad de Parkinson (EP).
La FA en los pedúnculos cerebelosos medios o en la sustancia blanca cerebelosa está claramente reducida con respecto a estas entidades y a pacientes sanos del mismo grupo de edad Fig. 34).
La degeneración de las fibras transversas del puente se puede identificar claramente tanto en la imágenes 2D como 3D del tensor de difusión ( Fig. 34 )
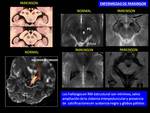
PARKINSON
Aunque la definición de la enfermedad de Parkinson está en continua evolución ,
podemos referirnos al parkinsonismo clásico como una entidad clinicopatológica progresiva de aparición adulta con respuesta en su mayoría a la levodopa y que asocia complicaciones motoras.
Estos desórdenes motores son la bradiquinesia,
el temblor de reposo y la rigidez entre otros.
Existe una degeneración de la vía nigroestriada-cortical (Fig. 35 )
Ante una sospecha de posible EP la prueba standard es el DAT-SCAN con alta fiabilidad si resulta positiva (depleción de DA en putamen y caudado) pero no definitiva si resulta negativa,
hecho que ocurre en el 20% de los casos en el diagnóstico inicial.
La RM convencional,
morfológica no evidencia generalmente alteraciones,
salvo en ocasiones calcificaciones de la sustancia negra,
globos pálidos,
acompañadas de discreta atrofia cortical y ampliación de la cisterna interpeduncular (Fig. 36 ).
La imagen funcional avanzada,
concretamente la espectroscopía-RM,
el tensor de difusión y la RM funcional de activación,
pueden ser de utilidad en pacientes con datos equívocos en el DAT-SCAN.
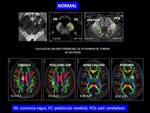
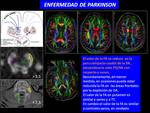
Los estudios de tensor de difusión en EP identifican incremento de la ratio de los valores de la FA entre el pedúnculo cerebral y la sustancia negra,
siendo > de 2,5,
a expensas de teórica depleción de dopamina en sustancia negra.
Puede identificarse también disminución de los valores de FA en el genu del calloso secundaria a la afectación frontal (Fig. 37,Fig. 38 )
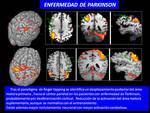
En los pacientes con posible EP, existe mayor reclutamiento neuronal en el estudio funcional motor,
tanto en el cortex primario contralateral como en el ipsilateral pero la activación es siempre de predominio post-Rolándica,
por desplazamiento hacia áreas parietales teóricamente por la deaferenciación de la vía nigrocortical.
Este hecho condiciona escasa activación del área motora suplementaria,
aunque ésta se activa con el entrenamiento,
por lo que es muy importante la realización de paradigmas cortos (Fig. 39 )
La espectroscopía-RM en los pacientes con EP pueden presentar discreta reducción del pico de NAA en sustancia blanca prefrontal,
secundario a posible daño neuroaxonal por la deaferenciación de la vía nigrocortical ,
siendo la curva espectral cerebelosa siempre normal,
a diferencia del temblor esencial,
la atrofia multisistémica o la parálisis supranuclear progresiva (Fig. 40 ).
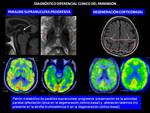
El diagnóstico diferencial clínico de la enfermedad de Parkinson,
se realiza con otros dos tipos de enfermedades neurodegenerativas.
Una es la páralisis supranuclear progresiva que radiológicamente aparece con adelgazamiento y aplanamiento del mesencéfalo (en forma de pico) yatrofia de los colículos superiores y calcificación de ambos globos putámenes.
La otra es la degeneración corticobasal que cursa radiológicamente con atrofia frontoparietal con remarcamiento de los surcos corticales periRolándicos (fig).
Estas entidades se diferencian con estudios de PET-FDG,
presentando patrones metabólicos diferentes (Fig. 41 )
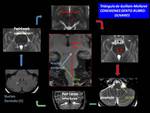
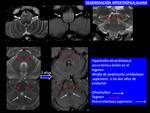
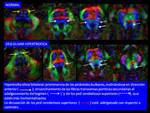
DEGENERACION OLIVAR HIPERTROFICA
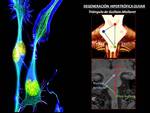
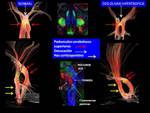
Degeneración secundaria del núcleo olivar inferior (NOI) causada por una lesión en el triángulo de Guillain.Mollaret o circuito dento-rubro-olivar (Fig. 42 ).
Este circuito conecta el núcleo dentado del cerebelo con el núcleo rojo mesencefálico y el núcleo olivar inferior de la médula.
Las fibras de conexión parten del núcleo dentado y llegan al núcleo rojo contralateral,
a través de la decusación de los pedúnculos cerebelosos superiores .
Del núcleo rojo parten fibras hacia el núcleo olivar inferior ipsilateral a través de las fibras centrales del tegmen y finalmente de la oliva inferior parten fibras al núcleo dentado contralateral,
a través del pedúnculo cerebeloso inferior,
completando el triángulo (Fig. 43 ).
Por tanto lesiones en cerebelo,
pedúnculo cerebeloso superior o protuberancia pueden afectar al núcleo olivar inferior,
que aparece hipertrófico ( secundario a degeneración vacuolar y aumento de la astrocitosis).
La afectación será ipsilateral a la lesión si se afecta el tegmen,
contralateral si la lesión está en cerebelo o en el pedúnculo cerebeloso superior y bilateral si se afectan tegmen y pedúnculo cerebeloso superior.
La RM estructural presenta hallazgos muy característicos en la imagen potenciada en T2 o FLAIR,
con aumento de tamaño de la oliva inferior y marcada hiperseñal (Fig. 44 ).
La hipertrofia aparece generalmente entre los 4-6 meses del insulto cerebeloso o pontino y suele desaparecer a partir de los 10-16 meses,
aunque estos períodos de tiempo son solamente orientativos.
Los estudios de imagen funcional como la espectroscopía-RM o la RM de activación no son útiles en estos pacientes; la localización anatómica de la lesión impide establecer una homogeneidad adecuada del campo magnético para obtener curvas espectrales apropiadas y el temblor palatal de estos pacientes impiden una valoración de los estudios de activación motora por excesivo movimiento.
Sí son en cambio muy útiles los estudios de tensor de difusión,
que permiten identificar anomalías en la decusación de los pedúnculos cerebelosos superiores,
adelgazamientos o asimetrías en el tegmen (Fig. 45,
Fig. 46 ).
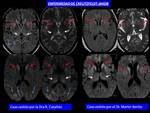
ENFERMEDAD DE CREUTZFELDT-JACOB
Enfermedad neurodegenerativa con demencia,
ocasionada por proteína priónica potencialmente transmisible que presenta un curso fatal.
Los hallazgos estructurales en RM son tan característicos (Fig. 47 ) que no son necesarios estudios de imagen avanzada.
Se identifica una alteración de la señal bilateral en secuencias T2, FLAIR y difusión de los núcleos caudados,
putámenes y tálamos.
Otras posibles localizaciones son los globos pálidos y el córtex (más frecuente frontal o temporal).
Estos cambios de señal van acompañados de atrofia.