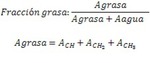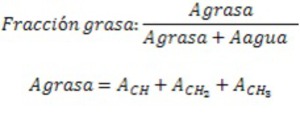La espectroscopía con RM es una técnica funcional que es capaz de diferenciar los metabolitos que componen un tejido,
pudiendo también ser cuantificados los mismos.El núcleo más comúnmente utilizado in vivo es el del Hidrógeno (1H),
existiendo también estudios espectrográficos utilizando el átomo de fósforo(31P) o el del sodio ( 23Na).
El agua es el metabolito que se usa como referencia en los estudio de espectroscopia con RM con núcleo de (1H) para la localización del resto de metabolitos,
ya que es el metabolito más abundante en los tejidos del cuerpo humano.
La espectroscopía ,
al igual que cualquier estudio de RM convencional se genera tras la aplicación de pulsos de radiofrecuencia que son recogidos y medidos por la transformada de Fournier,
solo que mientras que en una RM convencional las variaciones de frecuencia se utilizan para crear un vóxel de una imagen,
en espectroscopía son usadas para separar y caracterizar los metabolitos presentes en un voxel ,
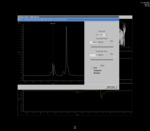
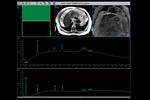
que se localizan en un eje de coordenadas x nombrado en partes por millón (ppm),
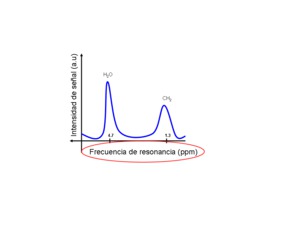
Fig. 1
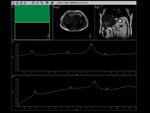
mientras que la intensidad de señal es la que sirve para cuantificar los diferentes metabolitos,
estando localizados en el eje y.
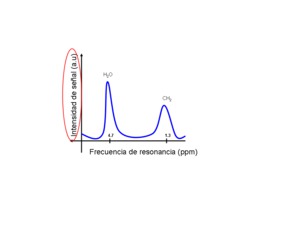
Fig. 2
Fig.
1
Las ppm reflejan la frecuencia de resonancia de cada metabolito o lo que es lo mismo,
su localización en el eje x,
siendo la frecuencia de los principales metabolitos
|
Metabolito
|
Frecuencia de resonancia (ppm)
|
|
Agua
|
4.6
|
|
Lípidos
|
0.9-1.4
|
|
Lactato
|
1,3
|
|
Glutamina
|
2,2-2,4
|
|
Citrato
|
2,5
|
|
Creatina
|
3,0
|
|
Colina
|
3,2
|
|
Alanina
|
1,48
|
|
Glucosa
|
3,4-3,8
|
Dado que los metabolitos se reflejan en un eje de coordenadas,
la altura de cada pico,
o intensidad de señal del mismo,
reflejada en el eje y,
nos podría ayudar a cuantificar ese metabolito,
calculando el área bajo la curva,
pero esa la escala de la intensidad no es una escala absoluta,
por lo que para realizar la cuantificación de los metabolitos tenemos que realizar ratios y no unidades absolutas.
Utilizamos la técnica PRESS (point-resolved spectroscopy) que se basa en la adquisición de un voxel cúbico o rectangular generado por un pulso de radiofrecuencia de 90º,
seguido por dos pulsos de 180º.
Existe otra técnica de adquisición no utilizada en nuestro centro,
que es la llamada STEAM ( stimulated-echo acquisition mode),
que genera el voxel con tres pulsos de 90º.
La diferencia entre ambas técnicas en la práctica es,
que con STEAM conseguimos generar un vóxel que no se contamina nada de información externa al mismo,
y con PRESS el vóxel no es tan homogéneo pero tiene el doble de relación señal ruido (SNR).
Para adquirir un buen espectro necesitamos que nuestro campo magnético sea muy homogéneo,
ya que pequeñas inhomogeneidades del campo hacen que los picos mtabólicos sean mucho menos uniformes y que disminuyan.
Para optimizar la homogeneidad de nuestro campo se utiliza el llamado “shimming”del campo,
que es el “preparador” de nuestro espectro,
ya que ajusta la frecuencia del campo,
optimiza la supresión y localización de los pulsos en un tiempo record,
para un estudio de hígado puede tardar unos 15 segundos.
Otra condcición técnica indispensable de la secuencia es una alta SNR,
pudiendo mejorarse aumentando el tiempo de adquisición,
aumentando el tamaño del voxel a estudiar,
utilizando un imán de mayor intensidad (mejor 3T que 1,5T),
utilizando antenas con mayor número de canales ( mejor 32 que 8 o 4 canales conectados en fase),
aunque estas dos últimas mejoras son posibles en menos casos de los que nos gustarían…
El tercer parámetro importante para adquirir un buen espectro es una supresión del agua muy potente y homogénea,
ya que en el interior de los tejidos su concentración es,
a veces,
hasta 100000 veces mayor que otros metabolitos,
perdiéndose la adquisición de los picos pequeños si no eliminamos la señal del agua.
Para suprimir el agua podemos utilizar la técnica CHESS (Chemically selective saturation),
que es una técnica que suprime el agua antes de la localización.
Es decir se aplican tres pulsos con frecuencia selectiva para suprimir el agua después de haber realizado la preparación del espectro,
eliminando así el agua.
También se puede realizar con la misma técnica la supresión de los lípidos,
utilizando frecuencias selectivas para ellos,
como se realiza en estudios de próstata.
El único problema que acarrea la utilización de CHESS es que se pierde parte de la señal de los metabolitos.
Repasaremos por los distintos órganos cómo adquirir un buen espectro y cuáles son sus aplicaciones clínicas.
1.Higado:
La mayor aplicación de la espectroscopía en abdomen y por supuesto la más validada es la cuantificación de la grasa hepática en hígado no alcohólico,
muy utilizada en la monitorización de la respuesta al tratamiento.
Los requerimientos técnicos para realizar esta adquisición son algo distintos al resto de aplicaciones clínicas:
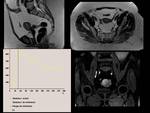
Utilizamos un vóxel único en hígado,
por lo que la elección del área de estudio es importante,
aunque se pueden realizar cuantas repeticiones de adquisición necesitemos o nos permita el paciente.
En nuestra experiencia realizamos una RM basal con adquisiciones en trigger en los tres planos del espacio de secuencias SSh-TSE-T2,
para localizar la región donde vamos a colocar nuestro vóxel y lo hacemos en trigger ya que la adquisición del espectro va a ser con respiración libre,
debido al largo tiempo de adquisición,
y por lo tanto si utilizaramos como referencia secuencias en apnea,
variaría de forma importante esa localización.
Elegimos el área con mayor cantidad de grasa per se en las secuencias realizadas con desplazamiento químico.
Colocamos el voxel de estudio,
siendo este lo mayor posible para aumentar la SNR,
alejado al menos un centímetro de los grandes vasos intrahepáticos y de los bordes hepáticos para que no exista contaminación por parte de los mismos.
Colocamos una antena de superficie multicanal.
En nuestro caso, utilizamos una antena de superficie de 6 conectores en fase para campos de 3T y de 4 conectores en campos de 1,5T.
Utilizamos técnica PRESS sin CHESS,
ya que necesitamos cuantificar la fracción grasa comparando los lípidos con el agua.
Tanto en 3T como en 1,5T,
nuestros valores son TE:35/70,
mientras que los TR son TR:8000ms para 3T y TR:4000ms para 1,5T.
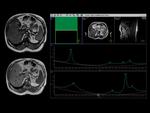
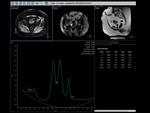
El postproceso es complicado,
realizando como primer paso un ajuste de la fase,
intentando que el agua y la grasa estén en fase.
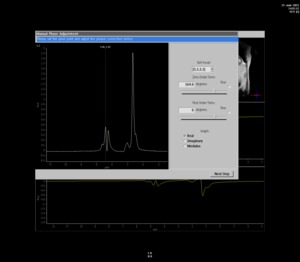
Fig. 3
Fig.3
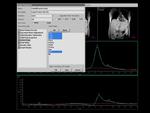
El segundo paso es la elección de los metabolitos,
que en este caso utilizaríamos el H2O y las tres fracciones lipídicas más importantes (CH,
CH2 y CH3).
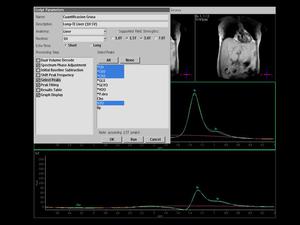
Fig. 4
Fig.4
Ajustando la línea base si es necesario.
Una vez postprocesado nuestro espectro,
calculamos la fracción lipídica con la siguiente fórmula.
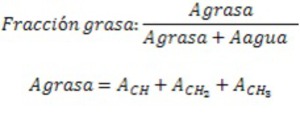
Fig. 5
Fig.5.
Cuando existe alto contenido de agua,
realizamos la cuantificación por separado del agua y de los lípidos en dos análisis distintos para que no se nos pierda ningún pico de los que queremos estudiar.
La clasificación de la esteatosis hepática subdivide a la misma en 4 subtipos:
| Grados |
% de grasa |
| Grado 0 |
< 5% |
| Grado 1 |
6-33% |
| Grado 2 |
34-66% |
| Grado 3 |
> 66 % |
Clasificación de la esteatosis hepática
Indicando el siguiente esquema una gráfica de cada uno de los cuatro grados de esteatosis que podemos encontrar.
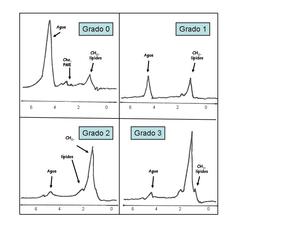
Fig. 6
Fig 6
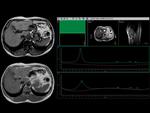
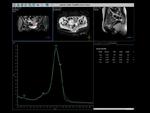
El primer ejemplo objetivado es el de un espectroscopía hepática en un paciente que no presenta esteatosis hepática,
nio existiendo apenas lípidos en ninguno de los dos ecos,
tampoco objetivamos pérdida de señal del parénquima en fase opuesta con respecto a fase.
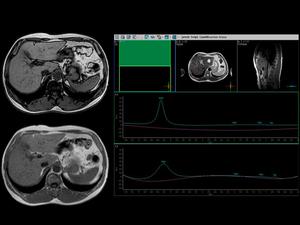
Fig. 8
Fig.7
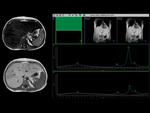
En el siguiente ejemplo visualizamos una pérdida marcada de señal en secuencias en fase opuesta con respecto a fase,
objetivando un aumento en el pico de los lípidos en ambos ecos,
presentando el paciente una fracción grasa del 18% .
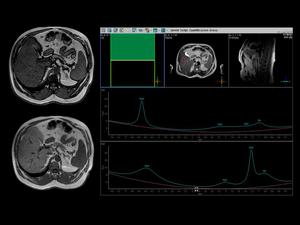
Fig. 7
Fig.8
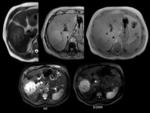
El siguiente paciente presentaba un afracción grasa del 83% y por lo tanto una esteatosis severa o grado 3,
con marcada pérdida de señal en fase opuesta con respecto a fase y una importante inversión en la relación lípidos/agua.
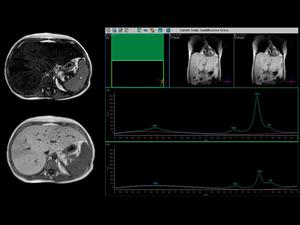
Fig. 9
Fig.9
Otra de las aplicaciones que nos permite realizar la espectro de hígado es la detección de colina en tumoraciones malignas,
lo que ayuda a diferenciar entre tumoraciones malignas y benignas,
siendo factor pronóstico desfavorable el aumento de colina.
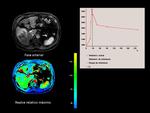
El las Fig.10 y Fig.11 visualizamos una masa hepática que ocupa el segmento 5,
isointensa en T2,
hiperintensa en T1,
indicando su contenido graso,
con una curva de perfusión que presenta una importante captación en fase arterial y posterior lavado de la misma,
tratandose de un hepatocarcinoma bien diferenciado.
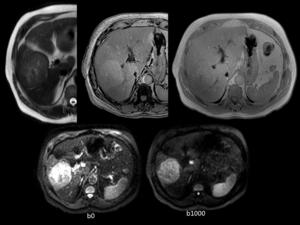
Fig. 10
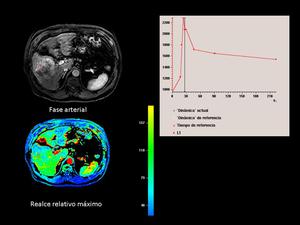
Fig. 11
Objetivamos un dicreto pico de colina en el estudio espectroscópico.
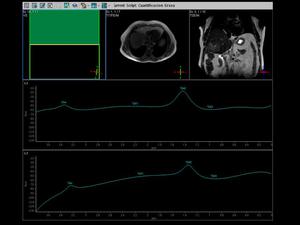
Fig. 13
Fig.
12
A diferencia del caso anterior,
en el siguiente ejemplo que también se trataba de un hepatocarcinoma,
aunque en este caso mal diferenciado,
el pico de colina es mucho más acentuado,
lo que indica un mayor grado de agresividad biológica y potencialmente peor pronóstico.
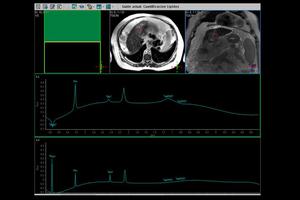
Fig. 12
Fig.13
2.
Próstata:
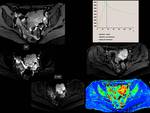
Es el órgano abdominal y pélvico, donde el estudio espectroscópico con RM está más validado es en la próstata.
Los aspectos técnicos a tenes en cuenta para adquisición de un buen espectro son:
- realizar un T2TSE axial con misma orientación que el volumen espectroscópico como referencia anatómica.
- Utilizamos técnica multivoxel 3D con desplazamiento químico PRESS,
con TE:100 ms y TR: 1500ms,
con tecnica CHESS asociada para supresión de agua y lípidos para 3T.
- Empleamos shimming automático para reducir el ancho de línea.
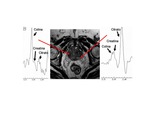
En próstata se realiza la medición de otros metabolitos específicos de la misma como son: citrato (2,6ppm),
creatina (2,83ppm),
poliaminas (3,1ppm) y colina (3,2ppm).
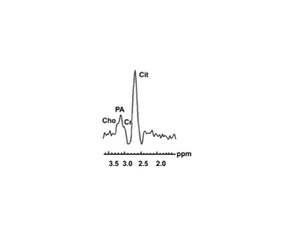
Fig. 14
Fig.
14
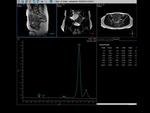
Dado que no se pueden determinar valores absolutos se utilizan índices para diferenciar el tejido normal del patológico: Cho/Ci,
Cho+Cr/Ci,
Pa/Cho.
De tal forma que el aumento de l índice Cho+Cr/Ci por encima de 0,7-0,8 sugiere malignidad.
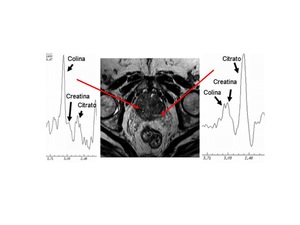
Fig. 15
Fig.15
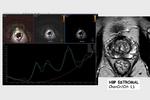
Podemos diferenciar 5 tipos de espectros prostáticas,
espresadas en el siguiente esquema Fig.16,
que van desde los bajos niveles de colina y altos de citrato que presenta el espectroscopia de una zona prostática sana a la ausencia de citrato con aumento marcado de colina de una espectroscopia con perfil metabólico muy típico de carcinoma.
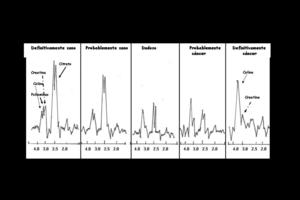
Fig. 16
Las indicaciones clínicas de la espectroscopía RM de próstata son:
1.Mejorar la localización y detección del carcinoma de próstata en la zona periférica,
sobre todo en carcinomas de pequeño tamaño y de bajo grado.
De esta forma en el siguiente ejemplo,
que en el estudio basal se visualiza un carcinoma de próstata en la zona periférica prostatica,
parasagital derecho,
que no parece presentar invasión extracapsular,
al realiza el espectro con vóxel pequeño visualizamos aumento de colina cambiando el estadiaje de un T2 a un T3,
ya que se demuestra invasión extracapsular.
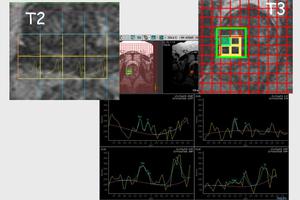
Fig. 17
Fig.17
2.
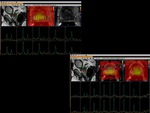
La RM espectroscopía es superior a la RM convencional en la detección del volumen tumoral.
En la siguiente figura podemos cuantificar el volumen que corresponte a un carcinoma de alto grado.
Amenor tamaño de voxel en la espectroscopía 3D,
mejor estimación real de los voxeles afectos,
como se demuestra en la siguiente figura
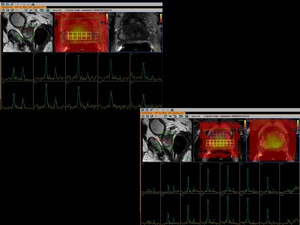
Fig. 18
Fig.
18
3.
Mejora la detección del carcinoma en la zona de transición,
aunque es importante conocer la limitación existente para discernir entre carcinoma e hiperplasia benigna de próstata estromal,
ya que puede existir un aumento de la colina y una disminución del pico del citrato,
como ocurre en el siguiente ejemplo.
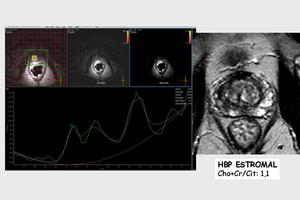
Fig. 19
Fig.19.
4.
Aporta información en la evaluación de la respuesta terapeútica,
ya que disminuye de forma temprana el pico de citrato y poliamidas y de forma tardía el de colina y creatina.
5.
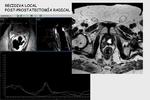
Ayuda a la detección de la recidiva postratamiento,
ya que existe un incremento del índice Cho/Cr.
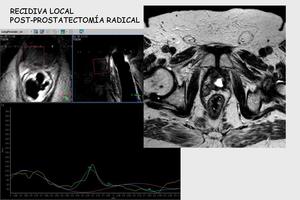
Fig. 20
Fig.20
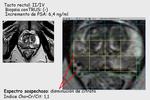
6.
Juega un papel importante a la hora de dirigir biopsias en pacientes con PSA elevado de forma persistente y biopsias negativas repetidas y en tumores de cara anterior o lateral.
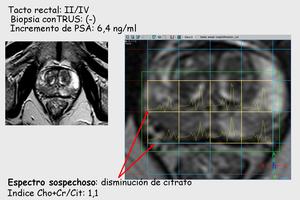
Fig. 21
Fig.21
Aunque también presenta limitaciones como son el que nos encontramos ante una técnica compleja,
con resultados dependientes del postproceso y del shimming,
con tiempos de adquisición muy largos,
siendo muy susceptibles a artefactos como la hemorragia postbiopsia.
3.
Otros órganos:
En nuestra experiencia realizar estudios espectroscópicos intaabdominales fuera de los dos órganos antes descritos es bastante complicado,
ya que los estudios se artefactan de forma importante por los movimientos respiratorios y de las asas intestinales.
A pesar de ello existen estudios recientes en la literatura que demuestran las aplicaciones de la espectroRM en ovario,
como el estudio de Takeuchi et al.
(European Radiology,
2011) que demuestran que en tumores ováricos de estirpe mucinosa,
existe un importante pico en 2 ppm,
que es capaz de diferenciarlos de los tumores no mucinosos o como el estudio de Esseridou et al (Invest Radiol.2011), que demuestra que en las lesiones malignas existe un pico e colina,
no evidenciandose en las tumoraciones benignas.
En el siguiente ejemplo,
realizado con ténica PRESS asociada a CHESS para suprimir el agua,
en imán de 3T,
con un TE:135 y TR:1600,
visualizamos como la paciente que presenta una masa dependiemte del ovario izquierdo,
mixta, presenta un importante pico de lípidos ,
así como un aumento de la colina y una inversión del pico en 2ppm,
tratandose de un cistoadenocarcinoma seroso.
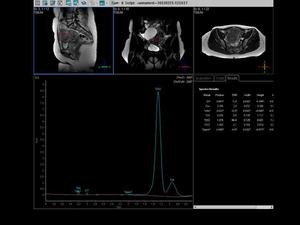
Fig. 22
Fig.22.
De la misma forma también existen estudios relacionados con el cuerpo uterino y la diferenciación de tumores benignos y malignos,(Takeuchi et al.
(European Radiology,
2011)),
donde se confirma que la presencia de colina en lesiones endometriales está asociada con la malignidad tumoral,
asociandose la amplitud de la curva con un mayor grado histológico.
Así en el siguiente ejemplo observamos una lesión de pequeño tamaño en cavidad endometrial que invade a la zona de transición y miometrio
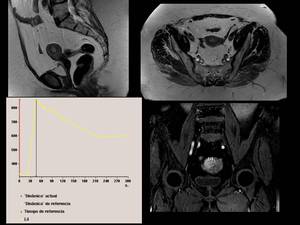
Fig. 23
Fig.
23,
que se trata de un adenocarcinoma de endometrio bien diferenciado,
que en el estudio espectroscópico muestra un pico de colina significativo, aunque no demasiado pronunciado
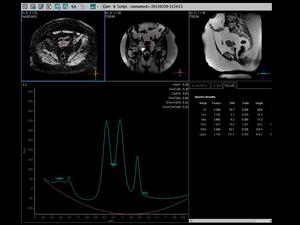
Fig. 24
Fig.
24,
Un último ejemplo es el que muestra una gran masa pélvica que presenta marcada restricción de la difusión e importante captación tras la administración de gadolinio con posterior lavado de la lesión,
trantandose de un linfoma.
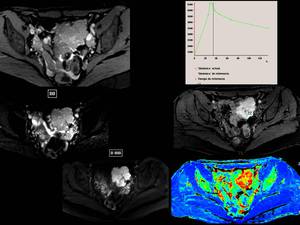
Fig. 25
Fig.25
En el estudio con espectrografía nos muestra un alto contenido lipídico y un pico de colina,
indicando la malignidad del proceso.
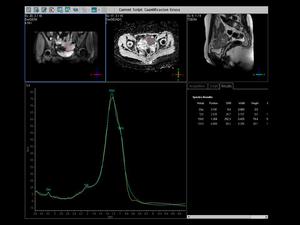
Fig. 26
Fig.26