El protocolo de estudio con TC multimodal del ictus agudo,
consiste en la realización de tres series,
con el objetivo de obtener una información básica que debemos proporcionar al neurólogo.

Fig. 1: Protocolo de estudio con TC multimodal del ictus agudo.
Habitualmente,
cuando analizamos un angioTC nos centramos en localizar la arteria concreta donde se encuentra el “stop”.
Sin embargo,
existen otros parámetros que se pueden evaluar.
Vamos a ir revisando la importancia de cada uno de ellos.
- Localización de la oclusión o estenosis:
- Parámetro fundamental a evaluar en el angioTC.
- Hay que revisar las principales arterias intracraneales en los tres planos del espacio,
empleando un reformateo multiplanar de máxima intensidad de proyección (MIP) de 20-25 mm,
para una rápida identificación de oclusiones o estenosis en las arterias carótidas o cerebrales medias.
- En nuestro centro,
el análisis básico está estandarizado con nueve imágenes predefinidas reformateadas con MIP del polígono de Willis (cuatro axiales, tres sagitales -línea media y una en cada valle silviano- y dos coronales).
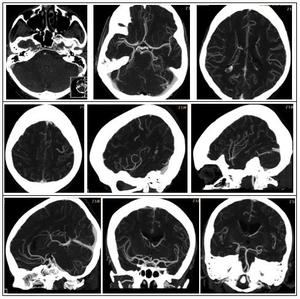
Fig. 2: Planos básicos a buscar en el reformateo.
- Posteriormente,
una revisión rápida de las imágenes axiales,
sin MIP,
de los vasos desde la aorta hasta el vertex,
especialmente para valorar ambas carótidas internas y vertebrales.
Tras ello,
obtener imágenes adicionales para detectar obstrucciones en vasos menores como ramas CM2-CM3.
- Finalmente, se pueden obtener imágenes de dichos vasos realizando un reformateo curvo y 3D-volume rendering de los mismos.
Sobre estas imágenes,
evaluamos la presencia de placas de ateroma calcificadas o no,
ulceraciones,
y cuantificación del grado de estenosis.
Este reformateo curvo es especialmente útil para la evaluación de arterias con características morfológicas complejas.
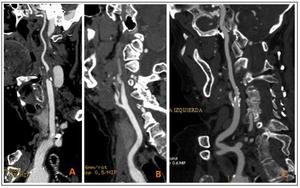
Fig. 3: Imágenes de reformateo curvo de vasos carotídeos. A)Estenosis en arteria carótida interna (ACI). B)Oclusión de ACI. C) Placas de ateroma calcificadas en bifurcación carotídea.
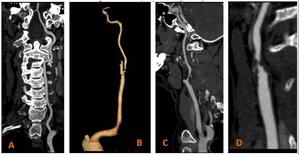
Fig. 4: Ejemplos de imágenes de reformateo curvo y 3D-volume rendering de los vasos carotídeos y vertebrales. A)Imagen de reformateo curvo de la arteria vertebral izquierda. B, C Y D)Imágenes de 3D-volume rendering y reformateo curvo de la arteria carótida, donde se observa una placa de ateroma que condiciona una estenosis significativa.
- Cuando el vaso afectado por la oclusión o estenosis es uno de gran o mediano calibre,
resulta sencillo localizarlo.
Sin embargo,
si se trata de un vaso muy distal de pequeño calibre,
la detección del mismo puede ser muy complicada.
Un truco para localizar la oclusión en estos casos,
es buscar una rama arterial distal que presente un mayor calibre del que debería tener en condiciones normales.
Se trata de un vaso distal a la oclusión,
que recibe flujo colateral retrógrado,
lo cual condiciona aumento de su diámetro.
Buscando ahora el tramo vascular que se continúa con dicha arteria de mayor calibre,
llegaremos al punto de obstrucción.
- En los procedimientos neurointervencionistas se emplea una escala de Trombolisis en el infarto cerebral (TICI),
para la evaluación de la perfusión distal a la oclusión a través de flujo anterógrado.
Se trata de una escala obtenida a partir de la modificación del TIMI (escala utilizada por los cardiólogos intervencionistas).
Existen una serie de inconsistencias en dicha clasificación,
por lo que muchos casos no pueden ser categorizados usando la escala TICI original.
Por ello,
otras escalas han sido propuestas para graduar los resultados angiográficos de la intervención en el infarto cerebral.
Algunas añaden una subcategoría 2C,
otras usan el 50%,
en lugar de los 2/3,
como punto de corte entre 2A y 2B,
y otras incluyen el flujo colateral en los resultados.

Fig. 5: Escala de Trombolisis en el infarto cerebral (TICI), con la que se evalúa la perfusión distal a la oclusión a través de flujo anterógrado.
El éxito de la recanalización por trombolisis intravenosa de un vaso obstruido,
en el contexto de un ictus agudo,
depende de la longitud del trombo,
es decir,
de la cantidad de trombo intravascular a disolver.
Se ha demostrado que,
un trombo de longitud menor de 5 mm es altamente probable que se disuelva con trombolisis intravenosa,
mientras que tan sólo el 1% de los trombos mayores de 8 mm pueden recanalizarse con este tratamiento.
En estos últimos pacientes,
la terapia intraarterial inmediata puede ser el tratamiento de elección.
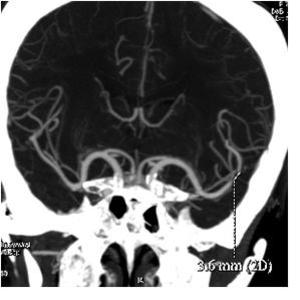
Fig. 6: Imagen de reformateo con MIP en el plano coronal, donde se visualiza un trombo de longitud menor de 5 mm, que es altamente probable que se disuelva con trombolisis intravenosa.
Existen pacientes en los que se aprecia una aparente obstrucción desde la bifurcación carotídea,
realmente causada por un trombo más distal y bloqueo del flujo proximal al mismo.
Es decir,
no toda la carótida obstruida es un trombo.
Resulta interesante estimar la densidad del trombo,
mediante la cuantificación de sus Unidades Hounsfield (UH) en un TC sin contraste,
puesto que es un parámetro útil para predecir la probabilidad de recanalización precoz con trombolisis intravenosa.
Para ello,
es necesario realizar reconstrucciones finas (con un grosor de corte menor de 3 mm) del TC sin contraste rutinario.
Existen varios tipos de trombos,
que se clasifican en función de su composición.
Trombos blancos,
que presentan cantidades variables de fibrina,
plaquetas,
ateromatosis,
debris celular y pocos eritrocitos,
lo que resulta en valores de UH menores y mayor resistencia a los agentes fibrinolíticos.
Trombos rojos,
que contienen altas concentraciones de eritrocitos y pequeñas cantidades de fibrina,
resultando en valores de UH más elevados y mayor susceptibilidad al tratamiento fibrinolítico.
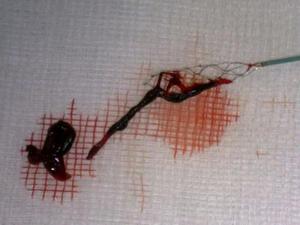
Fig. 7: Se realiza tratamiento endovascular (embolectomía), extrayéndose un trombo rojo. Imagen cedida por el Dr. A. González Mandly (Neuro-radiólogo del HUMV).
Trombos mixtos,
presentando en ese caso un comportamiento variable en función de la proporción de sus componentes.
Trombo graso. Existen casos excepcionales,
en los cuales identificamos una arteria hipodensa en el estudio basal,
con valores de densidad grasa en UH. Este hallazgo puede confirmarse en el angioTC y en la RM.
Trombos calcificados presentan poca respuesta al tratamiento fibrinolítico,
que únicamente condiciona fragmentación parcial de los mismos,
con el consiguiente riesgo de migración distal de dichos fragmentos.
Parece razonable pensar,
que en estos casos,
el tratamiento de elección será el manejo endovascular.
Se ha descrito que la cuantificación de las HU del trombo en un TC sin contraste puede predecir el éxito de la recanalización tras trombolisis intravenosa.
El punto de corte establecido en algunos estudios es de rHU* 1.382,
valor obtenido con análisis ROC.
De esta forma,
valores de HU menores de dicho punto de corte se asociaban con ausencia de recanalización tras el tratamiento fibrinolítico endovenoso.
Este método,
por tanto,
podría resultar de utilidad para el triaje rápido de los pacientes,
decidiendo si son subsidiarios de trombolisis intravenosa,
intraarterial o tratamiento endovascular.
[J.
Puig et al.]
*(rHU: ratio de HU: valor de HU corregido con la determinación de las HU del segmento normal contralateral.
Esto es necesario porque el valor de las HU está condicionado por el hematocrito.
Así el cálculo del rHU = ACM del lado sintomático/ ACM del lado asintomático.
ACM= arteria cerebral media).
<< El signo de la arteria cerebral hiperdensa es un indicador de trombo intraluminal,
que constituye un hallazgo precoz del TC sin contraste descrito en hasta la mitad de los casos de ictus isquémicos agudos. Se ha comprobado que la desaparición de este signo durante el seguimiento es un indicador de resultado favorable tras la fibrinolisis intravenosa.>>
- Flujo arterial colateral distal:
Los vasos arteriales leptomeníngeos colaterales,
probablemente mejoran los resultados neurológicos,
por dos razones fundamentales:
1.Limitan la extensión del parénquima cerebral infartado,
al mantener la viabilidad del tejido penumbra.
2.La circulación colateral intensa se ha relacionado con mayores ratios de recanalización,
porque puede incrementar la entrada de los fibrinolíticos dentro del coágulo y facilitar su disolución,
o incluso,
podría ayudar a la revascularización,
al alterar el grado de impactación del trombo dentro de los vasos sanguíneos cerebrales.
La circulación arterial colateral leptomeníngea constituye un marcador fiable de buen pronóstico en pacientes con ictus por obstrucción en una arteria intracraneal proximal,
con la disminución del volumen infartado y,
por consiguiente,
la mejora de los resultados funcionales,
menor mortalidad intrahospitalaria y a los 6 meses post-infarto.
EVALUACIÓN DE LA CIRCULACIÓN COLATERAL
Ésta es una versión simplificada de la escala clásica de clasificación angiográfica de la circulación colateral:

Fig. 8: Escala para la evaluación de la circulación colateral.
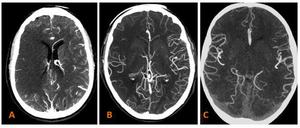
Fig. 9: A)No hay vasos colaterales visibles en el sitio de isquemia (grado 1).
B)Existen escasos vasos colaterales visibles en el lecho isquémico (grado 2).
C) Se identifica flujo colateral normal (igual que en el lado contralateral)(grado 3).
- Imágenes fuente del angio-TC (CTA ‘source images’):
Se ha demostrado que la valoración de las imágenes fuente del angio-TC es más sensible que la realizada en el TC sin contraste en cuanto a la detección de signos de isquemia irreversible precoz,
y más precisa en la predicción del volumen infartado final.
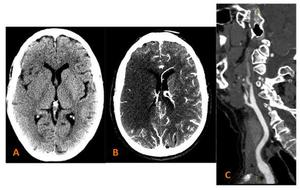
Fig. 10: A) TC basal (sin contraste ev): Discreto borramiento de los surcos fronto-temporales derechos, con ligera pérdida de la diferenciación sustancia blanca-gris. B) Angio-TC imágenes fuente: Hipodensidad llamativa en la región fronto-temporal derecha. C) Reformateo curvo de la arteria carótida derecha, donde se observa una oclusión de la ACI.
Se demuestra que la valoración de las imágenes fuente del angio-TC es más sensible que la realizada en el TC sin contraste, en cuanto a la detección de signos de isquemia irreversible precoz, y más precisa en la predicción del volumen infartado final.
Las imágenes fuente del angio-TC proporcionan un mapa de perfusión de todo el cerebro (más allá del volumen estudiado con la perfusión),
ya que el agente de contraste rellena la microvasculatura del tejido sano,
pero no la microvasculatura de las regiones cerebrales infartadas,
viéndose estas últimas zonas como áreas hipoatenuadas.
Para visualizar correctamente potenciales alteraciones de densidad en el parénquima cerebral,
se debe emplear una ventana estrecha.
Se puede facilitar la visualización de las áreas hipodensas bien con pequeños MIP de 10-15 mm o incluso minIP,
según la localización a valorar y el hábito del explorador.
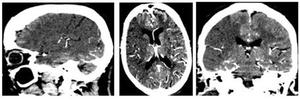
Fig. 11: Ejemplo de imágenes fuente del angio-TC, en donde las regiones cerebrales infartadas se visualizan como áreas hipoatenuadas. Como en este ejemplo, se debe emplear una ventana estrecha, que permita identficar correctamente potenciales alteraciones de densidad en el parénquima cerebral.
Si el estudio del angio-TC se obtiene en una fase muy precoz (arterial),
como es frecuente en máquinas muy modernas,
las áreas hipodensas del parénquima cerebral se correlacionan con las alteraciones del mapa de flujo del TC perfusión (zona penumbra + infartada).
Si el estudio del angio-TC se obtiene en una fase más tardía (venosa),
como sucede en la mayoría de casos tras realizar estudio de TSA,
las zonas hipodensas de las imágenes fuente se correlacionan con las lesiones hiperintensas vistas en las imágenes potenciadas en difusión (RM) y con las alteraciones del mapa de volumen del TC perfusión (zona infartada).
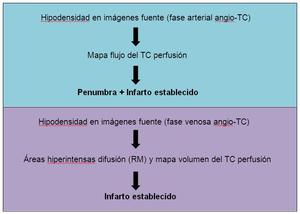
Fig. 12: Resumen de la interpretación de las imágenes fuente del angio-TC, en función de si el estudio se ha realizado en fase arterial o venosa.
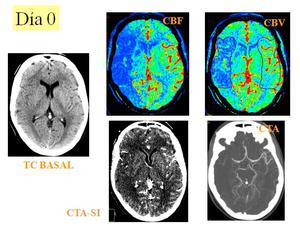
Fig. 13: Caso de un paciente con clínica de ACM derecha, a las pocas horas del inicio de la sintomatología. TC craneal basal: Discreto borramiento de surcos y pérdida de la diferenciación sustancia blanca-gris en la región fronto-temporal derecha. CBF: Disminución del flujo en todo el territorio de la ACM derecha. CBV: Disminución del volumen en gran parte del territorio de la ACM derecha, con volumen conservado en la región más anterior y posterior de dicho territorio. CTA-SI (imágenes fuente del angio-TC): Estudio adquirido en fase venosa. Hipodensidad en el parénquima cerebral, en donde se observa la disminución del volumen. Angio-TC reformateo con MIP axial: Interrupción de la ACM derecha en CM1 proximal por la presencia de un trombo.
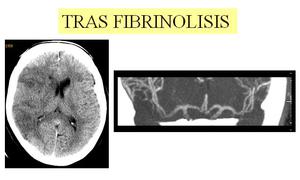
Fig. 14: Mismo paciente del caso anterior, tras el tratamiento fibrinolítico. Control a las 24h: TC craneal basal: Áreas hipodensas y borramiento de los surcos adyacentes en región fronto-temporal derecha, compatibles con isquemia aguda. La zona infartada es bastante superponible al área hipodensa que se veía en las imágenes fuente del angio-TC, que cuando se adquiere en fase venosa, aporta una buena aproximación de qué tejido presenta isquemia irreversible. Angio-TC: Repermeabilización de la ACM derecha.
Valoración del parénquima con CTA-si + ASPECTS.
Existe una escala para el territorio de la arteria cerebral media y otra para la circulación posterior.
En el caso de la arteria cerebral media (ACM),
la topografía del ASPECTS divide el territorio en 10 regiones (caudado,
núcleo lenticular,
cápsula interna,
ínsula y M1-M6).
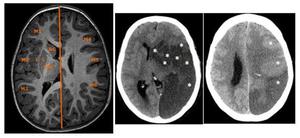
Fig. 15: Esquema de la topografía del ASPECTS en el caso de la arteria cerebral media: territorio dividido en 10 regiones (caudado, núcleo lenticular, cápsula interna, ínsula y M1-M6). Imágenes, en donde con los asteriscos aparecen señaladas las 10 regiones, estando afectadas las áreas hipodensas.
El paciente sano tiene un ASPECTS de 10.
Se resta un punto por cada región afectada (hipodensidad en las imágenes fuente del angioTC).
Así,
por ejemplo,
si encontramos 4 de estas regiones hipodensas,
la puntuación en este caso sería 6.
En el territorio de la arteria cerebral posterior (ACP),
la topografía del ASPECTS divide el territorio en 10 regiones (tálamo,
hemisferio cerebeloso,
territorio de la ACP,
mesencéfalo y puente,
considerando el lado derecho e izquierdo por separado en cada estructura anatómica). En este caso,
se resta un punto por cada región afectada,
salvo en el caso del mesencéfalo o el puente que se restan 2 puntos.
- Patología vascular subyacente de TSA
1- Ateromatosis carotídea:
Sobre las imágenes, especialmente las reconstrucciones curvas, evaluamos la presencia de placas de ateroma calcificadas o no,
ulceraciones,
y cuantificación del grado de estenosis.
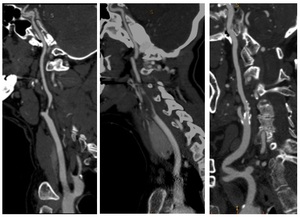
Fig. 16: Ejemplos de ateromatosis carotídea en imágenes de reconstrucciones curvas.
Para un correcto cálculo de la estenosis se emplean aplicaciones semiautomáticas,
que obtienen el área seccional y los diámetros luminales ortogonales.
De este modo,
se reduce la variabilidad interobservador en la medida del diámetro de la luz del vaso.
Sin embargo,
es importante correlacionar estos datos con los que obtenemos con la visualización directa de las imágenes fuente axiales del angio-TC.
Estudios recientes han demostrado que estas medidas son comparables con las de la angiografía.
Trucos para una correcta valoración:
- Realizar un ajuste de la ventana apropiado,
debido a que las alteraciones en la densidad de contraste intraluminal pueden producir diferencias significativas en la medida de la luz residual.
- El artefacto provocado por la presencia de placas ateromatosas calcificadas puede condicionar una sobreestimación del grado de estenosis,
aún más acusado en pacientes con stent.
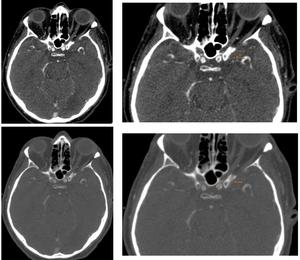
Fig. 17: El artefacto provocado por la presencia de placas ateromatosas calcificadas puede condicionar una sobreestimación del grado de estenosis. En este caso, se demuestra la importancia de la ventana empleada para valorar la luz del vaso. Cuando se emplea una ventana de partes blandas el artefacto del calcio es más patente que cuando se emplea una ventana de hueso, sobreestimándose el grado de estenosis en el primer supuesto.
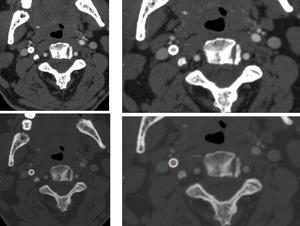
Fig. 18: El artefacto provocado por la presencia de un stent puede condicionar una sobreestimación del grado de estenosis, aún más acusada que en el caso de las placas ateromatosas calcificadas. En este caso, se demuestra la importancia de la ventana empleada para valorar la luz del vaso. Cuando se emplea una ventana de partes blandas el artefacto del stent es más patente que cuando se emplea una ventana de hueso, sobreestimándose el grado de estenosis en el primer supuesto.
2- Disección de la arteria carótida:
- Desgarro de la pared de la arteria,
que permite la entrada de sangre y la separación de las capas murales.
Se visualiza como un estrechamiento de la luz del vaso +/- dilatación focal aneurismática.
A veces,
se identifica un trombo intramural (semiluna de baja atenuación).
- Normalmente ocurre en la arteria carótida interna (ACI).
Es menos común en la arteria carótida común,
que suele ser una extensión superior de la disección del arco aórtico.
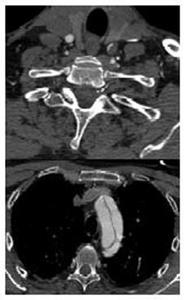
Fig. 19: Ejemplo de un paciente que presenta una disección del arco aórtico, con extensión superior hacia la arteria carótida común izquierda.
- Hallazgos de imagen:
- Patognomónico: flap intimal o doble luz (en menos del 10% de los casos).
- Dilatación aneurismática (en el 30% de los casos): es común en el segmento distal subcraneal de la ACI.
- En la fase aguda: oclusión de la ACI en forma de llama.
- No realce del vaso si la oclusión es completa,
+/- recanalización distal de la porción cavernosa de la ACI por vasos colaterales.
- La disección normalmente se origina en la ACI en los 2-3 cm distales al bulbo carotídeo.
Se extiende con una longitud variable a lo largo de la ACI distal.
El stop de la disección ocurre antes de la porción petrosa.
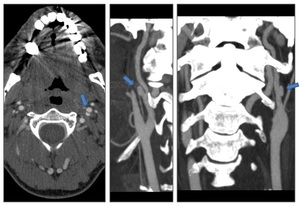
Fig. 20: Disección de la arteria carótida interna(ACI)izquierda. Se visualiza un estrechamiento de la luz del vaso, con una dilatación focal aneurismática. Como ocurre típicamente, se origina en la ACI en los 2-3 cm distales al bulbo carotídeo.
3- Aneurismas arteriales:
Normalmente,
es más común encontrar pseudoaneurismas,
que pueden aparecer por múltiples causas (secundarios a una disección,
post-traumáticos,
por enfermedad aterosclerótica,
iatrogénicos etc).
Se visualizan como un aumento focal del vaso,
existiendo en ocasiones trombo intraluminal.
Con el angioTC podemos valorar el tamaño del aneurisma,
la extensión del trombo intraluminal y el flujo sanguíneo en la luz del vaso.
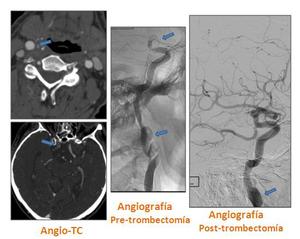
Fig. 21: Angio-TC: Se identifica un aumento focal de la ACI derecha en su porción cervical, en relación con un aneurisma. Presenta también, un defecto de repleción en la luz de la ACI derecha en su porción cavernosa, compatible con un trombo a dicho nivel. Angiografía de la misma paciente: Imagen pre-trombectomía y post-trombectomía. Se visualiza también el aneurisma de la ACI.
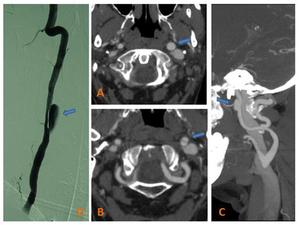
Fig. 22: Angio-TC: Paciente que presenta un aneurisma en la ACI izquierda en su porción cervical secundario a una disección. Se visualiza(A)un aumento focal de la ACI izquierda y, en otro corte más superior(B), un estrechamiento de la luz del vaso con una dilatación aneurismática focal. (C)Reconstrucción sagital del angio-TC.
Angiografía de otra paciente (D), que pone de manifiesto otro aneurisma disecante de la ACI.
4- Displasia fibromuscular:
Se trata de una enfermedad arterial de etiología desconocida,
que afecta a los vasos de gran y mediano calibre.
La clínica típica de sospecha es una mujer joven con un accidente isquémico transitorio.
En el angioTC se identifican cambios morfológicos en las arterias carotídeas y vertebrales:
- Irregularidad en la pared de los vasos: Imagen en “cadena de perlas”.
- Estenosis segmentaria larga sin calcio mural.
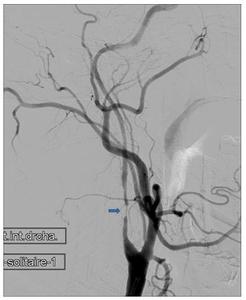
Fig. 23: Mujer joven que acude con clínica de accidente isquémico transitorio.
En la angiografía se identifica una estenosis segmentaria larga, compatible con displasia fibromuscular.
Puede estar asociada a una disección,
un pseudoaneurisma o un aneurisma intracraneal.
El angioTC constituye una herramienta de utilidad para definir un mapa vascular ,
que permita conocer la disposición de los vasos (TSA y polígono de Willis),
con el fin de facilitar la realización de las maniobras intervencionistas.
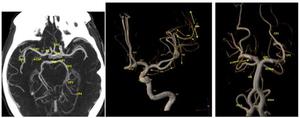
Fig. 24: Ejemplo de mapa vascular obtenido a partir del angio-TC, con el que conocemos la disposición de los vasos del paciente.
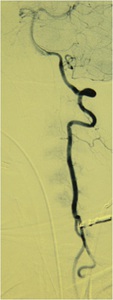
Fig. 25: Angiografía: Ejemplo de variante anatómica, consistente en una duplicación de V1 izquierda (origen en arteria subclavia izquierda y en cayado). Imagen cedida por el Dr. A. González Mandly (Neuro-radiólogo del HUMV).


























