La clásica clasificación de las miocardiopatías propuesta en 1995 por la Organización Mundial de las Salud (OMS)1,
se ha visto obsoleta debido al mayor conocimiento de las miocardiopatías,
con el apoyo de la biología molecular.
En el año 2006,
la Sociedad Americana del Corazón (AHA) y posteriormente en el año 2008,
la Sociedad Europea de Cardiología (ESC),
establecieron nuevas definiciones y clasificaciones de las miocardiopatías,
que ha iniciado un debate acerca de cuál de ellas es la más apropiada.
Fig. 1
La AHA define las miocardiopatías como "un grupo heterogéneo de enfermedades del miocardio asociadas con disfunción mecánica y/o eléctrica,
que usualmente (pero no invariablemente) exhiben hipertrofia o dilatación ventricular inapropiadas,
debidas a una variedad de etiologías que frecuentemente son genéticas.
Las miocardiopatías son tanto confinadas al corazón o como parte de desórdenes sistémicos generalizados,
y a menudo llevan a muerte cardíaca o fallo cardíaco progresivo con la discapacidad relacionada".2
La ESC presenta la siguiente definición de miocardiopatía: "es un desorden miocárdico en el cual el músculo del corazón es estructuralmente y funcionalmente anormal en ausencia de enfermedad arterial coronaria,
hipertensión,
enfermedad valvular o cardiopatía congénita".3
La AHA defiende una clasificación basada en un enfoque genético-molecular,
con ampliación del concepto de miocardiopatía al ámbito eléctrico y manteniendo la división en primarias y secundarias.
Sin embargo,
la Sociedad Europea expresa un claro desacuerdo en estos puntos,
planteando además que su clasificación tiene más utilidad en la práctica clínica diaria.
Basándonos en la clasificación de la AHA,
nos centraremos en las miocardiopatías secundarias,
que son aquellas que muestran afectación miocárdica como parte de un amplio grupo de trastornos sistémicos generalizados (Tabla 1).
El desarrollo de campos magnéticos de alta intensidad,
antenas de superficie,
muestreo rápido del espacio K,
técnicas de postproceso y secuencias para la caracterización miocárdica,
han hecho de la RM una técnica imprescindible en el manejo de las miocardiopatías complejas.
Los pacientes fueron sometidos a una exploración de RM en un equipo de 1,5 Tesla (Intera,
Philips) y ninguno de ellos requirió anestesia.
El protocolo habitual consistió en:
- Secuencias cine (SSFP) en planos dos cámaras,
cuatro cámaras y eje corto.
- Secuencia morfológica FSE sangre negra en plano axial.
- Secuencia de contraste de fase.
- Secuencia FFE IR potenciada en T1,
a los 10-15´ de la administración de gadolinio,
a dosis de 0,2 mmol/Kg de peso.
Las secuencias de sangre negra representan el primer paso en la evaluación de las miocardiopatías,
por su alta resolución espacial y contraste de los tejidos.
Las imágenes cine son importantes en la evaluación de volúmenes cardíacos y contractilidad,
siendo imprescindibles para estimar la función cardíaca.
Las secuencias de contraste de fase permiten estudiar el flujo transvalvular y las de realce tardío son fundamentales en la caracterización de las miocardiopatías.
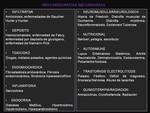
MIOCARDIOPATIAS SECUNDARIAS
INFILTRATIVAS
Amiloidosis
Es una enfermedad sistémica caracterizada por el depósito extracelular y/o intracelular de fibras insolubles de amiloide anómalo.
En el caso del corazón el depósito de amiloide tiene lugar en el intersticio miocárdico,
siendo esto más frecuente en las formas sistémica primaria (depósito de cadenas ligeras) y sistémica senil (depósito de transtirretina).
Esto condiciona un engrosamiento del miocardio,
asociado a una función ventricular deprimida y disminución de la complianza que conduce en fases tardías a una miocardiopatía restrictiva.4A menudo asocia fibrosis endomiocárdica que contribuye a la disfunción diastólica.
Las aurículas pueden estar dilatadas y alterarse el patrón de flujo transvalvular.
Aunque la técnica ideal para su diagnóstico debería ser la biopsia cardiaca,
esta puede no ser concluyente dado que el depósito de amiloide es heterogéneo.
Por ello habitualmente se llega al diagnóstico mediante biopsia no cardíaca,
valoración de las anomalías electrocardiográficas,
ecocardiografía y RM.
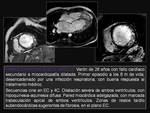
Hallazgos en RM: 5,6 Fig. 2
- Engrosamiento mural de ambos ventrículos,
que suele ser difuso más que focal,
a diferencia de la MCH.
- El engrosamiento del septo interauricular (>6 mm) y de la pared posterior de la aurícula derecha,
son sugestivos.
- Disfunción sistólica y diastólica con patrón restrictivo.
- Patrón de realce característico: difuso,
heterogéneo y subendocárdico,
que recuerda a una supresión incorrecta de la señal miocárdica,
debido a un TI inapropiado.
El realce focal se correlaciona con áreas de hipoquinesia o aquinesia.7
- El miocardio afecto por depósito de amiloide tiene un T1 a los 4 minutos,
sustancialmente menor que los controles y este dato representa un marcador directo de la carga de amiloide cardíaco8.
- Derrame pleural y pericárdico.
El patrón típico de realce tardío está asociado a un mayor acúmulo de amiloide intersticial,
peor clase funcional,
mayor hipertrofia miocárdica y a peor función sistólica9.
La RM ha demostrado ser útil en la valoración cuantitativa de la carga de amiloide tras recibir tratamientos específicos para la enfermedad.
8
DEPOSITO
Hemocromatosis
La miocardiopatía por sobrecarga de hierro es una complicación de la hemocromatosis hereditaria,
que afecta predominantemente a los descendientes del Norte de Europa,
donde la mutación homocigota del gen HFE se aproxima al 0,5%.
La hemocromatosis secundaria se produce por trastornos de la eritropoyesis (talasemia,
anemia de células falciformes,
anemia sideroblástica ligada a X,
déficit de piruvato quinasa….) o secundaria a transfusiones.
El depósito de hierro produce un deterioro en la función de la cadena respiratoria mitocondrial,
que se manifiesta clínicamente como fallo cardíaco.
En fases iniciales,
se deposita hierro ligado a transferrina,
produciendo una caída de la señal en T2*,
con escaso efecto sobre la función cardíaca.
Cuando la capacidad de almacenaje se satura,
comienza a depositarse hierro no ligado a transferrina (forma muy tóxica),
que afecta de forma grave a la función cardíaca.
Esto explica que la alteración de la función sistólica sea un signo tardío de toxicidad por hierro y de difícil solución,
dado que el hierro cardíaco se elimina más lentamente que el hepático,
a pesar del tratamiento quelante intensivo.10
El contenido férrico del miocardio no puede estimarse en base al nivel de ferritina sérica o a los niveles hepáticos de hierro y,
solo aquellos pacientes con enfermedad avanzada,
podrán ser detectados mediante las pruebas de función cardíaca convencionales.
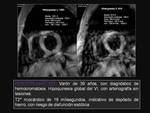
Las secuencias Eco de Gradiente T2* son una forma rápida,
no invasiva y reproducible de cuantificar la sobrecarga de hierro miocárdico.
Dicha sobrecarga es responsable de una caída de la señal que es proporcional a su concentración y valores T2*<20 ms indicarían riesgo de disfunción ventricular.
Por el contrario,
la valoración convencional con ecocardiografía,
únicamente es capaz de detectar aquellos casos con disfunción ventricular establecida. Fig. 3
La biopsia es una técnica invasiva,
difícil de utilizar como método de monitorización y que en ocasiones no detectará la severidad de la afectación,
por ser el depósito de hierro en el miocardio heterogéneo.11
Es importante realizar un diagnóstico y tratamiento precoz,
con agentes quelantes,
que disminuya el riesgo de muerte en pacientes con disfunción ventricular establecida y que revierta la disfunción diastólica en fases más precoces de la enfermedad.
Enfermedad de Anderson-Fabry
Es una enfermedad autosómica recesiva ligada al cromosoma X,
producida por la disminución de la enzima α-galactosidasa A,
que condiciona una acumulación progresiva de glucoesfingolipidos en varios órganos,
incluyendo el sistema nervioso periférico (dolor neuropático),
riñon (hipertensión, proteinuria y fracaso renal),
piel (telangiectasias y angioqueratomas),
y sistema nervioso central (ceguera y accidentes cerebrovasculares).12
La padecen tanto hombres como mujeres,
aunque en mujeres la afectación sueles ser más tardía.
En ausencia de antecedentes familiares,
sueles diagnosticarse en la edad adulta,
ya que el inicio de los síntomas puede infravalorarse en la infancia.
El depósito de esfingolípidos produce arritmias,
valvulopatías,
infiltración miocárdica con desarrollo de hipertrofia miocárdica y miocardiopatía restrictiva secundaria.
Puede cursar con isquemia miocárdica debida a disfunción endotelial de las arterias coronarias y también al incremento de la demanda de oxígeno por el miocardio hipertrófico.
Hallazgos en RM:13 Fig. 4
- Engrosamiento mural simétrico,
predominantemente izquierdo aunque también puede afectar al ventrículo derecho.
Existe una fuerte correlación entre la edad y la severidad de la HVI y que está presente en todos los pacienyes mayores de 45 años.
- 25% presentan engrosamientos ligeros de los velos aórticos y/o mitrales.
Prolapso mitral en 11%.
- Las secuencias de realce tardío ponen de manifiesto una captación mesocárdica y subepicárdica,
de localización característica en caras inferolateral de segmentos basales.14 Este hallazgo es de utilidad en el diagnóstico diferencialcon la miocardiopatía hipertrófica.
Su presencia traduce acúmulo de esfingolípidos en el miocardio y presencia de fibrosis.
TOXICIDAD
Drogas: Cocaína
La cocaína es actualmente la segunda droga de abuso en los Estados Unidos tras la marihuana.
Hasta el 40% de pacientes que acuden al departamento de urgencias tras haber consumido cocaína,
refieren dolor torácico.
El efecto de la cocaína en el sistema cardiovascular se debe fundamentalmente al efecto simpaticomimético y a las propiedades anestésicas.
La combinación del efecto β1 simpaticomimético en el miocardio y sobre los receptores α1 de los vasos epicárdicos puede alterar el balance entre la demanda de oxígeno y el aporte al miocito,
poniendo en riesgo isquémico al corazón.15 El efecto anestésico local de la cocaína es secundario a la inhibición de los canales de sodio,
bloqueando el inicio y transmisión de impulsos eléctricos en las membranas celulares.16 Tiene también un efecto intrínseco procoagulante provocando la formación de trombos y la oclusión de vasos,
que también contribuye al desarrollo de isquemia e infartos de múltiples órganos.
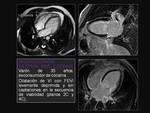
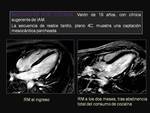
Posibles efectos cardíacos: 17,18 Fig. 5 Fig. 6 Fig. 7
- Isquemia miocárdica: independiente de la cantidad ingerida,
vía de administración o frecuencia de abuso.
- Miocarditis: relacionado con una hipersensibilidad a los adulterantes o a la propia cocaína o por efecto tóxico directo.
El patrón de realce tardío es mesocárdico y estriado,
sin relación con un territorio vascular.
También se ha descrito un cuadro similar al abalonamiento apical transitorio del VI (miocardiopatía de Takotsubo)
- Hipertrofia ventricular,
secundaria a la elevación transitoria de la presión sanguínea tras el consumo.
- Miocardiopatía dilatada: el realce tardío puede ayudar a diferenciar un origen isquémico de no isquémico.
Puede apreciarse ausencia de realce o un realce parcheado mesocárdico y longitudinal que no se corresponde con un territorio vascular.
Alcohol:
El mecanismo por el que el alcohol produce toxicidad sobre el miocardio continúa siendo una incógnita.
Las teorías iniciales se centraban en déficit nutricionales (tiamina),
exposición a otros agentes (tabaco,
cobalto,
arsénico),
y otras comorbilidades (hipertensión).
Sin embargo,
aunque estos mecanismos pueden estar implicados en determinados pacientes,
existe evidencia en la literatura que indica que el efecto sobre el miocardio es debido a toxicidad directa del etanol o sus metabolitos.
El abuso de alcohol debe mantenerse durante 5 a 10 años con un consumo de 90 gramos diarios (p.
ej: 1 litro de vino/dia) para que tenga un efecto clínico relevante en el miocardio,
por ello suele verse en personas de edad media.
El abuso de alcohol tiene múltiples efectos sobre el sistema cardiovascular y se ha asociado con arritmias,
hipertensión,
infarto y muerte súbita.
Además,
la abstinencia de alcohol se ha relacionado con miocardiopatía de Takotsubo.
Posibles hallazgos por técnicas de imagen son: dilatación de las cuatro cámaras,
disminución global de la función ventricular,
regurgitación mitral y tricúspide,
hipertensión pulmonar,
formación de trombos,
hipertrofia ventricular izquierda y disfunción diastólica,
generalmente asociada a disfunción sistólica. Fig. 8
ENDOMIOCARDICA
Fibroelastosis endocárdica
Es una enfermedad rara caracterizada por un engrosamiento difuso endomiocárdico,
progresando a fallo cardíaco congestivo y muerte,
habitualmente en los primeros 6 meses de vida.
La etiología es poco clara,
sugiriéndose un origen infeccioso viral (parotiditis,
virus coxsackie B),
un déficit primario de carnitina,
paso transplacentario de anticuerpos maternos (anti-Ro,
anti-La)19,
trastornos metabólicos o incluso una respuesta inespecífica a la disfunción miocárdica crónica.
Habitualmente es esporádica,
aunque se han descrito casos familiares (10%).20
La enfermedad puede ser primaria o secundaria a varias enfermedades congénitas,
más frecuentemente al síndrome del corazón izquierdo hipoplásico y a la estenosis o atresia aórtica.
En el 80% de los casos se presenta entre los 3 y los 6 meses de vida,
con progresión de las alteraciones a lo largo de los años en las formas de curso más crónico.
Cursa con un depósito de colágeno y elastina,
responsable del engrosamiento endocárdico difuso.
Esto se traduce en una dilatación e hipertrofia ventricular izquierda,
disminución de la complianza ventricular y fibrosis endocárdica progresiva.
La forma dilatada de la fibroelastosis miocárdica se caracteriza por un marcado aumento globular del corazón,
fundamentalmente a expensas del ventrículo izquierdo y aurícula izquierda.
El endocardio está engrosado,
con mayor afectación del tracto de salida,
pero el grosor de la pared ventricular puede estar dentro de rangos normales.
También puede encontrarse engrosado el endocardio de las cavidades derechas y en el 50% de los casos,
la válvula mitral y aortica están afectas,
condicionando regurgitación o estenosis.
No es infrecuente encontrar microtrombos adheridos al endocardio. Fig. 9 Fig. 10
La forma restrictiva de la fibroelastosis miocárdica,
menos común,
muestra un ventrículo izquierdo relativamente hipoplasico o de tamaño normal.
Sin embargo,
las aurículas y el ventrículo derecho están muy aumentados e hipertrofiados,
con poca esclerosis del endocardio.
Un evento precoz en la vida fetal puede resultar en una fibroelastosis endocárdica dilatada,
que más tardíamente se transforme en una forma restrictiva.
La fibroelastosis endocárdica secundaria asociada a malformaciones cardiacas,
se atribuye a la hipertrofia cardiaca y al disbalance entre el aporte miocárdico de oxígeno y la demanda.
El engrosamiento resultante es generalmente focal y menos severo.
La secuencia de realce tardío pone de manifiesto áreas de realce parcheado endocárdico y puede mostrar hipointensidad de señal en la secuencia de perfusión.
Fibrosis endomiocárdica y Síndrome de Löffler
Es un trastorno idiopático de las regiones tropicales y subtropicales del mundo que se caracteriza por el desarrollo de miocardiopatía restrictiva.
La forma primaria en niños da origen a la fibrosis endomiocárdica y la forma secundaria a hipereosinofilia y leucemia,
se conoce como endocarditis de Löffler o síndrome hipereosinofílico.
Es una entidad rara,
producida por un daño subendocárdico,
mediado por eosinófilos,
que cursa con necrosis,
trombosis y finalmente fibrosis de la superficie endomiocárdica de ambos ventrículos.
21
Se manifiesta como fallo cardiaco congestivo,
miocardiopatía restrictiva y fenómenos tromboembólicos.
La fibrosis endomiocárdica produce una disminución de la complianza y la afectación de la superficie endomiocárdica de forma más generalizada,
es responsable del desarrollo de una fisiología restrictiva.
Afecta predominantemente a los ápices de ambos ventrículos y puede afectar a las válvulas atrioventriculares,
inmovilizando los músculos papilares y produciendo secundariamente regurgitación tricúspide y mitral.
La analítica muestra eosinofilia periférica,
sin causa aparente.
Hallazgos en RM:22 Fig. 11
- Realce intenso de la superficie subendocárdica en secuencias de realce tardío.
- Obliteración del ápex ventricular.
- Formación de trombos,
predominantemente en los ápex ventriculares.
- Desarrollo de miocardiopatía restrictiva y posible desarrollo de incompetencia valvular,
con dilatación atrial secundaria.
El principal diagnóstico diferencial a considerar es la miocardiopatía isquémica.
El patrón de realce de distribución no vascular y la ausencia de anomalías de la contracción en las áreas de realce,
permite diferenciar estas entidades.
INFLAMATORIA
Sarcoidosis
Enfermedad granulomatosa sistémica de etiología desconocida,
aunque factores genéticos y medioambientales parecen desempeñar un papel.
Su incidencia es 5-40 casos por cada 100.000 habitantes,
con una prevalencia 10 veces mayor en Afroamericanos que en blancos.
Es más frecuente en varones que en mujeres,
con una relación 2:1 y tiene preferencia por personas de 25-35 años,
con un segundo pico de edad en mujeres de 45-65 años.
Aproximadamente un 7% de pacientes con sarcoidosis desarrolla síntomas cardíacos,
aunque los estudios de autopsia demuestran afectación en el 20-50% de los casos.23 La sarcoidosis cardíaca se manifiesta por arritmias potencialmente malignas,
disfunción ventricular izquierda y desarrollo de miocardiopatía restrictiva.
La afectación cardiaca es inusual en ausencia de otros hallazgos sistémicos y representa la causa de muerte más frecuente en Estados Unidos,
siendo la afectación pulmonar la causa más frecuente en Europa y Japón.
Hallazgos en RM:23 Fig. 12
- En fase aguda,
el miocardio está engrosado y muestra focos parcheados e hiperintensos en mesocardio y/o subepicardio,
en las secuencias potenciadas en T2 y STIR,
que pueden ser transmurales.
En fase crónica,
los granulomas condicionan un adelgazamiento mural izquierdo,
secundario a la cicatrización.
- Alteración del patrón de llenado ventricular izquierdo,
en relación con una fisiología restrictiva secundaria
- Las alteraciones de la contractilidad segmentaria son frecuentes.
- Realce parcheado y nodular,
en las secuencias de realce tardío,
en las zonas de formación de granulomas y cicatrices,
teniendo predilección por unas localizaciones específicas como son el segmento basal del septo interventricular y la pared lateral del ventrículo izquierdo24.
También puede realzar el miocardio del ventrículo derecho y el tracto de salida del mismo.
La RM permite confirmar la sospecha clínica de sarcoidosis de cara a iniciar tratamiento esteroideo o con otros inmunosupresores y ayuda a guiar la biopsia endomiocárdica a aquellas zonas con una mayor rentabilidad diagnóstica.25
ENDOCRINA
Miocardiopatía diabética
La diabetes,
en especial la tipo 2,
es capaz de producir daño miocárdico por un mecanismo mixto asociado al daño microvascular,
a las alteraciones del sistema renina-angiotesina,
trastornos del metabolismo miocárdico y del transporte del calcio,
aumento del stress oxidativo y disregulación de la apoptosis.
En pacientes diabéticos el riesgo cardiovascular de sufrir un infarto agudo de miocardio e insuficiencia cardíaca secundaria a un evento isquémico coronario,
es significativamente mayor que en pacientes no diabeticos.26
Sus primeras manifestaciones clínicas se deben a la insuficiencia cardíaca,
que morfológica y funcionalmente se manifiestan como hipertrofia,
dilatación,
caída de la fracción de eyección y disminución de la complianza.
Estructuralmente se identifica fibrosis e infiltración grasa.
En la práctica clínica el uso de la ecocardiografía como prueba de cribado y la microalbuminuria son los mejores indicadores del riesgo de un paciente de sufrir una miocardiopatía diabética.27
En resonancia magnética puede identificarse un aumento de la masa ventricular izquierda y áreas de fibrosis en las secuencias de realce tardío,
sin un patrón o localización específica.
Más recientemente se ha descrito el uso de la espectroscopia por resonancia magnética para la identificación de triglicéridos,
y la espectroscopia del fósforo para la estimación de la relación fosfocreatina/ATP,
todavía en un plano experimental.28
NEUROMUSCULAR/NEUROLÓGICA
Muchas de las enfermedades neuromusculares pueden afectar al corazón,
en ocasiones con gran relevancia clínica.
Las distrofias musculares (distrofinopatías,
distrofia muscular de cinturas,
distrofia de Emery-Dreifuss o distrofia miotónica de Steinert),
las miopatías congénitas,
las miopatías inflamatorias y las enfermedades metabólicas (glucogenosis,
parálisis periódicas o enfermedades mitocondriales) pueden producir miocardiopatía dilatada o hipertrófica,
así como trastornos del ritmo y de la conducción.
También algunas enfermedades heredodegenerativas (ataxia de Friedreich y enfermedad de Kugelberg-Welander) y las neuropatías periféricas adquiridas (síndrome de Guillain-Barré) o hereditarias (enfermedad de Refsum y de CharcotMarie-Tooth) pueden tener repercusión cardiológica.
Dado que el manejo de estos pacientes y el curso de la enfermedad están muy influenciados por el grado de afectación cardíaca,
tan pronto como se diagnostican estas enfermedades,
debe iniciarse el estudio cardiológico de cara a instaurar la terapia adecuada.
Para un correcto diagnóstico es fundamental un alto grado de sospecha clínica del cardiólogo y la realización,
de un estudio sistemático del músculo esquelético y nervio periférico que incluya enzimas musculares,
estudio neurofisiológico y biopsia muscular.
En algunos casos serán necesarias técnicas más sofisticadas de análisis bioquímico y genético para completar el estudio.
La realización de biopsia endomiocárdica para analizar el músculo cardíaco no suele ser necesaria.
Enfermedad de Duchenne
Es la forma más grave de las distrofinopatias.
La muerte sobreviene antes de los 20 años de edad por insuficiencia respiratoria o cardíaca.
Se hereda de forma autosómica recesiva ligada al cromosoma X,
aunque existe un alto porcentaje de mutaciones de novo.
El corazón se ve afectado frecuente y precozmente.
Se producen alteraciones electrocardiográficas del ritmo y de la conducción.
Pueden detectarse los hallazgos típicos de una miocardiopatía dilatada como dilatación ventricular derecha e izquierda,
disminución de la fracción de eyección y alteraciones segmentarias de la contracción.29
Ataxia de Friedreich
Enfermedad hereditaria autosómica recesiva,
de inicio en la primera o segunda décadas de la vida,
que cursa con ataxia cerebelosa,
ataxia sensorial y piramidalismo,
asociándose además leve neuropatía periférica,
pie cavo,
retinopatía,
sordera y cardiopatía.
Mediante electrocardiograma y ecocardiograma se detectan alteraciones cardiológicas hasta en el 95-100% de los enfermos con un patrón de miocardiopatía dilatada o hipertrófica.30
Miopatia miofibrilar
Aunque no se considera una distrofia muscular de cinturas,
comparte múltiples características fenotípicas con esta entidad.
Es una enfermedad de debut en el adulto,
que puede aparecer desde la primera década de la vida hasta los 60/70 años,
con debilidad lentamente progresiva que afecta a los músculos proximales y distales.
Los rasgos característicos de las miopatías miofibrilares en la biopsia muscular son fibras musculares vacuoladas e inclusiones de múltiples proteínas como la desmina,
αB-cristalina (αBC),
distrofina y material amiloide. De hecho,
previamente se conocía a esta entidad como miopatía por depósito de desmina,
por ser la primera proteína encontrada y por ser la más dominante.
La enfermedad cardiaca puede presentarse como miocardiopatía restrictiva o hipertrófica,
arritmias y bloqueos de la conducción,
y está presente en aproximadamente el 50% de casos.31 Fig. 13
AUTOINMUNE
Enfermedades del colágeno
En la artritis reumatoide puede producirse lesión miocárdica entre el 3 y 30% de los pacientes 32
Los hallazgos de anatomía patológica incluyen alteraciones focales inespecíficas,
miocarditis necrotizante difusa y miocarditis granulomatosa.33
El hallazgo ecocardiográfico asociado a miocardiopatía,
se reduce a la existencia de hipertrofia ventricular,
con prevalencias reportadas entre el 11 y el 36%.34 La afectación miocárdica por artritis reumatoide,
podría tener un origen mixto,
condicionado por la propia enfermedad,
así como por la amiloidosis secundaria y el tratamiento esteroideo.35
En pacientes con artritis reumatoide y ecografía normal,
la resonancia magnética permitió identificar áreas de edema en secuencias T2,
realce precoz en afectación aguda y realce tardío en fases crónicas,
sin un patrón característico.
En una serie de 18 pacientes el 39% presentaban signos de afectación miocárdica,
con una muy buena correlación con los criterios clínicos y paraclínicos de actividad de la enfermedad.36,37
En el lupus eritematoso sistémico el 40-70% de los pacientes presentan lesiones en las necropsias,
siendo sintomáticos sólo el 5-10% 38
Los hallazgos son los propios de la miocarditis,
con aumento de la señal en secuencias T2/STIR y realce tardío meso y subepicárdico,
siendo este último más frecuente en los procesos agudos.39 El tratamiento con esteroides reduce la prevalencia de afectación inflamatoria miocárdica secundaria a esta entidad40
El diagnóstico de miocarditis,
si bien no parece condicionar complicaciones que pongan en riesgo la vida de los pacientes,
implica mayor gravedad y peor pronóstico de la enfermedad.41 Estos hallazgos parecen justificar la intensificación del tratamiento inmunosupresor.42
Otras alteraciones descritas son engrosamiento valvular con insuficiencia,
y más raramente endocarditis verrugosa.
El pericardio se encuentra afectado entre el 11 y el 54% de los pacientes.43
En el caso de la esclerodermia su prevalencia es difícil de definir,
porque existen formas leves de la enfermedad que no se diagnostican.
Es una enfermedad que afecta al tejido conectivo y visceral con proliferación fibrosa y que cuando afecta al corazón lo hace a nivel pericardico,
miocárdico y del sistema de conducción,
respetando válvulas y endocardio.
En una serie de 24 pacientes se reportaron hallazgos de afectación miocárdica en el 66%.44 Se han descrito en la esclerodermia,
patrones de realce tardío con una localización y disposición más característica,
lineal y mesocárdica,
que afectan preferentemente a las bases y segmentos medios ventriculares.44
QUIMIOTERAPIA
Secundario a la infusión de agentes quimioterápicos,
se describen alteraciones agudas (arritmias,
hipotensión,
edema,
derrame pericárdico) y crónicas,
que incluyen las producidas por toxicidad directa y por mecanismos indirectos (inflamación/fibrosis,
isquemia).
Las antraciclinas son uno de los agentes quimioterápicos mejor estudiados,
conocidos por su capacidad de producir lesión miocárdica,
mediante la generación de radicales libres,
siendo ésta proporcional a la dosis acumulada (en especial con dosis superiores a los 500mg/m2).
El tratamiento con doxorubicina puede inducir un aumento de la masa del ventrículo izquierdo y de los volúmenes telediastólicos,
que preceden a la reducción de la fracción de eyección.45 Hemos encontrado escasa información publicada sobre los hallazgos por resonancia magnética,
si bien,
un reporte describió,
el realce mesocárdico lineal en un paciente con el diagnóstico confirmado,
que aunque inespecífico,
permite diferenciarlo de otros patrones más característicos.46
Otros quimioterápicos producen también disfunción ventricular entre los cuales se describen los agentes alquilantes como el cisplatino (cuando se usa con radioterapia o tras el empleo de una antraciclina) y la ciclofosfamida (que a altas dosis y de forma esporádica puede producir miocarditis hemorrágica).47
RADIACIÓN
La lesión miocárdica por radioterapia,
incide de forma más importante en pacientes con enfermedad coronaria pre-existente.
Guarda relación con la dosis,
el tiempo transcurrido desde el tratamiento y el uso previo de antraciclinas.
Suele acompañarse de alteraciones pericárdicas en forma de derrame/pericarditis constrictiva,
de disminución de la fracción de eyección y de lesión valvular.
En lo que se refiere al miocardio,
se describen dos patrones de lesiones: El subendocárdico,
indiferenciable del isquémico,
debido a la lesión endotelial que produce la radioterapia y el patrón de afectación parcheada con una disposición mesocárdica y subepicárdica,
explicado por una anormal producción de colágeno y/o por la cicatrización de lesiones tipo miocarditis.
En una serie de pacientes tratados con radioterapia para enfermedad de Hodgkin,
evaluados mediante cardioresonancia magnética,
reportaron un 26% de lesiones miocárdicas,
de los cuales un 22,6% mostraron un patrón isquémico de realce tardío.48