De entre las alteraciones benignas que pueden presentarse en el urotelio constan las afectaciones inflamatorias y/o infecciosas agudas,
crónicas,
granulomatosas y xantogranulomatosas en forma de pielonefritis,
pieloureteritis,
ureteritis,
cistitis (incluyendo la cistitis glandular) y uretritis,
todo ello en diferentes contextos clínicos.
La patología maligna incluye el carcinoma de células transicionales (fenotipo plasmocitoide,
células en anillo de sello,
linfoepitelioma,
diferenciación escamosa o glandular),
el carcinoma escamoso,
el carcinoma glandular o adenocarcinoma,
tumores neuroendocrinos (carcinoma de célula pequeña) y lesiones metastásicas.
Hemos revisado nuestra casuística seleccionando aquellos pacientes con patología urotelial que disponían de imagen morfológica y correlación anatomopatológica. Las alteraciones evaluadas pueden ser benignas,
incluyendo lesiones inflamatorias.
|
UN PASEO POR LA NORMALIDAD
|
Repaso Histológico
El epitelio de transición o urotelio es un epitelio estratificado especializado y distensible compuesto por varias capas celulares (3 a 8) entre las que destacan las células más superficiales o células de cubierta,
con una función protectora y de mantenimiento de la integridad del urotelio. Una importante propiedad del urotelio es la distensibilidad,
variando su grosor dependiendo del estado de repleción.
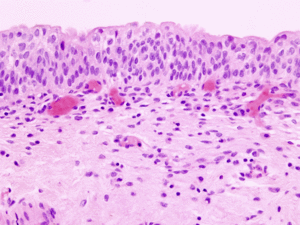
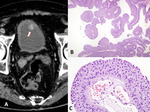
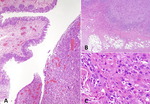
Fig. 1: Urotelio normal. Epitelio transicional, estratificado, constituido por cuatro a seis capas de células columnares superpuestas, con núcleos ovalados orientados perpendicularmente al eje mayor del tejido, algunos de ellos con hendiduras. Las células de la capa más superficial son las denominadas células en paraguas, perpendiculares al urotelio subyacente, sobre el cual ejercen una función protectora.
Dicho epitelio tapiza la vía urinaria desde el sistema pielocalicial hasta la uretra,
siendo encontrado en el revestimiento del sistema colector renal (cálices,
infundíbulo,
pelvis),
uréter,
vejiga urinaria,
además de algunos segmentos uretrales.
Con respecto a la uretra,
los segmentos iniciales son de uroepitelio y los segmentos distales son de epitelio escamoso estratificado.
El urotelio de la vejiga normal puede mostrar múltiples invaginaciones epiteliales llamadas nidos de von Brunn.
Estos pueden estar recubiertos de células columnares secretoras de moco en vez de urotelio.
Estudios más recientes apuntan que las células epiteliales,
más que simples barreras físicas,
estarían involucradas en una serie de mecanismos sensoriales,
respondiendo a estímulos químicos,
mecánicos y térmicos,
con consecuente liberación de mediadores químicos.
Repaso anatómico
Se puede considerar que las vías urinarias se inician en la papila renal.
La orina sale a través de los cálices renales hacia la pelvis renal,
situada sobre el seno renal,
que por su vez se continua con el uréter.
Los uréteres son estructuras retroperitoneales que miden alrededor de unos 25 - 30 cm de largo y 2 cm de diámetro,
descendiendo en un trayecto paralelo a los cuerpos vertebrales de L3,
L4 y L5 hasta desembocar en el interior de la vejiga.
El uréter atraviesa la pared posterior de la vejiga de forma oblicua durante algunos centímetros,
formando en el interior vesical lo que se conoce como trígono vesical ,
en la base de la vejiga,
que es una zona más lisa con forma triangular,
delimitada por los dos meatos ureterales y el orificio para la uretra.
TÉCNICAS DE IMAGEN
La urografía intravenosa (UIV) fue durante muchos años la principal técnica utilizada en la valoración de la enfermedad del tracto urinario superior.
Sin embargo,
otras modalidades como la ecografía,
la TCMD y la RM han asumido una buena parte de estas indicaciones a lo largo de los años.
A pesar de ello,
en la actualidad todavía es frecuentemente solicitada en la valoración de hematuria y para complementar la exploración de pacientes con enfermedad litiásica pre o post-tratamiento.
La secuencia de imagen en urografía está diseñada para optimizar el estudio de zonas específicas del tracto urinario durante la máxima opacificación de este.
Hay que considerar que la técnica es operador dependiente,
exigiendo buena experiencia para la obtención de las imágenesy para una interpretación más precisa de estas.
La ecografía constituye la técnica de imagen inicial en la valoración de sospecha de patología de la vía urinaria.
La TCMD con estudios multifase permite evaluar la totalidad de los riñones y la vía urinaria en diferentes fases de captación del contraste.
Las tres fases de perfusión renal definidas en el diagnóstico por TC son la fase cortico-medular (FCM),
la fase nefrográfica (FN) y la fase de eliminación renal o fase excretora (FE).
El estudio basal sin contraste (EB) será útil para determinar el grado de captación de las lesiones así como para detectar lesiones hiperdensas,
densidad grasa y calcificaciones.
En la FCM se contrasta el sistema vascular y el espacio intersticial extracelular,
teniendo una duración aproximada de 40 segundos.
La FN se inicia alrededor de 70 segundos después de la administración del contraste que se filtra a través de las asas de Henle y túbulos colectores,
obteniendo una captación homogénea del parénquima renal.
La opacificación del sistema colector se inicia a los 180 segundos y constituye la FE.
Con relación a otras técnicas diagnósticas,
el estudio helicoidal de la vía urinaria aporta una información morfológica muy precisa:
- Determinando a menudo el nivel lesional y la extensión de la lesión.
- Demostrando el tipo de relación de la vía urinaria con las estructuras adyacentes (compresión benigna,
compromiso/ infiltración)
- Objetivando disrupción de la vía excretora al detectar fuga de contraste en fase de eliminación renal.
- Los tumores de urotelio son hipercaptantes en fase vascular (FCM y FN).
La administración de contraste e.v.
(condicionada por los valores de creatinina y disposición de unidad de hemodiálisis),
aporta valiosa información sobre la situación funcional renal mostrando un retraso o ausencia de eliminación del contraste en caso de afectación de la misma.
La TCMD multifase es una técnica de gran precisión morfológica en la evaluación de la patología de la vía urinaria y su repercusión en las estructuras adyacentes,
aportando además información relevante sobre el funcionalismo renal.
La RM es la técnica más reciente y es útil en la evaluación de distintas alteraciones del tracto urinario,
tales como el diagnóstico y estadiaje del cáncer renal,
vesical y prostático.
Al no exponer a radiaciones ionizantes es la técnica complementaria indicada en la valoración de niños o embarazadas.
Como desventajas,
cabe destacar que esta técnica tiene una baja sensibilidad en la detección de litiasis pequeñas de las vías urinarias o pequeños carcinomas uroteliales,
además de su mayor coste y su menor disponibilidad.
|
UN PASEO POR LA INFLAMACIÓN/INFECCIÓN
|
La Infección del tracto urinario es la patología urológica más frecuente.
La estructura anatómica del epitelio urotelial que se abre al exterior,
favorece el desarrollo de infecciones,
más frecuentemente por Escherichia coli.
La mayoría de las infecciones se quedan aisladas en las vías urinarias bajas,
pero parte de ellas asciende de manera directa o por diseminación hematógena.
El papel de las pruebas de imagen en el diagnóstico inicial es controvertido,
no estando por lo general indicados en los casos no complicados.
PIELONEFRITIS BACTERIANA AGUDA
En los adultos,
las infecciones del tracto urinario se presentan habitualmente con un cuadro clínico de fiebre,
temblor y dolor lumbar uni o bilateral (puño percusión positiva).
Pueden presentar además síntomas gastrointestinales como dolor abdominal,
vómitos y/o diarrea).
La mayoría de los pacientes responden bien al tratamiento antibiótico y no requieren otras exploraciones.
En el diagnóstico por imagen,
la radiografía convencional se utiliza actualmente para identificar presencia de litiasis o de aire en el tracto urinario.
La ecografía suele ser la técnica de imagen inicial en la valoración de este grupo de pacientes,
pudiendo detectar desde áreas de nefritis focal a cambios inflamatorios parenquimatosos más difusos.
Los principales hallazgos ecográficos:
- Riñón aumentado de tamaño ,
voluminoso
- Hidronefrosis
- Pérdida de la diferenciación córtico-subcortical
- Abscesos focales
- Zonas de hipoperfusión valorables por doppler.
La urografía Intravenosa (UIV) mostrará un aumento del tamaño renal y un posible retraso en la eliminación del contraste,
en caso de componente obstructivo,
mostrando una dilatación asociada del sistema pielocalicial en grado variable.
En cuadro de pielonefritis aguda complicada,
la tomografía computarizada es la modalidad de elección ya que permite una adecuada visualización de la perfusión del parénquima renal y del posible componente obstructivo asociado de la vía urinaria.
El estudio basal detectará la presencia de gas,
litiasis y/o hemorragia.
La fase nefrográfica podrá identificar zonas bien delimitadas de menor coeficiente de atenuación el parénquima renal,
además de engrosamiento mural difuso de la pelvis renal y de la pared ureteral.
La hidronefrosis puede estar presente o no.
Se suele asociar un engrosamiento de la fascia de gerota,
trabeculación de la grasa perirrenal y en casos evolucionados pueden aparecer abscesos.
PIELONEFRITIS CRÓNICA
El concepto de pielonefritis crónica puede corresponder a una infección crónica activa o traducir los cambios producidos por los diferentes episodios infecciosos agudos previos.
En la TCMD podemos identificar cicatrices corticales,
atrofia o adelgazamiento cortical,
hipertrofia del tejido normal residual,
asimetría renal.
La hipertensión es una secuela descrita con relativa frecuencia. Fig. 3
PIELONEFRITIS XANTOGRANULOMATOSA (PNFX)
La pielonefritis xantugranulomatosa es un proceso granulomatoso crónico del parénquima renal que se asocia a historia de obstrucción e infección prolongadas del tracto urinario.
Se caracteriza por la destrucción y sustitución del tejido renal por un infiltrado celular de macrófagos mononucleares cargados de lípidos (histiocitos espumosos) que aumenta el tamaño renal manteniendo su morfología reniforme y con mínimo o ausente funcionalismo renal.
La presencia de un cálculo obstructivo coraliforme completo o incompleto está presente en aproximadamente un 70% de los casos.
Es un proceso típicamente unilateral y puede ser focal o difuso.
Existe una fuerte asociación con nefrolitiasis y patógenos infecciosos (E.
coli y Proteus mirabilis).
El perfil del paciente con PNFX son mujeres de mediana edad que presentan fiebre recurrente y dolor en flanco.
Los síntomas más comunes son dolor abdominal,
disuria,
fiebre y en ocasiones masa palpable,
hematuria y pérdida de peso.
Las pruebas de imagen indican una afectación difusa en la mayoría de los casos (84,6%). De forma menos frecuente la PNFX puede afectar solo una porción del riñón.
Se asocia una afectación en grado variable del espacio perirrenal.
Por ecografía los cambios inflamatorios se visualizan en forma de masas hipoecogénicas con focos centrales más ecogénicos,
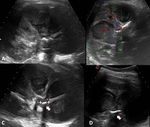
pudiendo identificar cálculos de disposición central. Fig. 4
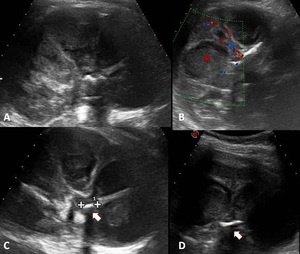
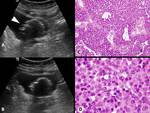
Fig. 4: PIELONEFRITIS XANTOGRANULOMATOSA. Mujer de mediana edad con clínica de fiebre y dolor lumbar derecho. La ecografía muestra un riñón derecho aumentado de tamaño con dilatación calicilial y contenido heterogéneo/ecogénico, objetivando foco hiperecogénico central con sombra acústica posterior (flechas) correspondiente a un cálculo alojado en la pelvis renal.
Los hallazgos por TC son patognomónicos en la mayoría de casos e incluyen nefromegalia difusa de morfología reniforme con baja atenuación central mal definida,
adelgazamiento cortical aparente y la presencia de cálculo central.
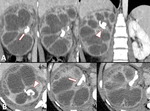
Fig. 5 y Fig. 6
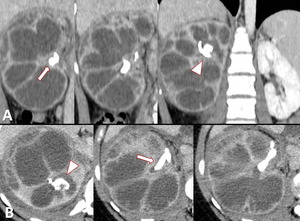
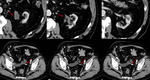
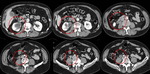
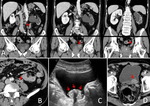
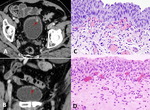
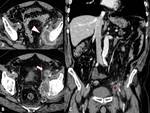
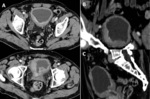
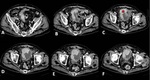
Fig. 5: Pielonefritis xantogranulomatosa. Se practicó estudio con TCMD visualizando MPR coronal (A) e imágenes axiales (B) que muestran nefromegalia derecha (14 cm de longitud) con adelgazamiento cortical aparente y extensas áreas centrales de baja atenuación identificando litiasis alojada en la pelvis renal (flecha). Se identifica además otra litiasis ubicada en grupo calicial superior (punta de flecha).
Las áreas centrales de baja atenuación representan material xantomatoso no captante que puede mostrar valores de atenuación menores a los de densidad agua.
La nefrectomia suele ser curativa.
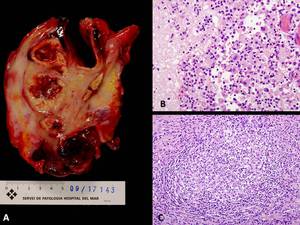
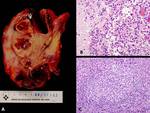
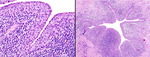
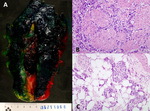
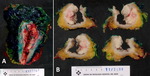
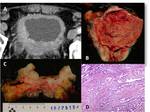
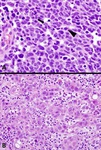
Fig. 6: PIELONEFRITIS aguda y crónica XANTOGRANULOMATOSA. A) Imagen macrocópica que corresponde a pieza de nefrectomía derecha seccionada coronalmente. La arquitectura normal del riñón se encuentra borrada por múltiples lesiones nodulares amarillentas correspondientes a abscesos, algunas de ellas con quistificación y hemorragia central. El parénquima renal es marcadamente atrófico y se aprecian extensas áreas de fibrosis tanto en el hilio renal como en la grasa perirrenal. Nótese la presencia de un cálculo coraliforme alojado en la pelvis. B) Imagen microscópica de un granuloma con histiocitos epitelioides en el centro y una corona linfocitaria en la periferia. C) Componente inflamatorio agudo constituido por leucocitos polimorfonucleares neutrófilos y componente inflamatorio crónico xantomatoso integrado por histiocitos con citoplasma finamente vacuolado o espumoso.
PIELOURETERITIS
Podemos encontrar cambios inflamatorios por pieloureteritis en pacientes con uropatía obstructiva por cálculos o que presenten estasis urinario relacionado con estenosis ya sea de anastomosis uretero-vesicales (reimplantación ureteral) o anastomosis uretero-ileales (cirugía urológica tipo Bricker). Fig. 7
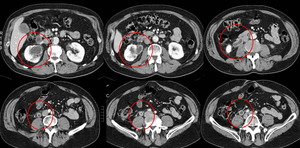
Fig. 7: PIELOURETERITIS derecha post cistectomia radical con anastomosis ureteroileal tipo Bricker. Estudi axial con TCMD que muestra engrosamiento mural hipercaptante de todo el sistema pieloureteral derecho.
Los cambios morfológicos por TCMD mostrarán un engrosamiento mural hipercaptante piélico y ureteral,
con trabeculación y edema de la grasa peripiélica y periureteral.
Usualmente tiene una extensión menor que la esperada para un CCR.
Infección secundaria puede inducir mayor extensión de la afectación
Cuando la litiasis es eliminada o cambia de posición,
los cambios inflamatorios pueden persistir, simulando el aspecto de un CCT infiltrativo,
siendo en algunos casos recomendable realizar seguimiento. Fig. 8
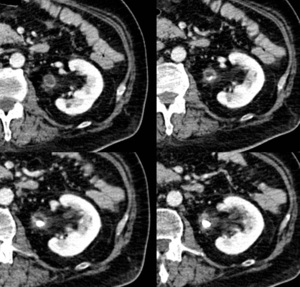
Fig. 8: Pieloureteritis izquierda litiásica. Imágenes axiales con TCMD en fase nefrográfica que muestran un engrosamiento mural en unión pieloureteral inflamatorio causado por cálculo impactado en esta localización.
Fig.9
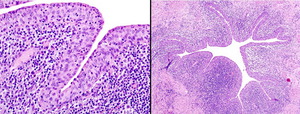
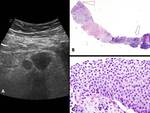
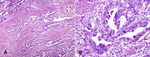
Fig. 9: A) Ureteritis aguda y crónica. Imagen microscópica panorámica de una sección de pared ureteral en la que destaca un prominente infiltrado inflamatorio en lámina propia y submucosa. B) Detalle de la imagen anterior en el que se aprecia marcado componente inflamatorio de tipo crónico en la lámina propia ureteral, así como inflamación aguda en forma de exocitosis de leucocitos polimorfonucleares neutrófilos a través del urotelio.
La radioterapia provoca cambios inflamatorios y fibrosis que pueden afectar la vía urinaria fundamentalmente a nivel vesical y ureteral pudiendo condicionar estenosis ureteral y retracción vesical.
Los procesos inflamatorios infecciosos o no infecciosos (colitis granulomatosa,
pancreatitis...) también pueden comprometer la vía urinaria.
La fibrosis retroperitoneal puede comprometer la vía urinaria al retraer y comprimir los uréteres junto con los grandes vasos retroperitoneales presentando un aspecto morfológico indistinguible de la afectación metastásica,
fibrosis por radioterapia y amiloidosis.
ADENOMA NEFROGÉNICO
La metaplasia nefrogénica o adenoma nefrogénico es una proliferación benigna de estructuras de tipo glandular que afectan la vejiga urinaria con mayor frecuencia. Se considera que esta lesión se origina por metaplasia del urotelio subyacente.
La lesión se ha asociado a tratamiento radioterápico,
cirugía,
cálculos,
instrumentación e instilaciones intravesicales de BCG.
|
UN PASEO POR LA MALIGNIDAD
|
La patología maligna incluye el carcinoma de células transicionales (fenotipo plamocitoide,
células en anillo de sello,
linfoepitelioma,
diferenciación escamosa o glandular),
el carcinoma escamoso,
el carcinoma glandular o adenocarcinoma,
tumores neuroendocrinos (carcinoma de célula pequeña) y lesiones metastásicas.

Fig. 2
References: WHO
Carcinoma de células transicionales
El carcinoma de células transicionales (CCT) constituye el 90% de todos los cánceres de la pelvis renal y uréter.
Otros procesos malignos que afectan al urotelio incluyen el carcinoma escamoso (10%) y adenocarcinomas (menos del 1%).
La incidencia y la mortalidad aumentan con la edad,
situándose el pico de mayor incidencia en la 6ª-7ª décadas de la vida,
siendo más frecuentes en varones.
El síntoma más común es la hematuria indolora,
que se produce en el 75 a 90 % de los pacientes.
El dolor en flanco aparece en el 20-25 % de los pacientes,
pudiendo desencadenarse por obstrucción causada por un tumor o por coágulo.
La disuria y el dolor son más frecuentes en los tumores ureterales.
De acuerdo con sus características patológicas,
pueden clasificarse en carcinoma papilar,
papilar infiltrante y difusamente infiltrante,
correspondiendo la mayoría (alrededor de 95%) a carcinoma papilar infiltrante.
Los carcinomas papilares tienen morfología papilar y presentan una base ancha y un aspecto verrucoso.
El factor de riesgo más importante para desarrollar CCT es el tabaco,
aumentando el riesgo en hasta 4 veces.
1/3 de los casos de cáncer vesical se diagnostican en pacientes fumadores.
La patogenia tiene una relación directa con el tiempo de exposición a carcinógenos excretados,
por lo cual la aparición de procesos neoformativos en la vejiga urinaria es hasta 30 a 50 veces más frecuente que en resto de la vía urinaria.
La estasis urinaria favorece la carcinogénesis,
identificándose un riesgo aumentado en los pacientes que presentan anomalías en la estructura renal (riñón en herradura),
divertículos vesicales y obstrucción crónica de la unión pieloureteral (UPU).
Tumores de la vía urinaria superior
El aumento detectado en la incidencia se relaciona con la mejora de las técnicas diagnósticas y con el aumento de la supervivencia en los pacientes con cáncer vesical que presentan un alto riesgo de desarrollar neoplasia urotelial en vía urinaria superior.
El carcinoma de células transicionales (CCT) afecta mayoritariamente el urotelio vesical,
localizándose en el urotelio de la pelvis renal y el uréter en un 5% de casos.
Aproximadamente el 40% de pacientes con carcinoma de células transicionales del tracto superior desarrollaran carcinomas del tracto urinario inferior y esto explica la importancia del seguimiento sistemático de este grupo de pacientes.
La histología y citología de los tumores uroteliales superiores es similar a la del CCT vesical: 85% de los CCT de vía urinaria superior presentan un estadio bajo y son superficiales y aproximadamente un 15% son infiltrantes.
Sin embargo,
estos tumores son más agresivos que los tumores infiltrantes de vejiga urinaria.
La detección de los tumores de la vía urinaria superior se realiza utilizando técnicas radiológicas.
La urografía intravenosa se ha utilizado tradicionalmente, pero en la actualidad se ha implementado la TCMD multifásica de vía urinaria como una técnica fundamental que permite diagnosticar y estadificar este tipos de tumores.
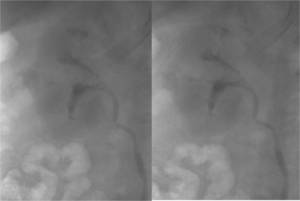
Fig. 11: NEOPLASIA UROTELIAL PIELOCALICIAL DERECHA. La UIV muestra defecto de repleción pièlico irregular que se extiende a grupo caliacial superior.
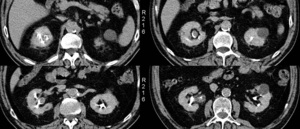
Fig. 12: NEOPLASIA UROTELIAL PIELOCALICIAL DERECHA. El estudio axial por TC demuestra el defecto de repleción piélico irregular que se extiende a grupo calicial superior correspondiente a la neoproliferación.
El tumor de pelvis renal por ecografía se muestra como una masa central de ecogenicidad intermedia en el seno de la hiperecogenicidad sinusal habitual,
acompañada o no de hidronefrosis.
Por TCMD el 85% de los casos identificados son del tipo papilar infiltrativo,
presentando una base de sustentación amplia y un aspecto irregular.
En la fase nefrográfica se observa lesión con densidad de partes blandas,
moderadamente captante.
En la fase excretora se identifican defectos de repleción aislados o múltiples y/o amputación o distensión calicial.
Cabe destacar que este tipo de tumores no suelen distorsionar el contorno renal (a diferencia del carcinoma de células renales).
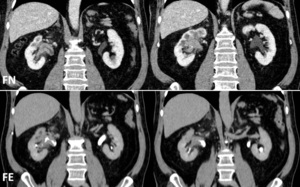
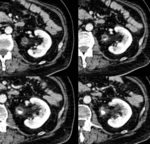
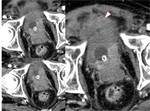
Fig. 13: TUMOR UROTELIAL PIELOCALICIAL. Reconstrucciones coronales de TCMD en fase nefrográfica y en fase excretora que demuestran la existencia de una lesión neoproliferativa piélica derecha. La lesión presenta densidad de partes blandas y realza con contraste en FN, mostrándose como un defecto y distorsión de la repleción en FE.
La urografía por resonancia magnética (RM) está indicada en los pacientes que no pueden someterse a una TCMD.
La tasa de detección de la RM es del 75 % tras la inyección de contraste en el caso de los tumores menores de 2 cm.
La urografía por RM es más rentable con inyección de contraste,
sin embargo,
en los pacientes con insuficiencia renal grave (aclaramiento de creatinina < 30 ml/min) sigue estando contraindicada la administración de gadolinio por el riesgo de fibrosis sistémica nefrogénica.
La RM sin contraste resulta menos útil que la urografía por TCMD para diagnosticar patologías malignas uroteliales.
Los CCTs de pelvis renal se localizan más frecuentemente en la porción extrarenal seguida de la región infundíbulo-calicial y los de uréter asientan normalmente en el tercio ureteral distal.
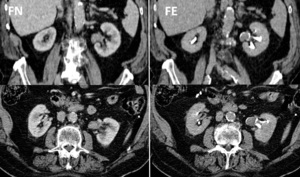
Fig. 14: CARCINOMA DE CÉLULAS TRANSICIONALES PIÉLICO. Imágenes axial y coronal en FN que muestran formación sólida hipercaptante ocupando pelvis renal izquierda. En las imágenes axial y coronal en FE la lesión se identifica como un defecto de repleción.
Los tumores localizados en la pelvis renal,
si bien suelen estar confinados en la luz del sistema colector pueden extenderse hacia el parénquima renal con un patrón típicamente infiltrativo.
Cuando la localización es ureteral el uréter distal es la ubicación más frecuente (73%).
Un 24 % se ocalizan en uréter medio y solo un 3% en el uréter proximal.
La afectación del tracto urinario superior de forma bilateral se produce en un 2-5%.
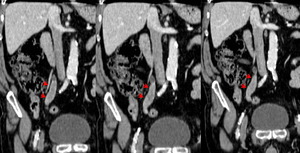
Fig. 15: CARCINOMA URETERAL DISTAL DERECHO. Imágenes coronales de TCMD que muestran tumoración sólida endoluminal ocupando uréter distal derecho (flechas).
Los tumores ureterales representan un 2.5-5% de todos los tumores uroepiteliales.
En la fase vascular (FCM I FN) el tumor ureteral se muestra como un engrosamiento circunferencial de la pared presentando realce anormal y presencia de lesiones endoluminales que en fase excretora se identifican como defectos de repleción.
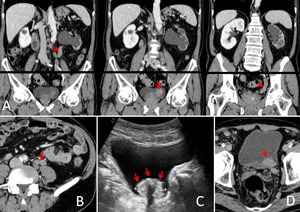
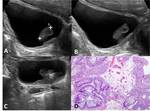
Fig. 16: CARCINOMA UROTELIAL MULTIFOCAL, ureteral izquierdo y vesical. A) Las RMP de TC muestran focos de engrosamiento tumoral afectando el uréter izquierdo proximal y distal además de proliferación sólida endovesical (flechas). B) Imagen axial que muestra tumoración endoureteral izquierda (flecha). C) Imagen ecográfica que nuestra la lesión sólida perimeatal izquierda (flechas). D) Imagen axial de TC que demuestra afectación vesical y ureteral inferior (flecha).
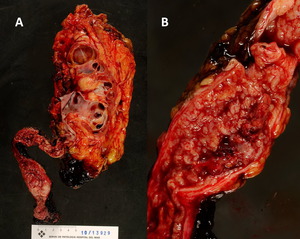
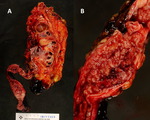
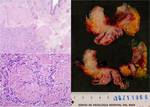
Fig. 17: A) Carcinoma urotelial papilar, grado 2, pTa. Pieza de nefroureterectomía izquierda con marcada atrofia parenquimatosa renal e hidronefrosis. En el uréter se identifica una lesión exofítica, carnosa, friable y con áreas hemorrágicas, que se extiende a lo largo de prácticamente todo el trayecto ureteral y que ocupa el 100% de su perímetro. B) Detalle de la imagen anterior.
Debemos recordar que un 20% de los tumores ureterales son benignos destacando por su frecuencia el papiloma benigno y el pólipo fibroepitelial que presentan una morfología cilíndrica y pueden tener un tallo que los haga móviles.
Su localización más frecuente es el tercio ureteral proximal.
Morfológicamente pueden ser muy difíciles de diferenciar del CCT siendo necesario realizar un diagnóstico histológico.
Los tumores de vía urinaria superior diseminan más frecuentemente por invasión directa y por vía linfática,
que por vía hematógena a causa de la fina pared del uréter y su rico drenaje linfático.
Los ganglios linfáticos retroperitoneales se afectan con frecuencia.
Es rara la invasión de las venas renales y de la vena cava inferior.
Tumor vesical
El cáncer de vejiga es el tumor más frecuente del sistema urinario caracterizándose por su alta recurrencia y por su multiplicidad.
Presenta un pico de incidencia que se sitúa entre la 6ª y 7ª décadas de la vida.
El CCT constituye aproximadamente un 90% de los tumores de vejiga urinaria.
El segundo tipo celular más frecuente es el carcinoma de células escamosas (8%),
seguido del adenocarcinoma.
Otros subtipos más raros como el carcinoma de células pequeñas constituyen menos del 1% de los casos.
Estos tumores tienden a ser multicéntricos,
identificando afectación sincrónica y metacrónica en un 30-40% de los casos.
La cistoscopia con biopsia es el método de elección para diagnóstico y estadiaje.
Ejemplos de DISPLASIA Fig. 19 y Fig. 18
Ecográficamente los detectaremos como engrosamientos murales focales más o menor nodulares que pueden ser múltiples o como tumoraciones mayores con ocupación variable de la luz vesical.
Por TCMD podemos visualizar una o varias captaciones murales planas o nodulares de tamaño variable,
un engrosamiento mural más o menos difuso o una masa de extensión variable.
La sensibilidad es del 79-89% con una especificidad del 91- 95%.
Ocasionalmente puede presentar pequeñas calcificaciones. En los tumores planos (limitados a mucosa/submucosa) la sensibilidad es más baja.
Por RM el tumor es discretamente hiperintenso respecto al músculo en secuencias potenciadas en T2 e isointenso en secuencias T1.
Histopatológicamente el CCT vesical se caracteriza como de bajo grado (grado I),
moderadamente diferenciado (grado II) o pobremente diferenciado (grado III).
Morfológicamente se dividen en dos categorías,
superficial o invasiva,
con un comportamiento completamente diferente.
Los tumores superficiales constituyen el 70-80% estando limitados a la mucosa y la lámina propia.
Presentan un pronóstico excelente pero una elevada tendencia a la recurrencia (el 70% a los 3 años).
Entre el 10-20% de los que recurren pueden progresar a la forma invasiva.
Fig. 20
Los tumores invasivos presentan un pronóstico peor pudiendo invadir las diferentes capas de la pared vesical y eventualmente estructuras extravesicales. Fig. 21 , Fig. 22 y Fig. 23
Fig. 24
El CCT presenta el ratio de recurrencia más alto de todos los cánceres siendo necesario un riguroso seguimiento después del tratamiento.
La diseminación linfática se produce por invasión inicialmente loco regional perivesical,
sacra,
presacra,
hipogástrica,
obturatriz y cadenas ilíacas externas.
Fig.
25
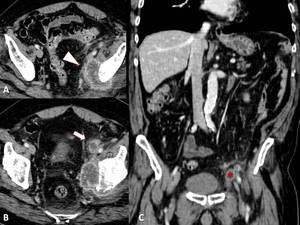
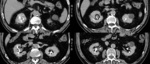
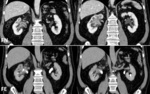
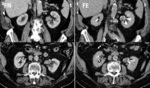
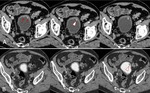
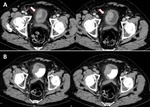
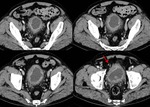
Fig. 25: METASTASIS GANGLIONAR DE CARCINOMA UROTELIAL. A) Imagen axial de TCMD que muestra importante componente adenopático ilíaco izquierdo con centro de aspecto necrótico y periferia hipervascular afectando parcialmente hueso ilíaco homolateral (punta de flecha en A). B) Adenopatía inguinal izquierda de similares características siendo todas ellas compatibles con afectación metastásica. C) Reconstrucción multiplanar coronal. Adenopatía inguinal izquierda referida previamente (asterisco).
Fig.
26
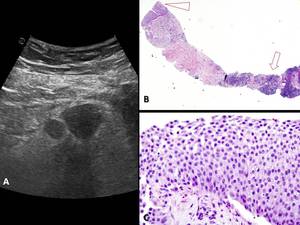
Fig. 26: METÁSTASIS GANGLIONAR de carcinoma urotelial en adenopatia inguinal izquierda. A) La ecografía muestra dos nóduls sólidos correspondientes a adenopatías de aspecto patológico (la mayor de 30 mm) localizadas en área inguinal izquierda. B) Imagen microscópica panorámica de una biopsia de aguja realizada con tru-cut 16G en la que en el extremo inferior derecho se identifica celularidad linfoide, compatible con ganglio linfático, y en el extremo superior izquierdo, una proliferación epitelial. C)Detalle de la imagen anterior. La celularidad epitelial corresponde a epitelio transicional o urotelio.
La afectación de cadena ilíaca común y la aparición de adenopatías paraaórticas,
que se produce en fases tardías de la enferemedad,
se considera metástasis a distancia.
La diseminación metastásica por vía hematógena afecta con mayor frecuencia pulmones,
huesos,
hígado y glándulas suprarrenales.
Fig.
27 y Fig.
28
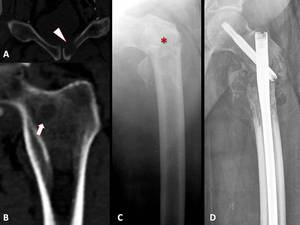
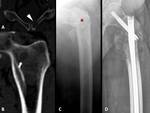
Fig. 27: METÁSTASIS ÓSEAS DE CARCINOMA DE CÉLULAS TRANSICIONALES pT1GIII. Paciente varón de 60 años con antecedente de RTU de tumor vesical correspondiente a carcinoma de células transicionales pT1GIII. Tres años después presentó además de una recidiva local, afectación ósea en forma de lesiones radiolucentes sobre pubis izquierdo (punta de flecha en A, reconstrucción coronal TCMD óseo) y metáfisis humeral izquierda (flecha en B). Posteriormente se produjo una fractura patológica de fémur que se trató con un enclavado medular.
Radiografía convencional en C y D. Fractura: asterisco en D.
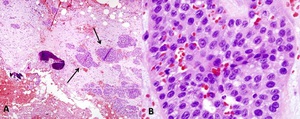
Fig. 28: METÁSTASIS ÓSEAS DE CARCINOMA DE CÉLULAS TRANSICIONALES pT1GIII(continuación de caso anterior):
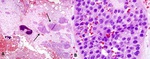
A. Biopsia de fémur proximal, metástasis de carcinoma urotelial. En la imagen se aprecia una trabécula ósea no decalcificada inmersa en tejido conectivo que muestra infiltración por una proliferación epitelial neoplásica formando nódulos de tamaño variable (flechas).
B. Detalle de la imagen anterior. La proliferación neoplásica muestra fenotipo urotelial.
La TC y la RM tienen un importante papel en la estadificación de la enfermedad invasiva.
Las técnicas seccionales (TC y RM) presentan todavía importantes limitaciones en la estadificación de tumores T1,
T2 y T3.
El estadio T se realiza mejor por cistoscopia con biopsia profunda.
Sin embargo,
cuando existe retracción de la pared externa de la vejiga constituye una evidencia indirecta de enfermedad músculo invasiva (T2b).
Las técnicas de imagen ayudan a diferenciar tumores invasivos confinados a la vejiga de tumores con extensión extravesical macroscópica (T3b) y afectación de órganos adyacentes (T4).
La extensión macroscópica extravesical morfológicamente se reconoce por irregularidad mural con márgenes externos de la pared vesical mal definidos pudiendo detectar nódulos sólidos y/o trabeculación de la grasa perivesical.
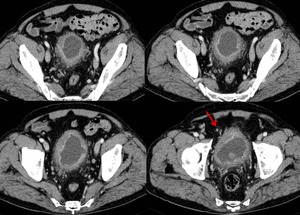
Fig. 37: TUMOR VESICAL INFILTRANTE. Imágenes Axiales de TC que muestran un engrosamiento mural vesical patológico de predominio anterolateral derecho. observando trabeculación de la grasa perivesical y nodularidad asociada (flecha).
Carcinoma escamoso
El carcinoma de células escamosas (CCE) de la vejiga urinaria es una neoplasia maligna infrecuente derivada del urotelio que muestra histológicamente un fenotipo de células escamosas puro.
Es mucho menos frecuente que el carcinoma urotelial constituyendo el 1.3% de los tumores vesicales en hombres y un 3.4% 3n mujeres.
Constituye menos del 5% de los carcinomas vesicales en áreas donde la esquistosomiasis no es endémica y un 75% en áreas donde la infección por S.
haematobiumes endémico.
Factores de riesgo en áreas no endémicas incluyen irritación crónica por catéteres,
cálculos vesicales o infección crónica.
En un 80% de casos son tumores de alto grado y localmente agresivos con invasión de la muscular.
Macroscòpicamente la mayoría de los CCE son masas necróticas sólidas,
voluminosas y polipoides que ocupan gran parte de la luz vesical. Tienen predilección por el trígono y las paredes laterales.
Microscópicamente el tumor invasivo puede ser bien diferenciado con islotes de células escamosas mostrando queratinización,
puentes intercelulares prominentes y mínimo pleomorfismo nuclear,
o pobremente diferenciado con marcado pleomorfismo nuclear y focos aislados de diferenciación escamosa evidente. Fig. 29, Fig. 30 y Fig. 31
Adenocarcinoma
El adenocarcinoma es una neoplasia derivada del urotelio que histológicamente muestra un fenotipo glandular puro y constituye menos del 2% de todos los tumores vesicales malignos.
Incluye el adenocarcinoma vesical primario de vejiga urinaria y el carcinoma uracal.
Es más frecuente en varones en una proporción 2.6:1 y presenta un pico de incidencia en la sexta década de la vida.
El síntoma más frecuente es la hematuria seguido de la disuria y raramente presenta mucosuria.
Macroscópicamente este tumor puede ser exofítico,
papilar,
sesil,
ulcerado o infiltrante exhibiendo un aspecto gelatinoso.
Microscópicamente el adenocarcinoma puro puede mostrar diferentes patrones de crecimiento.
Estos incluyen: tipo entérico (colónico),
forma de adenocarcinoma no específica,
células en anillo de sello,
mucinoso (coloide),
células claras,
hepatoide y mixto.
Fig. 32 , Fig. 33 y Fig. 34
Carcinoma de célula pequeña
El carcinoma de célula pequeña es una neoplasia neuroendocrina maligna derivada del urotelio que histológicamente simula su homólogo pulmonar.
El síntoma más frecuente es la hematuria macroscópica.
Otros síntomas incluyen disuria y dolor abdominopélvico localizado.
Aproximadamente un 56% de los pacientes presentan enfermedad metastásica en el momento del diagnóstico.
La mayoría de los carcinomas de célula pequeña del tracto urinario se originan en la vejiga urinaria.
El tumor puede presentarse como una masa sólida aislada,
polipoide,
nodular con o sin ulceración y puede infiltrar de forma extensa la vejiga urinaria.
Están constituidos por células pequeñas con molde nuclear,
citoplasma discreto y núcleo con cromatina finamente punteada siendo el nucleolo apenas visible.
Las mitosis están presentes y pueden ser frecuentes.
La expresión neuroendocrina se identifica habitualmente por métodos inmunohistoquímicos.
Este tipo de tumores se caracteriza por presentar un curso clínico agresivo con invasión vascular y muscular precoz.
La supervivencia media a los 5 años en pacientes con enfermedad vesical local por carcinoma de célula pequeña es del 8%.
Fig. 35 y Fig. 36
Afectación secundaria maligna
La causa más frecuente de afectación secundaria maligna de la vía urinaria es la extensión directa fundamentalmente de sarcomas y carcinomas de cérvix,
próstata,
vejiga urinaria,
colon y útero.
Por TC se identifican como estenosis irregulares con engrosamientos murales focales hipercaptantes.