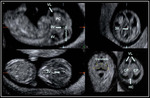
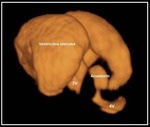
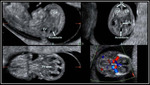
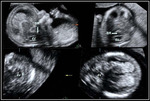
INTRODUCCIÓN
Las malformaciones de fosa posterior (PF) son las anomalías más comunes diagnosticadas y abarcan un amplio espectro de entidades diferentes,
que pueden ser consideradas desde variantes de la normalidad a anomalías graves.
Unas y otras pueden tener un aspecto por imagen similar,
no siendo infrecuentes los errores diagnósticos con implicaciones significativas a la hora de asesorar a la gestante.
Aunque la ecografía es primer método de imagen en el diagnóstico prenatal,
la resonancia magnética (RM) permite un estudio anatómico más detallado de estructuras cerebrales,
especialmente de la fosa posterior.
Existen numerosas controversias relacionadas con la clasificación y sobre todo con el pronóstico de las malformaciones de la FP, siendo la literatura pre y postnatal extremadamente confusa.
Es necesario,
por tanto,
establecer una estrategia para el diagnóstico y poder así ofrecer a la familia información,
consejo genético o alternativas terapéuticas según la anomalía detectada.
Dada la gran resolución anatómica y la capacidad de diferenciación tisular de la RM,
podemos establecer algoritmos diagnósticos basados en: la cantidad de líquido cefalorraquídeo en la FP,
tamaño de la FP,
posición del tentorio,
biometría del vermis y hemisferios cerebelosos,
alteraciones en la señal del cerebelo,
afectación simultánea de tronco y cerebelo o anomalías extraaxiales de la FP.
En este trabajo se ha realizado una revisión de las diferentes patologías de la FP según estos criterios,
así como de sus implicaciones pronósticas en el desarrollo neurológico postnatal.
EMBRIOLOGÍA Y ANATOMÍA
Durante la tercera semana de desarrollo embrionario o quinta semana de desarrollo postmenstrual aparece la estría primitiva sobre la superficie del disco bilaminar como un engrosamiento del extremo caudal del epiblasto.
La proliferación de células en su extremo craneal forma el nódulo de Hensen.
La invaginación de la estría primitiva origina la migración de estas células en sentido craneal,
lateral y ventral entre el epiblasto y el hipoblasto,
en un proceso llamado gastrulación,
formando el embrión trilaminar que consta de ectodermo (epiblasto),
el mesodermo intraembrionario (nueva capa) y el endodermo (hipoblasto).
El proceso de formación del tubo neural,
que se conoce como neurulación primaria,
se inicia en el día 18 de desarrollo embrionario con la aparición de la placa neural o neuroepitelio como un engrosamiento del ectodermo craneal inducido por la notocorda.
En la placa neural se desarrolla el surco neural longitudinal flanqueado por los pliegues neurales cuya fusión forma el tubo neural (día 23) [1].
En la sexta semana postmenstrual y cuarta de desarrollo embrionario,
el disco completa la neurulación con el cierre del neuroporo anterior el día 25 y el posterior el día 27-28.
El cierre del neuroporo rostral en la región craneal origina la formación de las 3 vesículas cerebrales primarias a partir de las cuales se desarrolla el encéfalo y que forman el cerebro anterior o prosencéfalo,
el cerebro medio o mesencéfalo y el cerebro caudal o rombencéfalo.
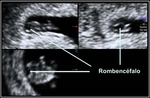
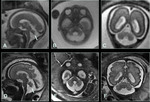
Al final de la 6º semana postmenstrual el embrión mide entre 3 y 9 mm y se separa del saco vitelino.
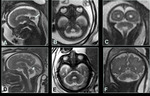
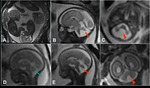
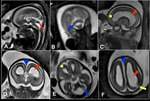
La primera estructura anatómica identificable es el tubo neural y en este momento solo se visualiza la cavidad alargada y estrecha del romboencéfalo en la parte más superior del embrión. Fig. 1
En la 7º semana postmenstrual el sistema ventricular se divide en 5 regiones cerebrales.
El cerebro anterior se divide en telencéfalo (que da lugar a los hemisferios cerebrales como pequeñas evaginaciones y cuyas paredes formarán los ventrículos laterales -VL-) y diencéfalo (que dará lugar a los tálamos y a la cavidad del tercer ventrículo (3V).
El cerebro medio permanece indiviso y su cavidad dará lugar al acueducto de Silvio.
Del rombencéfalo derivan el metencéfalo y mielencéfalo que darán lugar respectivamente a la protuberancia y cerebelo y al bulbo raquídeo y cuya cavidad se convierte en el cuarto ventrículo (4V).
Es en la 7º semana con una longitud cefalonalgas (CRL) de 10-15mm,
cuando las cavidades son más fácilmente identificables,
y ya se pueden observar en situación más anterior el 3V en el diencefálo,
más posterior la cavidad mesencefálica curvada y tubular que se convertirá en el futuro acueducto de Silvio y finalmente más posterior el 4V,
ancho y plano que es siempre visible. Los VL aún son demasiado pequeños y solo se identifican al final de la 7ª semana.
Fig. 2
En la sexta semana de desarrollo postconcepcional (8ª postmenstrual),
el embrión tiene un tamaño de entre 16 y 22 mm.
Las cavidades cerebrales se observan fácilmente y los hemisferios y vesículas telencefálicas se agrandan desarrollándose en forma de creciente.
El 3V es todavía amplio al igual que el acueducto.
El 4V tiene una forma piramidal con el vértice central profundizando en la flexura pontina.
Fig. 3
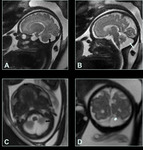
En la 9º semana postmenstrual el tamaño del embrión crece de 23 a 32mm.
El tamaño de los ventrículos laterales se incrementa rápidamente.
El córtex es liso y los plexos coroideos (PC) en el interior de los VL se hacen patentes.
La anchura del 3V se estrecha gradualmente mientras que el acueducto permanece amplio.
El istmo romboencefálico es siempre visible.
Un pliegue transversal se forma en el techo del 4V que engloba meninge primitiva vascular que formará el PC del techo del 4V dividiéndolo en área membranácea anterior (superior) y posterior (inferior).
Fig. 4
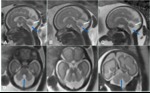
A partir de la 10ª semana postmenstrual,
el embrión se convierte en feto y más allá de este punto,
prácticamente todas las estructuras están desarrolladas. En la 10ª semana se observa un aumento del tamaño de los VL,
aparece la hoz cerebral y se siguen visualizando los PC prominentes con el signo de la mariposa.
El acueducto sigue siendo visible pero hay un estrechamiento del diencéfalo y una disminución relativa del 3V.
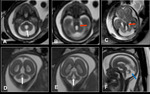
Fig. 5 Fig. 6
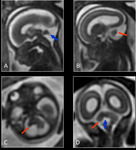
En la 11ª semana,
el embrión mide entre 41 y 52 mm.
Los PC siguen siendo muy patentes,
tanto en los VL como en el 4V.
Los hemisferios cerebelosos se visualizan claramente,
el acueducto es aún prominente y se puede observar el polígono de Willis.
El 3V se sigue estrechando.
Fig. 7
En la 12ª semana el embrión mide entre 52 y 64 mm.
En esta semana,
el encéfalo embrionario crece con rapidez y se dobla en sentido ventral,
lo que produce la flexura cervical y la flexura cerebral media; y en dirección opuesta a las anteriores,
la flexura pontina que divide el cerebro caudal en una parte caudal mielencéfalo y otra craneal o metencéfalo.
El mielencéfalo da lugar al bulbo raquídeo,
cuya parte caudal se asemeja a la médula espinal con el conducto neural central.
Más cranealmente,
enfrente de la acodadura pontina,
la parte rostral del bulbo es abierta ancha y plana,
y la cavidad que delimita,
el 4V,
adquiere forma de diamante.
Fig. 8
Sobre área membranácea anterior se origina el vermis cerebeloso,
y el área membranácea posterior forma la bolsa de Blake.
La bolsa de Blake se fenestra y origina el foramen de Magendie al final de la 10ª semana [2].
Los hemisferios cerebelosos se desarrollan a partir de engrosamientos en la parte dorsal de las placas alares (labios romboideos),
que se proyectan hacia el 4V para terminar cubriéndolo.
Los hemisferios cerebelosos se fusionan en sentido craneocaudal y dan lugar a un vermis visible al final de la 7ª semana.
El lóbulo floculonodular es visualizado a partir de la 10ª semana y la fisura primaria que separa lóbulos anterior y posterior en la 11ª-12ª semana.
El volumen del lóbulo posterior es mayor que el del anterior con una relación 2:1,
y está subdividido por tres fisuras mayores: prepiramidal,
horizontal y secundaria.
La fisura posterolateral separa el lóbulo posterior del floculonodular [3].
IMAGEN POR RM EN EL DESARROLLO DE LA FOSA POSTERIOR
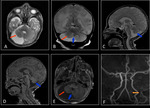
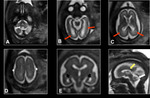
Entre las 16ª y 19ª semanas de gestación,
los hemisferios cerebelosos y la mayoría del tronco cerebral muestran una intensidad de señal intermedia y homogénea.
El tectum es visible como un área lobulada de baja señal en el margen dorsal del mesencéfalo.
Entre las 20ª y 23ª semanas aparece una banda periférica hipointensa en los hemisferios cerebelosos que corresponde a la cortical cerebelosa.
En esta misma edad gestacional se observa una banda vertical hipointensa en el margen posterior de la protuberancia y el bulbo que alcanza el mesencéfalo en la 32ª semana.
Esta banda corresponde al fascículo longitudinal medial.
Entre las 23ª a 26ª semanas,
aparecen las folias cerebelosas como ondulaciones en la superficie de los hemisferios cerebelosos que son más prominentes en la semana 32ª y aumentan en número hasta que el feto llega a término,
donde presentan el patrón definitivo de bandas hipo-hiperintensas.
En la semana 24ª se identifican los pedúnculos cerebelosos medios como bandas hipointensas bilaterales que conectan la protuberancia con los hemisferios cerebelosos.
Entre las semanas 26ªa 27ª, se visualizan las amígdalas cerebelosas y las tres capas cerebelosas: capa cortical externa hipointensa ,
capa intermedia de sustancia blanca cerebelosa hiperintensa y la capa profunda hipointensa que corresponde a los núcleos dentados [4].
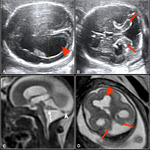
Fig. 9 Fig. 10
CLASIFICACIÓN DE LAS ANOMALÍAS DE FOSA POSTERIOR
Se define malformación como una aberración del normal desarrollo de un órgano que ocurre como consecuencia de una disposición genética,
infección,
exposición a agentes teratógenos o de forma esporádica [5].
A pesar de que se han propuesto muchas clasificaciones para las malformaciones de la FP,
ninguna ha sido ampliamente aceptada.
Barkovich et al [6] proponen una clasificación de las lesiones basada en el desarrollo embrionario y consideraciones genéticas que ayudan a entender la patogénesis de estas anomalías.
Sin embargo,
la clasificación más tradicional se basa en hallazgos morfológicos,
en la cual las malformaciones son agrupadas acorde a los hallazgos de imagen,
siendo la clasificación más simple y la más aceptada por los radiólogos.
Existe también confusión en la literatura en el uso de algunos términos como la malformación de Dandy-Walker (MDW),
que incluye un grupo heterogéneo de anomalías y el uso incorrecto de agenesia o hipoplasia.
Parisi y Dobyns recomiendan abandonar el término variante de Dandy-Walker,
ya que ha sido utilizado como sinónimo de hipoplasia de vermis,
hipoplasia de vermis inferior,
agenesia y disgenesia de vermis e incluso síndromes del signo molar que pueden confundirse con una MDW clásica [7].
El término agenesia completa de vermis indica ausencia de vermis,
en los casos de agenesia parcial de vermis,
sólo parte del vermis está ausente y el resto es normal.
El concepto hipoplasia de vermis indica un vermis con configuración normal,
pero de pequeño tamaño [8].
A continuación,
revisaremos los diferentes tipos de anomalías de la FP,
dividiéndolas en 6 grandes grupos en función de las siguientes características:Líquido cefalorraquídeo (LCR) en la FP,
tamaño de la FP,
posición del tentorio,
biometría del vermis y hemisferios cerebelosos,
alteraciones en la señal del cerebelo,
afectación simultánea de tronco y cerebelo o anomalías extraaxiales de la FP.
Fig. 11 Fig. 12
1.
Incremento del LCR en FP con inserción normal del tentorio: Dentro de este grupo,
debemos atender a la presencia o ausencia de otros hallazgos:
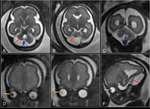
- No existen otras alteraciones asociadas. Debemos considerar el diagnóstico de mega cisterna magna.
El 4V,
el tronco cerebral,
el vermis y los hemisferios cerebelosos son normales y no existen anomalías supratentoriales.
La megacisterna magna es un espacio lleno de líquido por detrás del cerebelo.
Puede producir remodelación ósea de la tabla interna del occipucio.
Contiene pequeños septos que no deben ser confundidos con estructuras vasculares o quísticas.
La cisterna magna septada representa las paredes de la bolsa de Blake,
una estructura vestigial filogenética.
Los septos de cisterna magna,
por lo tanto,
son un marcador del desarrollo normal del techo del rombencéfalo.
La megacisterna magna aislada parece ser una variante anatómica sin significado clínico [9].
Fig. 13
- Vermis normal y malrotado. Si las medidas del vermis son las adecuadas para la edad gestacional,
visualizamos la fisura primaria,
el cociente vermis superior/vermis inferior es 1:2,
la protuberancia y el tallo cerebral son normales pero el vermis está malrotado (con incremento del ángulo tegmento-vermiano),
entonces debemos sospechar un quiste de la bolsa de Blake. Si el diagnóstico se hace precozmente,
en la semana 20,
debemos esperar a la semana 22-24,
ya que existen algunos casos de rotación tardía del vermis.
Entre un 30-50% de los casos tendrán una resolución espontánea durante la gestación.
Si no hay anomalías anatómicas o cromosómicas asociadas,
el desarrollo neurológico postnatal será normal.
Es posible que la persistencia de la bolsa de Blake y megacisterna magna representen anormalidades (menos graves) dentro de la MDW [8;10].
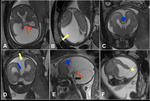
Fig. 14 Fig. 15
- Existe efecto de masa sobre el vermis y/o los hemisferios cerebelosos,
sin alteraciones cerebelosas. El diagnóstico a considerar es el quiste aracnoideo retrocerebeloso,
que para algunos autores forma parte de la MDW.
El quiste está localizado detrás del vermis y del 4V,
sin comunicación con este último.
No se asocia a hidrocefalia ni a disgenesia cerebelosa.
A diferencia de la megacisterna magna,
no es atravesada por los septos.
Un quiste aracnoideo pequeño,
situado detrás del vermis,
puede pasarse por alto durante el período prenatal debido a la ampliación fisiologica de la cisterna magna.
Un gran quiste retrocerebeloso puede crear efecto de masa en el vermis y sobre la inserción del tentorio; la orientación del tentorio será normal pero su inserción distal estará elevada.
Puede producir remodelación ósea del occipucio [11].
Fig. 16
- Uno de los hemisferios cerebelosos parece pequeño,
con o sin afectación del vermis. El diagnóstico diferencial incluye hipoplasia,
displasia cerebelosa unilateral,
síndrome de PHACE o síndrome de Pascual Castroviejo 2,
isquemia o hemorragia .
La hipoplasia cerebelosa unilateral es una entidad muy infrecuente que implica desde manifestaciones severas hasta pacientes prácticamente asintomáticos.
Los casos en los que las pruebas de imagen demuestran mayor asimetría de los hemisferios están por lo general asociados a otras alteraciones cerebrales y comisurales (en particular sobre tronco cerebral y cuerpo calloso) y a peor pronóstico.
Esta variabilidad de presentación tanto clínica como radiológica sugiere un origen adquirido intraútero,
relacionado con una lesión vascular o isquémica [12].
La displasia cerebelosa implica una formación anómala,
en este caso focal,
del cerebelo.
Existe siempre un patrón alterado de las folias hemisféricas,
que pueden estar agrandadas,
tener una orientación anormal o presentar desde fisuras profundas hasta ausentes con un patrón estriado con imágenes lineales hiperintensas en secuencias T2 entre el córtex cerebeloso isointenso.
También puede haber nódulos de heterotopia.
Puede asociarse a retraso psicomotor,
aunque en ocasiones ha sido un hallazgo incidental y probablemente su prevalencia es mayor de lo estimado actualmente.
El síndrome de Lhermitte-Duclos-Cowden asocia gangliocitoma cerebeloso displásico,
hamartomas faciales y en múltiples órganos [12] El síndrome neurocutáneo descrito con el acrónimo PHACE describe la asociación de un hemangioma,
habitualmente grande y segmentario (esto es,
que no sigue la distribución trigeminal típica de otros trastornos neurocutáneos) en forma de placa y que afecta la cara en un 98% de los casos a una o más de las siguientes alteraciones: anomalías de la FP,
anomalías arteriales cerebrovasculares,
afectación cardiaca/coartación de aorta y alteración ocular.
La presencia de defectos del desarrollo ventral,
especialmente del esternón y/o del rafe supraumbilical,
se denomina como PHACES [13;14].
Ante la presencia de hipoplasia unilateral de un hemisferio cereloso y del vermis,
tenga o no alteraciones oculares visibles en el estudio fetal,
debemos incluirla en el diagnóstico diferencial.
La hipoplasia cerebelosa y del vermis puede asociarse a afectación de la arteria cerebelosa posteroinferior,
con ausencia de visualización de la arteria en estudios postnatales [15].
Las hemorragias y los infartos hemorrágicos en el cerebelo fetal provocan hiperseñal en secuencias T1 en el hemisferio cerebeloso afectado,
que progresivamente disminuye de tamaño,
con o sin lesión quística asociada.
El pronóstico es difícil de establecer,
pero se cree que es mucho mejor (incluso con desarrollo normal) si la hemorragia no llega a implicar al vermis [8;16]. Fig. 17 Fig. 18 Fig. 19 Fig. 20
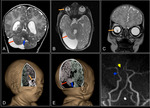
- Vermis de pequeño tamaño con hemisferios cerebelosos normales. El diagnóstico es hipoplasia vermiana.
El vermis está presente,
se observan los lóbulos y fisuras,
pero parte de él o la totalidad es de pequeño tamaño y no hay anomalías asociadas.
El pronóstico es impreciso ya que puede representar un rasgo dominante de pronóstico benigno o puede representar parte de un síndrome genético como el X frágil [8;17]. Fig. 21 Fig. 22 Fig. 23
- Vermis y hemisferios cerebelosos pequeños: El diagnóstico dehipoplasia cerebelosa debe ser considerado.
Se observará un cerebelo normalmente formado,
con un diámetro transverso pequeño,
cisterna magna normal o de tamaño reducido y 4V de forma normal.
El tentorio tendrá una orientación normal.
Puede asociarse a alteraciones cromosómicas,
y es por ello indicación de estudio de cariotipo (trisomía 21,
trisomía 18,
deleción 5p); infecciones (CMV); trastornos metabólicos,
entre ellos déficit de vitamina A o trastornos congénitos de la glicosilación.
Los pacientes presentan por lo general cierto grado de ataxia y se puede asociar a retraso mental,
aunque algunos pacientes diagnosticados habían consultado por síntomas como cefaleas recurrentes.
La asociación con otras alteraciones del sistema nervioso central (SNC) ensombrece el pronóstico muy significativamente [18;19].
Oligophrenin-1 (OPHN1),
con deleción de los exones16,17,
es uno de los principales genes en retraso mental ligado al X y está asociado a hipoplasia cerebelosa con disfunción córtico-cerebelosa [20].
La hipoplasia cerebelosa puede ser secundaria a una mutación patológica del gen Reelin,
que produce una proteína llamada reelina.
La reelina es crucial para la regulación de los procesos de migración neuronal y en el desarrollo del cerebro.
La hipoplasia cerebelosa se acompaña de lisencefalia [21].
- Vermis y hemisferios cerebelosos de pequeño tamaño,
con hipoplasia del tronco cerebral. Corresponde a una hipoplasia pontocerebelosa.
Barth describió el tipo I (con degeneración del asta anterior de la médula espinal; los individuos afectos presentan debilidad muscular,
dificultad en la deglución y distrés respiratorio) y el tipo II (con microcefalia progresiva y manifestaciones extrapiramidales como corea y distonía; los pacientes presentan retraso psicomotor,
convulsiones y fallecen precozmente).
Podemos hallar hipoplasia pontina con ausencia de la curvatura pontina,
que implica peor pronóstico pues se asocia tanto a hipoplasia como a displasia cerebelosa,
u observarla en el contexto de alteraciones cerebrales generalizadas o bien con un cerebro normal.
Suele haber además una degeneración progresiva del cerebelo añadida,
que continúa tras el nacimiento [12;22;23].
El síndrome de Walker-Warburg y síndrome músculo-óculo-cerebral muestran un cerebelo pequeño y displásico,
la protuberancia presenta una hendidura longitudinal en línea media y muestran lisencefalia tipo II [21;24]
- Vermis ausente. Puede tratarse de una agenesia completa o,
si existe una parte del vermis,
una agenesia parcial,
que es más frecuente y en la que la totalidad o la porción inferior del vermis está ausente.
El pronóstico dependerá de la presencia de anomalías asociadas.
En caso del síndrome de Joubert (JSRD o síndromes relacionados con el signo molar),
el 4V está agrandado,
el fastigium es anormal y en el plano axial se observa un agrandamiento de la fosa interpeduncular y unos pedúnculos cerebelosos superiores engrosados y elongados (signo del molar).
Fig. 24 Existe una amplia lista de anomalías asociadas al síndrome de Joubert,
tales como meningoceles,
alteraciones en la morfología de las extremidades,
enfermedad quística renal,
hidronefrosis bilateral,
colobomas,
macrocefalia,
discinesias,
paladar ojival,
micrognatia,
epispadias,
criptorquidia,
retraso estatoponderal y fibrosis hepática congénita.
Clínicamente,
se presentan con retraso en el desarrollo,
ataxia y anomalías óculomotoras y respiratorias.
Los neonatos pueden presentar nistagmus,
episodios de apnea e hiperpnea y crisis.
Entre los síndromes relacionados se encuentran síndrome CORS (en inglés cerebello-oculo-renal syndrome ),
síndrome orofacial digital tipo 6,
síndrome COACH (en inglés: cerebellar vermis hypoplasia,
oligophrenia,
ataxia,
ocular coloboma,
and hepatic fibrosis),
síndrome CHARGE (en inglés coloboma,
heart defects.
choanal atresia,
mental retardation,
genitourinary hypoplasia,
and ear defects),
síndrome Arima o síndrome Senior-Löken [25-28].
2.
Incremento del LCR en la FP con inserción anormalmente alta del tentorio:
La MDW comprende la agenesia total o parcial del vermis,
la dilatación quística del 4V y una FP amplia con elevación del seno transverso,
el tentorio y la tórcula.
Los hemisferios cerebelosos pueden presentar varios grados de hipoplasia.
En las formas más severas el remanente cerebeloso aparece desplazado anterolateralmente y el remanente del vermis aparece rotado y elevado sobre el quiste del 4V [29].
Fig. 25 Fig. 26 Fig. 27
Un defecto de la zona membranosa posterior es responsable de la fenestración variable de la bolsa de Blake con expansión posterior y elevación del tentorio.
Un defecto de la zona membranosa anterior es responsable de la disgenesia vermiana [3].
Aproximadamente el 75% de los casos presentan hidrocefalia obstructiva a los 3 meses de vida [30].
Es común la asociación con anomalías del sistema nervioso central (SNC) como la agenesia de cuerpo calloso,
polimicrogiria,
heterotopias y encefaloceles occipitales [30-33].
Además,
hasta en un 65% de los casos se han descrito anomalías no relacionadas con el SNC,
como anomalías cardiacas,
renales,
faciales y de extremidades como polidactilia o sindactilia.
La MDW puede estar asociada a cromosomopatías (trisomía 21,
18,
13 y síndrome de Turner) y más de 50 desórdenes genéticos como los síndromes de Cornelia de Lange,
Ellis van Creveld,
Goldenhar,
Meckel Gruber,
Warburg,
Coffin-Siris,
Joubert,
Ruvalcaba- Myhre-Smith y Pascual Castroviejo.
La presencia de anomalías asociadas presentan peor pronóstico [34;35].
Boddaert et al [36] compararon el coeficiente intelectual (IQ) de 21 niños con MDW con o sin normal lobulación del vermis,
y observaron que el 82% de los niños del primer grupo presentaba un IQ normal frente a ninguno del segundo grupo.
Además,
entre el subgrupo de normal lobulación y anormal IQ todos los niños tenían anomalías del SNC o anomalías extra-SNC.
La mortalidad varía entre el 12-50%,
las anomalías asociadas contribuyen al 83% de las muertes postnatales y un retraso en el desarrollo cognitivo está presente entre el 40-70% [35].
3.
Disminución del LCR en FP. El diagnóstico a considerar es Chiari tipo 2.
La malformación Chiari tipo 2 es una malformación congénita compleja,
casi siempre asociada a mielomeningocele.
La FP presenta pequeño tamaño con desplazamiento inferior del vermis y el bulbo.
El vermis impronta la cara posterior de la unión bulbo-medular.
El tectum del mesencéfalo presenta morfología en pico y el cerebelo está desplazado superiormente rodeando el tronco del encéfalo con imagen de “cerebelo en torre” que asciende por encima de la incisura tentorial.
El 4V está desplazado caudalmente y aparece adelgazado y elongado.
El 3V está frecuentemente aumentado de tamaño con prominente masa intermedia.
Se acompaña de deformidad y aplanamiento bilateral de la calota frontal (signo del limón).
Se asocia a malformaciones del desarrollo cortical como polimicrogiria,
giros estrechos y contraídos (estenogiria) y sustancia gris heterotópica.
La disgenesia de cuerpo calloso está presente en casi 2/3 de todos los casos y se asocia a siringohidromielia en un 50% de los mismos [37;38].Fig. 28 Fig. 29 Fig. 30
La malformación Chiari tipo 3 es la más rara de las MDW y consiste en la presencia de una FP pequeña con desplazamiento caudal variable del tronco cerebral y variable herniación de meninges/contenido de FP a través de un defecto óseo occipital bajo o cervical alto [39].
El diagnóstico diferencial incluye cefalocele occipital aislado,
iniencefalia y encefaloceles occipitales sindrómicos.
El cefalocele aislado carece de los hallazgos típicos de Chiari 2 y no está asociado a disrafismo cervical.
Iniencefalia es un cefalocele occipital con extenso disrafismo y cuello fijado en retrofexión ("stargazer" fetus) [40].
El encefalocele sindrómico tiene otros hallazgos específicos según el síndrome al que se asocie,
como en el síndrome Meckel-Gruber o síndrome de Klippel-Feil [41;42].
4.
Disminución de la biometría cerebelosa con LCR en FP normal. Los diagnósticos probables son algunas formas de hipoplasia cerebelosa (hemisferios cerebelosos y/o vermis) o rombencefalosinapsis.
La rombencefalosinapsis es una malformación de línea media caracterizada por ausencia de vermis cerebeloso y aparente fusión de los hemisferios cerebelosos.
Existen formas leves,
con ausencia parcial de los nódulos y del vermis anterior y posterior,
y formas con agenesia completa de vermis y nódulos.
Las folias transversas cerebelosas están fusionadas en la línea media,
en la región dorsal.
Las amígdalas,
los núcleos dentados y pedúnculos cerebelosos superiores están también fusionados.
Es frecuente la presencia de hidrocefalia y estenosis del acueducto de Silvio.
El cavum septi pellucidi está ausente en el 50% de los casos.
Los tálamos,
fórnices y el tectum pueden estar parcial o totalmente fusionados.
Otras anomalías asociadas son la agenesia de bulbos olfatorios y disgenesia de cuerpo calloso o el síndrome de VACTERL ( del inglés vertebral anomalies,
anal atresia,
cardiovascular anomalies,
tracheoesophageal fistulas,
renal anomalies,
and limb defects) [43;44].
Se han descrito casos con desarrollo cognitivo normal [45;46] y con retraso del mismo [43-46].
Pero todas se acompañan de alteraciones motoras [47-50],
que incluyen retraso en el desarrollo motor [50;51],
hipotonía [47;50],
parálisis cerebral [46],
alteraciones en el equilibrio [48] y alteraciones óculo-motoras [48;50].
5.
Alteración de la señal cerebelosa en RM. Puede ser secundaria a infección por CMV,
isquemia,
hemorragia o telangiectasia capilar.
La infección congénita de CMV es la infección intrauterina más común,
que ocurre aproximadamente en un 1% de todos los nacidos vivos [52].
Aproximadamente el 90% de los niños con afectación congénita por CMV son asintomáticos al nacer y un 10-15% de éstos y de todos los neonatos con síntomas de infección desarrollarán problemas neurológicos persistentes (sordera neurosensorial,
pérdida visual y retraso mental) [52].Los hallazgos radiológicos incluyen: Microcefalia,
calcificación cerebral en localización periventricular subependimaria (hiperintensas en secuencias T1),
ventriculomegalia,
quistes subependimarios,
sinequias o hemorragia intraventricular, anomalías del desarrollo cortical (lisencefalia,
paquigiria y polimicrocefalia difusa),
afectación de la sustancia blanca supratentorial con destrucción (áreas focales o difusas de hiperintensidad en secuencias T2 afectando fundamentalmente lóbulos parietales y polo anterior de temporales) o retraso en la mielinización,
quistes cerebelosos e hipoplasia cerebelosa [53-55].
La presencia de lisencefalia y paquigiria están asociadas a peor pronóstico neurológico que la polimicrogiria en pacientes con infección por CMV,
y son indicadores de infección precoz [56].
La MR fetal detecta anomalías cerebrales antes de la semana 24.
Los principales hallazgos,
tales como lesiones temporales anteriores,
microcefalia o malformaciones corticales,
implican peor pronóstico y pueden pasar desapercibidas por ecografía [54]. Fig. 31
La lesión isquémico-hemorragica intracerebelosa es muy infrecuente y asocia un pronóstico muy pobre.
Entre sus diferentes causas se incluyen las hemorragias de la matriz germinal o lesiones vasculars subyacentes tales como las malformaciones cavernosas [57].
Aunque es infrecuente,
existen también casos publicados secundarios a infección por CMV [58] y a hidrops fetal inmune y no inmune [59;60],
presumiblemente asociado a trastorno hematológicos y hemodinámicos.
El sangrado cerebeloso presenta hiperseñal en secuencias T1 e hiposeñal en secuencias eco de gradiente T2.
Las secuencias T2 y difusión nos ayudan a detectar el edema de la lesión isquémica [61].
Fig. 32
Las telangiectasias han sido descritas como lesiones focales del cerebelo sin efecto de masa,
ecogénicas y sin hiperseñal en secuencias T1 en los estudios de RM.
El diagnóstico se confirma con RM cerebral postnatal con contraste [62].
6.
Anomalías de FP que no afectan al cerebelo ni al tronco cerebral.
El diagnóstico incluye malformación del seno dural,
meningocele o quiste dermoide.
Las malformaciones de senos durales son malformaciones vaculares congénitas raras que se observan en fetos y niños pequeños.
Se clasifican,
según su localización,
en posteriores y laterales.
Las malformaciones laterales afectan a senos transversos,
sigmoides o bulbos yugulares,
tienen buen pronóstico y frecuentemente se diagnostican en el periodo postnatal.
Las malformaciones posteriores son las más frecuentes y presentan un gran lago venoso posterior en la prensa de Herófilo o seno longitudinal superior que comunica con otros senos o venas cerebrales.
Se observa una masa extraaxial en la FP posterior al vermis,
que se encuentra desplazado en dirección anterior.
Presenta una morfología triangular al envolver a la prensa de Herófilo y puede afectar al seno longitudinal superior y los senos transversos.
Se acompaña de trombosis venosa.
La malformación venosa dural muestra una señal heterogénea con zona central característica hipointensa en T2 e hiperseñal en secuencias T1,
debido a la presencia de trombo central [63;64].
El pronóstico no es malo en ausencia de complicaciones tales como hidrocefalia o infarto cerebral secundario a hipertension venosa.
Merzoug et al [63] estudiaron 13 casos con malformación de senos durales: En 3 de ellos se interumpió el embarazo; un niño falleció por hidrocefalia severa a los 5 meses,
y los 9 niños restantes evolucionaron bien,
7 sin tratamiento y 2 con tratamiento (embolizacion endovascular y derivación ventricular por hidrocefalia respectivamente).
Fig. 33
Un meningocele occipital es una herniación a través de un defecto óseo del hueso occipital que contiene LCR y meninges,
sin evidencia de tejido cerebral en el contenido herniado.
Ante un feto con una lesión quística en región occipital,
tenemos que pensar en meningocele como primera posibilidad Fig. 34 . Otras lesiones como el higroma quístico,
quistes epidermoides o dermoides,
senos dermicos,
hemangioma y tumores cutáneos pueden presentarse como lesiones quísticas occipitales,
pero son más infrecuentes [65;66].
La ausencia de hidrocefalia asociada es un signo de buen pronóstico alteraciones en el desarrollo psicomotor ausentes o leves [67] .
Los quistes dermoides de fosa posterior son lesiones benignas poco frecuentes.
Debido a su asociación a seno dérmico existe riesgo de infección intracraneal secundaria a la infección del quiste [68].
Tienen un origen embrionario, y pueden estar asociados a otras malformaciones congénitas como anomalía de Klippel-Feil [69].
A diferencia de los lipomas,
que presentan señal grasa en todas les secuencias de pulso,
los dermoides tiene mayor variabilidad de señal.
Aparecen hiperintensos en secuencias T1( debido al componente de colesterol),
y si existe rotura del quiste pueden observarse "gotas" hiperintensas en el espacio subaracnoideo.
La señal en secuencias T2 es variable,
desde hipo a hiperintenso,
y no realzan tras contraste [70].
La resección radical del quiste es el único tratamiento efectivo [68].
Los quistes epidermoides son tumores congénitos benignos,
resultado de defectos del cierre del tubo neural.
Las localizaciones más frecuentes son el ángulo pontocerebeloso,
la región suprasellar,
la FP,
el canal cervical o el diploe craneal,
normalmente en situación lateral a la línea media.
Muestran hiposeñal en secuencias T1 e hiperintensidad en T2,
sin realce tras contraste intravenoso.
La secuencia de difusión muestra hiperseñal,
lo que permite diferenciarlo de quiste aracnoideo,
El denominado epidermoide blanco aparecerá hiperintenso en T1 e hipointenso en T2.
El tratamiento de elección es la excisión quirúrgica,
aunque a veces es difícil ya que puede rodear vasos y nervios.
La recurrencia no es infrecuente,
con un crecimiento lento durante años,
sin sintomatología [71].