Material y métodos:
Estudio retrospectivo observacional que incluye todos los pacientes con lesiones pulmonares en los que se practicó punción aguja fina (PAF) o biopsia aguja gruesa (BAG) desde 1 de marzo de 2012 hasta 30 de septiembre de 2013.
Todos los pacientes disponían de un estudio previo de TC que sirvió para planificar la punción.
A todos los pacientes se les explicó en que consistía el procedimiento que se iba a realizar y se les entregó el consentimiento informado.
Todas las punciones fueron realizadas por un radiólogo intervencionista con 7 años de experiencia en la realización de estos procedimientos.
Todos los pacientes presentaban monitorización mediante pulsioxímetro de la frecuencia cardíaca y saturación de oxígeno.
Cuando las lesiones no contactaban con la pared torácica se empleó la TC o el fluoro-TC como técnica de imagen para guiar la punción.
El equipo de TC empleado era un Toshiba Aquilion (Toshiba Medical Systems Corporation.
Asian.
Otawara-Shi.
Tochig),
con capacidad para realizar fluoro-TC en los casos que fue necesario.
El paciente se colocó en decúbito supino,
prono o decúbito lateral derecho o izquierdo,
según la localización de la lesión que era conocida por el estudio de TC previo.
Se realizó un escanograma torácico con estos parámetros 120 Kv y 50 mA.
Los planos de corte se centraron en la región anatómica donde se localizaba la lesión con los siguientes parámetros 120 Kv,
mA variable según el grosor del paciente,
rot time 0,5; grosor de reconstrucción 5 mm con intervalos de 5 mm.
En los casos en los que se tuvo que emplear la fluoroscopia también se centró en la región anatómica donde se localizaba la lesión,
y se empleó fluoroscopia pulsada para irradiar menos tanto al paciente como a la persona que realizaba la punción (Fig. 1 y Fig. 2 Fig. 2).
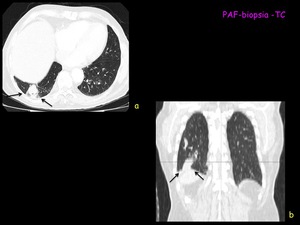
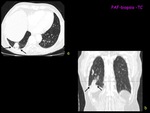
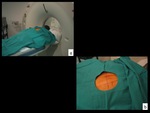
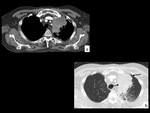
Fig. 1: Figura 1. TC torácica con contraste i.v. con ventana de parénquima pulmonar plano axial (a) y reconstrucción coronal (b) que muestra una lesión nodular sólida, sospechosa de malignidad localizada en segmento basal posterior de lóbulo inferior derecho (flechas negras). Este TC nos sirve para planificar la punción: decidir técnica de imagen y posición del paciente.
Figura 1.
TC torácica con contraste i.v.
con ventana de parénquima pulmonar plano axial (a) y reconstrucción coronal (b) que muestra una lesión nodular sólida,
sospechosa de malignidad localizada en segmento basal posterior de lóbulo inferior derecho (flechas negras).
Este TC nos sirve para planificar la punción: decidir técnica de imagen y posición del paciente.
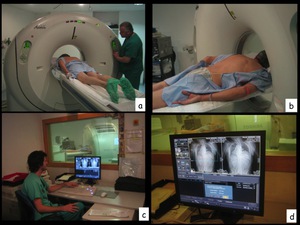
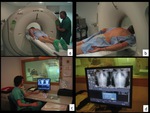
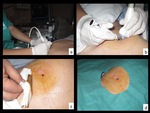
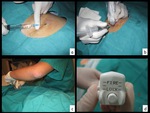
Fig. 2: Figura 2. Planificación de la punción. El paciente es colocado en decúbito prono (a,b) dada la localización de la lesión. Realizamos el escanograma (c) y sobre dicho escanograma centramos los planos de corte (d) según la localización de la lesión conocida por el TC previo.
Figura 2.
Planificación de la punción.
El paciente es colocado en decúbito prono (a,b) dada la localización de la lesión.
Realizamos el escanograma (c) y sobre dicho escanograma centramos los planos de corte (d) según la localización de la lesión conocida por el TC previo.
Se eligió el plano más adecuado para la punción evitando estructuras óseas y vasculares interpuestas en el trayecto de la aguja,
obteniendo así la primera coordenada para la punción de la lesión.
Una vez elegido dicho plano,
se colocaron unas marcas radiopacas (tira de agujas) sobre la piel del paciente las cuales sirvieron para determinar si la aguja debía entrar más medial o más lateral,
es decir nos daban la segunda coordenada para puncionar la lesión.
Una vez elegida la segunda coordenada se marcó el punto de entrada sobre la piel del paciente.
Se midió la distancia desde dicho punto de la piel hasta la pleura y desde dicho punto hasta la lesión.
Se pintó la zona con povidona yodada (Betadine®).
Se cubrió la zona con paños verdes estériles,
delimitando el campo quirúrgico (Fig. 3, Fig. 4 y Fig. 5).
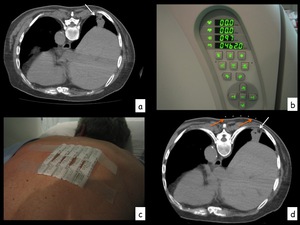
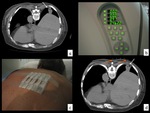
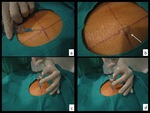
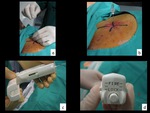
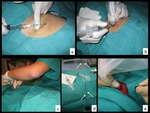
Fig. 3: Figura 3. Corte axial de TC torácico (a) que muestra el plano elegido para punción de la lesión (flecha). Con los mandos de la TC (b) se lleva al paciente al plano deseado y se coloca unas marcas radiopacas sobre la piel del paciente (c). Se repiten los cortes de TC (d) con las marcas radiopacas (flechas naranjas) que nos determinan la segunda coordenada para entrar en la lesión (flecha blanca).
Figura 3.
Corte axial de TC torácico (a) que muestra el plano elegido para punción de la lesión (flecha).
Con los mandos de la TC (b) se lleva al paciente al plano deseado y se coloca unas marcas radiopacas sobre la piel del paciente (c).
Se repiten los cortes de TC (d) con las marcas radiopacas (flechas naranjas) que nos determinan la segunda coordenada para entrar en la lesión (flecha blanca).
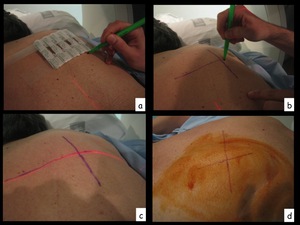
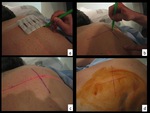
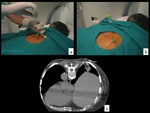
Fig. 4: Figura 4. Teniendo como referencia las marcas radiopacas (a), trazamos esta coordenada y la obtenida por el plano de TC previamente elegido (b,c). Se dibuja el punto sobre la piel del paciente y se pinta con povidona yodada.
Figura 4.
Teniendo como referencia las marcas radiopacas (a),
trazamos esta coordenada y la obtenida por el plano de TC previamente elegido (b,c).
Se dibuja el punto sobre la piel del paciente y se pinta con povidona yodada.
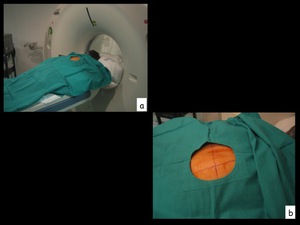
Fig. 5: Figura 5. Se colocan paños verdes estériles sobre el paciente para delimitar la zona de punción. Detalle de la zona de punción (b).
Figura 5.
Se colocan paños verdes estériles sobre el paciente para delimitar la zona de punción.
Detalle de la zona de punción (b).
Se administró anestésico local,
mepivacaína al 2% (Mepivacaína Braun 2%®),
realizando en primer lugar un habón intradérmico con una aguja subcutánea,
y posteriormente con una aguja intramuscular se fue anestesiando en profundidad,
sin llegar a tocar la pleura; dicha distancia la conocíamos por la medida efectuada previamente (Fig. 6).
Tras la anestesia se procedió a realizar la punción: PAF o BAG.
La aguja de PAF era una aguja tipo Chiba de 22G,
Biopsybell Srl (Via Lea Cazzuoli,
14/16,41037 Mirandola Modena,
Italia),
con marcas centimetradas y con una longitud de 100-150 mm según profundidad lesión.
Se introdujo la aguja con una profundidad variable según la distancia calculada desde la piel hasta la lesión,
ayudándonos de las marcas centimetradas que dispone la aguja.
Se comprobó el posicionamiento de la aguja,
y en caso de no estar en la lesión se corrigió el trayecto de la aguja o se profundizó la aguja hasta alcanzar la lesión.
Una vez en la lesión,
se extrajo el fiador metálico de la aguja y se realizaron movimientos repetidos de avance-retirada de la aguja de unos milímetros,
para conseguir que por capilaridad alguna célula se introdujese en la aguja de punción.
No se realizó aspiración para que la muestra fuese lo menos hemática posible (Fig. 7).
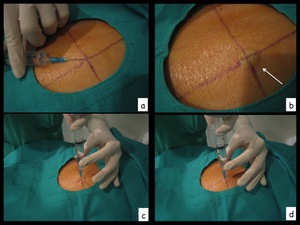
Fig. 6: Figura 6. Distintos momentos durante la anestesia local. Nótese el habón epidérmico realizado (flecha en b).
Figura 6.
Distintos momentos durante la anestesia local.
Nótese el habón epidérmico realizado (flecha en b).
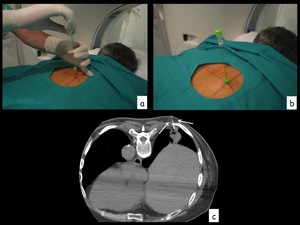
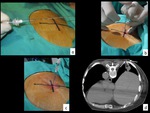
Fig. 7: Figura 7. Se introduce la aguja de punción a la profundidad que se ha calculado previamente en el plano de TC elegido para la punción, midiendo la distancia desde la piel a la pleura, y desde la piel a la lesión. Se realiza un comprobación del posicionamiento de la aguja ( flechas en c) y en caso de ser necesario se reposiciona o avanza más la aguja.
Figura 7.
Se introduce la aguja de punción a la profundidad que se ha calculado previamente en el plano de TC elegido para la punción,
midiendo la distancia desde la piel a la pleura,
y desde la piel a la lesión.
Se realiza un comprobación del posicionamiento de la aguja ( flechas en c) y en caso de ser necesario se reposiciona o avanza más la aguja.
La muestra se depositó sobre un porta,
y el anatomopatólogo,
presente en la punción,
realizó la extensión y tinción de la muestra.
En pocos minutos el anatomopatólogo indicaba si la muestra era válida o no para el diagnóstico.
En el caso de no ser válida para el diagnóstico se realizó otra punción de la lesión con la técnica descrita anteriormente hasta conseguir una muestra válida para el diagnóstico,
o si aparecía alguna complicación se detenía el procedimiento (Fig. 8).

Fig. 8: Figura 8. Tras la extensión de la muestra (a,b) se realiza una tinción rápida (c) y se mira la muestra al microscopio (d).
Figura 8.
Tras la extensión de la muestra (a,b) se realiza una tinción rápida (c) y se mira la muestra al microscopio (d).
En el caso de optar por realizar una BAG,
se realizaron los mismos pasos preliminares que en el caso de la PAF,
pero en el momento de introducir la aguja de punción se cambió la aguja de PAF por una aguja localizadora-coaxial con las siguientes características: aguja de 18-20G TSK aguja co-axial para Acecut (TSK Laboratory,
Europe,
Molenstraat 15,
2513 BH The Hague,
The Netherlands).
Se realizó una comprobación del posicionamiento de dicha aguja,
y en caso de ser necesario se corrigió el trayecto de la aguja o se profundizó la aguja hasta alcanzar la lesión (Fig. 9).
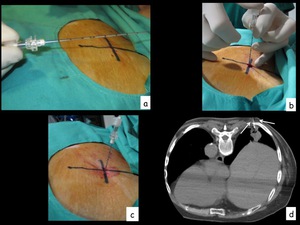
Fig. 9: Figura 9. Se coloca la aguja localizadora-coaxial con marcas centimetradas que se introduce según la profundidad calculada previamente en el plano de TC elegido para la punción, midiendo la distancia desde la piel a la pleura, y desde la piel a la lesión (a,b,c) y se realiza una comprobación del posicionamiento de la aguja (flechas en d) y en caso de ser necesario se reposiciona o avanza más la aguja.
Figura 9.
Se coloca la aguja localizadora-coaxial con marcas centimetradas que se introduce según la profundidad calculada previamente en el plano de TC elegido para la punción,
midiendo la distancia desde la piel a la pleura,
y desde la piel a la lesión (a,b,c) y se realiza una comprobación del posicionamiento de la aguja (flechas en d) y en caso de ser necesario se reposiciona o avanza más la aguja.
Una vez alcanzada la lesión,
se extrajo el fiador metálico de la aguja y a través de dicha aguja se introdujo la aguja de BAG.
La aguja para la BAG era una aguja de 18-20G,
Acecut de TSK (TSK Laboratory,
Europe,
Molenstraat 15,
2513 BH The Hague,
The Netherlands) y con una longitud 115-150 mm según la profundidad de la lesión.
En caso de que visualmente nos pareciese un cilindro de mala calidad,
se fragmentase o no hubiese cilindro por haber puncionado en una zona de necrosis tumoral,
se realizó una nueva punción con la técnica anteriormente descrita (Fig. 10 y Fig. 11).
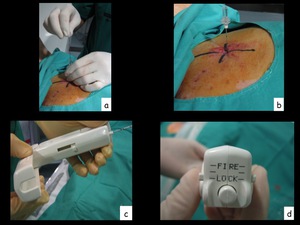
Fig. 10: Figura 10. Tras comprobar el correcto posicionamiento de la aguja localizadora-coaxial se retira del fiador metálico (a,b) y se procede colocar de forma coaxial la aguja de biopsia. Detalles de la aguja de biopsia (c,d).
Figura 10.
Tras comprobar el correcto posicionamiento de la aguja localizadora-coaxial se retira del fiador metálico (a,b) y se procede colocar de forma coaxial la aguja de biopsia.
Detalles de la aguja de biopsia (c,d).
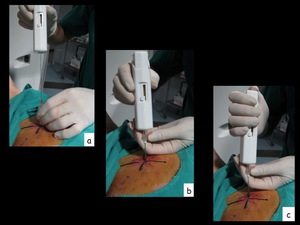
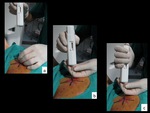
Fig. 11: Figura 11. Distintos momentos durante la introducción de la aguja de biopsia a través de la aguja localizadora-coaxial.
Figura 11.
Distintos momentos durante la introducción de la aguja de biopsia a través de la aguja localizadora-coaxial.
La muestra obtenida se introdujo en un bote con formaldehido.
En el caso de la realización de BAG no estaba el patólogo presente para validar la muestra dado que se obtenía un cilindro (Fig. 12).
Tras la finalización de la punción (PAF o BAG),
se realizó un control por TC para descartar complicaciones: neumotórax o hemorragia alveolar.
Se realizó un informe escrito con el procedimiento realizado,
número de pases efectuados y si habían existido complicaciones o no,
describiendo tipo de complicación y manejo de la misma (Fig. 13).
En el caso de presentar neumotórax se dejó al paciente incorporado en la cama y se administró oxígeno en gafas nasales a 3 litros/minuto,
se comprobó el grado de saturación de oxígeno y si presentaba dolor torácico o no.
Se comunicó telefónicamente la complicación al médico solicitante de la punción.
En el caso de presentar hemorragia alveolar visualizada en el TC de control,
se valoró la extensión de la misma y se comentó al paciente que podría presentar esputos hemoptoicos.
Se valoró la saturación de oxígeno y si el paciente refería disnea.
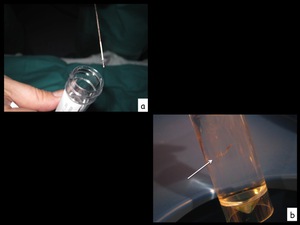
Fig. 12: Figura 12. La muestra obtenida se introduce en un bote con formaldehido. Nótese cilindro obtenido en el bote de formaldehido (flecha blanca en b).
Figura 12.
La muestra obtenida se introduce en un bote con formaldehido.
Nótese cilindro obtenido en el bote de formaldehido (flecha blanca en b).
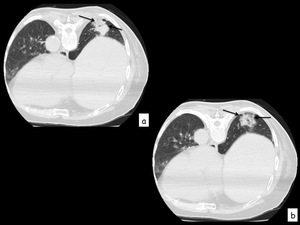
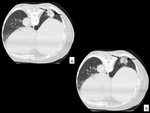
Fig. 13: Figura 13. TC de control tras finalizar la punción, se observa área de “vidrio deslustrado” alrededor de la lesión puncionada (flechas en a y b) en relación a hemorragia alveolar.
Figura 13.
TC de control tras finalizar la punción,
se observa área de “vidrio deslustrado” alrededor de la lesión puncionada (flechas en a y b) en relación a hemorragia alveolar.
Cuando las lesiones contactaban con la pared torácica se empleó la ecografía como técnica de imagen para guiar la punción (Fig. 14).
El ecógrafo empleado para la punción era un General Electric Healthcare LOGIQ P6 (GE Healthcare,
Fairfield,
Connecticut,
US).
Se empleó una sonda cónvex multifrecuencia de 4-5,5 MHz.
Se realizó un estudio en modo B para localizar la lesión,
así como una valoración con Doppler color para determinar la existencia de vasos de gran tamaño en la lesión o en vecindad y evitar la punción de los mismos en el trayecto de la aguja.
Se determinó el punto de entrada hasta la lesión y se marcó un punto sobre la piel del paciente.
Se pintó la zona con povidona yodada (Betadine®).
Se cubrió la zona con paños verdes estériles,
delimitando el campo quirúrgico (Fig. 15).
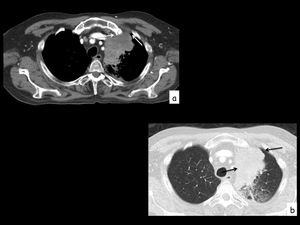
Fig. 14: Figura 14. TC torácica tras administración de contraste i.v., plano axial, ventana de mediastino (a) y de parénquima pulmonar (b) que muestra una masa de lóbulo superior izquierdo que contacta con la pared torácica anterior (flechas) lo que permite su visualización con ecografía y punción de la misma con dicha técnica.
Figura 14.
TC torácica tras administración de contraste i.v.,
plano axial,
ventana de mediastino (a) y de parénquima pulmonar (b) que muestra una masa de lóbulo superior izquierdo que contacta con la pared torácica anterior (flechas) lo que permite su visualización con ecografía y punción de la misma con dicha técnica.
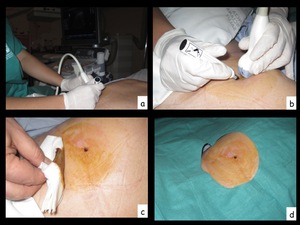
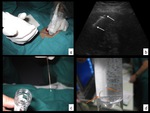
Fig. 15: Figura 15. Mediante ecografía se localiza la lesión (a) y se determina el punto de entrada para la punción en el que no existan estructuras óseas interpuestas y evitando puncionar grandes vasos. Se marca el punto sobre la piel del paciente (b), se pinta con povidona yodada (c) y se cubre con paños estériles (d) delimitando el campo estéril.
Figura 15.
Mediante ecografía se localiza la lesión (a) y se determina el punto de entrada para la punción en el que no existan estructuras óseas interpuestas y evitando puncionar grandes vasos.
Se marca el punto sobre la piel del paciente (b),
se pinta con povidona yodada (c) y se cubre con paños estériles (d) delimitando el campo estéril.
Se vistió la sonda del ecógrafo con una funda estéril (Fig. 16).
Se administró anestésico local,
mepivacaína al 2% (Mepivacaína Braun 2%®),
realizando en primer lugar un habón intradérmico con una aguja subcutánea,
y posteriormente con una aguja intramuscular se fue anestesiando en profundidad.
El trayecto de la aguja intramuscular fue controlado ecográficamente,
visualizando en tiempo real el avance y posicionamiento de la aguja ( Fig.
17).
Posteriormente se realizó bien PAF o BAG con las agujas ya mencionadas anteriormente.
En el caso de realizar PAF la aguja empleada era la descrita anteriormente para la punción por TC.
El avance de la aguja hasta la lesión fue controlado en tiempo real,
y una vez en la lesión,
se realizó el procedimiento descrito anteriormente de extracción del fiador metálico,
no aspirar,
introducir y sacar la aguja de punción y validación de la muestra inmediatamente por el anatomopatólogo.
En el caso de no ser válida para el diagnóstico se realizó otra punción de la lesión con la técnica descrita anteriormente hasta conseguir una muestra válida para el diagnóstico (Fig. 18,
Fig. 19 y Fig. 20).
Fig.
17).
Posteriormente se realizó bien PAF o BAG con las agujas ya mencionadas anteriormente.
En el caso de realizar PAF la aguja empleada era la descrita anteriormente para la punción por TC.
El avance de la aguja hasta la lesión fue controlado en tiempo real,
y una vez en la lesión,
se realizó el procedimiento descrito anteriormente de extracción del fiador metálico,
no aspirar,
introducir y sacar la aguja de punción y validación de la muestra inmediatamente por el anatomopatólogo.
En el caso de no ser válida para el diagnóstico se realizó otra punción de la lesión con la técnica descrita anteriormente hasta conseguir una muestra válida para el diagnóstico (Fig. 18,
Fig. 19 y Fig. 20).
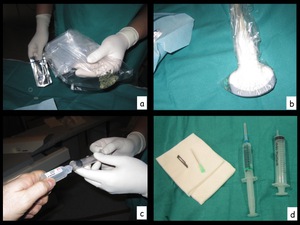
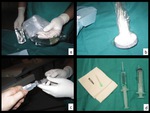
Fig. 16: Figura 16. La sonda del ecógrafo se viste con una funda estéril (a,b). Se carga la anestesia (c,d).
Figura 16.
La sonda del ecógrafo se viste con una funda estéril (a,b).
Se carga la anestesia (c,d).
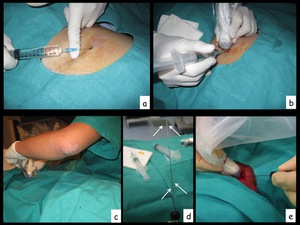
Fig. 17: Figura 17. Momentos de la anestesia local (a,b,c). Detalle de la aguja de PAF (d). El avance de la aguja de PAF hacia la lesión es controlado ecográficamente (e).
Figura 17.
Momentos de la anestesia local (a,b,c).
Detalle de la aguja de PAF (d).
El avance de la aguja de PAF hacia la lesión es controlado ecográficamente (e).

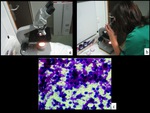
Fig. 18: Figura 18. Microscopio y botes para realizar la tinción rápida (a). La muestra (flechas en b) es depositada sobre el porta, y posteriormente extendida (flechas en c). Una vez extendida, se introduce en alcohol para fijar la muestra (d).
Figura 18.
Microscopio y botes para realizar la tinción rápida (a).
La muestra (flechas en b) es depositada sobre el porta,
y posteriormente extendida (flechas en c).
Una vez extendida,
se introduce en alcohol para fijar la muestra (d).

Fig. 19: Figura 19. Distintos momentos de la tinción de la muestra (a,b) y lavado de la misma con agua (c). Visión macroscópica de la muestra tras el teñido y lavado (flechas en d).
Figura 19.
Distintos momentos de la tinción de la muestra (a,b) y lavado de la misma con agua (c).
Visión macroscópica de la muestra tras el teñido y lavado (flechas en d).
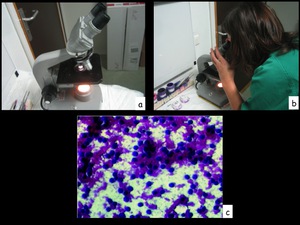
Fig. 20: Figura 20. La muestra es validada por el patólogo en el microscopio (a,b). Detalle de la muestra citológica (c).
Figura 20.
La muestra es validada por el patólogo en el microscopio (a,b).
Detalle de la muestra citológica (c).
En el caso de realizar BAG la aguja empleada era la descrita anteriormente para la guía por TC,
pero en este caso el calibre de la aguja variaba de 16-20G.
Con esta guía de imagen no se empleó la aguja localizadora-coaxial.
El avance de la aguja hasta la lesión fue controlado en tiempo real,
y una vez en la lesión,
se quitó el seguro de disparo del dispositivo y se obtuvo una muestra.
En caso de que visualmente nos pareciese un cilindro de mala calidad,
se fragmentase o no hubiese cilindro por haber puncionado en una zona de necrosis tumoral,
se realizó una nueva punción con la técnica anteriormente descrita.
La muestra obtenida se introdujo en un bote con formaldehido (Fig. 21 y Fig. 22).
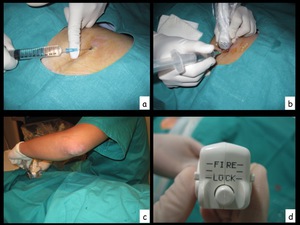
Fig. 21: Figura 21. Distintos momentos en la realización de la biopsia. Infiltrando la anestesia (a,b,c). Detalle de la aguja de biopsia (d).
Figura 21.
Distintos momentos en la realización de la biopsia.
Infiltrando la anestesia (a,b,c).
Detalle de la aguja de biopsia (d).
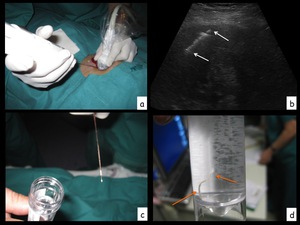
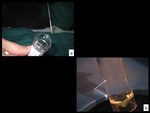
Fig. 22: Figura 22. La aguja de biopsia es dirigida a la lesión mediante control ecográfico (a). Visión ecográfica (b) de la localización de la aguja de biopsia en la lesión (flechas en b). El cilindro obtenido se introduce en un bote con formaldehido (c). Detalle del cilindro (flechas en d) en el bote con formaldehido.
Figura 22.
La aguja de biopsia es dirigida a la lesión mediante control ecográfico (a).
Visión ecográfica (b) de la localización de la aguja de biopsia en la lesión (flechas en b).
El cilindro obtenido se introduce en un bote con formaldehido (c).
Detalle del cilindro (flechas en d) en el bote con formaldehido.
Todos los pacientes que se puncionaron,
independientemente de la técnica de imagen empleada y de la realización de PAF o BAG,
se quedaron ingresados 24 horas.
A todos los pacientes se les realizó una Rx de tórax de control por la tarde para descartar complicaciones.
En caso de no existir complicaciones el día siguiente de la prueba se daba el alta a los pacientes.
En caso de existir alguna complicación,
el paciente quedaba ingresado hasta la resolución de la complicación.
Se valoraron los siguientes parámetros: sexo,
edad medida en años,
localización de la lesión,
guía de imagen empleada para la punción,
tipo de punción realizada (PAF-BAG),
diámetro máximo de la lesión,
distancia desde la pleura hasta la lesión,
posición del paciente para realizar la punción,
número de pases realizados,
calibre de la aguja,
complicaciones en cada técnica,
rentabilidad diagnóstica y diagnóstico histológico.
El estudio estadístico se realizó con un paquete estadístico para Ciencias Sociales (SPSS) software estadístico (SPSS v.19.0,
SPSS Inc.,
Chicago,
IL,
EE.UU.).
Realizamos un análisis descriptivo de la media,
mediana y desviación estándar de las distintas variables y empleamos el Chi-cuadro como prueba paramétrica para el contraste de hipótesis.
Se consideró como un resultado estadísticamente significativo un valor de p ≤ 0,05.