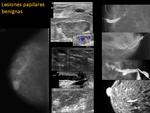
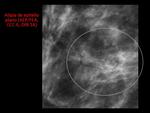
1- Lesiones papilares benignas:
Los papilomas pueden ser:
a)-Solitarios:
Normalmente tiene localización central o retroareolar .
Si se asocian a síntomas: suele ser a secreción.
La mayoría son benignos.
b)-Múltiples:
Son menos frecuentes,
y normalmente son de localización periférica.
Es más rara su asociación a secreción; típicamente se presentan como masa palpable.
Normalmente están asociados con atipia,
CDIS o cáncer invasivo.
-Mamografía:
Los pequeños: pueden estar ocultos; los mayores suelen apreciarse como masa ovalada bien definida.
La esclerosis o el infarto puede causar distorsión.
Un 25% presentan calcificaciones asociadas (groseras o microcalcificaciones),
las cuales a veces son el único hallazgo mamográfico.
-Ecografía:
Pueden ser nódulos bien definidos hipoecoicos ,
o nódulos con base mural dentro de un ducto dilatado (quiste complejo),
o un ducto dilatado no anecoico .
Con el empleo de doppler color: se demuestra casi siempre flujo,
por ser lesiones muy hipervasculares.
-Galactografía:
Pueden verse como un defecto de repleción con base mural con contornos lisos o lobulados o como un stop en el ducto.
-RM:
Es una técnica muy sensible para lesiones papilares.
Se manifiestan como nódulos que realzan con o sin componente intraductal (realce uniforme o irregular,
con “washout “o plató”,
siendo difícil la diferenciación con carcinoma invasivo).
Es muy útil para evaluación de pacientes con múltiples lesiones papilares: para planificación de tratamiento preoperatorio (escisión quirúrgica amplia) o para detectar lesiones que no han sido detectadas ecográficamente.
Puede ayudar a ver la extensión del CDIS asociado si lo tiene.
La RM es útil cuando hay descarga por pezón con mamografía o ecografía normales,
porque ayuda a excluir malignidad (VPN 98%: ausencia de realce ayuda a excluir malignidad).
Los hallazgos radiológicos no permiten diferenciar lesiones papilares benignas de malignas .
Fig. 3
Cuando se valora la infraestimación de malignidad en la literatura tras un diagnóstico por BAG (biopsia con aguja gruesa) previo de lesión papilar benigna,
se encuentra que varía entre un 0-25%,
con una media de un 9,8% (si hay atipia asociada,
asciende a valores entre un 22-67%).
Fig. 4
Fig. 5
Por ello,
las rcomendaciones tras diagnóstico por BAG de lesión papilar benigna serían:
Fig. 6
Pero si el diagnóstico de lesión papilar benigna es mediante BAV (biopsia asistida por vacío),
o si a lesiones diagnosticadas por PAAF o BAG se les realiza extirpación mediante BAV (VAE) y seguimiento,
el grado de infraestimación de malignidad disminuye drásticamente, a valores cercanos al 0% (entre 0-5%).
Fig. 7
Fig. 8
En algunos trabajos,
encontramos indicación de una serie de criterios para extirpación de papilomas (ej: Ko-12):
Fig. 9
Así pues,
si el diagnóstico de lesión papilar benigna es mediante BAV o si se ha extirpado una lesión papilar benigna con BAV tras su diagnóstico por PAAF o BAG y estamos seguros de que hemos extirpado por imagen toda la lesión,
la BAV y el seguimiento posterior sería una alternativa a la exéresis quirúrgica (hay que tener en cuenta los criterios de selección descritos en la literatura que se han reseñado,
y no olvidar especialmente que los mayores de 1,5 cm y periféricos se asocian con mayor frecuencia a malignidad y quizá deban ser subsidiarios de exéresis quirúrgica directa por ello):
Fig. 10
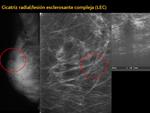
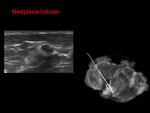
2- Cicatriz radial/Lesión esclerosante compleja:
Lesión estrellada con área central estromal elastótica que contiene ductos benignos atrapados y cuyo diagnóstico diferencial con neoplasias es a veces difícil.
Se denomina cicatriz radial si mide < o = 1 cm ,
y lesión esclerosante compleja si mide > 1cm.
-Mamografía:
Se manifiesta como una distorsión de la arquitectura con espículas elongadas (con centro radiodenso o radiotransparente,
hallazgo éste último no específico,
con o sin microcalcificaciones asociadas).
También puede manifestarse como microcalcificaciones (aunque es más frecuente verlas microscópicamente que en la mamografía; su frecuencia es variable del 11-64%).
-Ecografía:
Se manifiesta como un área/masa hipoecoica mal definida que puede exhibir mala transmisión acústica posterior,
o una distorsión arquitectural.
Hasta 1/3 no tiene traducción ecográfica.
En torno a un 8% se ven solo por ecografía.
Si vemos una distorsión arquitectural,
no hay signos que orienten a malignidad.
-RM:
La mayoría tienen un realce pequeño o retardado (aunque hay excepciones).
Existe “solapamiento” con CDIS y carcinoma tubular,
que pueden exhibir ausencia de realce ,
o realce lento o retardado.
La sensibilidad y especificidad rondan el 85%: no es posible excluir malignidad.
Fig. 11
Si el diagnóstico por biopsia percutánea de LEC es mediante BAG,
la infraestimación de malignidad tras la posterior exéresis quirúrgica oscila entre un 0-40%,
con una media de un 8,3% (Bianchi-12: artículo de revisión de la literatura,
con resultado resultado propio muy similar a la media,
de un 8,2%).
Cuando hay atipia asociada,
la infraestimación asciende drásticamente (24-37%).
Pero si el diagnóstico es mediante BAV o si se extirpan con BAV lesiones diagnosticadas por BAG,
disminuye drásticamente la infraestimación a valores cercanos al 0-5%.
De manera,
que puede concluirse que si tenemos la seguridad de poder extraer toda la lesión por imagen mediante BAV,
la exéresis mediante BAV y el seguimiento es una alternativa a la exéresis quirúrgica.
Ello tiene mayor probabilidad de ser factible cuando la lesión mide menos de 1 cm (Rajan -12).
Hay que recordar que si hay cáncer asociado,
éste suele encontrarse en la periferia de la lesión,
y a veces solo constituye un 5% de la lesión global.
Fig. 12
Fig. 13
Fig. 14
Fig. 15
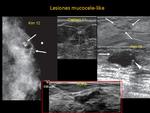
3- Lesiones “Mucocele-Like” (LML):
Lesión rara,
descrita por primera vez por Rosen.
Se definen como quistes que contienen mucina delimitados por epitelio plano o cuboidal,
con extravasación de mucina al estroma circundante.
Pueden tener alteraciones epiteliales acompañantes que van desde cambios de células columnares (CCL),
a hiperplasia ductal atípica (HDA) a carcinoma ductal in situ (CDIS) o mucinoso,
o a invasivo.
-Mamografía:
Se manifiestan más frecuentemente como microcalcificaciones,
y menos frecuentemente como masas (sin o con calcificaciones).
-Ecografía:
Hay algo de disparidad respecto a las características de presentación en ecografía y su frecuencia :
*Carkaci -11 habla de presentación más frecuente como:
-Masa (asociada o no a microcalcificaciones):
Redondeada u oval,
bien definida (si es LML)
Si bordes mal definidos/irregulares (si es LML asociada a CDIS)
-Quiste complejo
*Kim-12 habla de presentación más frecuente como:
-Quiste simple,
quiste complicado o quiste con septos finos (si es LML)
-Quistes en racimos,
con septos gruesos o complejos (si es LML asociado a malignidad).
Fig. 16
Si el diagnóstico por biopsia percutánea de LML es mediante BAG,
la infraestimación de malignidad tras la posterior exéresis quirúrgica es bastante baja,
de un 3,77% (Rakha-13: artículo de revisión de la literatura,
con resultado propio de infraestimación muy similar a la media,
de un 3,7%).
Cuando hay atipia asociada,
la infraestimación asciende drásticamente (21%).
Si se extirpa toda la lesión con BAV se puede evitar la cirugía en lesiones benignas (y parece una alternativa razonable),
decidido bajo comité-discusión multidisciplinario (Begum-09,
Ouldamer-10).
Fig. 17
Fig. 18
Fig. 19
4- Tumor Filodes (TF):
Tumor raro fibroepitelial mamario (1%) que según la clasificación (OMS) podemos dividir en: Benigno-TFB,
borderline-TFb,
maligno-TFM (en función de características como: márgenes –“interface”-,
crecimiento estromal -celularidad estromal-,
necrosis tumoral,
atipia celular y número de mitosis por campo).
Puede recurrir localmente entre un 8-40% de los casos (media 15%) y dar metástasis a distancia entre un 1-21% (media 10%).
La etiología exacta/relación con fibroadenoma no está clara (no claro si se origina de un fibroadenoma o si es un tumor totalmente distinto).
Habría varias teorías :
1-Una mutación somática resulta en una proliferación monoclonal con propensión a la recurrencia local y progresión a tumor filodes (la mayoría de los fibroadenomas tienen elementos policlonales y deberían considerarse como lesiones hiperplásicas más que neoplásicas).
2-Inducción estromal por factores de crecimiento producidos por el epitelio de la mama (trauma,
lactancia,
embarazo y aumento de la actividad estrogénica se han implicado como factores estimulantes del crecimiento).
Suele darse en pacientes entre 35-55 a (más tarde que el fibroadenoma),
con un tamaño medio 3-4 cm,
y se caracterizan por un rápido crecimiento.
El tratamiento recomendado es la excisión local amplia incluyendo > o = 1 cm de tejido normal a su alrededor.
-Mamografía:
Suele manifestarse como una masa lobulada oval o redonda,
bien definida ,
de alta densidad,
sin calcificaciones (raramente calcificado).
-Ecografía:
Se presenta como una masa lobulada (a veces oval o redonda) bien circunscrita con márgenes lisos,
hipoecogénica,
halo ecogénico ,
de ecoestructura heterogénea: áreas quísticas ,
hendiduras (no específico).
Sugieren malignidad: bordes irregulares,
hipoecogenidad,
sombra posterior, ecoestructura heterogénea,
y en doppler: aumento IR /IP/pico Vmáx (IR= índice de resistencia; IP= índice de pulsatilidad; pico Vmáx= pico de velocidad máxima).
Elastografía:
Podemos observar el “Ring Sign”: patrón elástico bastante específico,
con centro elástico y límtes externos inelásticos (efecto compresivo por rápido crecimiento: anillo inelástico).
-RM:
Son nódulos redondos o lobulados,
márgenes bien definidos,
hipointensos en T1,
hiperintensos en T2,
con estructura interna heterogénea.
Patrón realce: TFB (inicio lento-retardada persistente); TFM (inicio rápido-retardada plató o “washout”).
En un trabajo de Yabuchi-06 se describen una serie de hallazgos que se correlacionan significativamente con el grado histológico del TF,
así, describe como hallazgos de RM sugestivos de malignidad:
-Cambios quísticos con pared irregular
-Señal menor o igual al parénquima en T2
-Disminución del valor ADC
-Mayor señal que el tejido en T1
Fig. 20
Pero no es posible discriminar muchas veces por técnicas de imagen entre fibradenoma y TF,
e incluso,
aunque hay muchos trabajos que indican que hay muy buenos datos de concordancia,
sensibilidad y VPP tras la BAG para diagnóstico de TF,
hay algunos casos en que los patólogos tras la BAG no pueden llegar a definirse entre fibroadenoma y TF.
Ante un diagnóstico por BAG de TF,
lo aceptado es la exéresis quirúrgica del nódulo con un margen de 1 cm de tejido normal a su alrededor.
Si en la cirugía no está incluído ese cm de tejido normal alrededor,
en principio debe realizarse nueva cirugía (porque las recurrencias se relacionan con cirugía insuficiente del tumor primario).
Pero si estamos ante uno de esos casos en que el patólogo no puede diferenciar entre fibroadenoma y TFB,
existen 2 alternativas: o ir a la exéresis quirúrgica directamente,
o bien a la extirpación mediante BAV (de manera que habremos ahorrado muchas cirugías si finalmente es un fbroadenoma,
y se podrá realizar una posterior exéresis quirúrgica del lecho si se trataba de un TFB).
Incluso si se trata de esta segunda posibilidad (que resulta ser un TFB) hay un trabajo de Park-12 donde este autor concluye que tras extirpación por BAV de TFB es suficiente seguimiento a la alternativa de inmediata escisión quirúrgica extensa local,
porque obtiene unos valores de recurrencia local de un 3,2 % en el seguimiento (dato que es igual o incluso menor que las recidivas tras la escisión quirúrgica,
que es de un 4%).
Fig. 21
5- Atipia de epitelio plano (AEP/FEA,
CCC A,
DIN 1A):
Agrandamiento de las unidades ductolobulares terminales en las cuales hay reemplazamiento de las células nativas epiteliales por una o varias (3 a 5) capas de células que muestran bajo grado de atipia citológica.
La atipia citológica la distingue de los cambios de hiperplasia de células columnares (HCC),
y la ausencia de distorsión arquitectural del carcinoma ductal in situ (CDIS).
-Mamografía:
Suele manifestarse como microcalcificaciones (generalmente amorfas,
a veces heterogéneas,
o pleomórficas).
-Ecografía:
Es raro que tenga representación ecografica (está descrito en algunos casos pequeña masa).
Fig. 22
Parece que es un marcador de riesgo ( riesgo 2 veces mayor) y un posible precursor de malignidad.
Datos derivados de investigaciones genéticas,
IHQ y moleculares han mostrado que probablemente FEA representa la lesión más precoz reconocible en la progresión del CDIS y un precursor no obligado del carcinoma invasivo (CI) de bajo grado.
Está bien establecida la coexistencia de FEA con carcinoma tubular (CT),
hiperplasia ductal atípica (HDA),
neoplasia lobular (NL) y CDIS.
Hay debate en la literatura respecto al manejo tras un diagnóstico de FEA por biopsia percutanea: cirugía ? vs seguimiento?:
La infraestimación de malignidad en la literatura tras un diagnóstico por biopsia percutánea de FEA es del 17% con BAG y del 12% con BAV (Verschuur-Maes 12: artículo de revisión de la literatura,
con resultado propio cercano a la media,
de un 9%).
Algunos artículos revisados posteriores a él van en la misma línea (infraestimación entre un 6-15%).
Con esa media de infraestimación,
la mayoría de trabajos recomiendan exéresis quirúrgica.
Fig. 23
Fig. 24
Reseñar que entre esos trabajos,
en alguno (Bianchi-13) se indica que a pesar extracción de todas las microcalcificaciones en la BAV diagnóstica,
sigue habiendo infraestimación ( en torno a un 4%),
o que si hay asociación a otra lesión B3b aumenta la infraestimación y en uno de ellos (Rajan-11) se propone la extirapción por BAV en segunda línea como alternativa a la exéresis quirúrgica con similares resultados.
Pero encontramos también algunos trabajos (menor número) que son partidarios del seguimiento por sus bajas tasas de infraestimación.
Fig. 25
En resumen,
aunque no hay consenso absoluto,
la mayoría de trabajos recomiendan exéresis quirúrgica ante diagnóstico por biopsia percutánea de FEA.
Podríamos hablar de “una zona de penumbra” donde la alternativa del seguimiento estricto según resultados de algunos trabajos podría ser una actitud razonable debido al bajo grado de infraestimación de malignidad (p ej especialmente si se ha realizado BAV con aguja de gran calibre con gran muestreo extrayendo toda la lesión con buena correlación ante lesiones de pequeño tamaño sin otras lesiones de riesgo asociadas…).
Fig. 26
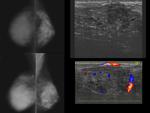
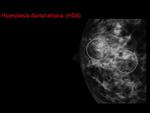
6- Hiperplasia ductal atípica (HDA):
Lesión hiperplásica que tiene atipia celular y rigidez estructural como el CDIS ,
pero afectando solo parte del ducto. Es una lesión proliferativa intraductal borderline.
Es un marcador de riesgo (si CDIS: tiene una 10 veces > riesgo de carcinoma invasivo,
la HDA: tiene unas 4-5 veces) y puede potencialmente progresar a carcinoma infiltrante.
-Mamografía:
Se manifiesta como microcalcificaciones (más frecuente),
y más rramente como densidades,
masas o distorsiones (con o sin microcalcificaciones).
Ecografía:
-A veces como masa (las lesiones que se manifiestan solo microcalcificaciones,
raramente traducción ecográfica).
Fig. 27
La infraestimación de malignidad en la literatura tras un diagnóstico de HDA está en torno al 19,07% con BAV (Villa-11: artículo de revisión de la literatura,
con resultado propio de diagnóstico con BAV,
de un 11,9%; y donde se refiere que la infraestimación está en torno al 20-56% % si el diagnóstico es con BAG).
Con esa media de infraestimación,
la recomendación es que ante diagnóstico de HDA por biopsia percutánea se ha de realizar exéresis quirúrgica.
Fig. 28
Reseñar que en los distintos trabajos,
no hay consenso respecto a si tras la extracción de todas las microcalcificaciones en la BAV diagnóstica sigue habiendo infraestimación de malignidad (Villa-11,
en su trabajo tiene una infraestimación si extirpa todas las microcalcificaciones muy baja,
de un 1,5%,
y otros autores incluso de un 0%,
por lo que recomiendan seguimiento en esos casos; pero en cambio otros autores hablan de persistencia de infrastimaciones de malignidad entre un 5-17% a pesar de la extracción completa de las microcalcificaciones y recomiendan exéresis quirúrgica).
Fig. 29
Trabajos posteriores a esta revisión de Villa-11,
en general también hablan de infraestimaciones de malignidad elevadas.
Fig. 30
Algunos autores ven predictores clínico-radiológicos que reducen la infraestimación de malignidad por debajo de un 2%,
y algunos estudios han encontrado subgrupos de pacientes a los que se podría tratar conservadoramente (ej: Foregard-08,
Wagoner-09,
Nguyen-11,
Villa-11…); pero otros autores aún mostrando correlación entre los predictores y la tasa de infraestimación,
ésta permanece mayor de 2% y por eso recomiendan escisión quirúrgica.
Los factores que en los diferentes trabajos se han descrito asociados a mayor probabilidad de malignidad y cuya presencia por tanto orienta a recomendar la exéresis quirúrgica (o indicando que no se cumplan condicionan el seguimiento) son los siguientes:
- Si > 3 focos en corebiopsia (2 focos algún estudio)
- FC ratio > 1 (FC ratio significa focos de ADH/nº de cores)
- Tipo histológico micropapilar
- Atipias y necrosis celular
- > Tamaño lesión
- > 50 a
- < o = al 95% de volumen de microcalcificaciones extraído/no extracción completa de las microcalcificaciones
- Bajo nº de cores (aquí hay que reseñar que lo importante es el volumen muestreado respecto al tamaño de la lesión; si una lesión es muy grande,
por mayor nº de cores que se hagan no conseguiremos anular la infraestimación si no se muestrea suficientemente)
- Historia personal de cáncer
- Masa palpable o masa en US
- Si biopsia guiada por RM…
En resumen,
la mayoría de trabajos recomienda ante un diagnóstico por biopsia percutánea de HDA realizar exéresis quirúrgica.
Aunque podríamos hablar de “una zona de penumbra” donde la alternativa del seguimiento estricto según resultados de algunos trabajos podría ser una actitud razonable debido al bajo grado de infraestimación de malignidad (p ej especialmente si se ha realizado BAV con aguja de gran calibre con gran muestreo-con buena correlación extrayendo toda la lesión/todas las microcalcificiones “determinantes”,
ante lesiones de pequeño tamaño, sin necrosis,
tipo no micropapilar,
sin otras lesiones de riesgo asociadas…….).
Fig. 31
7- Neoplasia lobular (NL):
Proliferación epitelial (células escasamente cohesivas) que rellenan y distienden los acini de la unidad ductolobular terminal (si la afectación es < 50%: HLA ,
y si es > 50%: CLIS).
Se considera hoy día un indicador de riesgo ( HLA: 3-5 veces; CLIS: 10-12 veces) y un precursor “no obligado” de malignidad.
-Mamografía:
Tradicionalmente se consideraba hallazgo incidental en el muestreo de hallazgo radiológico adyacente (generalmente microcalcificaciones “vecinas”).
Posteriormente se ha visto que la NL puede asociarse a anomalías mamográficas : microcalcificaciones (más frecuentemente) y masa,
asimetría focal o distorsión parenquimatosa (mucho más raro).
-Ecografía:
Puede asociarse a lesión hipoecoica o distorsión de la arquitectura.
-RM:
Se manifiestan como áreas de realce regional parcheado similar a CDIS o pequeñas masas realzantes.
Curvas de realce : normalmente no típicas (generalmente retardadas,
a veces con plató).
Fig. 32
Fig. 33
Fig. 34
Tampoco hay consenso absoluto,
al igual que ante FEA y HDA respecto al manejo tras un diagnóstico de NL por biopsia pecutánea: cirugía ? vs seguimiento?:
Sí hay claro consenso ante un subtipo especial: la variedad pleomórfica,
la cual se asocia con cáncer invasivo más frecuentemente (25-67%),
que se manifiesta generalmente como microcalcificaciones tipo “comedo” (sospechosas),
y que debe tratarse como el CDIS (escisión con márgenes negativos /seguida de RT).
La infraestimación de malignidad en la literatura tras un diagnóstico de NL tras BAV está en torno al 27% con BAV (Hussain-11: artículo de revisión de la literatura,
con resultado propio idéntico al de la media de la literatura,
de un 27%,
y en concreto y específicamente para HLA de 19%,
para CLIS de 32%,
y para CL pleomórfico de 41%). Con esa media de infraestimación,
la recomendación más generalizada es que ante diagnóstico de NL por biopsia percutánea se ha de realizar exéresis quirúrgica.
Fig. 35
Pero también encontramos algunos trabajos (menor número) que recomiendan seguimiento basándose en la baja infraestimación de malignidad que han obtenido tras la cirugía después de un diagnóstico de biopsia percutánea o bien en el bajo porcentaje de cánceres que han tenido si lo que han hecho es seguimiento del paciente.
Fig. 36
Y si nos fijamos en aquellos trabajos en que se ha indicado/especificado si hay concordancia o discordancia radiopatológica, o si la NL es el hallazgo “diana” (las microcalcificaciones determinates) o en cambio es un hallazgo incidental en el seno de otros hallazgos histológicos benignos que justifican el hallazgo de la imagen,
llama la atención las grandes diferencias de infraestimación de malignidad que encontramos:
Fig. 37
Fig. 38
Se deduce,
por tanto,
que si NL es un hallazgo incidental la infraestimación de malignidad es más baja,
y en cambio si NL coincide con lesión diana radiológica (microcalcificaciones determinantes) la infraestimación de malignidad es mayor ; si hay concordancia radiopatológica la infraestimación de malignidad es más baja que si no la hay (Atkins-13,
D´Alfonso-13, Bianchi-13,
Szynglarewicz-12,
…).
También reseñar que en alguno de los artículos (Bianchi-13) se recalca que extrayendo todas las “microcalcificaciones determinantes” no se acaba con la infraestimación de malignidad.
Al igual que ocurría con la HDA,
en la NL distintos trabajos han visto que hay algunos factores asociados a mayor probabilidad de malignidad,
y cuya presencia por tanto orientaba a recomendar la exéresis quirúrgica (o condicionaban el seguimiento indicando que no se cumpliera alguna de estas condiciones):
-Si variante pleomórfica o florida
-Si masa o distorsión (representa discordancia RX-AP)
-Si afecta múltiples ductos o lóbulos (>10); > 4 focos en core
-Si se diferencia mal histológicamente de CDIS (overlap)
-Si > categoría BI-RADS (4 ó 5)
-Si afectación ductal
-Si otra lesión B3 (FEA,
HDA…)
-Si microcalcificaciones residuales
-Si riesgo por historia familiar
-Hay mayor infraestimación con BAG que con BAV (y a menor calibre de aguja)
-Hay mayor infraestimación si menor nº de muestras (aquí hay que reseñar lo mismo que hemos referido en la HDA,
que lo importante es el volumen muestreado respecto al tamaño de la lesión; si una lesión es muy grande,
por mayor nº de cores que se hagan no conseguiremos anular la infraestimación si no se muestrea suficientemente)…
En resumen,
la mayoría de trabajos recomienda ante un diagnóstico por biopsia percutánea de NL realizar exéresis quirúrgica.
Aunque podríamos hablar de “una zona de penumbra” donde la alternativa del seguimiento estricto según resultados de algunos trabajos podría ser una actitud razonable debido al bajo grado de infraestimación (p ej especialmente si la NL es un hallazgo focal incidental en biopsia sin otros factores de riesgo,
con existencia de total correlación –concordancia RX-AP,
y tomando la decisión bajo comité multidisciplinario…).
Fig. 39
Para finalizar,
dos incisos respecto a las lesiones categoría B3:
- Si se identifica FEA,
HDA o NL en los márgenes de una escisión quirúrgica de un CDIS o cáncer infiltrante,
no hay evidencia de que sea necesario ampliar la cirugía para obtener márgenes negativos alrededor de esas lesiones.
- Papel de la RM ante LHAR:
Existen 2 escenarios posibles donde puede intervenir la RM:
1)- RM para evaluar coexistencia de lesiones malignas (Linda-08 y -12,
Pediconi-05 y -10 ,
Strigel-10 ,
Crystal-10,
Londero-12):
- Se puede afirmar que no hay características de imagen específicas (no parámetros morfológicos ni dinámicos) predictivas del tipo de lesión ni de malignidad asociada en las lesiones B3 .
- La RM tiene un alto VPN (parece que la ausencia de realces en la RM permitiría descartar cánceres invasivos a asociados al diagnóstico por biopsia percutánea de lesiones B3,
aunque en este sentido hay conclusiones distintas en diferentes trabajos:
a) Londero 12: indica que hay diferencia significativa de infraestimación de malignidad entre las que realzan y las que no (18% vs 3%) y que se podría recomendar un manejo no quirúrgico a las que no presentan realce en la RM,
refiriendo que se evitarian 30% de cirugias ).
b) Linda 12: indica que hay un 12% y 10% de falsos negativos para NL y HDA ,
que considera que no es aceptable ,
y por ello estima que todas las NL y HDA han de ser extirpadas quirúrgicamente (y no recomienda RM en el manejo de las NL y HDA).
2)- RM como método de seguimiento en pacientes con diagnóstico previo de CLIS,
HLA ,
HDA:
Estudios de “cribado con RM” han incluido este grupo de mujeres demostrando un pequeño beneficio sobre la mamografía en la detección de cáncer .
La tasa de detección de cáncer es similar a la mostrada en grupos de alto riesgo: 4% (Port-07) y 3,8% (Friedlander-11),
aunque genera alto nº de biopsias y seguimientos a corto plazo: (biopsias 25%/VPP13,
Port-07; y biopsias 18,5%/23,8% VPP,
Friedlander-11).
No está recomendado en este grupo de mujeres el cribado con RM ni por sociedad europea (EUSOMA) ni por la ACS americana (aunque la NCCN-09 sí lo recomienda y la ACR indica que “podría considerarse“).