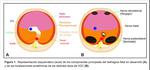
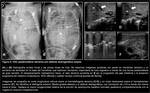
Para comprender el desarrollo de las HDC es imprescindible conocer el desarrollo embriológico del diafragma humano: comienza en la 4ª semana de gestación y se desarrolla hasta la 12ª semana de gestación.
Está formado a partir de componentes de 4 estructuras (Fig. 1):
- el septo transverso
- el mesenterio dorsal del esófago (en el mediastino primitivo)
- la membrana pleuroperitoneal
- y la musculatura de la pared lateral del cuerpo
Las membranas pleuroperitoneales crecen medial y ventralmente hasta la 7ª semana de gestación,
momento en que se fusionan con el septo transverso y el mesenterio dorsal del esófago.La muscularización del diafragma primitivo comienza con la migración de mioblastos de los miotomos cervicales,
que tiene como consecuencia la incorporación de los músculos intercostales con el diafragma.
En el desarrollo del componente muscular del diafragma permanece un remanente de la membrana pleuroperitoneal en la porción posterolateral de cada hemidiafragma,
que se conoce como trígono fibroso lumbocostal.
El septo transverso es anterior y se convertirá en el tendón central del diafragma.
En la patogenia del defecto diafragmático,
se ha considerado tradicionalmente que las hernias retroesternales (Morgagni) serían secundarias a un defecto en la fusión del septo transverso con la musculatura de la pared lateral del cuerpo; en las hernias posterolaterales (Bochdalek)la alteración principal consistiría en un fallo en la fusión de la membrana pleuroperitoneal y el septo transverso con los músculos intercostales en la 8ª semana de gestación.
(Fig. 1).
Por último,
una disminución en la muscularización del diafragma,
daría lugar a la eventración/relajación diafragmática.
Recientemente se ha propuesto la hipótesis del “mesenchymal hit” para explicar la asociación de las HDC con otras alteraciones acompañantes.Según esta hipótesis,
existen vías de señalización comunes en la diferenciación de las células mesenquimales en todas las estructuras afectadas y la función de estas células mesenquimales estaría alterada por desencadenantes genéticos o ambientales.
Se han implicado factores de transcripción como el GATA-4 y su corregulador transcripcional FOG-2 en la función normal de las células mesenquimales en el pulmón y diafragma en desarrollo en modelos experimentales.
Los defectos en la subestructura mesenquimal en estos modelos experimentales ocurren en la porción posterolateral de la membrana pleuroperitoneal y parecen tener una fuerte relación causal con alteraciones en el desarrollo de la musculatura diafragmática y por tanto con la HDC.
Entre los factores ambientales,
la exposición a toxinas como el herbicida Nitrofén (2,4-diclorofenil-p-nitrofeniléter),
el déficit de vitamina A y la toma de medicación antiepiléptica y talidomida producirían defectos diafragmáticos similares.
Las consecuencias de las HDC sobre la vía aérea y la vascularización pulmonar están relacionadas con el desarrollo embriológico pulmonar: el desarrollo normal de la vía aérea comienza en la 3ª semana de gestación y empieza a ramificarse hasta la semana 16ª de gestación.
Posteriormente,
los bronquiolos terminales,
acinos y sacos alveolares continúan desarrollándose durante el resto de la gestación y durante la infancia hasta los 8 años de edad,
aunque la mayoría del desarrollo se produce antes de los 2 años.
Las alteraciones en el desarrollo del diafragma a menudo afectan el proceso de desarrollo normal de las estructuras bronquiales.
La fisiopatología de las alteraciones pulmonares sería el resultado del daño en dos momentos diferentes sobre el desarrollo pulmonar (“dual-hit hypothesis”).
En un primer momento entre la 5ª y 16ª semana de gestación se produciría una pérdida de espacio para el pulmón en desarrollo,
que causaría una disminución en las ramificaciones bronquiales con el resultado de un número menor de alveolos.
En un segundo momento y con persistencia de la compresión pulmonar,
se produciría una disminución del tamaño de la vía aérea y de los alveolos,
aumento del tejido intersticial y disminución del espacio aéreo alveolar y de la superficie de intercambio gaseoso.
El desarrollo de la vascularización pulmonar sigue estrechamente al desarrollo de la vía aérea,
y puede verse afectada de una manera similar.
Las alteraciones en la vascularización pulmonar ocurrirían al mismo tiempo,
incluyendo una disminución en el número de vasos y una extensión anormal de la capa muscular en las arteriolas intraacinares.
Estas alteraciones son a menudo bilaterales y asimétricas,
con mayor afectación en el lado del defecto diafragmático.
Todas estas alteraciones,
según el tamaño y la localización del defecto diafragmático,
se pueden manifestar en el período postnatal como hipoplasia e hipertensión pulmonar secundarias,
que son los factores más directamente relacionados con el pronóstico y supervivencia en estos pacientes.
HDC POSTEROLATERAL
Características generales:
La HDC posterolateral o hernia del foramen de Bochdalek presenta una incidencia de 1/5000 recién nacidos vivos y alcanza 1/2500 si se tienen en cuenta los embarazos con resultado de muerte fetal (1).
Tradicionalmente se describe que un 85-90% de los defectos diafragmáticos posterolaterales son izquierdos y un 10-15% son derechos.
Las hernias posterolaterales bilaterales son raras,
pero pueden existir en un 2% de los casos.
El cierre más tardío de la membrana pleuroperitoneal en el lado izquierdo explicaría la mayor frecuencia de HDC izquierdas (2).
La existencia de un saco herniario íntegro compuesto de pleura y peritoneo se ha descrito en un 20% de los pacientes (3).
Sin embargo,
en una serie reciente de autopsias de casos de HDC,
se encontró que el 25% de las HDC diagnosticadas como hernias de Bochdalek eran anteriores,
centrales o mixtas,
en lugar de posterolaterales típicas (4).
La mayoría de las hernias posterolaterales se diagnostican antenatalmente mediante ecografía o bien se manifiestan en el nacimiento como distrés respiratorio.
Ocasionalmente,
se pueden presentar de manera tardía en un 11% de los casos (5),
mostrándose asintomáticas en el período neonatal (Fig. 6).
Los pacientes con HDC pueden ser divididos en dos grupos fenotípicos amplios,
según describe Pober (6):
1) HDC aislada:
La HDC es la única malformación mayor aparente; ocurre de manera aislada en aproximadamente un 60% de los casos.
Sin embargo a pesar de la ausencia de malformaciones congénitas asociadas,
a menudo está presente un espectro amplio de complicaciones acompañantes / asociadas que se pueden considerar parte de una secuencia de fenómenos en la HDC, entre los que se incluyen la hipoplasia pulmonar,
malrotación o rotación intestinal incompleta,
ductus arterioso permeable,
foramen oval permeable,
hipoplasia cardíaca y/o dextroposición,
insuficiencia tricúspide o mitral,
criptorquidia o presencia de bazo accesorio (2).
2) HDC compleja:
La HDC aparece asociada a otras anomalías en forma de asociación sindrómica,
asociada a una cromosomopatía o en forma de constelación no sindrómica de malformaciones mayores congénitas.
La forma de HDC compleja es frecuente en los casos de HDC posterolateral; la frecuencia descrita de las anomalías congénitas asociadas a HDC varía de manera importante dependiendo de la población estudiada.
Están presentes en un 25-50% de los recién nacidos vivos y puede alcanzar el 90-95% en los casos de muerte fetal (1).
Las malformaciones congénitas no sindrómicas más frecuentemente asociadas,
en orden decreciente,
son cardíacas,
renales,
del sistema nervioso central (defectos del tubo neural e hidrocefalia),
musculoesqueléticas (polidactilia,
sindactilia) y del tubo digestivo (paladar hendido,
atresia de esófago) (1,
2,
5,
6).
Lesiones pulmonares como el secuestro broncopulmonar y la malformación congénita de la vía aérea son asociaciones conocidas,
sin embargo presentes de manera infrecuente (2).
Presentamos un caso,
muy poco frecuente,
de HDC posterolateral izquierda asociado a secuestro pulmonar extralobar (Fig. 7).
La asociación con cardiopatías se describe en el 17 a 40% de los fetos con HDC e incluyen el síndrome de corazón izquierdo hipoplásico,
tetralogía de Fallot,
transposición de las grandes arterias,
ventrículo derecho de doble salida y defectos del tabique interventricular.
Las cardiopatías aumentan la mortalidad neonatal en los casos de HDC posterolateral,
con una tasa de supervivencia de aproximadamente el 41% en recién nacidos con cardiopatías asociadas comparado con un 70% en los pacientes sin patología cardíaca acompañante (1).
Por otra parte,
la determinación del cariotipo es imprescindible dado que entre el 10-20 % de los pacientes presentan cromosomopatías asociadas (1).
Las alteraciones cromosómicas más frecuentemente asociadas son la trisomía 13,
18 y 21 y la tetrasomía 12p (síndrome de Pallister-Killian).
Por último,
la aparición de HDC se ha descrito en asociaciones sindrómicas,
entre las que se incluyen los síndromes de Fryns,
Brachmann-De Lange,
Beckwith-Wiedemann,
Denysh-Drash y displasia craneofrontonasal (1,2,6).
Pronóstico:
No existe acuerdo sobre el incremento de la morbilidad en función de la lateralidad de la hernia. Todas las hernias bilaterales están asociadas con una mayor morbilidad.
Sin embargo,
en las hernias derechas se ha descrito igualmente una menor y una mayor morbilidad comparativamente con las izquierdas,
por lo que la relación entre la lateralidad del defecto diafragmático y el pronóstico es controvertida (2).
En cuanto a los marcadores prenatales,
los casos de HDC con estómago intratorácico se asocian con un peor pronóstico y con una menor tasa de supervivencia (2).
Sin embargo los factores pronósticos que tienen más impacto sobre la supervivencia en un paciente con HDC posterolateral,
son la herniación hepática y el grado de hipoplasia pulmonar e hipertensión pulmonar secundaria.
En las hernias posterolaterales izquierdas,
la herniación hepática se relaciona con un defecto diafragmático grande y herniación visceral precoz en el período fetal,
que conlleva hipoplasia pulmonar severa y mayor frecuencia de necesidad de oxigenación con membrana extracorpórea (ECMO) en el período postnatal (5).
El hígado intratorácico está asociado con una mortalidad del 57% y el hígado en posición intraabdominal del 7% (2).
En cuanto a la hipoplasia pulmonar,
tradicionalmente se ha determinado mediante ecografía fetal a través del lung-to-head ratio (obtenido al dividir el área pulmonar entre el perímetro cefálico) y,
más recientemente,
con el volumen pulmonar fetal (fetal lung volume,
FLV),
calculado mediante ecografía tridimensional y RM fetal (5). Los fetos con un FLV menor del 15-25% del esperado presentan una mortalidad significativamente superior (5).
Tratamiento:
El manejo primario de la hernia posterolateral consiste en la ventilación mecánica,
tratando de minimizar la toxicidad del oxígeno y el barotrauma a través de una ventilación poco agresiva.
El tratamiento médico de la hipertensión pulmonar con óxido nítrico y el soporte farmacológico de la función cardíaca son de especial importancia. Puede ser precisa la ECMO para estabilizar la hipertensión pulmonar.
La reparación quirúrgica se realiza de manera programada,
cuando se consigue la estabilización del paciente.
Habitualmente se utiliza un abordaje abdominal subcostal,
aunque en pacientes con una situación basal muy estable se está utilizando el abordaje mediante toracoscopia.
La técnica quirúrgica de reparación del defecto,
depende esencialmente del tamaño: los defectos pequeños se pueden reparar mediante cierre primario con suturas no reabsorbibles.
En los defectos grandes y las recurrencias hay múltiples opciones: parches,
materiales protésicos (Politetrafluoroetileno [Gore-Tex],
Polipropileno [Marlex],
submucosa de intestino delgado porcino [Surgisis]),
e injertos musculares (de pared torácica o de pared abdominal) (3).
Por último,
el tratamiento prenatal mediante oclusión con balón intratraqueal fetal (Fetoscopic endoluminal tracheal occlusion [FETO]) ha demostrado que puede prevenir la hipoplasia y acelerar el crecimiento pulmonar.
Aunque los resultados iniciales en ensayos clínicos controlados con fetos humanos fueron inicialmente desesperanzadores,
en la última década los resultados del Eurofetus Study Group han despertado de nuevo el interés por esta técnica y existe en marcha un estudio multicéntrico (TOTAL trial) mediante ensayos estandarizados y aleatorizados (14).
Hallazgos radiológicos postnatales:
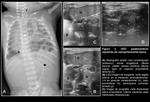
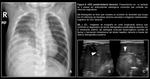
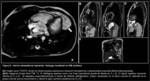
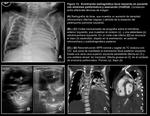
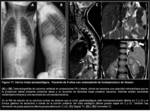
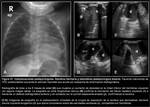
Hernia posterolateral izquierda (Fig. 2 y Fig. 3):
La radiografía simple postnatal inmediata suele mostrar opacificación del hemitórax izquierdo,
variable según el tamaño del defecto diafragmático y la mayor o menor herniación de contenido abdominal a la cavidad torácica.
Puede existir efecto de masa y desplazamiento mediastínico contralateral si el defecto es amplio (Fig. 2 y Fig. 3).
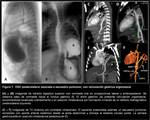
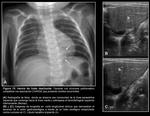
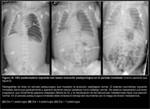
En un momento posterior,
la progresiva aireación del tubo digestivo tiene como consecuencia la aireación de las asas intestinales intratorácicas con aparición de imágenes “quísticas” en hemitórax izquierdo y escasez de aireación intestinal en un abdomen poco distendido; por el mismo motivo aumenta el efecto de masa,
y por tanto el desplazamiento mediastínico hacia el lado contralateral,
a la vez que puede verse comprometida la aireación del pulmón derecho (Fig. 2 y Fig. 3).
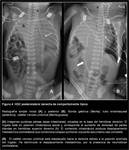
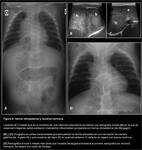
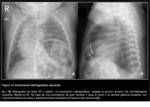
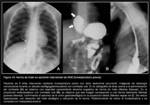
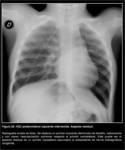
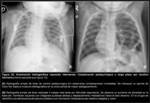
La ausencia de desplazamiento mediastínico puede ser secundaria a la existencia de neumotórax contralateral (derecho en el caso de HDC izquierdas),
habitual en niños con marcada hipoplasia pulmonar y ventilación vigorosa con presión positiva (Fig. 4).
En cuanto al desplazamiento intratorácico de otras vísceras abdominales, dependiendo del tamaño del defecto,
es frecuente encontrar un aumento de densidad de partes blandas en la base del hemitórax izquierdo,
con imágenes aéreas superpuestas,
que traduce el ascenso del lóbulo hepático izquierdo (LHI) (Fig. 2 y Fig. 3).
La participación gástrica en la herniación visceral se pone de manifiesto con la posición intratorácica de la sonda orogástrica (SOG) (Fig. 3).
Es frecuente encontrar una imagen de doble contorno de densidad partes blandas en la transición toracoabdominal y superpuesta al borde cardíaco derecho o paravertebral.
En nuestra experiencia,
esta imagen corresponde al desplazamiento del bazo hasta una posición pre/paravertebral derecha,
hallazgo frecuente cuando la lateralidad de la hernia es izquierda y que se demuestra en la ecografía abdominal con muy buena correlación entre ambas técnicas (Fig. 2 y Fig. 3).
Hay que tener en cuenta que los hallazgos iniciales en las radiografías simples,
incluyendo la aireación pulmonar,
el grado de desplazamiento mediastínico y el contenido herniario,
no predicen la evolución clínica de los pacientes,
por lo que su finalidad principal es confirmar el diagnóstico (5.1).
Posición de tubos y catéteres: La localización y el recorrido de los tubos y catéteres está alterado en la mayoría de los pacientes y ofrece información sobre el desplazamiento de las vísceras abdominales.
En las HDC posterolaterales izquierdas,
el tubo endotraqueal (TET) se desplaza hacia la derecha,
al igual que la porción esofágica de la SOG (Fig. 2 y Fig. 3).
El extremo distal de la SOG en el hemitórax izquierdo traduce la posición intratorácica de la cámara gástrica (Fig. 3).
En relación con los catéteres vasculares,
la posición del catéter venoso umbilical varía según el grado y dirección del desplazamiento hepático.
El catéter venoso umbilical normoposicionado en el neonato sigue el recorrido de la vena umbilical,
ligamento falciforme,
vena porta izquierda,
conducto venoso de Arancio,
vena cava inferior y aurícula derecha.
Cuando existe desplazamiento del LHI,
el tercio proximal del catéter está desplazado hacia el lado izquierdo,
teniendo que recorrer más distancia hasta la aurícula derecha (Fig. 2). Por el contrario,
la localización del catéter umbilical arterial se ve mínimamente afectada,
debido a la posición retroperitoneal de la aorta (1).
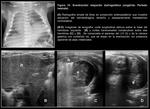
La ecografía (8) demuestra el desplazamiento mediastínico contralateral y puede ofrecer información sobre el tamaño relativo y la aireación del pulmón y la presencia de vísceras abdominales intratorácicas.
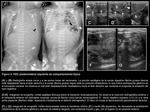
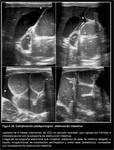
Mediante un abordaje longitudinal oblicuo en hipocondrio izquierdo (HCI) es posible demostrar el defecto diafragmático,
reconociendo la inserción diafragmática anterior,
el componente muscular del remanente diafragmático anterior como una banda hipoecogénica y una solución de continuidad en la superficie diafragmática en contacto con las vísceras abdominales (Fig. 3).
La herniación de LHI en las hernias posterolaterales izquierdas no es infrecuente por lo que habitualmente existe parénquima hepático intratorácico en contacto con el remanente diafragmático anterior y con el parénquima pulmonar aireado cranealmente () El pulmón no aireado puede tener una ecogenicidad similar a la del parénquima hepático.
La anatomía vascular ayuda en estos casos,
y la identificación de vasos portales que cruzan cranealmente,
permite diferenciar entre ambos (en las hernias izquierdas con más frecuencia la vena porta izquierda) (Fig. 2 y Fig. 3).
Igualmente,
es posible encontrar los vasos mesentéricos con un recorrido craneal hacia la cavidad torácica.
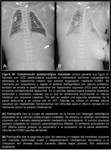
El parénquima hepático herniado se puede encontrar relativamente hipoecogénico respecto al resto del hígado,
traduciendo congestión secundaria al compromiso venoso (1) (Fig. 5).
El desplazamiento del bazo en las hernias izquierdas se produce habitualmente hacia una posición central y es importante insistir en la exploración hasta localizarlo; no es infrecuente encontrarlo en posición prevertebral/paravertebral derecha (Fig. 2 y Fig. 3) y en los casos en los que no se reconozca en su posición habitual hay que buscarlo en esta localización.
Las asas intestinales y cámara gástrica intratorácicas se visualizan mejor mediante cortes ecográficos transversales sobre el hemitórax izquierdo.
Se encontrarán asas intestinales y cámara gástrica con contenido líquido o aire intraluminal en función de la evolución del tránsito intestinal y del momento de la exploración (Fig. 2 y Fig. 3).
Es frecuente encontrar el aspecto característico del meconio cuando el marco cólico está desplazado a la cavidad torácica.
Si existen dudas sobre si la presencia de vísceras abdominales intratorácicas es debida a una agenesia pulmonar y a una eventración o elevación diafragmática secundaria,
la identificación de la arteria pulmonar confirma el diagnóstico de HDC (8).
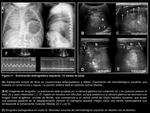
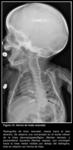
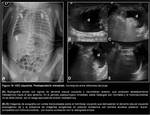
Hernia posterolateral derecha:
En los casos de lateralidad derecha del defecto diafragmático,
los hallazgos radiológicos son similares a los encontrados en las hernias izquierdas,
pero sobre el hemitórax derecho.
En las hernias posterolaterales derechas,
típicamente se desplaza el lóbulo hepático derecho (LHD) hasta una posición intratorácica,
seguido de asas intestinales,
que ocuparían una posición más inferior en el hemitórax derecho (Fig. 4).
Ocasionalmente,
si el defecto diafragmático es amplio,
puede existir mayor paso de asas intestinales hacia el tórax (Fig. 5).
El mediastino se desplaza hacia el lado izquierdo,
con desplazamiento del TET hacia ese lado; sin embargo,
la SOG ocupará habitualmente una posición infradiafragmática,
por la frecuente posición intraabdominal de la cámara gástrica en las hernias derechas.
La porción proximal del catéter venoso umbilical,
estará desviada hacia el lado derecho,
debido al desplazamiento hepático,
y la punta se dirigirá hacia el lado izquierdo para alcanzar la aurícula derecha.
La ecografía muestra el defecto diafragmático y el remanente anterior,
así como las vísceras desplazadas con una semiología similar a la descrita en las hernias posterolaterales izquierdas (Fig. 5 y Fig. 6).
En las HDC derechas,
habitualmente el bazo permanece en HCI.
HERNIA RETROESTERNAL
Las hernias retroesternales anteriores se presentan de dos formas.
La forma más frecuente es la hernia a través del foramen de Morgagni (FM). Se trata de un defecto anterior del diafragma que tiene como límites medial y lateral el esternón y la octava costilla respectivamente.
Las hernias del foramen de Morgagni representan un 9-12% de las HDC (1) y son más frecuentemente derechas (90%) y unilaterales.
A diferencia de las HDC posterolaterales,
las hernias del FM tienen habitualmente un saco herniario íntegro y bien definido.
La mayoría se diagnostican de manera incidental en niños mayores y adultos,
siendo de curso asintomático o presentándose en el contexto de una infección respiratoria o como una obstrucción intestinal,
tratándose,
en estos casos,
de defectos aislados sin asociación con otras patologías.
Por el contrario,
las hernias retroesternales del FM diagnosticadas en período neonatal son habitualmente sintomáticas (distrés respiratorio,
infección respiratoria o sintomatología gastrointestinal inespecífica) y se presentan habitualmente asociadas a otras anomalías congénitas,
que incluyen la trisomía 21 (14%) y las cardiopatías congénitas (58%) (1,9).
En los casos de diagnóstico incidental,
el hallazgo más frecuente es la presencia de asas intestinalesen mediastino anterior en la radiografía de tórax,
o en otras técnicas realizadas por otro motivo (TC,
RM).
Se puede presentar como masa localizada medialmente en mediastino inferoanterior cuando existe desplazamiento de vísceras abdominales a través del defecto (habitualmente hígado o bazo y menos frecuentemente cámara gástrica [Fig. 7] ) o herniación aislada de grasa omental (Fig. 9). La ecografía y la TC (eventualmente RM) demuestran con mayor precisión el contenido de la herniación (1) (Fig. 7 y Fig. 9).
Dado el riesgo asociado a las hernias retroesternales del FM de obstrucción intestinal con incarceración y estrangulación,
deben ser reparadas quirúrgicamente independientemente de la presencia de síntomas.
La corrección quirúrgica se realiza habitualmente mediante cierre primario y la mayoría de los casos se pueden resolver con abordaje laparoscópico (5).
La segunda forma de HDC retroesternal,
aparece como uno de los componentes de la pentalogía de Cantrell, que incluye diferentes anomalías congénitas asociadas a ectopia cordis: defecto de la línea media abdominal (onfalocele),
defecto de la parte inferior del esternón (cleft esternal inferior),
defecto del diafragma anterior,
defecto del pericardio diafragmático y malformaciones congénitas intracardiacas (10).
Esta entidad de mal pronóstico,
es el resultado del fracaso en el desarrollo del septo transverso en el diafragma primitivo.
El tratamiento incluye la corrección quirúrgica de la cardiopatía y de la pared abdominal; para la corrección del defecto diafragmático se requiere a menudo un parche protésico.
Por último,
se ha descrito una forma particularmente rara en forma de defecto central que afecta al diafragma y al pericardio,
con herniación de las vísceras abdominales hacia el saco pericárdico.
Estos defectos se han explicado como una forma truncada (forme fruste) de la pentalogía de Cantrell (11).
EVENTRACIÓN/RELAJACIÓN DIAFRAGMÁTICA
Características generales:
La eventración o relajación diafragmática consiste en una posición anormalmente alta de todo o una parte del diafragma,
resultado de una debilidad (relajación) o adelgazamiento de la musculatura diafragmática.
La eventración o relajación diafragmática congénita consiste en una anomalía en el desarrollo muscular del diafragma con hipoplasia del mismo,
a diferencia de la eventración adquirida,
en la que,
sobre un diafragma con una musculatura bien desarrollada,
se produce atrofia secundaria a una alteración en el movimiento diafragmático normal y al consiguiente desuso (3).
El defecto puede ser focal o completo; en las eventraciones focales,
la localización más habitual es la porción anteromedial del hemidiafragma derecho y son habitualmente hallazgos incidentales asintomáticos.
Sin embargo la eventración completa de un hemidiafragma ocurre típicamente en el lado izquierdo,
teniendo clínicamente el mismo efecto sobre la ventilación que la parálisis diafragmática (5).
Hay que recordar que la ventilación en el período neonatal y en el niño pequeño depende casi exclusivamente de una correcta función diafragmática,
debido a una musculatura intercostal débil y escasamente desarrollada y a la movilidad del mediastino.
Por tanto,
en niños, las alteraciones diafragmáticas son peor toleradas y presentan manifestaciones clínicas más graves (12).
Las manifestaciones clínicas de la eventración diafragmática varían desde los casos asintomáticos hasta el distrés respiratorio grave en función de la extensión de la afectación y de las consecuencias sobre la mecánica ventilatoria.
Se pueden manifestar tardíamente durante la infancia con bronquitis o neumonías de repetición y bronquiectasias y ocasionalmente sintomatología gastrointestinal (vómitos,
dispepsia,
epigastralgia) (3).
Hallazgos radiológicos:
El diagnóstico radiológico de eventración/relajación diafragmática se inicia mediante una radiografía de tórax en proyección anteroposterior (excepcionalmente se completa con una proyección lateral),
que pone de manifiesto un hemidiafragma elevado parcial o completamente (Fig. 10,
Fig. 11 y Fig. 12).
En ocasiones el aspecto en radiología simple es el de una opacidad en la base de un hemitórax,
consecuencia del ascenso diafragmático y de las vísceras abdominales (hígado,
bazo) que se asocia al aumento de densidad del parénquima pulmonar basal con pérdida de la aireación (Fig. 13).
Así,
el aspecto radiológico en radiografía simple de tórax de la eventración diafragmática puede simular el de una hernia diafragmática.
Por tanto,
en ocasiones, la diferenciación entre ambas entidades solamente es posible demostrando un diafragma intacto o íntegro en el borde superior de la deformidad,
mediante ecografía,
TC o RM.
Los hallazgos ecográficos consisten en un diafragma adelgazado pero íntegro,
ascendido o con una deformidad en sentido craneal en el caso de las eventraciones focales.
Además,
la ecografía permite identificar las vísceras abdominales alojadas en la deformidad diafragmática (habitualmente hígado o bazo) y el grado de aireación del parénquima pulmonar basal (Fig. 10, Fig. 11 y Fig. 13).
La ecografía en modo M ofrece información sobre la dirección y amplitud de las excursiones diafragmáticas (12) .
Se puede encontrar movimiento paradójico del diafragma en casos de eventración completa,
haciendo imposible la distinción radiológica entre la eventración congénita completa y la parálisis diafragmática (3,13) (Fig. 11).
En los casos en los que sea necesario,
la TC o RM confirman la integridad diafragmática y el desplazamiento de los órganos abdominales (Fig. 13).
HERNIA DE HIATO
La hernia de hiato se define como la protrusión de una parte del estómago hacia el mediastino a través del hiato esofágico del diafragma.
Se reconocen tres tipos de hernia hiatal: deslizante,
en la que el estómago se mueve hacia el tórax a través de un hiato esofágico ensanchado; paraesofágica,
en la que no existe desplazamiento de la unión gastroesofágica y una porción del estómago asciende a través de un hiato ensanchado en su vertiente anterior; por último,
el esófago corto congénito,
que se asocia a un estómago intratorácico no reducible.
Una explicación para la hernia de hiato congénita sería un retraso en el descenso del estómago desde el tórax,
resultando en un hiato esofágico más grande con más espacio entre el esófago y el diafragma.
La hernias de hiato representan de manera global la mitad de todas las hernias diafragmáticas; sin embargo en la mayoría se trata de lesiones adquiridas.
En niños menores de un año,
representan únicamente el 9% de las hernias diafragmáticas (1) (Fig. 14).
La hernia paraesofágica es una entidad poco frecuente en la infancia (Fig.
17).
Habitualmente se trata de niños con ausencia de los ligamentos gastrocólico y gastroesplénico,
responsables de fijar el estómago en posición normal.
Entre las complicaciones graves están el vólvulo gástrico organoaxial y la herniación colónica.
Por otra parte,
las hernias de hiato pueden presentarse como complicación de una fundoplicatura de Nissen previa (5) (Fig. 16 y Fig. 17).
El diagnóstico prenatal de hernia hiatal se realiza mediante la identificación de una masa hipoecogénica en mediastino inferior en continuidad con la porción intraabdominal del estómago.
En el período postnatal,
el hallazgo típico en radiografía simple es la convexidad del borde inferior del receso acigoesofágico y de la línea paravertebral izquierda en la proyección anteroposterior (Fig. 14, Fig. 15, Fig. 16 y Fig. 17) una masa mediastínica retrocardíaca en la proyección lateral,
eventualmente con contenido aéreo o un nivel aire-líquido.
El esófago corto congénito se puede reconocer radiológicamente como un quiste aéreo intratorácico; la presencia de una sonda gástrica cruzando a su través sugiere fuertemente el diagnóstico.
La ecografía puede demostrar un hiato esofágico ensanchado y el ascenso de la unión gastroesofágica (Fig. 15).
Sin embargo,
en la mayoría de los casos,
la confirmación diagnóstica se obtiene con un estudio gastroesofágico con contraste oral hidrosoluble (Fig. 16),
reconociendo la posición del fundus gástrico y de la unión gastroesofágica y su relación con el hiato esofágico.
El tratamiento quirúrgico incluye la reducción de las vísceras herniadas en la cavidad abdominal,
la excisión del saco herniario y ocasionalmente hiatoplastia,
habitualmente mediante cirugía laparoscópica.
Dado que los niños con hernia de hiato presentan frecuentemente reflujo gastroesofágico concomitante,
se practica una fundoplicatura en el mismo tiempo quirúrgico (5).
ASPECTO POSTQUIRÚRGICO / COMPLICACIONES
En las hernias posterolaterales,
después de la reparación quirúrgica,
existe un extenso neumotórax ipsilateral.
En el período postquirúrgico inmediato el pulmón aparece colapsado en forma de “muñón” pulmonar paramediastínico.
A medida que ocurre la reexpansión pulmonar progresiva,
el neumotórax inicial evoluciona a hidroneumotórax con ocupación de la cavidad pleural por líquido.
Después de la reabsorción del aire rodeando al pulmón hipoplásico y la reexpansión pulmonar,
es frecuente la presencia de derrame pleural residual,
hallazgo que se debe considerar normal (Fig. 18 y Fig. 19).
Hay que señalar,
que en los neonatos el mediastino posee una mayor movilidad,
y la evacuación rápida del neumotórax esta asociada con riesgo de torsión mediastínica y obstrucción venosa.
El drenaje del neumotórax postquirúrgico se debe evitar; se reabsorbe gradualmente y el mediastino se recoloca hacia una posición centrotorácica de manera progresiva (Fig. 18 y Fig. 19).
Las radiografías de tórax de control son útiles para evaluar las consecuencias morfológicas de la hipoplasia pulmonar subyacente y sus complicaciones.
Las manifestaciones radiológicas de la hipoplasia pulmonar residual pueden ser un tamaño pulmonar disminuido con menor vascularización y asimétrico en relación con el pulmón contralateral (Fig. 20),
aunque en ocasiones es aspecto radiológico es normal.
La disminución de la perfusión pulmonar se puede confirmar con gammagrafía; la ventilación pulmonar suele permanecer relativamente conservada.
A largo plazo,
los pacientes con antecedentes de HDC tienen más probabilidad de sufrir patología respiratoria crónica como asma o infecciones recurrentes de la vía aérea.
Sin embargo,
sólo una minoría de estos pacientes tendrá secuelas graves como restricción severa de la capacidad respiratoria y oxigenodependencia.
La recidiva herniaria es una de las complicaciones más importantes y se produce entre un 3-22 % de los pacientes (5).
El mayor riesgo de recidiva y de otras complicaciones está asociado a los pacientes con defectos diafragmáticos amplios que requieren parches protésicos (Fig. 21 y Fig. 22).
Por otra parte,
el crecimiento del diafragma reparado puede asociarse a una movilidad reducida,
demostrable mediante ecografía.
Otra de las consecuencias a largo plazo en pacientes intervenidos de HDC es la presencia de reflujo gastroesofágico. Se debe a una alteración funcional en la unión gastroesofágica,
y puede tratarse médicamente o requerir corrección quirúrgica mediante fundoplicatura (15).
Aunque menos frecuentes,
los pacientes con antecedentes de HDC pueden sufrir complicaciones abdominales.
Por ejemplo,
se pueden producir cuadros de obstrucción intestinal (Fig. 23),
por incarceración de asas intestinales (sobre todo en las hernias retroesternales) o por formación de bridas peritoneales tras la reparación quirúrgica del defecto diafragmático (15).
Los pacientes con HDC,
al igual que sucede en otras patologías en las cuales las asas intestinales se localizan fuera de la cavidad peritoneal más allá de la 10ª semana de gestación (como sucede en la gastrosquisis y el onfalocele),
presentan invariablemente anomalías de la rotación y fijación intestinal.
Aunque existe la posibilidad teórica de vólvulo de intestino medio (Fig. 24),
se ha visto que el tipo de malrotación y las adherencias postoperatorias limitan el riesgo de que este ocurra (16,17).
No obstante,
por esta razón algunos cirujanos realizan un procedimiento de Ladd durante la cirugía de reparación del defecto diafragmático.
Se han descrito casos de vólvulo gástrico (Fig. 7) en pacientes con defectos diafragmáticos congénitos (tanto en defectos posterolaterales como en hernias de hiato paraesofágicas) (18,19).
Como complicación abdominal excepcional,
se ha descrito algún caso de torsión esplénica en el contexto de HDC posterolateral izquierda.