INTRODUCCION
El cÃĄncer de pÃĄncreas supone la cuarta causa de muerte por neoplasia en adultos y la segunda de cÃĄncer digestivo [1,2].
Presenta un pronÃģstico sombrÃo,
con una tasa de supervivencia global a los 5 aÃąos inferior al 5% [1,3,4] .
Esta situaciÃģn viene condicionada porque el 80% de los casos se diagnostican en estadios avanzados de la enfermedad,
debido a la inespecificidad de la sintomatologÃa clÃnica inicial [4],
siendo las posibilidades de tratamiento quirÚrgico radical en el momento del diagnÃģstico sÃģlo del 10â25% [2],
la Única opciÃģn potencialmente curativa [4].
DIAGNÃSTICO CLÃNICO.
ASPECTOS PATOLÃGICOS.
El 85 % de los adenocarcinomas de pÃĄncreas surgen del epitelio ductal.
Alrededor del 60-75% de tumores asientan en la cabeza pancreÃĄtica,
causando clÃnica de ictericia obstructiva,
habitualmente asociado a dolor epigÃĄstrico y pÃĐrdida de peso,
en etapas relativamente poco avanzadas de la enfermedad.
El 15% de las neoplasias se desarrollan en el cuerpo pancreÃĄtico y el 5-10% lo hacen en la cola.
En estos casos el pronÃģstico es peor,
ya que con frecuencia son asintomÃĄticos hasta alcanzar estadios mÃĄs avanzados.
El 20% restante afectan a la glÃĄndula de forma difusa.
El marcador tumoral mÃĄs extensamente utilizado es el CA 19-9,
Útil en la monitorizaciÃģn de la respuesta terapÃĐutica,
pronÃģstico y seguimiento de recidivas [4].
Dada la limitada sensibilidad (a menudo no se eleva en neoplasias asintomÃĄticas de pequeÃąo tamaÃąo) y especificidad (puede elevarse en otras neoplasias y trastornos benignos pancreatobiliares [4]),
este marcador tumoral no debe ser utilizado como prueba de diagnÃģstico para el cÃĄncer pancreÃĄtico.
A pesar de mÚltiples estudios para determinar los factores de riesgo de la enfermedad,
no se ha conseguido definir una poblaciÃģn de riesgo que permita poner en marcha programas de cribaje para este tumor [4].
Se ha establecido relaciÃģn con la exposiciÃģn activa al tabaco y con la edad,
ya que el 80% de estos tumores se presentan entre los 60 y 85 aÃąos.
TambiÃĐn se han identificado algunos sÃndromes hereditarios asociados a una mayor incidencia de cÃĄncer de pÃĄncreas,
como son el melanoma familiar hereditario,
el sÃndrome de Peutz-Jeghers,
el cÃĄncer colorrectal hereditario no polipoideo (tipo Lynch II),
la pancreatitis hereditaria,
el sÃndrome de cÃĄncer de mama-ovario hereditario (mutaciones de BRCA1 y BRCA2 [2]) y la ataxia-telangiectasia [2,4].
TÃCNICAS DE DIAGNÃSTICO. EVALUACIÃN PREOPERATORIA
Cualquiera que sea la modalidad de imagen que se emplee,
el objetivo de la evaluaciÃģn preoperatoria del cÃĄncer de pÃĄncreas serÃĄ detectar el tumor,
determinar la estatificaciÃģn local y a distancia y valorar su resecabilidad,
para llevar a cabo un tratamiento Ãģptimo [1,2,5].
La TC es la tÃĐcnica de elecciÃģn y mÃĄs empleada para este propÃģsito [1,2,4].
UltrasonografÃa abdominal (US)
El estudio inicial en pacientes con sospecha clÃnica de afectaciÃģn hepato-bilio-pancreÃĄtica es a menudo la ecografÃa abdominal,
debido a su inocuidad y amplia disponibilidad [2,4].
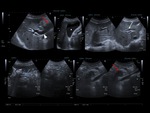
Permite detectar la neoplasia pancreÃĄtica (hipoecoica y mal definida),
valorar la vÃa biliar/conducto pancreÃĄtico (Figura 1),
evaluar las estructuras vasculares peripancreÃĄticas (tÃĐcnica Doppler color [5]),
metÃĄstasis hepÃĄticas y en ocasiones implantes peritoneales.
Si bien,
existen limitaciones para el estudio del pÃĄncreas debido a la interposiciÃģn de gas intestinal,
ser una exploraciÃģn ÂŦoperador-dependienteÂŧ y su baja sensibilidad y especificidad para determinar la resecabilidad (63% y 83% respectivamente) [2].
TomografÃa computarizada (TC)
La TC es el mÃĐtodo de imagen mÃĄs ampliamente utilizado para la detecciÃģn,
caracterizaciÃģn y evaluaciÃģn preoperatoria del adenocarcinoma pancreÃĄtico,
ya que aporta una buena resoluciÃģn espacial y amplia cobertura anatÃģmica [1].
Para ello resulta crucial conocer los parÃĄmetros tÃĐcnicos adecuados,
que permitan maximizar la diferencia de atenuaciÃģn entre el tumor y el parÃĐnquima pancreÃĄtico normal,
valorar los vasos cercanos y las estructuras distantes.
TambiÃĐn es una herramienta fundamental para la planificaciÃģn quirÚrgica y seguimiento de los pacientes tratados de cÃĄncer de pÃĄncreas [1].
TÃĐcnica de adquisiciÃģn
Aunque existe controversia en la literatura acerca de quÃĐ fase del estudio dinÃĄmico es la mÃĄs sensible para detectar el tumor,
actualmente se ha llegado a una mayor homogeneidad en la tÃĐcnica de adquisiciÃģn.
Se requiere un estudio dinÃĄmico bifÃĄsico [1,3,4] obtenido en fase parenquimatosa pancreÃĄtica (o pancreatogrÃĄfica) con un retraso con respecto al inicio de la inyecciÃģn de contraste de 40 segundos,
seguido de una fase venosa portal,
obtenida con una demora de unos 70 segundos [1,4].
La opacificaciÃģn mÃĄxima de la glÃĄndula tiene lugar durante la fase pancreatogrÃĄfica que maximiza las diferencias de atenuaciÃģn entre el pÃĄncreas normal (que muestra un realce vigoroso) y el tumor (hipodenso,
debido a proliferaciÃģn fibroblÃĄstica y la hipoperfusiÃģn).
Esta fase tambiÃĐn permite el adecuado realce de las estructuras vasculares criticas para la detecciÃģn de invasiÃģn vascular [1].
La fase venosa portal es ideal para la detecciÃģn de metÃĄstasis hepÃĄticas,
ganglios linfÃĄticos e implantes peritoneales asà como la creaciÃģn de reconstrucciones de imÃĄgenes de las estructuras venosas,
que podrÃan ser esenciales para la planificaciÃģn quirÚrgica.
TambiÃĐn proporciona una segunda mirada al pÃĄncreas,
lo que puede ser Útil en ocasiones [1].
La adquisiciÃģn de imÃĄgenes en fase arterial (retraso de 20 segundos) no aporta informaciÃģn adicional en la detecciÃģn y estadificaciÃģn del adenocarcinoma de pÃĄncreas,
puesto que la visibilidad de las lesiones es subÃģptima y la representaciÃģn de la anatomÃa venosa es inferior a la fase portal [4].
Es necesaria la evaluaciÃģn de los estudios en consolas de trabajo,
complementando las imÃĄgenes axiales con reconstrucciones multiplanares y 3D,
que permitan una mayor precisiÃģn para determinar la extensiÃģn local y a distancia [4].
DetecciÃģn tumoral
Aproximadamente el 90 % de los adenocarcinomas de pÃĄncreas se presentan como una masa focal,
el resto se manifiesta de forma difusa [1].
En la TC con contraste intravenoso,
la lesiÃģn suele ser hipodensa con respecto al tejido pancreÃĄtico.
Aunque hay que tener en cuenta que alrededor del 10% de los adenocarcinomas de pÃĄncreas son isodensos en relaciÃģn al parÃĐnquima pancreÃĄtico no tumoral [1],
y es una forma de presentaciÃģn mÃĄs caracterÃstica de lesiones de pequeÃąo tamaÃąo (âĪ 2 cm) [4].
En estos casos,
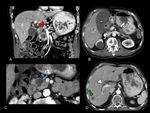
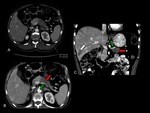
el diagnÃģstico de neoplasia pancreÃĄtica se puede apoyar en signos indirectos como [4]:
1.
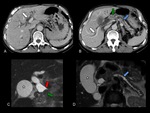
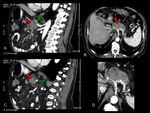
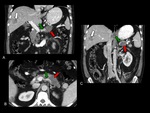
InterrupciÃģn y obstrucciÃģn ductal abrupta (Figuras 2,
3 y 4).
2.
Efecto masa y/o convexidad del contorno pancreÃĄtico.
3.
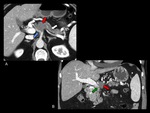
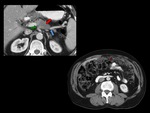
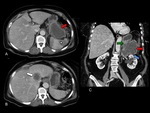
Atrofia distal del parÃĐnquima pancreÃĄtico (figuras 2 y 5).
4.
DilataciÃģn e interrupciÃģn de los conductos biliar y pancreÃĄtico: signo del doble conducto,
mÃĄs comÚn en tumores que asientan en la cabeza pancreÃĄtica (Figuras 2,
3,
y 4).
La pancreatitis crÃģnica focal y la pancreatitis autoinmune son los dos procesos benignos mÃĄs comÚnmente confundidos con cÃĄncer de pÃĄncreas en TC o ecografÃa.
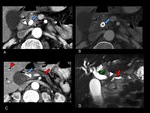
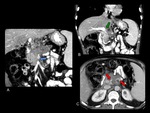
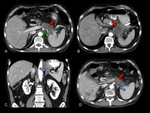
Los pacientes con adenocarcinoma de pÃĄncreas con frecuencia se someten a colangiopancreatografÃa retrÃģgrada endoscÃģpica (CPRE) para la colocaciÃģn de stent biliar previo a realizarse la TC,
el cual dificulta la valoraciÃģn de la exacta localizaciÃģn anatÃģmica de la obstrucciÃģn biliar o da lugar a la apariciÃģn de cambios inflamatorios locales que pueden ser confundidos con una lesiÃģn neoplÃĄsica pancreÃĄtica (Figura 3) [4].
EstadificaciÃģn y criterios de resecabilidad
La TC es la tÃĐcnica de elecciÃģn para una correcta evaluaciÃģn de la extensiÃģn local y a distancia.
Los valores predictivos positivos de la TC para irresecabilidad estÃĄ entre el 89% y 100% [5],
algo menor (76-90%) para valorar la resecabilidad,
siendo las principales limitaciones de la TC en el proceso de estadificaciÃģn la presencia de pequeÃąas lesiones hepÃĄticas y de implantes peritoneales.
TNM
El actual sistema de clasificaciÃģn TNM para la estadificaciÃģn de cÃĄncer de pÃĄncreas se basa en American Joint Committee on Cancer (AJCC) y la UniÃģn Internacional Contra el CÃĄncer (UICC) [1,2,5].
El principal factor que determina el estadio del tumor es el grado de invasiÃģn locorregional o a distancia y no el tamaÃąo de la tumoraciÃģn [5].
Tumor primario (T)
Tx - no se puede evaluar el tumor primario
T0 - no hay evidencia de tumor primario
Tis - carcinoma in situ
T1 - tumor limitado al pÃĄncreas,
hasta 2 centÃmetros de diÃĄmetro mÃĄximo
T2 - tumor limitado al pÃĄncreas,
mayor de 2 centÃmetros de diÃĄmetro mÃĄximo
T3 - tumor que se extiende fuera del pÃĄncreas,
sin afectar el tronco celÃaco ni la arteria mesentÃĐrica superior
T4 - tumor que afectar el tronco celÃaco o la arteria mesentÃĐrica superior
MetÃĄstasis en ganglios regionales (N)
Nx - no se pueden valorar los ganglios regionales
N0 - ausencia de metÃĄstasis en los ganglios regionales
N1- presencia de metÃĄstasis en los ganglios regionales
MetÃĄstasis a distancia (M)
Mx - no se puede evaluar la existencia de metÃĄstasis a distancia
M0 - ausencia de metÃĄstasis a distancia
M1 - presencia de metÃĄstasis a distancia
EvaluaciÃģn vascular
La infiltraciÃģn vascular es el factor mÃĄs crÃtico del que depende la potencial resecabilidad tumoral.
La invasiÃģn arterial es un criterio de irresecabilidad bien aceptado.
Sin embargo, la invasiÃģn venosa peripancreÃĄtica es una controvertida contraindicaciÃģn [3].
Un sistema de clasificaciÃģn de infiltraciÃģn puede basarse en el grado de contigÞidad circunferencial del tumor al vaso [5].
Los Criterios de Lu [2] establecen la probabilidad de infiltraciÃģn basÃĄndose en el porcentaje de contacto con el vaso.
Un Único contacto no implica infiltraciÃģn,
y por lo tanto,
se puede realizar cirugÃa con mÃĄrgenes libres de tumor (Tabla 1).
| GRADOS |
% de contacto entre el tumor y la circunferencia del vaso |
Probabilidad de infiltraciÃģn |
| 0 |
no contacto |
no invasiÃģn |
| I |
< 25 % de circunferencia |
invasiÃģn posible pero poco probable |
| II |
entre 25-50% |
invasiÃģn posible pero poco probable |
| III |
entre 50-75% |
invasiÃģn vascular |
| IV |
>75% o estenosis |
invasiÃģn vascular |
TABLA1: Criterios de Lu para evaluar la invasiÃģn vascular
InvasiÃģn venosa
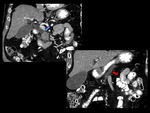
Los signos de irresecabilidad incluyen [1,2,5]:
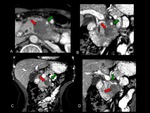
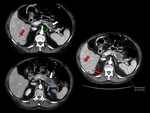
- estenosis e irregularidad de la vena porta (VP) o la vena mesentÃĐrica superior (VMS),
asà como una contigÞidad circunferencial del tumor con la vena porta superior a 90š (Figuras 6 y 7).
- aumento de grado de englobamiento circunferencial venosa por el tumor.
- invasiÃģn o trombosis de la VMS o VP.
- signo de la "lÃĄgrima" de la vena mesentÃĐrica superior : consiste en una deformidad de la morfologÃa redondeada de la vena adyacente al tumor en las secciones axiales,
como indicativo de invasiÃģn venosa [1].
- presencia de pequeÃąas venas peripancreÃĄticas dilatadas.
CirculaciÃģn colateral: venas pancreatoduodenales o tronco gastrocÃģlico).
InvasiÃģn arterial
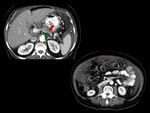
La afectaciÃģn (con pÃĐrdida de plano graso entre el tumor y el vaso) de la arteria mesentÃĐrica superior (AMS,
Figura 8),
tronco celÃaco (TH),
arteria hepÃĄtica (AH) Ãģ arteria gastroduodenal proximal (Figuras 6,7,9 y 10),
hace al tumor irresecable [1-3,5].
EvaluaciÃģn ganglionar
La TC no es exacta en la estadificaciÃģn ganglionar prequirÚrgica [5,7].
El tamaÃąo no es una caracterÃstica discriminatoria entre ganglios linfÃĄticos metastÃĄsicos y no metastÃĄtico,
ademÃĄs que la detecciÃģn de ganglios metastÃĄticos peripancreÃĄticos tiene una importancia limitada porque la mayorÃa se resecan en bloque junto con el tumor.
Por tanto en pacientes con un tumor resecable por lo demÃĄs,
la descripciÃģn en TC de ganglios peripancreÃĄticos agrandados no debe impedir una resecciÃģn con intenciÃģn curativa [1].
EvaluaciÃģn de metÃĄstasis a distancia
La detecciÃģn de metÃĄstasis hepÃĄticas o peritoneales constituye un criterio definitivo de irresecabilidad tumoral,
no obstante la TC tiene limitaciones [1,2,5].
ESTADIAJE Y CRITERIOS DE RESECABILIDAD
Se consideran tumores resecables aquellos que cumplen los siguientes criterios:
- Ausencia de enfermedad extrapancreÃĄtica.
- No evidencia de afectaciÃģn de AMS,
TC Ãģ AH,
definida como la presencia de plano graso entre el tumor y las arterias.
- La afectaciÃģn de la confluencia entre VMS-VP,
si la resecciÃģn y reconstrucciÃģn son posibles,
no es criterio de irresecabilidad.
No hay evidencia de contacto,
distorsiÃģn,
invasiÃģn o trombosis de VMS o VP.
Tumores irresecables:
- InfiltraciÃģn extrapancreÃĄtica incluyendo amplia afectaciÃģn linfÃĄtica peripancreÃĄtica,
afectaciÃģn ganglionar mÃĄs allÃĄ de los tejidos peripancreÃĄticos,
y / o metÃĄstasis a distancia (Figuras 2,10,11-16).
- AfectaciÃģn directa de la arteria mesentÃĐrica superior (AMS),
vena cava inferior,
la aorta,
tronco celÃaco (TC) o la arteria hepÃĄtica (AH),
definido como la ausencia de plano graso entre el tumor y la arteria (Figuras 6-10).
- Revestimiento de mÃĄs de la mitad de la circunferencia o la oclusiÃģn/trombosis de la vena mesentÃĐrica superior (VMS) o la confluencia con la vena porta,
sin posibilidades de reconstrucciÃģn (Figuras 6 y 7).
La afectaciÃģn de la vena esplÃĐnica,
invasiÃģn a duodeno y ganglios locorregionales no son criterio de irresecabilidad ya que pueden ser resecados en bloque con el tumor (Tabla 2).
| Estadio |
DescripciÃģn |
TNM |
Comentarios |
| I |
resecable |
T1/T2,N0,M0 |
no enfermedad extrahepÃĄtica |
| II |
resecable |
T1/T2,N1,M0
T3,N0/N1,M0
|
puede haber extensiÃģn a tejidos peripancreÃĄticos sin invasiÃģn vascular |
| III |
resecable borderline/irresecable |
T4,N0/N1,M0 |
invasiÃģn vascular venosa o arterial,
estÃģmago o colon |
| IV |
irresecable |
Cualquier T N0/N1,M1 |
metÃĄstasis a distancia |
TABLA 2
Enfermedad resecable borderline:
- Impronta de VP o VMS < 180 š.
- Englobamiento de VMS/VP de un segmento venoso corto (15 mm) que permita la resecciÃģn segura y reconstrucciÃģn.
- AfectaciÃģn de arteria gastroduodenal Ãģ hepÃĄtica en un segmento corto sin extensiÃģn al tronco celÃaco.
- AfectaciÃģn de AMS que no exceda > 180š de su circunferencia.
- Tumores de cola-cuerpo con menos de 180š de afectaciÃģn de la circunferencia de tronco celÃaco Ãģ AMS.
- InfiltraciÃģn del colon o mesocolon.
Resonancia magnÃĐtica (RM)
La RM presenta mayor sensibilidad para detectar tumores de pequeÃąo tamaÃąo (hipointensos y escaso realce con el contraste) o enfermedad a distancia (metÃĄstasis hepÃĄticas pequeÃąas e implantes peritoneales).
ColangiopancreatografÃa por RM (CPRM) Útil en evaluar el ÃĄrbol biliar y conducto pancreÃĄtico,
y determinar el nivel de la obstrucciÃģn [4] (Figuras 3 y 5).
UltrasonografÃa endoscÃģpica (USE)
La ventaja mÃĄs patente de la USE es la posibilidad de intervencionismo diagnÃģstico al permitir realizar la PAAF bajo control ecogrÃĄfico continuo [4].
AdemÃĄs ofrece una excelente visualizaciÃģn de todo el pÃĄncreas,
lo que es Ãģptimo para detectar lesiones de muy pequeÃąo tamaÃąo (< 2 cm) [2],
y para el estadiaje ganglionar [1].
TomografÃa por emisiÃģn de positrones (PET)
La PET no ha demostrado utilidad aÃąadida en la estadificaciÃģn del adenocarcinoma de pÃĄncreas,
pero puede ser Útil en demostrar metÃĄstasis a distancia en lugares insospechados o en el seguimiento postquirÚrgico en los que las alteraciones anatÃģmicas dificultan la valoraciÃģn locorregional de la recidiva tumoral en TC y RM.
AdemÃĄs la combinaciÃģn PET/TC abre nuevas expectativas para el diagnÃģstico,
estadificaciÃģn y seguimiento del adenocarcinoma pancreÃĄtico [4].
Laparoscopia
Puede ser Útil en detecciÃģn de implantes peritoneales y metÃĄstasis hepÃĄticas superficiales que rara vez son visibles en estudios de imagen preoperatorios [5],
a la vez que permite biopsiar las lesiones observadas.
Las limitaciones en la predicciÃģn de la resecabilidad tumoral han llevado a sugerir la combinaciÃģn de varias tÃĐcnicas para minimizar el riesgo de infraestadificaciÃģn antes de tomar una decisiÃģn terapÃĐutica concreta.