La angiografía obtenida por TCMD es la técnica de elección en el estudio de la patología vascular de la extremidad superior.
Es una técnica no invasiva,
explorador independiente,
con adquisición rápida y alta resolución espacial que permite valorar el flujo de toda la extremidad superior incluso en pacientes con calcificación de arterias nativas o sometidos recientemente a cirugía.
Ha sustituido a la angiografía que es una técnica invasiva y por lo tanto no exenta de complicaciones que solo valora la luz del vaso pero no analiza la pared arterial ni las estructuras no vasculares.
La ecografía se suele realizar como prueba de imagen inicial pero tiene algunas limitaciones: es operador dependiente,
tiene resolución espacial limitada y no permite valorar las venas centrales ni el origen de los troncos supraórticos.
La RM tiene la ventaja de no utilizar radiaciones ionizantes ni contraste yodado y de realizar adquisiciones 3D dinámicas en múltiples fases vasculares por lo que solemos utilizarla en pacientes con intolerancia al yodo y en pacientes con malformaciones vasculares en la extremidad superior.
Sin embargo,
es una exploración que consume mucho tiempo particularmente si hay que valorar toda la extremidad y tiene las limitaciones de cualquier exploración RM.
TÉCNICA ADQUISICIÓN
PREPARACIÓN DEL PACIENTE:
Se deben retirar todos los objetos metálicos externos del teórico campo de cobertura porque pueden degradar la calidad de la imagen.
El campo de cobertura incluye al menos el tórax y la extremidad afecta.
Si la TC se realiza con el brazo elevado,
la cabeza y el cuello también están incluidos en el campo de cobertura por lo que deben retirarse los objetos metálicos de cabeza y cuello y si se realiza la exploración con el brazo a lo largo del cuerpo,
el abdomen y la pelvis están incluidos en el campo de cobertura por lo que deben retirarse los objetos metálicos de abdomen y pelvis.
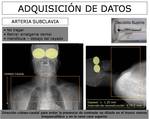
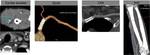
Para la angiografía obtenida por TC de la extremidad superior es necesaria una vía venosa periférica con aguja 18-20G colocada en una vena antecubital de la extremidad contralateral para evitar la alta densidad del contraste entrando en la vena ipsilateral que artefactaría la exploración (FIGURA 1).
Se prefiere una vena antecubital por los altos flujos que se precisan en esta exploración y si no es posible habrá que recurrir a la mano y reducir el caudal de inyección del contraste.
Si tampoco es accesible la mano se debe considerar la utilizacion de un catéter venoso central.
Se puede colocar al paciente en decúbito supino con la cabeza primero en el escáner y la extremidad afecta por encima de la cabeza y la extremidad contralateral a lo largo del cuerpo,
utilizar una posicion modificada del nadador con el paciente en decúbito prono o si el paciente no puede elevar la extremidad superior por encima de la cabeza puede realizarse la exploración con los brazos a lo largo del cuerpo. Se pueden utilizar cuñas para acomodar al paciente siempre que no sean muy grandes para no aumentar el FOV,
sábanas para fijar el cuerpo y esparadrapo para asegurar la posicion del antebrazo y la mano.
En nuestro centro para la exploración de toda la extremidad superior,
preferimos siempre que es posible la posición modificada del nadador.
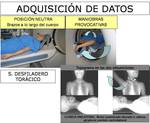
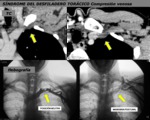
En pacientes con sospecha de síndrome de desfiladero torácico se coloca al paciente en decúbito supino con la cabeza primero en el escáner y se realiza una adquisición con la cabeza y los de brazos en posicion neutra y otra adquisición con maniobra provocativa con el brazo/s sintomático/s hiperabducido/s y elevado/s por encima de la cabeza y la cabeza del paciente rotada contralateralmente para simular la maniobra de Wright.
Esta elevación de la extremidad superior no modifica el triángulo interescalénico pero estrecha los espacios costoclavicular y retropectoral menor.
Cuando se sospecha compresión venosa se puede realizar una adquisición 90 segundos despues del inicio de la inyección de contraste con maniobras posturales.
Si se precisa explorar las dos extremidades puede realizarse simultáneamente o por separado.
Por ejemplo en pacientes con sospecha de síndrome de martillo hipotenar se pueden explorar simultáneamente ambos antebrazos y ambas manos.
ADQUISICIÓN
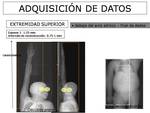
Topograma AP y lateral: Para decidir el campo de cobertura (FIGURA 2 y 3).
En los pacientes con síndrome de desfiladero torácico debe obtenerse un topograma en AP y lateral para cada una de las adquisiciones (en posición neutra y con maniobras) (FIGURA 4).
Campo de cobertura:
Para obtener una arteriografía mediante TCMD de toda la extremidad superior con el paciente en decúbito supino o decúbito prono con la extremidad superior elevada por encima de la cabeza,
el campo de cobertura comienza justo por debajo del arco aórtico y se extiende en dirección caudocraneal hasta los dedos.
Si el paciente está en decúbito supino con el brazo a lo largo del cuerpo,
el campo de cobertura comienza en el desfiladero torácico y se extiende hasta los dedos en dirección craneocaudal.
Si solo se quiere explorar las arterias subclavia o axilar puede realizarse la exploración con el paciente en decúbito supino con las extremidades a lo largo del cuerpo y el campo de cobertura desde debajo de mandíbula hasta debajo de cayado aórtico en dirección craneocaudal para evitar la presencia de contraste no diluído en el tronco venoso braquiocefálico y la vena cava superior.
En la sospecha de síndrome de desfiladero torácico,
en la adquisición en posición neutra el campo de cobertura se extiende en dirección craneocaudal desde suelo de la órbita hasta debajo del cayado aórtico y en la adquisición con maniobras en dirección craneocaudal desde mandíbula hasta por debajo del cayado aórtico.
Para realizar venografía indirecta mediante TCMD,
el campo de cobertura debe incluir las venas periféricas y centrales hasta la unión cavoauricular.
Cuando el paciente está en decúbito supino con la extremidad elevada se realiza la adquisición en dirección craneocaudal y si la extremidad está a lo largo del cuerpo en dirección caudocraneal.
Es necesario que el paciente no respire si en el scan se incluye el tórax. Si se sospecha tromboembolismo cardiogénico,
se podría realizar además TC cardiaco con sincronización ECG.
Serie sin contraste: se puede utilizar en pacientes politraumatizados para valorar la presencia de hematoma mural y cuerpos extraños o para decidir el campo de cobertura y el sitio apropiado para colocar el cursor de seguimiento del bolo (ROI).
La mayoría de la información se puede obtener con un protocolo de baja dosis,
limitando la exposición a radiaciones ionizantes.
Se puede realizar con un campo de cobertura idéntico al de la adquisición angiográfica o limitarse a la región de interés.
Inyección monofásica de contraste yodado de alta concentración (350-370 mg/mL).
Si queremos explorar toda la extremidad superior inyectamos 80-100 cc de contraste con una caudal de 3-4 cc/s.
En las exploraciones de SDT (o si solo queremos valorar arteria subclavia o axilar) inyectamos 40-50 cc de contraste a 4 cc/s en cada adquisición.
La utilización de contraste de alta concentración nos permite reducir la velocidad de la inyección y el volumen de contraste. Inyectamos salino inmediatamente después de la inyección de contraste para empujar la columna de constraste desde las venas del brazo a la circulación,
mejorar la opacificación arterial,
reducir la cantidad de contraste necesaria y reducir el los artefactos venosos.
Serie en fase arterial: El tiempo de tránsito del contraste desde la inyección intravenosa hasta la llegada a las arterias varia de unos individuos a otros por ejemplo en relación con el gasto cardiaco,
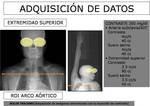
por ello el tiempo de tránsito debe determinarse en cada paciente utilizando la técnica de bolus tracking (FIGURA 5).
El bolus tracking nos permite controlar la atenuación de las arterias en tiempo casi real y una vez que el vaso de referencia alcanza un determinado umbral de opacificación activamos la exploración.
Para las exploraciones de toda la extremidad superior y del síndrome del desfiladero torácico colocamos el ROI en el cayado aórtico y en nuestro centro preferimos utilizar la técnica del bolus tracking manual frente al automático.
En la arteriografía obtenida por TC se suele programar una serie en fase retardada de toda la extremidad o del antebrazo y la mano que se inicia inmediatamente después de la fase arterial inical si no se han opacificado las arterias de la mano o del antebrazo en la primera adquisición.
También se puede programar serie en fase venosa (flebografía indirecta) con un retraso empírico de 40 s desde que termina la exploración en fase arterial en pacientes con sospecha de enfermedad oclusiva venosa,
vasculitis,
masa vascular o hemorragia.
Parámetros de reconstrucción:
Los conjuntos de datos se reconstruyen cada 0.8 mm a 1.0 mm de espesor. Sin embargo,
en la evaluación del arco palmar y las arterias digitales puede ser necesaria mayor resolución espacial (espesor de 0.5 mm e intervalo de reconstrucción de 0.3 mm).
Las principales limitaciones de la TCMD son la insuficiencia renal y la intolerancia al yodo.
POSTPROCESADO
Se deben concocer los principios básicos de las técnicas de postprocesado para comprender mejor sus limitaciones (FIGURA 6).
- Cortes axiales: permiten obtener una idea inicial de todo el territorio vascular y evaluar posible patología extravascular.
También se pueden analizar en un segundo tiempo para confirmar lesiones visualizadas en 2D o 3D.
Permiten valorar la presencia de calcificaciones,
placas de ateroma,
trombo mural,
manguito perivascular y colecciones de vecindad.
- MIP: son las imágenes más parecidas a las de la arteriografía por lo que es una técnica adecuada para transmitir los resultados al médico peticionario y para planificar el tratamiento.
Si en el plano estudiado existe otro material de alta densidad como hueso,
calcio o metal,
se proyecta superpuesto a las estructuras vasculares y las oculta,
por lo que para obtener imágenes MIP de calidad es necesario eliminar el hueso y esto consume tiempo y puede provocar falsas lesiones por la eliminación inadvertida de un vaso situado en la vecindad de un hueso.
- MPR: incluyen información sobre los tejidos adyacentes y permite visualizar la pared de la arteria.
Como los vasos no tienen un curso coplanar MPR no resulta útil y por ello se utiliza RCP que estira la totalidad de la línea media del vaso en una imagen 2D.
Son útiles para analizar vasos que muestran gruesas calcificaciones y la luz de los stents ya que en esos casos las reconstrucciones MIP y VR no sirven porque la luz queda oculta por la placa calcificada o el stent.
- 3DVR : Permiten obtener información rápida y de calidad sobre la anatomía vascular,
variantes anatómicas,
tortuosidad vascular,
áreas de obstrucción y circulación colateral.
La rotación interactiva permite visualizar el curso completo de los vasos en diferentes ángulos sin necesidad de eliminar las estructuras óseas.
Sus inconvenientes son que no representa arterias de pequeño calibre,
sobreestima estenosis y visualiza de forma incompleta los vasos con calcificaciones parietales.
En el síndrome del desfiladero torácico,
RCP permite evaluar el grado de compresión arterial inducida por la hiperabducción en comparación con las dimensiones de la arteria en las imágenes obtenidas en posición neutra y 3DVR permite analizar las relaciones de la arteria con las estructuras óseas y planificar el tratamiento.
La eliminación de la clavícula con las herramientas de eliminación de hueso permite ver el punto de compresión arterial entre la clavícula y la primera costilla.
ANATOMÍA Y VARIANTES ANATÓMICAS
La arteria innominada es la primera arteria que se origina del arco aórtico izquierdo y da lugar a la arteria subclavia derecha.
La arteria subclavia izquierda surge directamente desde el arco aórtico justo distal a la arteria carótida común izquierda.
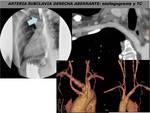
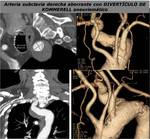
Existen variantes anatómicas en el arco aórtico como el arco aórtico izquierdo con una arteria subclavia derecha aberrante que constituye la anomalía vascular congénita más común del arco aórtico y se encuentra en un 0.5-2% de la población (FIGURA 7).
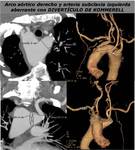
También podemos encontrar un arco aórtico derecho con arteria subclavia izquierda aberrante en 0.05-1% de la población (FIGURA 8).
Las arterias subclavias se dividen en 3 segmentos,
cada uno de los cuales pueden exhibir una patología específica.
Las principales ramas de la arteria subclavia son la arteria vertebral,
la arteria mamaria interna,
los troncos tirocervical y costocervical y la arteria escapular dorsal,
que proporcionan importantes vías de circulación colateral.
También podemos encontrar variantes anatómicas en el origen de estas ramas.
Lo más frecuente es encontrar una arteria vertebral izquierda con origen desde el cayado aórtico,
pero en ocasiones observamos otras anomalías (FIGURA 9).
La arteria axilar se extiende desde el margen lateral de la primera costilla hasta el margen inferior del músculo redondo mayor.
La arteria braquial se extiende desde el borde lateral del músculo redondo mayor a la fosa antecubital,
donde se divide en las arterias radial y cubital.
Se puede ver duplicación de la arteria braquial como variante anatómica.
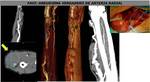
La arteria interósea surge de la arteria cubital. Las arterias radial y cubital pueden tener orígenes altos aberrantes y surgir desde las arterias axilar o braquial (el origen alto de la arteria radial se ve en 14% de autopsias y el origen alto de la arteria cubital es más infrecuente) (FIGURA 10).
Las arterias cubital y radial rellenan el arco palmar superficial y profundo,
respectivamente.
Ambos arcos palmares suelen estar en continuidad con la arteria contralateral a través de pequeñas ramas.
Se habla de arco incompleto cuando no hay continuidad de la arteria radial con el arco superficial y falta de aporte de la arteria cubital a los dedos pulgar e indice (se ve en 20% de población).
El sistema venoso superficial de disposición subcutánea drena en la vena profunda axilar.
Las venas cefálica y basílica van a lo largo de los aspectos lateral y medial del antebrazo y el brazo respectivamente y están unidas por la vena cubital mediana.
Las venas del sistema venoso profundo se sitúan intramuscularmente,
profundas a la fascia superficial y acompañando a las arterias de las extremidades.
En la mano,
el antebrazo y la parte superior del brazo,
las venas profundas se duplican y en axila y tórax son únicas.
En el antebrazo,
las principales venas profundas son las venas radiales,
cubitales e interóseas y en la parte superior del brazo las venas braquiales y la axilar.
En el espacio costoclavicular se produce la transición de vena axilar a vena subclavia. La vena subclavia se une a la vena yugular interna para formar el tronco venoso braquiocefálico.
Los troncos venosos braquiocefálicos derecho e izquierdo se unen para formar la vena cava superior que desemboca en la aurícula derecha.
APLICACIONES CLÍNICAS:
1.
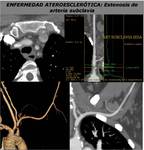
ENFERMEDAD ESTENOOCLUSIVA ATEROESCLERÓTICA
La TCMD detecta la enfermedad ateroesclerótica estenooclusiva con mejor S/E cuando se trata de estenosis severas y oclusiones,
valora la composición de la placa de ateroma,
su grado de calcificación y la presencia de ulceración,
el nº de lesiones,
localización,
morfología,
longitud y diámetro de la/s lesión/es,
el % de estenosis y los diámetros adyacentes en la zona de vaso sano,
evalúa la presencia de ateroembolias y circulación colateral,
permite planificar el tratamiento: decidir ruta de acceso y seleccionar dispositivos (balón o stent) y valorar el resultado tras la intervención (FIGURA 11).
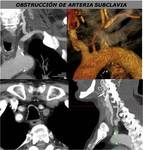
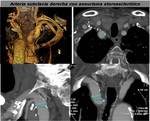
La enfermedad ateroesclerótica suele afectar al segmento proximal de arteria subclavia y con menos frecuencia a la arteria innominada.
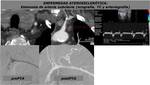
La enfermedad ateroesclerótica sintomática es más frecuente en la extremidad superior izquierda que en la derecha y la oclusión del segmento proximal de la arteria subclavia puede ser asintomática (FIGURAS 12 y 13).
Estos pacientes pueden presentar dolor de reposo,
claudicación,
pérdida de tejido,
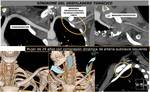
diferencia de pulsos entre las dos extremidades y síntomas neurológicos por robo de subclavia (FIGURA 14).
Además en pacientes con bypass de arteria mamaria interna a arteria coronaria una estenosis proximal de la arteria subclavia puede provocar flujo retrógrado desde el bypass durante el ejercicio y provocar un síndrome de robo coronario-subclavio y en pacientes con un bypass extraanatómico (bypass axilobifemoral) una estenosis proximal de la arteria subclavia puede conducir a la isquemia de la pierna o precipitar la trombosis del bypass.
2.
SÍNDROME DEL DESFILADERO TORÁCICO
El síndrome del desfiladero torácico es un síndrome inducido dinamicamente,
los síntomas se reproducen o exacerban con la elevación o sobreutilización de los brazos.
Suele aparecer en mujeres de 20-40 años.
El diagnostico clínico es complejo porque los síntomas son inespecíficos y los test clínicos que se realizan en la exploración pueden ser positivos en un 10-15% de sujetos normales.
Es necesario realizar pruebas de imagen que demuestren la compresión neurovascular y determinen la naturaleza y la localización de la estructura comprimida y de la estructura causante de la compresión.
La angiografía obtenida por TC es particularmente útil en la evaluation de la compresión arterial y de la relación de los vasos con las estructuras óseas adyacentes (FIGURA 15).
Resulta más complejo el diagnóstico de la compresión venosa mediante TCMD porque se observa compresión de vena subclavia con maniobras dinámicas en sujetos sanos.
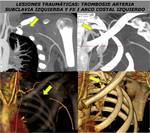
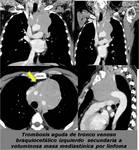
Solo se puede realizar el diagnóstico de compresión venosa cuando se observan signos indirectos como trombosis y circulación colateral (FIGURA 16 y 17).
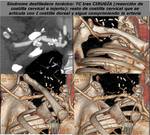
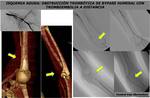
En pacientes con isquemia aguda por obstrucción arterial el tratamiento consiste en la revascularización mediante tromboembolectomía y recostrucción quirúrgica si existen lesiones arteriales oclusivas o aneurismas (FIGURA 18 Y 19).
No se debe realizar tratamiento endovascular porque esta lesiones son secundarias a una compresión extrínsea.
La trombosis venosa requiere venografía indirecta mediante TCMD o flebografía para realizar tratamiento fibrinolítico directo y la mayoría de pacientes son candidatos a descompresión quirúrgica (FIGURA 20) mediante resección de la primera costilla y/o escalenectomía supraclavicular.
3.
FÍSTULAS ARTERIOVENOSAS DE HEMODIÁLISIS
Las opciones para obtener un acceso vascular para hemodiálisis son el cateter venoso central permanente o temporal y la fístula arteriovenosa autógena o mediante injerto,
siendo preferible la fístula arteriovenosa autógena porque tiene mejor tasa de la permeabilidad a largo plazo,
menos complicaciones y menos costes.
Se puede realizar TCMD antes de realizar una fístula como mapa anatómico prequirúrgico ya que permite definir el calibre y la permeabilidad de las venas centrales,
de las arterias y venas que se van a utilizar para la derivación y de los arcos palmares nativos.
La TCMD también tiene elevada sensibilidad y especificidad en la detección de complicaciones de las fístulas arteriovenosas de hemodiálisis y permite planificar el tratamiento quirúrgico o percutáneo de esas complicaciones.
2/3 de las complicaciones se dan cerca de la anastomosis arteriovenosa,
pero la TCMD no solo detecta las complicaciones perianastomóticas sino que también detecta complicaciones situadas en otras localizaciones como arteria nutriente,
venas de drenaje o vena central.
Se debe realizar TCMD cuando disminuye el thrill a través del shunt,
existe bajo flujo arterial,
elevada presión venosa,
el flujo de la fístula en menor de 600 ml/s,
se sospecha formación de aneurisma,
estenosis,
trombosis u oclusión,
existe edema en la extremidad,
se sospecha lesión de la vena central o existe dificultad para canular la fístula.
Las complicaciones más frecuentes son:
Estenosis yuxtaanastomótica: Es la causa más común de fallo precoz de la fístula. Se define como estenosis yuxtaanatómica la que se da dentro de los 5 cm perianastomóticos. Generalmente se localiza en la vena y es secundaria a hiperplasia de la íntima (FIGURA 21).
Aneurismas verdaderos: son dilataciones que mantienen íntegra la estructura de la pared venosa o arterial.
Son más frecuentes los aneurismas venosos de fístulas autólogas de larga duración.
Por el contrario los aneurismas arteriales,
a veces de gran tamaño,
son muy poco frecuentes,
y debido a sus potenciales complicaciones deben tratarse de forma preferente mediante la resección del aneurisma y reconstrucción arterial (FIGURA 22).
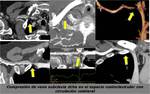
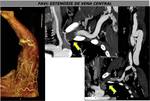
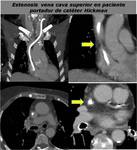
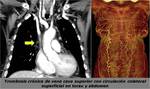
Estenosis/obstrucción de vena central generalmente causada por catéteres que ha portado el paciente antes de la realización de la fístula y menos frecuentemente secundaria a síndrome del desfiladero torácico (FIGURA 23).
Se puede localizar en vena subclavia,
tronco venoso braquiocefálico o vena cava superior.
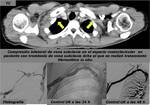
Los pacientes con acceso de hemodiálisis en la extremidad superior también pueden experimentar isquemia distal por robo del injerto y enfermedad arterial subyacente (FIGURA 24).
4.
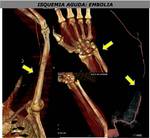
ISQUEMIA AGUDA (EMBOLIA O TROMBOSIS)
La isquemia aguda de la extremidad superior es menos común que la isquemia aguda de la extremidad inferior por la extensa circulación colateral existente en la extremidad superior.
La embolia y sobre todo la embolia de origen cardiaco es la causa más frecuente de isquemia aguda en la extremidad superior (FIGURA 25).
Otras causas potenciales de embolia son la placa ateroesclerótica en aorta o arterias proximales de la extremidad superior,
el aneurisma de arteria subclavia con trombo,
la endocarditis y la embolia paradójica.
Una cuarta parte de los casos de isquemia aguda de la extremidad superior se deben a trauma accidental o iatrogénico que provoca trombosis arterial.
Menos frecuente es la trombosis secundaria a diseccion,
rotura de placa ateroesclerótica subyacente,
síndrome del desfiladero torácico,
aneurisma o arteritis.
También puede producirse isquemia aguda por oclusión de un stent o un injerto (FIGURA 26).
Estos pacientes presentan dolor,
frialdad,
cianosis,
disminución o ausencia de pulsos y ocacionalmente déficitis motores y precisan un diagnóstico y tratamiento precoz para preservar la viabilidad de la mano.
TCMD permite valorar la localización y extensión del trombo,
detectar causas potenciales de embolia ya que se explora desde el cayado aórtico hasta las arterias digitales,
valorar enfermedad distal oculta o embolización a distancia y planificar el tratamiento quirúrgico (embolectomia,
trombectomia,
reconstrucción quirúrgica con parche o bypass) o percutáneo (trombolisis).
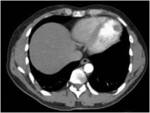
Si está incluído el tórax en la exploración se debe valorar cardiomegalia y presencia de trombo en cavidades para determinar la probabilidad del origen cardiogénico del émbolo (FIGURA 27).
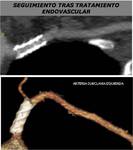
5.SEGUIMIENTO DESPUÉS DE REVASCULARIZACIÓN QUIRÚRGICA O PERCUTÁNEA
La TCMD valora el resultado de intervenciones,
la presencia de enfermedad residual y complicaciones.
Permite valorar la permeabilidad de injertos o stents (FIGURAS 26 y 28),
detectar hiperplasia intimal y trombo in situ y es especialmente útil en el postoperatorio inmediato en el que la ecografía resulta complicada
6.
ANEURISMAS
La TCMD valora el tamaño y la morfología del aneurisma,
la presencia y cantidad de trombo en el aneurisma,
la existencia de embolias a distancia,
de enfermedad estenoocluisva significativa proximal y/o distal al aneurisma y la presencia de aneurismas coexistentes (FIGURA 29 y 30).
7.
LESIONES TRAUMÁTICAS
La TCMD permite detectar y tratar precozmente las lesiones vasculares en el paciente politraumatizado,
reduciendo su morbimortalidad y a diferencia de la arteriografía,
define las lesiones vasculares en relación con fracturas óseas o lesiones de partes blandas adyacentes (FIGURA 31). Las lesiones vasculares más frecuentes son compresión o desplazamiento arterial,
hemorragia,
pseudoaneurisma,
disección,
trombo intraluminal,
vasoespasmo,
hematoma intramural,
laceración,
transección,
fístula arteriovenosa o s.compartimental.
Ante un paciente con pulsos distales disminuidos o ausentes,
soplo,
hematoma expansivo o masa pulsátil se debe realizar TCMD que permite realizar el diagnóstico y decidir la mejor opción terapéutica.
Ante un segmento sin contraste es difícil distinguir entre vasoespasmo y oclusión traumática (FIGURA 32) y ante un retorno venoso precoz asimétrico hay que diferenciar hiperemia y fístula arteriovenosa.
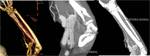
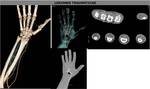
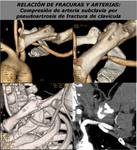
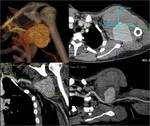
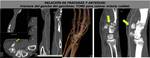
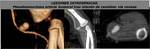
La TCMD también resulta útil para detectar complicaciones vasculares tardías secundarias a fracturas (FIGURA 33) o luxaciones traumáticas (FIGURA 34) y para valorar lesiones arteriales en pacientes con fractura del hueso del ganchoso en los que la lesión asociada de arteria o nervio cubital tiene una clínica similar (FIGURA 35).
8.
LESIONES IATROGÉNICAS
Secundarias a diferentes procedimientos como arteriografías o accesos venosos (FIGURA 36).
9.
ARTERITIS O PROCESOS INFLAMATORIOS
La arteritis de Takayasu y la arteritis de células gigantes afectan a arterias de mediano y gran calibre.
La tromboangeítis obliterante (enfermedad de Buerger) y la enfermedad de Behcet pueden afectar a arterias de pequeño o mediano calibre,
además de las venas de la extremidad superior.
La vasculitis de pequeños vasos que pueden afectar a las extremidades superiores son la artritis reumatoide,
síndrome de Sjogren,
granulomatosis de Wegener,
poliarteritis nodosa,
esclerodermia,
lupus eritematoso sistémico,
polimiositis,
dermatomiositis y enfermedades mixtas del tejido conjuntivo.
Los pacientes con vasculitis presentan síntomas constitucionales junto con signos de isquemia arterial como fenómeno de Raynaud y marcadores inflamatorios celulares elevados.
Los hallazgos en la TCMD incluyen el engrosamiento de la pared con o sin cambios inflamatorios adyacentes,
estenosis focal corta o segmentaria larga,
oclusiones focales o en tándem,
aneurismas y
pseudoaneurismas (FIGURA 37).
En la tromboangeítis obliterante se pueden ver además arterias colaterales "en sacacorchos". Además la TCMD permite excluir lesiones proximales concomitantes y otras patologías arteriales.
10.
MALFORMACIONES VASCULARES
Aunque para el estudio de las malformaciones vasculares preferimos la angioRM por su capacidad para realizar estudios dinámicos,
la TCMD permite obtener un mapa vascular de la malforación,
evaluar estructuras irrigadas por los mismos vasos que la malformación y valorar el resultado tras la embolización.
Puede ser necesario realizar una fase retardada para definir con mayor precisión las malformaciones venosas o venolinfáticas.
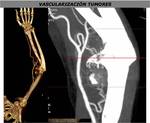
11.EVALUAR LA VASCULARIZACIÓN DE TUMORES
La TCMD permite evaluar la vascularización de tumores para planificar la cirugía y/o embolización y es particulamente útil en lesiones complejas con múltiples aportes arteriales.
Analiza el aporte vascular arterial,
el drenaje venoso,
la extensión a tejidos adyacentes y la proximidad de estructuras vecinas con las que comparte aporte sanguineo (FIGURA 38).
12.
MAPEO VASCULAR: RECONSTRUCCIÓN QUIRÚRGICA CON COLGAJOS
En la reconstrucción quirúrgica con "colgajo libre" se puede realizar TCMD en la extremidad donante y en la receptora para planificar el procedimiento quirúrgico,
garantizar la viabilidad del colgajo y evitar la isquemia.
En la extremidad donante se debe realizar TCMD de toda la extremidad (desde el arco aórtico hasta las arterias digitales) para evaluar la permeabilidad y calibre de las arterias,
la permeabilidad de posibles vías colaterales (arco palmar),
detectar variantes normales (origen alto de arterias radial o cubital) y enfermedad arterial o fibrosis perivascular.
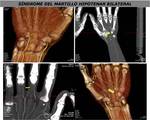
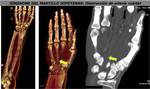
13 SÍNDROME MARTILLO HIPOTENAR
El Síndrome del Martillo Hipotenar está causado por un traumatismo repetido de la arteria cubital y del arco palmar contra el gancho del hueso ganchoso.
El impacto repetido provoca hiperplasia de la íntima,
estenosis y oclusión o la formación de un aneurisma sacular o fusiforme que se puede trombosar.
La trombosis de la arteria aneurismática puede provocar microembolias a distancia.
Se suele dar en varones con un trabajo o algun hobby que conlleva traumatismo repetitivo en las manos.
Suelen presentar intolerancia al frio,
dolor en la palma de la mano,
S.
Raynaud,
isquemia y entumecimiento en 4º-5º dedos de la mano.
Los hallazgos de la exploración fisica son los mismos que los de pacientes con compresón del nervio cubital y la angiografía obtenido por TCMD es la prueba de elección para valorar lesiones arteriales (FIGURAS 39 y 40).
14.
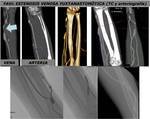
ENFERMEDAD OCLUSIVA VENOSA
Afecta más frecuentemente al sistema venoso profundo y provoca edema,
dolor,
debilidad y palidez en la extremidad.
Puede ser primaria o secundaria.
La trombosis primaria ocurre espontáneamente en pacientes con trombofilia y/o compresión extrínseca (S.
Paget-Schroetter) y ya hemos visto algunos ejemplos al explicar el síndrome del desfiladero torácico.
La trombosis secundaria se debe a factores externos como dispositivos intravenosos (FIGURA 41),
tumores (FIGURA 42),
anticonceptivos orales,
cirugía,
embarazo,
puerperio e inmovilización prolongada.
Se suele realizar ecografía en un primer tiempo y a continuación se puede realizar flebografía indirecta mediante TC que identifica la presencia de trombo,
determina si es oclusivo o no,
demuestra estenosis u oclusiones crónicas (FIGURA 43).
y puede detectar alguno de los factores de riesgo.