El Sarcoma de Ewing (SE) es un tumor de células redondas de alto grado que comparte características histológicas y rasgos cromosómicos con un espectro de neoplasias neuroectodérmicas (tumor neuroectodérmico primitivo -PNET-,
tumor de Askin y neurooepitelioma),
actualmente englobadas junto al sarcoma de Ewing óseo y extraóseo bajo el término tumores de la familia del Sarcoma de Ewing.
Citogenéticamente,
comparten una anomalía cariotípica consistente en una traslocación que afecta a los cromosomas 11 y 22 (1).
El SE oseo representa el 2º tumor primario óseo maligno más frecuente en niños y adolescentes,
y el 4º tumor maligno primario óseo más frecuente en la población general.
Es más frecuente en las 3 primeras décadas (entre los 4 y los 25 años).
Característicamente afecta a región metafisodiafisaria de huesos largos,
con predominio proximal. La afectación ósea,
en orden decreciente de frecuencia,
es la siguiente: fémur,
iliaco,
tibia,
húmero,
peroné,
costillas y sacro (2).
En contraste,
la mitad o más de los casos de SE de diagnóstico en la edad adulta son extraóseos (SEEO) (3).
El manejo actual es multidisciplinar,
jugando los métodos de imagen un papel clave en el diagnóstico,
así como en dirigir la biopsia,
planificar la cirugía y detectar diseminación a distancia o recidivas locorregionales.
Las técnicas de imagen permiten además evaluar la respuesta al tratamiento,
siendo la la RM la modalidad de elección,
y en especial los estudios de perfusión,
que como se expondrá más adelante permiten cuantificar el grado de necrosis que se correlaciona histológicamente con respuesta favorable.
El tratamiento actual se basa en quimioterapia (QT) sistémica neoadyuvante multiciclo multiagente con el doble fin de reducir la carga tumoral y tamaño del tumor primario con vistas a cirugía más conservadora (preservación de extremidades) y de erradicar las potenciales micrometastasis (4,5).
La respuesta positiva a la QT se correlaciona con tasas de supervivencia a los 5 años de casi el doble que en los no respondedores,
y además es un factor pronóstico para el control local (6),
que incluye resección,
radioterapia (RT) o ambas.
El tratamiento QT incluye QT neoadyuvante (antes del control local) y adyuvante (después) durante aproximadamente 6 meses a un año (1).
No entraremos en detalle en los fármacos empleados al considerar que excede el objetivo de este trabajo.
La respuesta negativa,
por otra parte,
predispone a recurrencia,
pero esta tendencia puede revertirse con QT pre y postoperatoria más agresiva con mayor supervivencia libre de enfermedad (6).
El papel por tanto de la imagen en la evaluación de la respuesta al tratamiento tiene importante implicación pronóstica y de manejo.
I-DIAGNÓSTICO
LOCAL: (Table 1)
1.
SARCOMA DE EWING ÓSEO.
El diagóstico puede ser sugerido por imagen: lesión de características agresivas en región metadiafisaria de huesos largos de adolescentes o adultos jóvenes con masa de partes blandas asociada,
generalmente circunferencial excéntrica en torno al hueso afecto.
Anatomopatológicamente,
puede tener áreas de hemorragia o necrosis ,
no siendo frecuente que la necrosis sea extensa antes del tratamiento,
si bien cuando está presente se ha descrito como factor de mal pronostico (7).
La destrucción cortical ósea puede ser extensa,
si bien es posible la comunicación entre el el canal medular y el componente de partes blandas mediante permeación del sistema de canales corticales haversianos y a través de canales neurovasculares (1,8).
Es posible la formación de hueso nuevo dentro del hueso desvitalizado en el canal medular (1).
RX SIMPLE
Útil para valora la agresividad,
plantear el diagnóstico diferencial,
y ver fracturas patológicas (5).
Hallazgos:
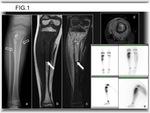
-Más frecuente: Destrucción ósea con patrón moteado o permeativo y márgenes pobremente delimitados (zona de transición amplia) (Fig. 1).
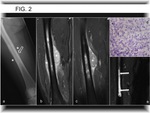
A veces sutil y predomina la masa de partes blandas (Fig. 2).
-15% de los casos: patrón geográfico con zona de transición amplia (1).
-La reacción perióstica es frecuente,
generalmente agresiva multilaminada (capas de cebolla) o espiculada (rayos de sol,
púas de peine).
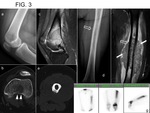
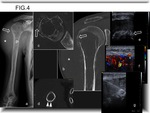
(Fig. 1) (Fig. 3) (Fig. 4).
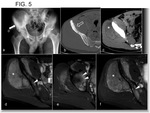
-Componente escleroso (hasta 40%),
más frecuente en el componente intraóseo y en lesiones de huesos planos (1),
de apariencia osteoide (Fig. 5).
-Existen manifestaciones atípicas como la localización perióstica,
la erosión cortical extrínseca o el defecto diafisario con aplanamiento (“saucerization”),
y la calcificación de partes blandas (Fig. 2) (1,8).
TAC
Útil en la valoración de destrucción de hueso cortical,
y en la demostración de reacción perióstica fina y mineralización tumoral (5) .Muestra la diferencia entre esclerosis resultante de aposición de nuevo periostio o esclerosis tumoral directa (Fig. 5) (9).
Hallazgos:
-Destrucción ósea agresiva y gran masa de partes blandas con atenuación similar al músculo que rodea a la afectación ósea,
a menudo circunferencial asimétrica (Fig. 4) (Fig. 5).
-A veces existe afectación cortical sutil que premite comunicación entre los componentes intraóseo y de partes blandas en forma de canales lineales de baja atenuación extendiéndose a través de la cortical densa (30% de los casos)(Fig. 3)(Fig. 4); o incluso el córtex puede aparecer intacto sin evidencia de comunicación entre los 2 componentes en 17% de los casos (1) .
Comportamiento tras la administración de contraste yodado:
- Realce postcontraste frecuente,
difuso o periférico (1).
RM
Útil para determinar la extensión medular y extramedular; determinar la extensión a fisis,
compartimentos musculares adyacentes y estructuras neurovasculares,
datos importantes de cara a cirugía de preservación de extremidades (5,10).
Protocolo:
En la literatura existe un relativo acuerdo en emplear al menos las siguientes secuencias (Table 2) en la realización de RM convencional:
- T1 longitudinal al eje largo del hueso,
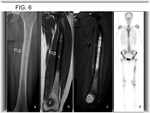
que muestra correlación con anatomía patológica en cuanto a extensión a médula ósea y detección de metástasis óseas en el mismo hueso separadas por médula ósea normal (skip metastasis) (5) (Fig. 3 y Fig. 6),
y permite valorar la relación con articulación.
La relativa buena delimitación del borde de infiltración tumoral con la médula ósea normal en secuencias potenciadas en T1 se ha descrito como rasgo característico del SE en el diagnóstico diferencial con osteomielitis (11) (Fig. 1). Puede realizarse también secuencia STIR siguiendo el eje longitudinal del hueso,
muy sensible al edema óseo.
- T2,
preferentemente con saturación de la grasa,
en plano axial: para diferenciar entre extensión intra y extracompartimental,
visualizar la interfase entre el tumor y partes blandas adyacentes y la relación con estructuras neurovasculares (5).
- T1 con supresión grasa tras la dministración de gadolinio intravenoso (estudio postcontraste “estático” tardío) ,
para la demarcación del tumor de las lesiones peritumorales.
Hallazgos:
-Reemplazamiento medular,
destrucción cortical y masa de partes blandas (Fig. 1) (Fig. 2) (Fig. 3) (Fig. 5).
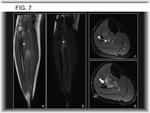
-Destrucción cortical sutil en forma de canales de intensidad de señal intermedia surcando el cortex hipointenso en 74% de los casos (Fig. 7).
- en 4% casos el cortex aparece intacto (1).
Características de señal:
Intensidad de señal homogénea e intermedia en secuencias potenciadas en T1.
En T2,
señal homogénea,
hipointensa a intermedia (relacionada con la alta celularidad tumoral) (Fig. 7).
La heterogeneidad y alta señal en secuencias de TR largo es más frecuente en lesiones más grandes (Fig. 2) (Fig. 5) y representan hemorragia o necrosis (1).
Los niveles líquido-líquido en relación con hemorragia son más frecuentes post-tratamiento.
Comportamiento tras la administración de contraste paramagnético:
-Realce postcontraste frecuente,
difuso (Fig. 2) o periférico que se ha descrito como nodular (1),
aunque en nuestra experiencia la captación periférica puede ser más lineal o peor definida (Fig. 3) (Fig. 5).
Se ha descrito el uso de secuencias dinámicas de alta resolución temporal post-contraste (RM PERFUSIÓN) para diferenciar el tumor del edema no-neoplásico e indicar el lugar óptimo para biopsia (tejido tumoral viable) (5).
A veces,
las secuencias de TR largo muestran extensión de la alta intensidad de señal hasta el plano fisario o la interlínea articular planteando el diagnóstico diferencial entre extensión tumoral o edema.
El uso de este tipo de secuencias resulta últil para detectar las partes más viables del tumor ,
diferenciando el edema (sin realce) del tumor (con realce rápido),
y ayudan a determinar la verdadera extensión tumoral .
Representan además el estandar inicial para seguimiento de la actividad metabólica (12).
Nuestro protocolo,
consistente con la literatura,
consiste en realizar series de eco de gradiente T1 ultrarrápidas (resolución temporal de 3-5 segundos) repetidas cíclicamente durante al menos 4-5 minutos sobre el área a explorar,
incluyendo la parte más representativa de la masa tumoral (si no es posible su inclusión completa) con extensión intra y extraósea.
La dosis de gadolinio es de 0,1 mmol/kg,
en perfusión mediante bomba inyectora,
a flujo no inferior de 3ml/s,
seguido de bolo de suero salino.
El postproceso incluye sustracción (sustraer la primera imagen sin contraste de todas las subsiguientes imágenes postcontraste del estudio dinámico),
y obtención de curvas de intensidad de señal-tiempo con ROIs trazado por consenso entre 2 observadores .
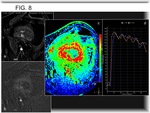
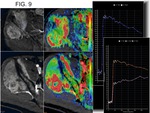
Resulta especialmente útil la codificación de color con imágenes paramétricas,
y especialmente las llamadas imágenes de “velocidad de entrada” (13),
donde las esturcturas que muestran realce rápido (arterias y tumor viable) se representan en color rojo (6) (Fig. 8).
En varias series con correlación histopatológica,
se ha descrito que los focos de tumor viable se caracterizan por captación de contraste precoz,
mayor y más rápida (5),
por aumento de la perfusión tumoral.
Se ha descrito que el realce precoz de áreas tumorales viables ocurre entre los 0-5 segundos desde la llegada del contraste a la arteria (12) (Fig. 8).
Cuanto más perfundido y viable el tumor,
más rápido será el realce y mayor la pendiente de la curva (6) (Fig. 9).
2.
SARCOMA EWING EXTRAOSEO (SEEO).
El SEEO puede presentarse virtualmente en cualquier localización de la cabeza a los pies (3),
presentándose como masas de partes blandas no específicas,
aunque característicamente sin afectación medular ósea demostrable por TAC,
RM o gammagrafía,
aunque sí puede asociar afectación ósea extrínseca (erosión,
engrosamiento cortical,
reacción perióstica agresiva o invasión ósea franca) (1).
En RM muestran apariencia heterogénea con áreas hemorrágicas,
necrosis y niveles líquido líquido.
Como hallazgo adicional,
se ha descrito la presencia de canales vasculares serpiginosos de alto flujo con baja intensidad de señal en todas las secuencias,
no específicos de este tipo de tumores (1).
--Los tumores de cabeza y cuello son poco frecuentes.
--El tumor de Askin (PNET extrapulmonar) es la localización única más frecuente de SEEO.
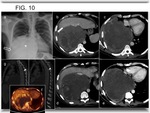
Se presentan como una gran masa de pared torácica con extensión intratorácica,
cuyo espectro de agresividad varía entre desplazamiento pulmonar y reacción perióstica ósea a invasión parenquimatosa y destrucción costal (3) (Fig. 10).
Suelen asociar gran cantidad de derrame pleural,
en muchos casos loculado (1).
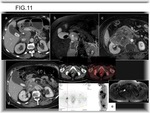
--En el abdomen,
puede tener origen en las vísceras sólidas,
siendo más frecuentes en riñón y retroperitoneo (Fig. 11).
Las masas bulky peritoneales pueden desplazar,
englobar o invadir los órganos adyacentes (Fig. 11).
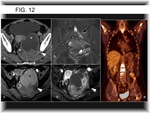
La enfermedad pélvica asocia peor pronóstico (Fig. 12) (3).
---Partes blandas y extremidades (frecuentes en región glutea,
EEII).
La presencia del hallazgo de canales hipointensos serpiginosos en una gran masa intramuscular en una persona joven debe hacer sospechar SEEO (1).
DISEMINACIÓN A DISTANCIA (Estadificación):
Las metástasis más frecuentes son pulmonares y óseas (14).
Como previamente mencionamos,
se denomina skip metástasis a la presencia de tumor en el mismo hueso que la lesión primaria pero separado por médula ósea normal (Fig. 3 y Fig. 6).
Los estudios de estadificación suelen incluir TAC (alta sensibilidad para diagnóstico de metástasis pulmonares) y gammagrafía ósea para descartar metástasis óseas (14).
El SE muestra captación en gammagrafía con TC99m y con Talio 201 (Fig. 1).
El PET muestra aumento de la captación del radionúclido en lesión primaria con valores de SUV que van desde 5,3 (sin metástasis en la presentación) hasta 11,3 (con metástasis) (1).
Los estudios de PET TAC: ha demostrado alta precisión,
sensibilidad y especificidad en el diagnóstico y reestadificación,
superior a la gammagrafía en detección de metástasis en tumores óseos y en concreto en el SE (15) (Fig. 10)(Fig. 11)(Fig. 12).
La sensibilidad del PET para la detección de metástasis óseas es incluso superior a la de la RM de cuerpo entero (14).
También se ha empleado la RM difusión de cuerpo entero con el mismo fin,
con resultados prometedores.
II-RESPUESTA AL TRATAMIENTO QT,
RT o ambos (Table 3)
La anatomía patológica es el gold standard para la evaluación de la respuesta al tratamiento.
La respuesta es favorable si <o = 10% de tumor viable (>90 de necrosis) (5,
6).
Se han descrito localizaciones santuario para tumor viable en el SE en región subperióstica,
partes blandas y compartimento intramedular (5).
RX
-Respuesta favorable: Maduración (solidificación) de la reacción perióstica,
reconstitución del hueso cortical y desarrollo de trabeculación grosera dentro del tumor necrótico intraóseo,
aumento de la esclerosis ósea y progresiva mineralización,
y reducción del componente de partes blandas (Fig. 6).
Estos cambios se inician en 3-6 meses (5),
completándose típicamente al año el tratamiento (1).
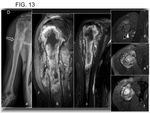
Estos hallazgos presentan variabilidad intraobservador,
no son cuantificables,
y no pueden usarse para predicción pronóstica (Fig. 13 y Fig. 14).
-La ausencia de estos hallazgos y la presencia de mayor destrucción ósea sugiere falta de respuesta favorable.
Áreas líticas de mayor distribución pueden estar en relación con oesteitis rádica.
TAC
-Respuesta favorable: La TAC permite mejor valoración de la reducción de la masa extraósea como signo de buena respuesta pero peor que la RM.
Otros signos sugestivos de buena respuesta son el reestablecimiento de planos grasos intramusculares,
el aumento de la calcificación periférica o central y la menor extensión de la afectación intramedular (5).
-Pobre respuesta si existe aumento del componente de partes blandas (Fig. 14),
destrucción ósea progresiva y aumento de la afectación medular (1,
5).
Menos frecuentemente,
la osteolisis puede ser una manifestación de necrosis tumoral,
y si el paciente ha recidivido RT puede tener osteoporosis inicial,
especialmente en el portal de radiación (6).
RM
Modalidad óptima para evaluar la respuesta al tratamiento por su mayor resolución.
-Hallazgos indicativos de respuesta favorable para sarcoma de Ewing óseo y extraóseo son:
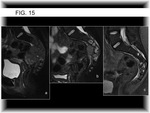
-Reducción en el tamaño del componente extraóseo (Fig. 2) (Fig. 3 y Fig. 6) (Fig. 15) ( Fig. 5 y Fig. 16) y en capsulación del mismo (desarrollo de un anillo circunferencial de baja señal) (5,
6,
16) .
-Disminución global de la señal del componente de partes blandas en imágenes potenciadas en T2 (5).
-Aumento de la intensidad de señal de la médula ósea.
Intensidades de señal similar al líquido (Fig. 2) (Fig. 6) (Fig. 16) se correlacionan histológicamente con matriz mixoide hipocelular con pequeña cantidad de fibras colágenas (5,
6).
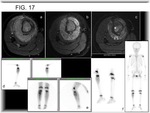
Si no es tan alta como el fluido tanto en componente intra como extraóseo puede estar en relación con tumor viable,
o bien con necrosis,
tejido fibroblástico reparativo o áreas quísticas hemorrágicas (Fig. 17) (5).
-Aumento de áreas de hemorragia o necrosis (1).
Los hallazgos descritos son indicativos de respuesta favorable pero carecen de sensibilidad para detectar más del 90% de necrosis relacionada con el tto (5).
La RM post-contraste estándar representa una adquisición tardía,
por lo que la captación puede deberse a tumor viable,
tejido necrótico revascularizado,
hiperemia reactiva,
tejido inflamatorio inmaduro,
o incluso cambios post-biopsia (5,
6).
Los estudios dinámicos con alta resolución temporal (RM PERFUSIÓN),
en cambio,
permiten cuantificar el grado de necrosis.
-Las áreas con realce rápido (<6 segundos) con mayor pendiente en las curvas intensidad de señal-tiempo han sido correlacionadas con la presencia de tumor viable, y pueden ser cuantificadas mediante ROI (1,
12).
La localización de los restos de tumor viable puede ser periférica ,
o de distribución difusa dentro de las partes blandas,
hueso cortical y regiones subperiósticas,
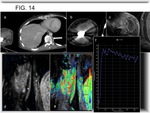
e incluso bordeando áreas necróticas en la cavidad medular. Esta técnica permite detectar nódulos de tumor viable de hasta 3-5 mm,
con limitación para la detección de tumor viable microscópico (12,
16) (Fig. 14).
Por otra parte,
se ha descrito realce precoz de vasos patológicos en área de formación de hueso nuevo subperióstica (realce precoz y rápido) (12),
sin presencia de tumor viable.
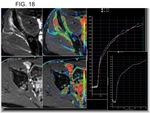
-Realces más tardíos y progresivos se correlacionan con liquefacción,
áreas quísticas,
edema,
inflamación peritumoral o regiones mixoides o cartilaginosas paucicelulares (12) ( Fig. 16 y Fig. 18).
Áreas sin realce durante toda la secuencia (generalmente centrales y bien delimitadas) se correlacionan con lagunas debidas a necrosis o degeneración mucoide (12).
Se considera respuesta favorable si sólo pequeño maguito de realce residual sin nodularidad en el estudio postcontraste (Fig. 18).
La respuesta es pobre si la reducción en tamaño es <25% y se identifican nódulos hipercaptantes > 3mm ( Fig. 13 y Fig. 14) (1,
12).
Además del análisis de la pendiente de la curva,
recientemente se ha descrito el uso de modelos framacocinéticos compartimentales para la cuantificación de necrosis postquimioterapia (13,
17) .
Se ha descrito también el uso de las secuencias de RM DIFUSION.
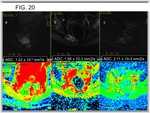
En general por su alta celularidad y la elevada relación núcleo/citoplasma,
los tumores de células redondas o azules tienen valores de ADC (coeficiente de difusión aparente) muy bajos.
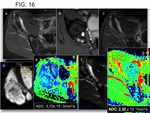
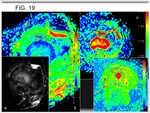
Diferentes estudios concluyen que hay diferencia en los valores de difusión entre pacientes respondedores y los que presentan baja respuesta, con aumento de los valores de ADC en el curso del tratamiento en pacientes con buena respuesta al mismo (Fig. 16) (Fig. 19) (Fig. 20).
No obstante,
la técnica empleada no es la misma, siendo necesarias aún series más amplias y mayor reproducibilidad en los resultados que permitan la estandarización (18,
19,
20).
Doppler
Limitado a la valoración del componente extraóseo.
Buena respuesta:Aumento de la resistencia periférica y reducción en desplazamiento doppler.
Pobre respuesta: disminución de la resistencia periférica y desplazamientos doppler de alta -frecuencia (1)
Gammagrafía ósea
Disminución de la captación del radionúclido en respuesta a la terapia (Fig. 17).
Puede detectar nódulos de tumor residual viable si son > 1 cm (6).
El 201Tl se correlaciona más con la necrosis tumoral,
mientras que le 99mTc puede presentar captación persistente en buenos respondedores posiblemente por curación parcial (6).
PET TAC
SUV máximo después de QT < de 2,5 asociado con mayor tiempo de supervivencia libre de enfermedad y FPP para respuesta favorables (<10% tumor viable) (21).