INTRODUCCIÓN
Los sarcomas uterinos constituyen alrededor del 2 al 5 % de todos los tumores malignos uterinos,
según las series [1,2].
Son tumores muy agresivos y de peor pronóstico que los adenocarcinomas endometriales,
con una tasa de supervivencia a 5 años menor del 35%,
ya que a diferencia de éstos presentan un comportamiento,
patrón de diseminación y manejo distintos [1,9,10].
Existen tres subtipos principales de sarcomas uterinos según su composición tisular,
ya sea epitelial,
mesenquimal o mixto (mesenquimal y epitelial) [3].
Las variantes histológicas más frecuentes son los carcinosarcomas (también denominados tumores müllerianos mixtos),
los leiomiosarcomas,
los sarcomas del estroma endometrial, y los rabdomiosarcomas.
En torno al 50 % de estos tumores corresponden a carcinosarcomas [1,
2,
3,
9].
Recientemente,
el carcinosarcoma ha sido incluido dentro de los adenocarcinomas endometriales como una forma desdiferenciada o metaplásica del mismo,
lo que ha condicionado que para ambos tumores se emplee la misma clasificación en la estadificación FIGO de la última revisión de 2009 [4,
9,
15].
No obstante,
al presentar un comportamiento más agresivo que el adenocarcinoma endometrial,
histológicamente este tumor sigue considerándose como un sarcoma según la clasificación anatomopatológica de la WHO de 2003 [5],
que no ha sido modificada.
La distinción entre los diferentes subtipos de tumores hoy en día es esencial,
ya que cada vez conocemos mejor sus mecanismos moleculares,
lo que nos permite emplear terapéuticas más dirigidas.
A pesar de que el diagnóstico final es histológico generalmente tras la histerectomía (las biopsias muchas veces son incompletas),
el diagnóstico puede sugerirse por hallazgos de la imagen [2,9].
RESULTADOS
Demografía y presentación clínica
El motivo de consulta en la práctica totalidad de los casos fue metrorragia en mujeres postmenopaúsicas.
La edad de presentación fue discretamente menor en los sarcomas uterinos,
presentándose entre los 31 y 79 años,
siendo la media de edad de 66 años.
En los adenocarcinomas,
la media de edad de presentación fue de 68 años,
con edades comprendidas entre 47 y 85 años.
Nuestros datos son similares a los descritos en la literatura,
la mayoría de casos en mujeres postmenopaúsicas con alguna excepción en mujeres menores de 40 años [5,7,8].
Hallazgos en RM
Se comparan los siguientes hallazgos radiológicos por RM en relación con los sarcomas uterinos respecto a los adenocarcinomas: edad de la paciente en el momento del diagnóstico,
dimensiones del tumor y el estadio de la FIGO. Tabla 1.
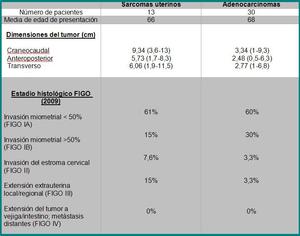
Table 1: Tabla comparativa entre sarcomas y adenocarcinomas en relación a la edad de presentación, dimensiones tumorales y estadio histológico clasificado según la FIGO.
En cuanto al tamaño,
el 77% de los sarcomas uterinos presentaron un diámetro cráneo-caudal (CC) mayor o igual a 8 cm en el momento del diagnóstico (siendo la media de 9,34 cm) en contraposición con los adenocarcinomas que presentaron un diámetro CC de 2,91 cm.
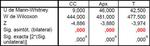
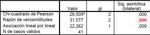
Analizamos estadísticamente estos resultados mediante el test no paramétrico de Mann-Whitney en los tres ejes siendo las diferencias entre ambos tumores estadísticamente significativas (p<0,001). Tablas 2 y 3.
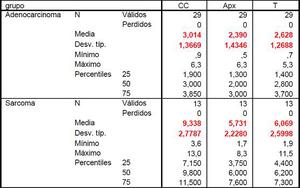
Table 2: Tabla estadística comparativa entre sarcomas y adenocarcinomas en relación a sus dimensiones.
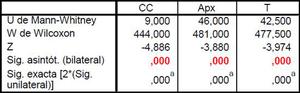
Table 3: Tabla resumen del test estadístico utilizado para comparar los dos grupos de tumores respecto a sus dimensiones medidas en los tres planos del espacio; antero-posterior, cráneo-caudal y transversal.
Por tanto los sarcomas se presentan con un tamaño mayor que los adenocarcinomas en el momento del diagnóstico,
hallazgo descrito previamente en la literatura como una característica común de estos tumores [2,
3,
5,
6,
7,
9,
11,
12].
Fig.
1
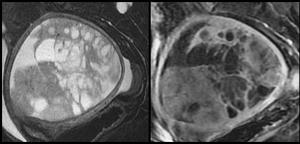
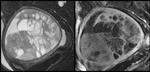
Fig. 1: Mujer de 62 años con carcinosarcoma. Figura de la izquierda: Imagen TSE potenciada en T2 con supresión grasa en proyección sagital. Se observa una gran masa endometrial heterogénea con áreas hiperintensas de aspecto quístico o necrótico y otras de aspecto sólido. Condiciona adelgazamiento e infiltración focal del miometrio. Figura de la derecha: Imagen T1 con gadolinio y supresión grasa en proyección sagital. Las áreas sólidas de la tumoración experimentan un realce similar o algo menor al del miometrio.
En la literatura,
los sarcomas presentaron una apariencia más agresiva,
visualizando masas que obliteraban la arquitectura normal uterina,
en ocasiones con márgenes mal delimitados y afectación extrauterina.
Sin embargo en nuestra serie,
la mayoría de tumores se presentaron en fases tempranas de la enfermedad,
fundamentalmente en estadios IA y IB.
Evaluamos estadísticamente las dos series no hallando diferencias estadísticamente significativas entre ambos grupos mediante un test de chi-cuadrado (p <0,093).
En las series publicadas generalmente estos tumores se presentan en estadios más avanzados,
si embargo en la nuestra no ha sido así,
presentándose ambos tumores en estadios tempranos de la enfermedad.
Además comparamos nuestros resultados de estadificación mediante RM y los obtenidos en el diagnóstico histológico postquirúrgico observando resultados dispares.
En líneas generales hubo concordancia entre nuestra estadificiación y la de anatomía patológica.
En algún caso infraestimamos la extensión tumoral (en un caso con mínima cantidad de líquido peritoneal no visto mediante RM resultó presentar carcinomatosis peritoneal y lo catalogamos de IB) y en otros sugerimos invasión profunda miometrial cuando en el examen histológico se catalogaron de IA.
 Respecto a su señal en secuencias potenciadas en T2,
el 92% de los sarcomas mostraban una señal heterogénea predominantemente hiperintensa.
Se hallaron mediante un test estadístico chi-cuadrado diferencias significativas respecto a la señal de los adenocarcinomas (p<0,001),
que presentaban globalmente una señal más baja en T2.
Tablas 4 y 5.
Respecto a su señal en secuencias potenciadas en T2,
el 92% de los sarcomas mostraban una señal heterogénea predominantemente hiperintensa.
Se hallaron mediante un test estadístico chi-cuadrado diferencias significativas respecto a la señal de los adenocarcinomas (p<0,001),
que presentaban globalmente una señal más baja en T2.
Tablas 4 y 5.
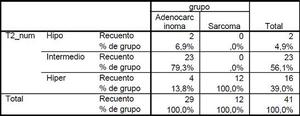
Table 4: Tabla estadística comparando si existen diferencias entre sarcomas y adenocarcinomas en relación a su señal en secuencias potenciadas en T2.
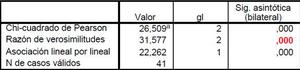
Table 5: Tabla mostrando el test estadístico empleado para demostrar si existen diferencias significativas entre ambos tumores en secuencias potenciadas en T2.
En secuencias potenciadas en T1,
el 85% de las lesiones eran hipointensas.
Solo dos lesiones mostraron una señal diferente en esta secuencia: una de las lesiones mostró una señal intermedia en T1 (que correspondió con un sarcoma del estroma endometrial) y la otra era heterogénea predominantemente hipointensa en T1 con áreas periféricas hiperintensas (que correspondió a un leiomiosarcoma).
De los adenocarcinomas,
la mayoría presentaron una señal intermedia en T2 salvo tres de los 30 casos que presentaron una señal más heterogénea e hiperintensa en secuencias potenciadas en T2.
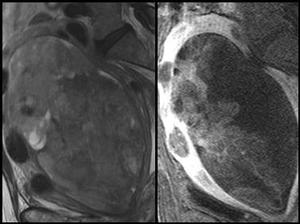
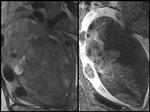
Fig. 2: Paciente de 63 años con carcinosarcoma uterino. Figura de la izquierda: Imagen TSE potenciada en T2 con supresión grasa en proyección sagital. Se observa una gran masa endometrial heterogénea con áreas hiperintensas. Figura de la derecha: Imagen potenciada en T1 con gadolinio y supresión grasa en proyección sagital. La tumoración experimenta un realce heterogéneo menor que el del miometrio. Además de esta gran masa se identifican otras lesiones miometriales hipointensas en T2 que corresponden a miomas.
En el estudio dinámico potenciado en T1 tras la administración de gadolinio,
el 64% de los sarcomas presentó realce heterogéneo e isotenso respecto al miometrio en fases tardías,
siendo en el 36% de los casos el realce heterogéneo e hiperintenso con respecto al miometrio,
también en fases tardías.
En dos de los casos no se realizó estudio con contraste.
Los adenocarcinomas por el contrario se mostraron hipointensos respecto al miometrio en el estudio postcontraste.
Figs.
2 y 3.
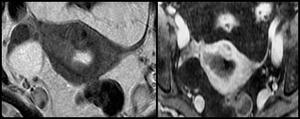
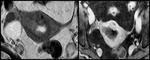
Fig. 3: Mujer de 57 años con adenocarcinoma endometrial. Figura de la izquierda: Imagen TSE potenciada en T2 en proyección coronal. Muestra una lesión endometrial hipo-isointensa en T2 con invasión miometrial. Figura de la derecha: Imagen potenciada en T1 con gadolinio y supresión grasa en proyección coronal. La tumoración no realza de forma significativa en el estudio postcontraste.
Para valorar si existen diferencias en el realce entre ambos grupos distribuimos el patrón de realce en hipointenso respecto al miometrio o hiperintenso respecto a éste.
Los tumores con un patrón de realce isointenso respecto al miometrio se incluyeron en el grupo de hiperintensos.
En el análisis estadístico observamos que existen diferencias significativas en cuanto al patrón de realce entre ambos tumores (p<0,001).
Tablas 6 y 7.
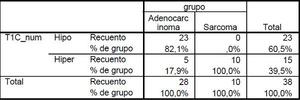
Table 6: Tabla estadística mostrando si existen diferencias entre sarcomas y adenocarcinomas en secuencias potenciadas en T1 con gadolinio.


Table 7: Tabla estadística mostrando el test estadístico utilizado para demostrar si existen diferencias significativas entre ambos tumores en secuencias potenciadas en T1 con gadolinio.
Los resultados en relación con el realce de estos tumores tras la administración de gadolinio son variables según las series,
si bien los autores en general están de acuerdo en que los sarcomas presentan realce mayor o igual que el miometrio en contraposición con los adenocarcinomas [1,
2,
3,
6,
9,
11,
13].
La variabilidad hallada puede deberse a que estos tumores presentan histológicamente varias estirpes celulares distintas por lo que su realce dependerá del componente predominante del tumor (epitelial,
mesenquimal o mixto).
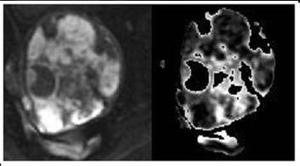
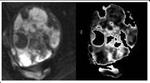
Fig. 4: Mujer de 63 años con carcinosarcoma. Figura de la izquierda: Imagen potenciada en difusión en proyección sagital. Se aprecia una gran masa intrauterina heterogénea con áreas marcadamente hiperintensas. Figura de la derecha: mapa paramétrico del ADC en escala de grises. Las áreas hiperintensas se muestran marcadamente hipointensas traduciendo restricción de la difusión.
En las secuencias potenciadas en difusión se estudiaron 10 casos diagnosticados como sarcomas y 22 casos diagnosticados como adenocarcinomas por anatomía patológica.
Los sarcomas mostraron valores de ADC muy dispares dentro de la misma tumoración debido a la heterogenicidad de los mismos,
identificando áreas con restricción y otras con difusión facilitada (áreas que parecían corresponder con zonas de necrosis en las secuencias potenciadas en T2). Respecto a las zonas que subjetivamente mostraron mayor restricción en el mapa ADC,
los valores obtenidos (en regiones de interés con un diámetro similar) mostraron una media de 7,608 x 10-3 (5,52 x 10-3 - 9,24 x 10-3).
Figs.
4 y 5.
Los adenocarcinomas presentaron restricción de la difusión de las lesiones de una forma más homogénea,
si bien los valores obtenidos fueron similares.
En 8 de los 30 casos con anatomía patológica de adenocarcinoma,
y en 3 de los 13 casos no fue posible evaluar esta secuencia ya que no estaba incluida en sus respectivos estudios.
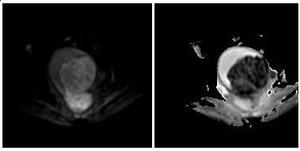
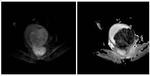
Fig. 5: Mujer de 54 años con diagnóstico de carcinosarcoma. Figura de la izquierda: Imagen potenciada en difusión en proyección axial. Se observa una gran masa intrauterina predominantemente hiperintensa. Figura de la derecha: mapa paramétrico del ADC en escala de grises. La tumoración experimenta una marcada pérdida de señal debido a la restricción de la difusión.
Pocos estudios han aportado datos sobre la imagen de RM potenciada en difusión de estos tumores.
En nuestra serie observamos que estos tumores muestran áreas con gran restricción de la difusión (similar a los adenocarcinomas) y otras áreas sin restricción (probablemente correspondientes a zonas necróticas).
Los resultados que se extrapolan de esta secuencia pueden explicarse dada la naturaleza mixta y heterogénea de estos tumores [2,
9,
13].
En conclusión,
nuestro estudio es uno de los pocos descritos en la literatura sobre las características por RM de estos tumores y aporta datos concordantes con los pocos estudios publicados en la literatura al respecto.
Por los resultados obtenidos pensamos que esta técnica de imagen puede ayudar a sugerir el diagnóstico de estos tumores y tener repercusión en el manejo de las pacientes.
[2,
3,
6,
7,
8,
9,
11].
Limitaciones del estudio
Las limitaciones de nuestro estudio incluyen su diseño retrospectivo,
el tamaño muestral,
y la posibilidad de pequeñas variaciones en los protocolos de RM durante el período en que se realizaron (10 años).
Sin bien la baja incidencia de estos tumores puede justificar la difícil realización de un estudio prospectivo.











 Respecto a su señal en secuencias potenciadas en T2,
el 92% de los sarcomas mostraban una señal heterogénea predominantemente hiperintensa.
Se hallaron mediante un test estadístico chi-cuadrado diferencias significativas respecto a la señal de los adenocarcinomas (p<0,001),
que presentaban globalmente una señal más baja en T2.
Tablas 4 y 5.
Respecto a su señal en secuencias potenciadas en T2,
el 92% de los sarcomas mostraban una señal heterogénea predominantemente hiperintensa.
Se hallaron mediante un test estadístico chi-cuadrado diferencias significativas respecto a la señal de los adenocarcinomas (p<0,001),
que presentaban globalmente una señal más baja en T2.
Tablas 4 y 5.







