DIAGNOSTICO POR NEUROIMAGEN
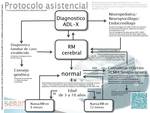
ALGORITMO DE MANEJO DIAGNOSTICO-TERAPÉUTICO [i]
[i]
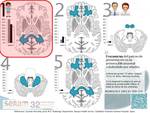
La complejidad de la enfermedad (las presentaciones de los diferentes fenotipos no son definitivas pudiendo ocurrir cambios a veces de rápida evolución para los que hay que estar muy alerta con una vigilancia rigurosa) hace necesario una actuación interdisciplinar (incluyendo disciplinas pediátricas como la neurología,
endocrinología,
nutrición,
psiquiatría infantil,
y apoyo social a las familias) para intentar mejorar la calidad de vida de estos pacientes.
El diagnóstico de chicos y varones adultos con X-ALD se iniciará a partir de pistas de la exploración clínica que son a menudo inespecíficas (la RM es también útil excluyendo patologías mucho más frecuentes como tumores,
infartos o hidrocefalia),
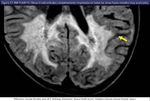
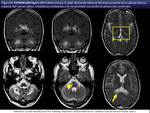
con diagnostico bioquímico mediante la determinación de AGCML en sangre total y el definitivo se establecerá mediante el análisis de la mutación genética y las alteraciones características en la RM cerebral que preceden a las manifestaciones clínicas (fig 11).
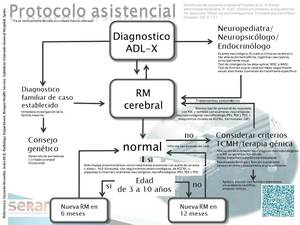
Fig. 11
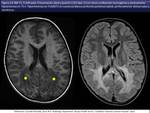
Papel de la RESONANCIA MAGNETICA
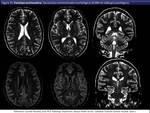
La neuroimagen con RM es la herramienta clave sobre la que pivota el manejo de la enfermedad (fig 12).
Aunque la interpretación de los estudios de imagen en las enfermedades dismielinizantes puede ser frustrante por el solapamiento de los hallazgos especialmente en etapas tardías cuando predominan el edema y la atrofia,
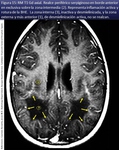
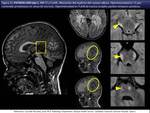
quizás los hallazgos específicos más frecuentemente identificados se dan en la X-ALD con afectación preferente de la sustancia blanca posterior y realce en el borde anterior (fig 13,
14,
15,
16).
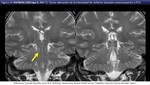
Además el respeto de las fibras subcorticales Ues típico de la X-ALD y la leucodistrofia metacromática [ii] (fig 17).
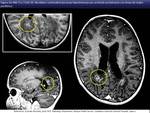
El realce con gadolinio es típico en las leucodistrofias con componente inflamatorio especialmente de la X-ALD.
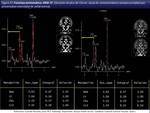
Un descenso en el pico de NAA indica afectación neuronal en las enfermedades de la sustancia blanca primarias.
Una puntuación cuantitativa de las lesiones por RM ha sido establecida para la X-ALD y es ampliamente usada para asesorar la elección del TCMH (fig 18).
[ii] (fig 17).
El realce con gadolinio es típico en las leucodistrofias con componente inflamatorio especialmente de la X-ALD.
Un descenso en el pico de NAA indica afectación neuronal en las enfermedades de la sustancia blanca primarias.
Una puntuación cuantitativa de las lesiones por RM ha sido establecida para la X-ALD y es ampliamente usada para asesorar la elección del TCMH (fig 18).

Fig. 12

Fig. 13
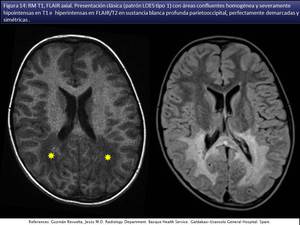
Fig. 14
References: Igualatorio Medico Quirurgico
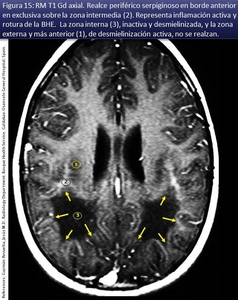
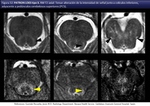
Fig. 15
References: Cortesía del Dr Antonio Luna. Grupo Health Time. Jaen. España.
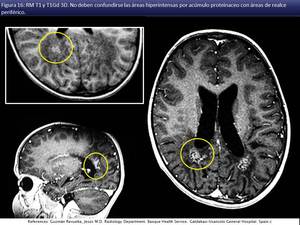
Fig. 16
References: Igualatorio Medico Quirurgico
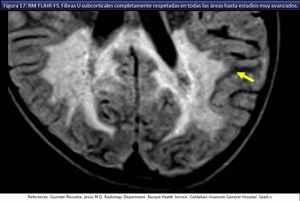
Fig. 17
References: Cortesía del Dr Alberto Cabrera. Osatek

Fig. 18
References: NEUROLOGY 2003;61:369–374.
APROXIMACION SISTEMATICA AL DIAGNOSTICO POR RM EN LAS LEUCODISTROFIAS [iii],
[iii], [iv]
[iv] [v]
[v]
La prueba auxiliar más importante en un paciente sospechoso de tener una leucodistrofia es la RM cerebral [vi],
siendo crucial la evaluación de ciertos patrones y localizaciones para la diferenciación de las características metabólico-degenerativas respecto a otras etiologías puramente inflamatorias,
vasculares o tumorales.
Los niños tras 1,5 años de edad ya han acumulado suficiente mielina en la sustancia blanca para permitir que esta aparezca hipointensa en secuencias ponderadas en T2,
así que a partir de esa edad cualquier hiperintensidad en T2 en SB es anormal.
Para diferenciar entre hipomielinización permanente y la retrasada y para reconocer la desmielinización en marcha se hacen RM seriadas con intervalos apropiados.
Lo típico en las leucodistrofias genéticas es la confluencia bilateralidad y simetría de las lesiones,
mientras que en las alteraciones de SB adquiridas son multifocales y asimétricas (fig 19).
[vi],
siendo crucial la evaluación de ciertos patrones y localizaciones para la diferenciación de las características metabólico-degenerativas respecto a otras etiologías puramente inflamatorias,
vasculares o tumorales.
Los niños tras 1,5 años de edad ya han acumulado suficiente mielina en la sustancia blanca para permitir que esta aparezca hipointensa en secuencias ponderadas en T2,
así que a partir de esa edad cualquier hiperintensidad en T2 en SB es anormal.
Para diferenciar entre hipomielinización permanente y la retrasada y para reconocer la desmielinización en marcha se hacen RM seriadas con intervalos apropiados.
Lo típico en las leucodistrofias genéticas es la confluencia bilateralidad y simetría de las lesiones,
mientras que en las alteraciones de SB adquiridas son multifocales y asimétricas (fig 19).

Fig. 19
References: Neurology 2009, 72, 750-9
PROTOCOLO RM CONVENCIONAL Y AVANZADA (fig 20)
El mejor marcador pronóstico actualmente es la presencia de realce con Gadolinio en RM cerebral convencional (fig 15).
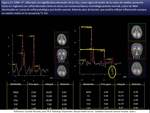
Las secuencias que proporcionan información adicional con valor predictivo son la espectroscopia protónica por RM [vii] con elevación del ratio colina-creatina total (fig 21) en la SB sin aparente lesión en secuencias convencionales que refleja inicio de la mielinolisis,
la disminución de la fracción de anisotropía
[vii] con elevación del ratio colina-creatina total (fig 21) en la SB sin aparente lesión en secuencias convencionales que refleja inicio de la mielinolisis,
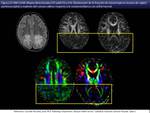
la disminución de la fracción de anisotropía [viii] (habiéndose demostrado una estabilización en su caída,
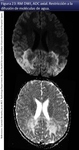
e incluso un aumento de la FA en pacientes tratados precozmente con TCMH) (fig 22) y el aumento de la difusión media (fig 23),
y la disminución de la perfusión cerebral dinámica por contraste de susceptibilidad magnética
[viii] (habiéndose demostrado una estabilización en su caída,
e incluso un aumento de la FA en pacientes tratados precozmente con TCMH) (fig 22) y el aumento de la difusión media (fig 23),
y la disminución de la perfusión cerebral dinámica por contraste de susceptibilidad magnética [ix].
La RM abdominal pudiera demostrar hipoplasia de las glándulas adrenales.
[ix].
La RM abdominal pudiera demostrar hipoplasia de las glándulas adrenales.

Fig. 20
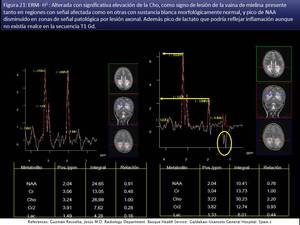
Fig. 21
References: Igualatorio Medico Quirurgico
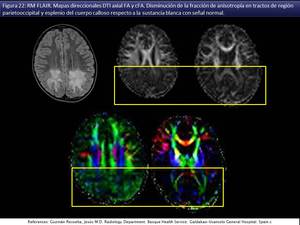
Fig. 22
References: Cortesía del Dr Alberto Cabrera. Osatek
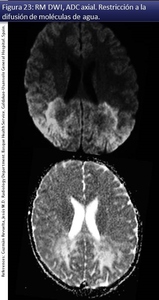
Fig. 23
References: Igualatorio Medico Quirurgico
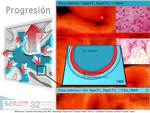
PROGRESION POR RM [x]
[x]
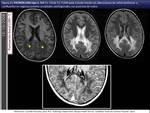
La lesión comienza en el patrón clásico en el esplenio del cuerpo calloso con diseminación interhemisférica extendiéndose hacia la SB periventricular y profunda parietooccipital y occipitotemporal (fig 24,
25,
26,
27) y después anteriormente.
Precozmente también se afectan los cuerpos geniculados medial y lateral,
el aspecto inferolateral del tálamo,
el brazo posterior de la capsula interna y la capsula externa.
Después los centros semiovales y centrípetamente la SB subcortical,
las radiaciones ópticas,
y la afectación troncoencefálica de los tractos occipito-temporo-parieto-protuberanciales y piramidales,
el brazo del colículo superior (fig 31) (vías auditivas) y el lemnisco lateral.
El cerebelo y los tractos fronto-protuberanciales se mantienen respetados.
Por tanto la progresión es normalmente concéntrica y simétrica en alas de mariposa y con un gradiente posteroanterior difundiendo hacia lóbulos frontales,
y centrífugo desde SB profunda hacia la SB periférica subcortical (respetando relativa o completamente las fibras arcuatas en U subcorticales (fig 17).
En concordancia con los hallazgos histopatológicos y de neuroresonancia morfológica y molecular se distinguen 3 zonas en el patrón concéntrico: GLIOSIS,
INFLAMACION y DESMIELINIZACIÓN (fig 15,24).
La zona interna presenta una completa desmielinización (fibrillas gliales y astrocitos dispersos hipertrofiados y total ausencia de axones sin mielina ni oligodendroglia) con necrosis (reblandecimiento)-cicatriz-(±Ca)-atrofia de la sustancia blanca (disminuyendo todos los metabolitos cerebrales).
Atrofia por perdida parenquimatosa con cavitación y dilatación ex vacuo del sistema ventricular (fig 26) pero conservando intacto el revestimiento ependimario ventricular.
La intermedia de inflamación activa (infiltrados inflamatorios linfocitarios y macrófagos perivasculares) donde se acumula el Gadolinio.
La capa externa refleja desmielinización en curso activa (pero con integridad axonal) sin inflamación (alteraciones espectroscópicas consistentes con↓NAA y Cr,
↑↑Cho y pequeño pico de lactato).
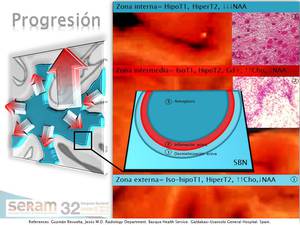
Fig. 24
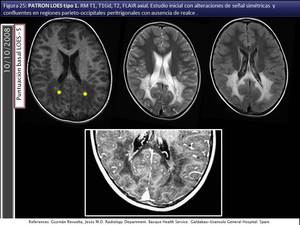
Fig. 25
References: Igualatorio Medico Quirurgico
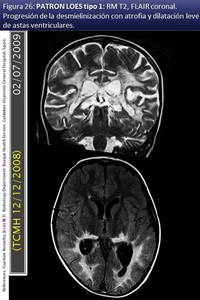
Fig. 26
References: Igualatorio Medico Quirurgico
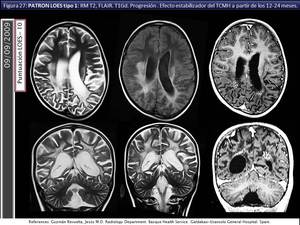
Fig. 27
References: Igualatorio Medico Quirurgico
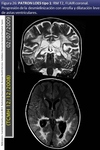
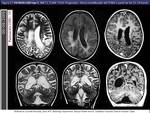
PATRONES POR RM
Según la localización anatómica predominante Loes y colaboradores describieron 5 patrones principales por imagen (correspondientes con diferentes fenotipos,
edades de presentación y tasas de progresión) (fig 28,
29,30).
El más frecuente en niños es el clásico tipo 1 [xi] o parietooccipital (fig 31).
El tipo 3 afectando al tracto corticoespinal (fig 32,
33).
El tipo 4 tanto al tracto corticoespinal como a cerebelo (fig 34).
Además es esencial el estricto seguimiento por RM de los niños asintomáticos o con clínica exclusiva de Addison cuando presentan RM convencional normal,
pudiendo aparecer como marcador precoz los hallazgos espectroscópicos (fig 35,36,37),
para procurar la indicación efectiva de un potencial TCMH.
[xi] o parietooccipital (fig 31).
El tipo 3 afectando al tracto corticoespinal (fig 32,
33).
El tipo 4 tanto al tracto corticoespinal como a cerebelo (fig 34).
Además es esencial el estricto seguimiento por RM de los niños asintomáticos o con clínica exclusiva de Addison cuando presentan RM convencional normal,
pudiendo aparecer como marcador precoz los hallazgos espectroscópicos (fig 35,36,37),
para procurar la indicación efectiva de un potencial TCMH.
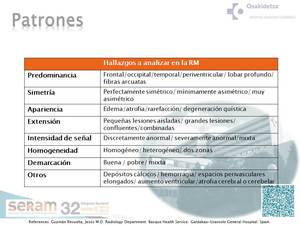
Fig. 28
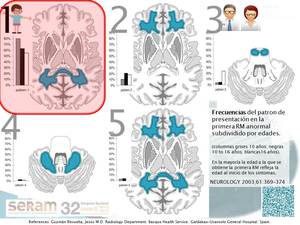
Fig. 29
References: NEUROLOGY 2003;61:369–374
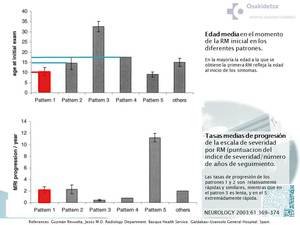
Fig. 30
References: NEUROLOGY 2003;61:369–374
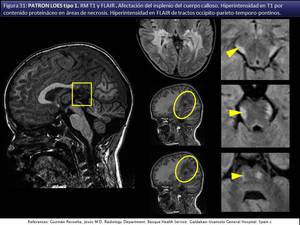
Fig. 31
References: Cortesía del Dr Alberto Cabrera. Osatek
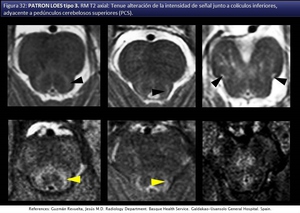
Fig. 32
References: Cortesía del Dr Alberto Cabrera. Osatek
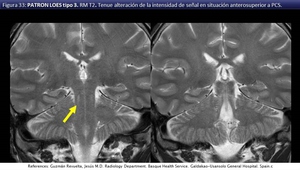
Fig. 33
References: Cortesía del Dr Alberto Cabrera. Osatek
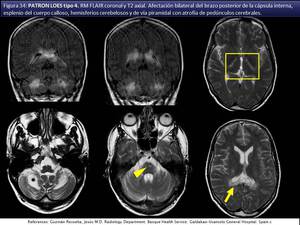
Fig. 34
References: Cortesía del Dr Alberto Cabrera. Osatek
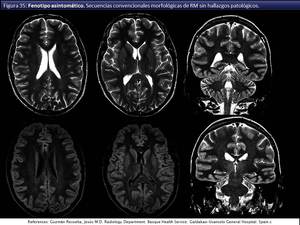
Fig. 35
References: Cortesía del Dr Alberto Cabrera. Osatek
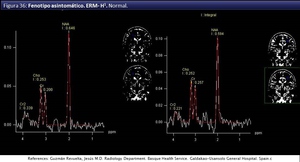
Fig. 36
References: Cortesía del Dr Alberto Cabrera. Osatek
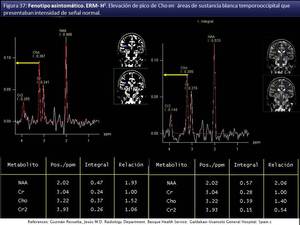
Fig. 37
References: Cortesía del Dr Alberto Cabrera. Osatek
INDICE DE SEVERIDAD POR RM
Loes y colaboradores introdujeron una escala cuantitativa (34 puntos) de las lesiones por RM usada para asesorar la idoneidad del TCMH (LOES ≥1 es anormal y a mayor puntuación mayor severidad) que debe de incluirse siempre en el informe ayudando además al análisis del patrón (fig 18,
28,
29).
El realce periférico tiene valor predictivo de progresión con efecto profundamente negativo en el pronóstico,
y su ausencia está asociada con enfermedad estable.
Es de esperar que cuando estén validados en estudios apropiados se incluyan en la fórmula que predice la severidad por RM los hallazgos de la espectroscopia y del tensor de difusión,
aunque de hecho la elevación de los ratios de Cho/NAA en la sustancia blanca aparentemente normal (fig 35,36,37) en el seguimiento ya es un indicador para el TCMH resultando en estabilización clínica [xii].
[xii].
PRONOSTICO SEGÚN RM INICIAL
Con puntuación en escala de LOES >3,
casi todos los pacientes (90%) empeoraran,
independientemente de la edad,
sólo el 10% permanecen neurológicamente estables.
Con puntuación de 1 a 3,
el 60% de los pacientes empeoran,
independientemente de la edad,
pero la supervivencia es más larga.
Si puntuación por debajo de 1,
el pronóstico depende de la edad del paciente: Entre los pacientes de edades comprendidas entre 3 y 7 años,
30% desarrollará desmielinización cerebral rápidamente progresiva.
En el grupo de edad entre 7 y 10 años,
10% desarrollará desmielinización cerebral rápidamente progresiva.
En el grupo de edad mayor de 10 años,
la desmielinización cerebral rápidamente progresiva es rara y es más probable AMN.
(fig 38)

Fig. 38
 [i] Engelen et al.
X-linked adrenoleukodystrophy (X-ALD): clinical presentation and guidelines for diagnosis,
follow-up and management.
Orphanet Journal of Rare Diseases.
2012; 7:51.
[i] Engelen et al.
X-linked adrenoleukodystrophy (X-ALD): clinical presentation and guidelines for diagnosis,
follow-up and management.
Orphanet Journal of Rare Diseases.
2012; 7:51.
 [ii] Jung-Eun Cheon,
et al.
Leukodystrophy in children: A pictorial review of MR imaging features.
Radiographics 2002; 22: 461-476.
[ii] Jung-Eun Cheon,
et al.
Leukodystrophy in children: A pictorial review of MR imaging features.
Radiographics 2002; 22: 461-476.
 [iii] Schiffmann R,
et al.
Invited article: an MRI-based approach to the diagnosis of white matter disorders.
Neurology 2009,
72,
750-9.
[iii] Schiffmann R,
et al.
Invited article: an MRI-based approach to the diagnosis of white matter disorders.
Neurology 2009,
72,
750-9.
 [iv] Alfried K,
et al.
Childhood leukodystrophies: a clinical perspective.
Expert Rev.
Neurother.
2011,
11,
1485–96.
[iv] Alfried K,
et al.
Childhood leukodystrophies: a clinical perspective.
Expert Rev.
Neurother.
2011,
11,
1485–96.
 [v] J.R.Hesselink.
Differential diagnostic approach to MR imaging of white matter diseases.
Top Magn Reson Imaging 2006; 4: 243-63.
[v] J.R.Hesselink.
Differential diagnostic approach to MR imaging of white matter diseases.
Top Magn Reson Imaging 2006; 4: 243-63.
 [vi] Cheon JE,
Kim IO,
Hwang YS et-al.
Leukodystrophy in children: a pictorial review of MR imaging features.
Radiographics.
2002; 22; 461-76.
[vi] Cheon JE,
Kim IO,
Hwang YS et-al.
Leukodystrophy in children: a pictorial review of MR imaging features.
Radiographics.
2002; 22; 461-76.
 [vii] Rossi A,
Biancheri R.
Magnetic resonance spectroscopy in Metabolic Disorders.
Neuroimag Clin N Am.
2013; 23; 425–448.
[vii] Rossi A,
Biancheri R.
Magnetic resonance spectroscopy in Metabolic Disorders.
Neuroimag Clin N Am.
2013; 23; 425–448.
 [viii] A.M.
McKinney,
et al.
Childhood Cerebral X-Linked Adrenoleukodystrophy: Diffusion Tensor Imaging Measurements for rediction of Clinical Outcome after Hematopoietic Stem Cell Transplantation.
AJNR 2013; 34: 641–49.
[viii] A.M.
McKinney,
et al.
Childhood Cerebral X-Linked Adrenoleukodystrophy: Diffusion Tensor Imaging Measurements for rediction of Clinical Outcome after Hematopoietic Stem Cell Transplantation.
AJNR 2013; 34: 641–49.
 [ix] P L Musolino et al.
Hypoperfusion predicts lesion progression in cerebral X-linked adrenoleukodystrophy.
Brain 2012: 135; 2676–2683.
[ix] P L Musolino et al.
Hypoperfusion predicts lesion progression in cerebral X-linked adrenoleukodystrophy.
Brain 2012: 135; 2676–2683.
 [x] Van der Knaap M.S,
Valk J.
X-Linked Adrenoleukodystrophy.
In: Magnetic Resonance of Myelination and Myelin Disorders.
Third Edition.
Germany.
Springer,
2005; 176-190.
[x] Van der Knaap M.S,
Valk J.
X-Linked Adrenoleukodystrophy.
In: Magnetic Resonance of Myelination and Myelin Disorders.
Third Edition.
Germany.
Springer,
2005; 176-190.
 [xi] D.J.
Loes,
et al.
Analysis of MRI patterns aids prediction of progression in X-linked adrenoleukodystrophy.
NEUROLOGY 2003;61:369–374.
[xi] D.J.
Loes,
et al.
Analysis of MRI patterns aids prediction of progression in X-linked adrenoleukodystrophy.
NEUROLOGY 2003;61:369–374.
 [xii] Wilken B,
et al.
Quantitative proton magnetic resonance spectroscopy of children with adrenoleukodystrophy before and after hematopoietic stem cell transplantation.
Neuropediatrics 2003;34(5):237–246.
[xii] Wilken B,
et al.
Quantitative proton magnetic resonance spectroscopy of children with adrenoleukodystrophy before and after hematopoietic stem cell transplantation.
Neuropediatrics 2003;34(5):237–246.