DEFINICIÓN
El tumor fibroso solitario extrapleural es un tumor mesenquimal raro y ubicuo,
formado por células fusiformes,
con diversos grados de fibrosis,
con vasos entremezclados y ramificados en forma de “cuerno de ciervo”.
Puede ser benigno o maligno.
EPIDEMIOLOGÍA
Aparece con mayor frecuencia entre los 20 - 70 años (mediana de 50 años),
y no tiene predilección de sexo.
Inicialmente se describió como de origen pleural, aunque ahora se sabe que puede desarrollarse en cualquier lugar del organismo:
- Cabeza y cuello: Extracompartimental
- Tórax: Pared torácica,
mediastino,
pericardio y pulmón
- Abdomen: Peritoneo,
hígado,
páncreas
- Retroperitoneo y riñón
- Pelvis: Vejiga,
próstata,
cordón espermático,
testículos
- Columna vertebral: Meninges y médula espinal
- Músculos y tejidos blandos
ANATOMÍA PATOLÓGICA
Morfológicamente,
el tumor fibroso solitario extrapleural se asemeja al tumor fibroso solitario pleural.
Macroscópicamente se presenta como una masa bien delimitada,
parcialmente encapsulada,
que puede medir entre 1-30 cm (media 5-8 cm),
multinodular,
blanquecina y firme al corte,
altamente vascular,
con cambios mixoides y hemorrágicos.
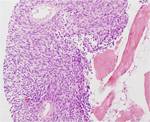
El diagnóstico es histológico y el patrón arquitectural es característico,
con zonas hipocelulares y otras hipercelulares,
separadas por bandas gruesas de colágeno.
(Fig.
1)

Fig. 1: Tumor fibroso solitario hepático. Proliferación de células fusiformes de alta densidad con patrón fasciculado y formación de luces de colágeno. Hay dos lagos vasculares tipo hemangiopericitoma y fibras de músculo estriado extra-hepático en el lado derecho (HE, magnificación original, 40 x)
Dependiendo de la cantidad de estroma fibroso se calsifican en:
- Variante fibrosa (la más común)
- Variante celular
La inmunohistoquímica puede ayudar en el diagnóstico histológico:
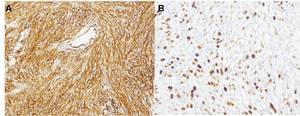
Fig. 2: Tumor fibroso solitario hepático. A) El estudio inmunohistoquímico muestra una intensa expresión citoplasmática de CD34 en las células neoplásicas, un hallazgo característico de este tumor. (CD34, ampliación original 100 x). B) Alto porcentaje de núcleos teñidos con el antígeno de proliferación Ki67, un indicador de comportamiento agresivo (Ki67, ampliación original 200 x)
El 75-80% de estos tumores son benignos.
Los tumores localmente agresivos o malignos aparecen con frecuencia a partir de una transformación maligna de lesiones benignas preexistentes y son habituales la necrosis intratumoral y/o los márgenes infiltrantes.
La probabilidad de malignidad aumenta con el tamaño del tumor.
Los signos histológicos de malignidad son:
- Lesiones hipercelulares con marcada atipia celular
- Numerosas mitosis (≥ 4 mitosis por 10 campos de aumento)
- Pleomorfismo nuclear
- Necrosis tumoral
PRESENTACIÓN CLÍNICA
La clínica de presentación es inespecífica,
y en el 90% de los casos secundaria al efecto de masa del tumor.
Su comportamiento es impredecible,
ya que tanto los tumores benignos como los malignos pueden mostrar características clínicas agresivas con recurrencia local,
metástasis a distancia o ambas.
El factor pronóstico más importante,
con influencia en la evolución clínica,
es la completa y amplia escisión local,
ya que los márgenes positivos se asocian a un 40% de recurrencias locales y a un 65% de metástasis hematógenas.
La mayoría de las recurrencias ocurren en los primeros dos años tras la cirugía. Por eso el seguimiento clínico y de imagen de estos pacientes se realiza cada seis meses durante los dos primeros años tras la cirugía.
Posteriormente el seguimiento es anual a largo plazo dado que no se conoce a ciencia cierta la historia natural del tumor.
TUMOR FIBROSO SOLITARIO EXTRAPLEURAL Y RM
La RM es la técnica de imagen de elección para su estudio porque permite definir la relación del tumor con las estructuras adyacentes, lo que es vital de cara a la planificación quirúrgica.
Su aspecto en RM es variable,
dependiendo de su celularidad y de su contenido fibroso.
Las imágenes potenciadas en T1 son en general inespecíficas.
Las imágenes potenciadas en T2 permiten definir las características histológicas del tumor,
ya que las zonas hipocelulares y fibrosas,
con componente colágeno denso,
tienen menor intensidad de señal en las imágenes potenciadas en T2; por el contrario,
las zonas más celulares y con estroma mixoide,
focal o difuso,
son hiperintensas en las imágenes potenciadas en T2.
De forma característica el tumor fibrosos solitario muestra focos de baja intensidad de señal en T1 y T2,
atribuibles al contenido colágeno y baja celularidad,
que hacen que se parezcan a "galletas con pepitas de chocolate".
Tras administración de contraste la masa presenta realce moderado/ marcado y heterogéneo,
reflejando las diferencias de realce los distintos componentes tumorales: celularidad y cantidad de tejido colágeno.
(Fig.
3)
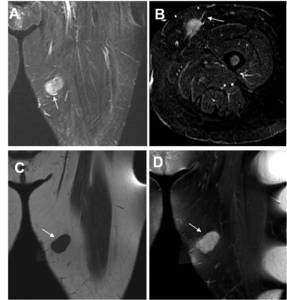
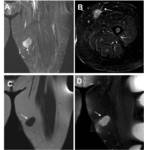
Fig. 3: Tumor fibroso solitario. Mujer de 70 años, con masa de crecimiento lento en el tercio proximal del muslo izquierdo. Imágenes STIR en plano coronal A) y axial B), que muestran una masa bien definida, con alta intensidad de señal, heterogénea y estructuras vasculares que se dirigen al tumor(flecha). C) Imagen en plano coronal eco de espín potenciada en T1 que muestra una masa bien definida con señal similar al músculo (flecha. D) Imagen coronal eco de espín potenciada en T1 con supresión grasa tras administración de contraste de gadolinio que muestra una masa con intenso realce (flecha)
Durante el estudio dinámico puede observarse en las fases arteial y portal una captación precoz en la periferia del tumor,
con septos lineales hacia el centro de la masa o patrón “en rayos de sol”.
El análisis del realce muestra una curva de captación con realce progresivo en las áreas fibrosas y densas,
y una pendiente de ascenso rápido con una meseta o lavado tardío en las zonas vasculares.
(Fig.
4)
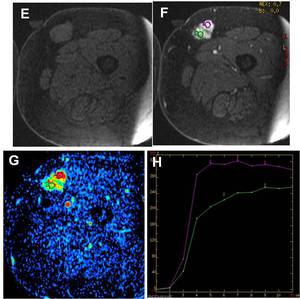
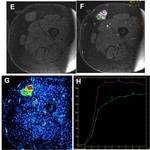
Fig. 4: Cinética de captación y correlación patológica. E) T1 axial SPGR con saturación grasa sin contraste y F), tras contraste, mostrando una masa bien definida con intenso realce.
G) y H) Patrón de captación estudiado en dos zonas diferentes del tumor. La parte más anterior de la masa estudiada con el ROI número 1 (morado) muestra una curva con ascenso inicial rápido y lavado en fases más tardías(curva de color morado), que histológicamente correspondía a la presencia de áreas vasculares dentro del tumor. La parte posterior del tumor estudiada con el ROI número 2 (verde) muestra una curva de realce progresivo en fase inicial y persistente en fases más tardías que se correspondía con las áreas más fibrosas del tumor(curva verde).
Las imágenes potenciadas en difusión son sensibles a las características biofísicas de los tejidos (densidad celular,
integridad de las membranas celulares,
espacio extracelular y microcirculación) y en el tumor fibroso solitario extrapleural se observan difrentes comportamientos dependiendo de la composición tisular:
- Áreas vasculares tienen valores altos de ADC
- Áreas fibróticas tienen valores bajos de ADC
- Necrosis,
áreas quísticas y mixoides muestran valores altos de ADC (Fig.
5)
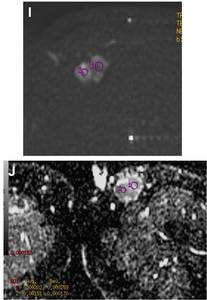
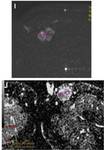
Fig. 5: Difusión y correlación patológica. I) La imagen de difusión con valor b=600 muestra una masa hiperintensa. J) el valor medio en el mapa de ADC es 2.02 x10 mm2/s en la parte más anterior del tumor, en relación con la presencia de áreas vasculares en el estudio patológico. El valor medio del ADC en la parte posterior del tumor es de 1.51 x10 mm2/s debido a la presencia de mayor cantidad de tejido fibroso en el estudio histológico.
Existe una buena correlación entre el estudio de difusión,
el estudio cinético de captación y el estudio histológico.
TUMOR FIBROSO SOLITARIO INTRACRANEAL
El tumor fibroso solitario intracraneal generalmente es de origen dural y puede presentar cola dural.
Característicamente es una masa bien definidas con intenso realce tras contraste,
que semiológicamente se parece a los meningiomas.
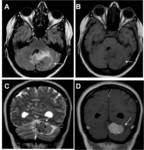
El tumor fibroso intracraneal debe ser incluido en el diagnostico diferencial en masas de origen dural que presentan focos hipointensos en su interior en FLAIR (A) y T2 (aspecto de "galleta con pepitas de chocolate") que corresponden a depósitos focales de tejido colágeno con baja celularidad.
(Fig.
6)
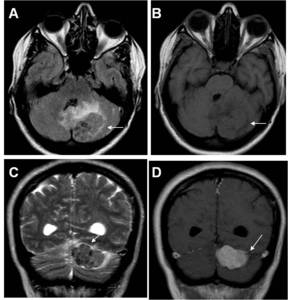
Fig. 6: Masa cerebral extraaxial: tumor fibroso solitario. Mujer 46 años con dolores de cabeza y náuseas. A)FLAIR axial que muestra una masa heterogénea en el lóbulo occipital izquierdo (flecha), con focos hipointensos dispersos, edema peritumoral y efecto de masa sobre el cuarto ventrículo. B) T1 eco de espín axial que muestra una masa isointensa (flecha). C) T2 turbo eco de espín coronal mostrando una masa isointensa con focos hipointensos en su interior. La masa está rodeada de líquido cefalorraquídeo (flecha) indicando un origen extraaxial. D)Ti eco de espín coronal tras contraste que muestra un intenso realce de la masa con imagen de cola dural (flecha).
Tumor fibroso intracraneal generalmente es de origen dural y pueden presentar cola dural. Característicamente son masas bien definidas con intenso realce tras contraste, que semiológicamente se parecen a los meningiomas.
Tumor fibroso intracraneal debe ser incluido en el diagnostico diferencial en masas de origen dural que presentan focos hipointensos en su interior en FLAIR (A) y T2 (C) "chocolate chip cookie appearance“ que corresponden a depósitos focales de tejido colágeno con baja celularidad
TUMOR FIBROSO SOLITARIO ESPINAL
El tumor fibroso solitario espinal es raro.
Generalmente aparece como una masa bien definida,
intradural y extramedular que puede crecer con morfología en "reloj de arena",
simulando un tumor neurogénico.
(Fig.
7)
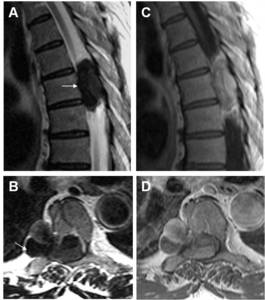
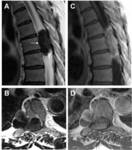
Fig. 7: Masa intadural extradural: tumor fibroso solitario. Varón de 66-años con dolor dorsal, parestesias y debilidad de extremidades. Imágenes T2 turbo eco de espín A) Sagital y B) axial que muestran áreas de baja intensidad de señal (flechas) dentro de la masa, que tiene una morfología en "reloj de arena". Imagen T1 eco de espín C) Sagital y D) axial tras contraste con realce intenso de la lesión excepto en la porción anterior del tumor, que correspondia a estroma fibroso organizado, en el estudio histológico.
TUMOR FIBROSO SOLITARIO HEPÁTICO
Debemos incluir el tumor fibroso solitario en el diagnóstico diferencial de una masa hepática de tamaño grande,
bien definida,
heterogénea,
moderadamente hiperintensa en T2,
en paciente sin tumor primario conocido,
con marcadores tumorales negativos y realce periférico en fase arterial,
con relleno progresivo (centrípeto),
sin demostrarse lavado en fases tardías y persistiendo en su interior áreas con ausencia de realce secundarias a necrosis.
(Fig. 8)
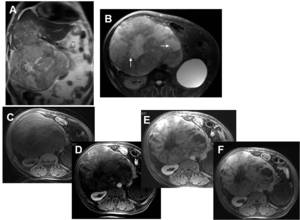
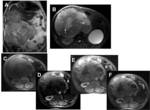
Fig. 8: Masa hepática: tumor fibroso solitario. Varón de 71 años con hipoglucemia y dolor abdominal. A) HASTE Coronal y B) T2 turbo eco de espín con supresión grasa axial que muestran una masa pedunculada con origen en el lóbulo hepático derecho, de señal heterogénea, con zonas más hiperintensas localizadas en zona central y periférica de la masa, que correspondían a necrosis en el estudio histológico (flechas en B). En el estudio dinámico: fases basal (C) arterial (D) portal (E) y tardía (F), se observa captación periférica en fase arterial con septos intratumorales (patrón “en rayos de sol”) con relleno progresivo en fases tardías y ausencia de realce de las zonas necróticas. No se demostró lavado dentro del tumor.
En el diagnóstico diferencial debe incluirse el colangiocarcinoma,
el hepatocarcinoma escirro y las metástasis .
TUMOR FIBROSO SOLITARIO PERITONEAL
El diagnóstico se debe sospechar en presencia de una masa peritoneal de señal heterogénea, grande,
bien definida,
moderadamente hiperintensa en secuencias T2, con realce periférico en fase inicial con patrón en "sunburst",
y areas focales en su interior hipocaptantes de contraste que se corresponden a zonas de degeneración quística en un paciente asintomático.
(Fig.
9)
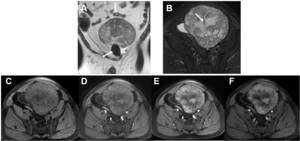
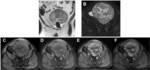
Fig. 9: Masa peritoneal: tumor fibroso solitario. Varón de 59 años de edad con masa abdominal sin dolor u otros síntomas. A) HASTE coronal y B) STIR axial que muestran una masa peritoneal de señal heterogénea, con una zona central hiperintensa (flecha en B) correspondiente a degeneración quistica y mixoide. Nódulo hipointenso pedunculado (flecha en A), que correspondía a calcificación en el estudio patológico. En el estudio dinámico, fases basal (C) arterial (D), portal (E) y tardía (F) se observa un realce periférico en las fases arterial y venosa, con septos intratumorales, "patrón en rayos de sol" y captación progresiva del contraste alrededor del área central con degeneración quistica y mixoide.
El diagnóstico diferencial es amplio e incluye: mesotelioma,
carcinoma de uraco,
metastasis…
TUMOR FIBROSO SOLITARIO RETROPERITONEAL
El riñón y el retroperitoneo son también localizaciones poco habituales donde el tumor fibroso solitario puede localizarse.
El comportamiento es similar al que presenta en otras localizaciones anatómicas.
(Fig.
10)
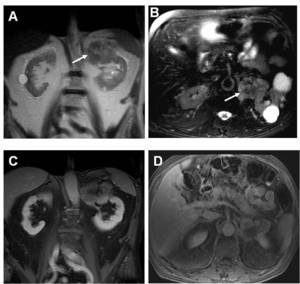
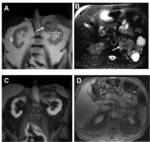
Fig. 10: Masa retroperitoneal: tumor fibroso solitario. Varón de 76 años, asintomático, con masa descubierta de forma incidental en una ecografía. A) HASTE coronal y B) T2 axial con supresión grasa que muestran una masa retroperitoneal con señal heterogénea, que infiltra el riñon izquierdo (flechas). C) T1 coronal y D) axial con saturación grasa tras contraste que muestran una masa que realza tras contraste, con una zona central hipocaptante que correspondía a estroma fibroso focal en el estudio histológico.
En el diagnóstico diferencial,
hay que incluir el linfoma,
el sarcoma de tejidos blandos y la enfermedad metastásica.
TUMOR FIBROSO SOLITARIO MUSCULAR
La mayoría de los tumores fibrosos que afectan a las extremidades ocurren en el tercio proximal del muslo.Son altamente vasculares y realzan después de la administración del contraste.
El diagnóstico diferencial de una masa de tejidos blandos altamente vascular y solitaria incluye sarcoma de tejidos blandos (histiocitoma fibroso maligno,
leimiosarcoma),
tumor desmoide,
tumor de vaina nerviosa periférica,
lesión metastática (carcinoma de células renales) y el tumor fibroso solitario.
Una característica distintiva de imagen útil,
aunque no específica,
es la presencia de vasos que se dirigen al tumor.
(Fig.11)
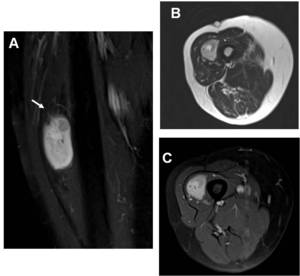
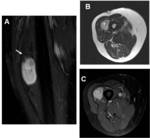
Fig. 11: Masa intramuscular: tumor fibroso solitario.Mujer de 65 años con masa de crecimiento lento, bien definida, en el muslo derecho A) STIR coronal que muestra una masa intramuscular bien definida, de señal heterogénea, con focos de baja señal en su interior y vasos que se dirigen al tumor (flecha). B) T2 turbo eco de espín axial que muestra una masa bien definida, heterogénea, con una zona focal central hiperintensa (área vascular en el estudio patológico) y una zona periférica hipointensa (fibrosis en el estudio patológico). C) T1 eco de espin axial con saturación de la grasa tras contraste, apreciándose realce de la masa. El área vascular muestra mayor realce que zona fibrosa.