El linfoma cerebral primario (LCP) es una entidad de origen controvertido,
ya que el sistema nervioso central (SNC) carece de tejido o circulación linfática.
Su denominación hace referencia a una afectación exclusiva del SNC,
bien sea cerebral,
leptomeníngea,
medular u ocular.
Por lo tanto,
siempre es necesario descartar compromiso en cualquier otra parte del organismo.
El LCP supone el 1% de los linfomas y el 16% de los tumores primarios del SNC y la mayoría corresponde a linfomas no Hodgkin tipo B,
siendo muy raros los de estirpe T; ambos comparten una presentación clínica y radiológica similar.
El LCP del SNC raramente afecta a otras localizaciones durante su evolución,
a diferencia del linfoma nodal,
que se extiende al SNC en el 5-10% de los casos.
La linfomatosis intravascular,
forma de linfoma no Hodgkin tipo B del SNC extremadamente rara,
se caracteriza por una proliferación intravascular importante de células linfoides.
A pesar de que el LCP aparece en individuos con inmunidad normal,
su incidencia es mayor en los inmunodeprimidos (en ambos grupos parece ir en aumento en los últimos años).
Así,
se ha descrito principalmente en el SIDA (asociado al virus de Epstein Barr) y también en inmunodeficiencias congénitas o secundarias al tratamiento de neoplasias o trasplantes.
El LCP en inmunocompetentes es más frecuente en los varones en la 6ª-7ª décadas de la vida.
Clínicamente se manifiesta con alteración del estado mental y focalidad neurológica; con menor frecuencia aparecen trastornos cognitivos o neuropsiquiátricos,
cefalea,
alteraciones visuales,
hemiparesia,
ataxia,
aumento de la presión intracraneal o convulsiones.
La supervivencia es mayor si la lesión es única,
sin compromiso meníngeo o periventricular,
y en sujetos menores de 60 años.
El uso de radioterapia holocraneal (y espinal si procede) y quimioterapia posterior (dosis altas de metotrexato,
corticoides,
vincritina y ciclofosfamida) ha mejorado el pronóstico de los pacientes,
aunque en cualquier caso continúa siendo desfavorable.
En los estudios de imagen,
el LCP del SNC suele aparecer como una lesión única,
localizada en la sustancia blanca supratentorial frontal,
parietal o subependimaria,
que cruza la línea media a través del cuerpo calloso,
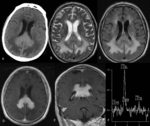
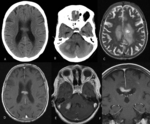
adoptando el clásico patrón en “alas de mariposa” (Fig. 2 y Fig. 7),
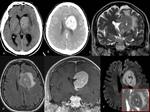
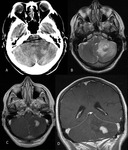
con edema vasogénico y efecto de masa (Fig. 1,
Fig. 3 y Fig. 7); puede incluso afectar a los ganglios basales y tálamos y extenderse a la leptomeninge.
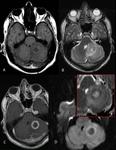
En raras ocasiones hay necrosis central (Fig. 3),
áreas quísticas,
hemorragia o calcificaciones (más frecuentes tras la quimio o radioterapia).
Tras administrar corticoides,
la masa puede ser poco visible,
presentar hallazgos equívocos o incluso desaparecer temporalmente,
por lo que el tratamiento debe ser posterior a las pruebas de imagen y la toma de muestras histológicas.
En la tomografía computarizada (TC),
la neoplasia es hiperdensa por su gran celularidad y capta intensa y homogéneamente el contraste intravenoso (Fig. 1).
En el estudio basal la necrosis aparecerá hipodensa,
las áreas quísticas con una atenuación similar a la del líquido cefalorraquídeo (LCR),
la hemorragia hiperdensa,
y las calcificaciones tendrán densidad calcio.
El edema vasogénico se visualiza como un halo hipodenso en la sustancia blanca peritumoral,
con o sin obliteración de los surcos de la convexidad o desplazamiento de estructuras cerebrales próximas (Fig. 1).
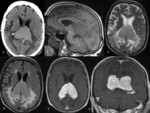
En la resonancia magnética (RM) el LCP está bien delimitado y es iso o hipointenso en las secuencias potenciadas en T1 (Fig. 7) e hipointenso en las ponderadas en T2 (Fig. 1) y FLAIR (aunque en esta última secuencia puede mostrar una mayor señal).
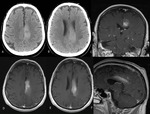
La mayoría de las lesiones presentan un realce homogéneo tras la administración de gadolinio (Fig. 1, Fig.
2, Fig. 3, Fig. 4, Fig.
5, Fig. 6 y Fig. 7); el realce lineal periférico a lo largo de los espacios de Virchow-Robin es muy específico.
Las áreas necróticas o quísticas serán hipointensas en T1 e hiperintensas en T2; la hemorragia hiperintensa en T1 y con artefactos de susceptibilidad magnética en eco de gradiente-T2; y las calcificaciones usualmente se mostrarán como vacíos de señal en todas las secuencias.
Estos tumores pueden restringir levemente la difusión (Fig. 1) y se caracterizan en espectroscopia por un aumento de la colina y una disminución del N-acetil aspartato, que refleja la práctica ausencia de tejido neuronal (Fig. 2).
El edema vasogénico aparece como un halo circundante de aumento de señal en T2 (Fig. 1,
Fig.
2, Fig. 3, Fig. 5, Fig. 6 y Fig. 7) y FLAIR (Fig. 1 y Fig. 2).
El diagnóstico diferencial del LCP del SNC en inmunocompetentes incluye:
- Glioblastoma multiforme,
principalmente si afecta al cuerpo calloso.
Suele presentar áreas de hemorragia y necrosis central y la captación es periférica o heterogénea.
- Absceso cerebral: realce periférico asimétrico (menor grosor adyacente al ventrículo) y típica restricción central de la difusión.
En la espectroscopia los aminoácidos están elevados.
- Leucoencefalopatía multifocal proresiva.
Afecta a las fibras en U corticales y al cuerpo calloso (hiperintensos en las secuencias potenciadas en T2).
No existe realce posgadolinio.
- Esclerosis múltiple pseudotumoral.
En jóvenes.
Realce en forma de herradura abierta hacia la corteza cerebral.
- Metástasis única.
Captación anular frecuente y con un gran edema vasogénico asociado.
- Linfoma secundario.
Es necesario descartar afectación en otra localización ajena al neuroeje.
Los hallazgos radiológicos descritos pueden sugerir un LCP del SNC en pacientes con inmunidad normal.
No obstante,
el diagnóstico definitivo requiere un estudio histológico previo al tratamiento (el análisis del LCR sólo es positivo en el 50% de los casos).