Introducción:
Los pseudoquistes inflamatorios constituyen la mayor parte de las lesiones quísticas de páncreas (más del 85% del total) y su diagnóstico diferencial con las verdaderas neoplasias quísticas es importante,
debido fundamentalmente al potencial de malignización de estas últimas.
Además,
algunas neoplasias sólidas como los tumores neuroendocrinos,
el adenocarcinoma o el tumor pseudopapilar sólido pueden presentar áreas de degeneración quística y simular una verdadera neoplasia quística por imagen,
por lo que,
debido a su diferente pronóstico y enfoque terapéutico,
es también importante su diferenciación.
Frecuencia y diagnóstico:
Las neoplasias quísticas de páncreas son un grupo heterogéneo de lesiones benignas,
premalignas y malignas cuyo diagnóstico precoz y tratamiento son importantes.
Recientes estudios basados en TCMD y RM estiman una prevalencia que varía entre el 2,4 y el 14%,
con una frecuencia global similar en ambos sexos y una incidencia que aumenta con la edad,
aunque se desconoce si este aumento refleja un riesgo real con la edad o es debido a la utilización cada vez más frecuente de estas técnicas de imagen en personas de edad más avanzada,
debido al aumento de la esperanza de vida.
Las neoplasias quísticas pancreáticas más frecuentes son el cistoadenoma seroso,
el cistoadenoma mucinoso y la neoplasia papilar intraductal mucinosa (NPIM).
Tanto la TCMD como la RM son indispensables en el estudio de las lesiones quísticas pancreáticas.
La TCMD es la técnica de elección inicial para la detección,
caracterización y valoración de la extensión extrapancreática de la lesión.
La colangio RM permite además determinar la relación de la lesión quística con el conducto pancreático (especialmente importante en la diferenciación de las NPIM).
A pesar del uso emergente de las secuencias potenciadas en difusión,
actualmente la utilidad de estas secuencias para el estudio de las neoplasias quísticas de páncreas está siendo menor que el que se pensaba en un principio.
Aunque existen hallazgos morfológicos característicos de cada una de las distintas neoplasias,
en ocasiones,
no es posible establecer un diagnóstico definitivo únicamente mediante TCMD y RM,
por lo que se requieren otras pruebas de imagen,
como la eco-endoscopia,
que además de proporcionar información morfológica muy precisa permite,
a través de la punción y aspiración del contenido,
obtener un análisis citológico y bioquímico de la lesión.
La combinación del análisis citológico,
los marcadores bioquímicos y los marcadores tumorales permiten establecer un diagnóstico y diferenciar lesiones mucinosas y no-mucinosas para,
de esta manera,
prevenir resecciones injustificadas de lesiones benignas.
En cuanto a los marcadores tumorales relacionados con este tipo tumores,
el antígeno carcinoembrionario (CEA) se encuentra elevado en los tumores mucinosos,
generalmente por encima de 192 ng/ml,
de tal forma que un CEA menor de 5 ng/ml excluye tumores no mucinosos con una sensibilidad cercana al 100% y una especificidad del 86%.
El resto de marcadores tumorales (CA 19-9,
CA,
CA 72-4 y CA 125) tienen un valor limitado. Respecto a los marcadores bioquímicos,
la amilasa se encuentra aumentada tanto en los pseudoquistes como en la neoplasia mucinosa papilar intraductal.
Características radiológicas:
CISTOADENOMA SEROSO
El cistoadenoma seroso es un tumor benigno que constituye aproximadamente el 20% del total de las lesiones quísticas del páncreas.
Es más frecuente en mujeres y la edad media de aparición es de 61,5 años.
Más del 80% se producen en el cuerpo y la cola pancreática y cursa generalmente de manera asintomática.
Se trata de un tumor bien delimitado,
formado por múltiples quistes de hasta 2 cm de tamaño,
conformando un patrón en "panal de abejas".
Presenta unos contornos lobulados con paredes delgadas que se intensifican tras la administración de contraste.
En la TCMD se ve en aproximadamente un 20-30% de los casos,
una cicatriz estrellada con calcificaciones centrales mientras que en RM se presenta como una masa constituida por pequeñas lesiones hiperintensas en T2,
con septos y una cicatriz central que realza tras la administración de contraste.
No comunica con el sistema ductal pancreático y no presenta dilatación de la vía biliar ni del Wirsung.
Existe una forma rara de cistoadenoma seroso con patrón oligomacroquístico,
indistinguible por imagen del cistoadenoma mucinoso.
A diferencia de otras neoplasias quísticas pancreáticas,
las características morfológicas en eco-endoscopia son altamente sugestivas de este tipo de lesión.
Se trata de una lesión constituida por múltiples formaciones anecoicas,
bien delimitadas,
de pequeño tamaño y con septos en su interior (figuras 1 y 2).
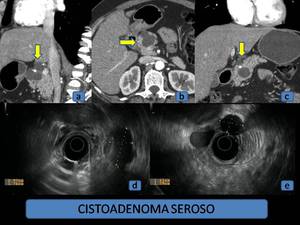
Fig. 1: Cistoadenoma seroso. (a), (b) y (c): TCMD con contraste intravenoso, reconstrucciones multiplanares planos sagital, axial y coronal, donde se identifica una lesión quística localizada en la cabeza pancreática con calcificación central. (d) y (e): Eco-endoscopia del mismo paciente, en la que se observa una lesión anecoica, polilobulada, de bordes bien definidos.
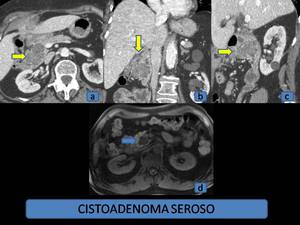
Fig. 2: Cistoadenoma seroso. (a), (b) y (c): TCMD con contraste intravenoso, reconstrucciones multiplanares, planos axial, coronal y sagital, donde se observa una lesión multitabicada situada en cabeza-proceso uncinado. (d): RM, T1 fase dinámica de otro paciente, donde se observa otra lesión de similares características, hipointensa, localizada en proceso uncinado.
Tras la punción-aspiración y análisis del líquido de la lesión,
las concentraciones tanto de amilasa como de CEA son indetectables.
CISTOADENOMA MUCINOSO
A diferencia del cistoadenoma seroso,
el cistoadenoma mucinoso es un tumor con potencial maligno.
Presenta un estroma similar al ovario (ovarian-like stroma) y está revestido por células epiteliales secretoras de moco,
con grado variable de atipia.
Constituye aproximadamente el 10% de las lesiones quísticas pancreáticas, es casi exclusivo del sexo femenino y presenta una edad media de aparición de 47 años.
Cursa de manera asintomática o bien con dolor abdominal inespecífico,
náuseas,
pérdida de peso o dolor de espalda.
Se trata de un tumor bien delimitado con quistes > 2 cm (patrón oligoquístico) llenos de moco y tabiques,
y cuya pared realza tras la administración de contraste.
El 95% de los casos se localizan en cuerpo o cola de páncreas y las calcificaciones periféricas en "cáscara de huevo" (15%) sugieren carácter maligno.
No comunica con el sistema ductal pancreático y en ocasiones produce dilatación de la vía biliar y del Wirsung por compresión.
En eco-endoscopia se presenta como una lesión unilocular u oliquística,
con septos internos de grosor variable.
Pueden presentar un contenido ecogénico debido a la producción de moco (figuras 3,
4,
5,
6 y 7).
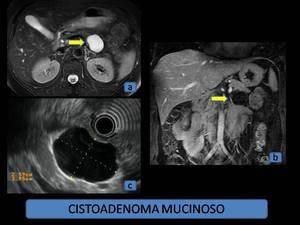
Fig. 3: Cistoadenoma mucinoso. (a) y (b). RM, secuencias axial T2 FSE y coronal LAVA dinámico, donde se identifica una lesión quística, unilocular, localizada en la cola pancreática, hiperintensa en T2 e hipointensa en LAVA. (c): Eco-endoscopia del mismo paciente, en la que se observa una lesión anecoica, bien delimitada, con un fino septo en su interior.
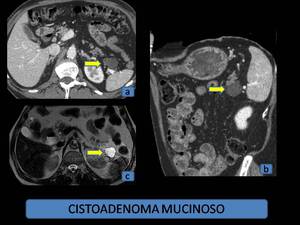
Fig. 4: Cistoadenoma mucinoso. (a) y (b): TCMD con contraste intravenoso, reconstrucciones multiplanares, planos axial y sagital, donde se observa una lesión en cola pancreática, de aspecto unilocular. (c): RM, secuencia T2 SSFSE, donde se confirma la ausencia de septos en el interior de la lesión.
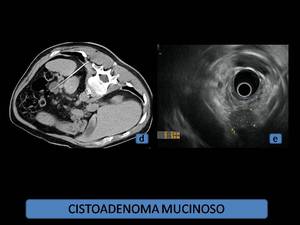
Fig. 5: Cistoadenoma mucinoso. (d): Punción-aspiración de la lesión, guiada mediante TCMD. (e): Eco-endoscopia, donde se observa la lesión unilocular, de ecogenicidad intermedia debido a su contenido mucoide.
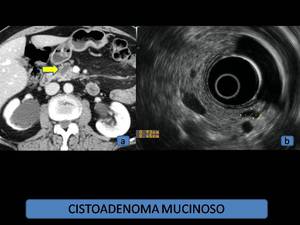
Fig. 6: Cistoadenoma mucinoso. (a): TCMD tras la administración de contraste intravenoso, reconstrucción multiplanar, plano axial, lesión de morfología fusiforme, de características quísticas, sin tabicaciones. (b): Eco-endoscopia del mismo paciente, donde se identifica la lesión, anecoica, bien delimitada, sin septos en su interior.
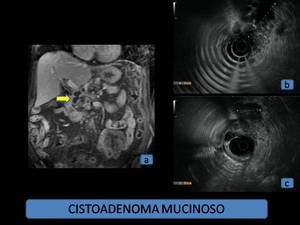
Fig. 7: Cistoadenoma mucinoso. (a): RM, secuencia T1 coronal en fase dinámica, lesión polilobulada, hipointensa, localizada en proceso uncinado de páncreas. (b) y (c): Eco-endoscopia del mismo paciente, donde se confirma la presencia de una lesión polilobulada, mal delimitada, de ecogenicidad intermedia en proceso uncinado.
Aproximadamente el 17,5% de los cistoadenomas mucinosos son malignos.
Los hallazgos de imagen que sugieren carácter maligno,
además de las calcificaciones en "cáscara de huevo",
son la presencia de nódulos murales,
un tamaño superior a los 6 cm y engrosamiento o irregularidad de la pared del conducto pancreático principal.
El líquido obtenido tras la punción-aspiración es viscoso por su contenido en moco y células columnares.
Típicamente la concentración de CEA se encuentra por encima de 192 ng/ml y los niveles de amilasa son bajos.
NPIM
La neoplasia papilar intraductal mucinosa se origina del epitelio ductal,
lo que da lugar a secreciones mucosas y,
por tanto,
dilatación de los conductos pancreáticos.
Constituyen aproximadamente el 20% de las lesiones quísticas pancreáticas y existen tres formas: lesión del conducto principal,
lesión de ramas laterales (benigna en la mayoría de las ocasiones) y lesión mixta.
Presenta una frecuencia similar en mujeres y hombres y una edad media de presentación de 65 años.
La mayoría de las lesiones son detectadas de forma causal en estudios de imagen,
aunque cuando son sintomáticos cursan con dolor abdominal,
pérdida de peso,
episodios de pancreatitis e insuficiencia pancreática.
Tanto en la TCMD como en RM,
la variante del conducto principal se manifiesta como dilatación segmentaria o difusa del conducto pancreático principal.
Es característica la presencia de pequeños nódulos intraductales y en ocasiones puede verse atrofia del parénquima pancreático.
En eco-endoscopia se observa una ectasia del conducto pancreático junto con una dilatación quística de las ramas laterales por obstrucción secundaria a la producción de mucina.
La variante de las ramas laterales tiene dos patrones distintos: macroquístico y microquístico.
En la TCMD se observa una lesión hipocaptante,
heterogénea,
clásicamente localizada en el proceso uncinado aunque puede presentarse en cualquier localización.
En RM se observa como pequeñas masas ovaladas hiperintensas en secuencias potenciadas en T2,
a menudo comunicadas con el conducto pancreático principal y que pueden ser multifocales hasta en el 30% de los casos.
La morfología en eco-endoscopia varía desde formas uniloculares anecoicas a lesiones complejas multiquísticas.
El calibre del conducto pancreático principal es normal y la comunicación entre la lesión y el conducto principal puede ser apreciada mediante esta técnica.
Los hallazgos de imagen son,
de forma aislada,
indistinguibles de otras neoplasias quísticas como el cistoadenoma mucinoso y la variante macroquística del cistoadenoma seroso (figuras 8,
9 y 10).
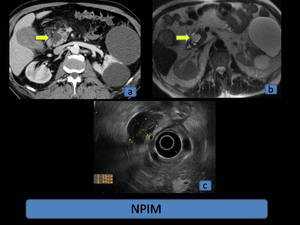
Fig. 8: NPIM. (a): TCMD con contraste intravenoso, reconstrucciones multiplanares, plano axial, lesión multiquística localizada en porción cefálica. (b): RM, secuencia axial T2 SSFSE, se confirma la presencia de una lesión bien delimitada, hiperintensa, con tabiques en su interior. (c): Eco-endoscopia del mismo paciente, lesión bien delimitada, de ecogenicidad intermedia y con septos en su interior.
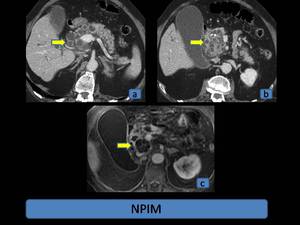
Fig. 9: NPIM. (a) y (b): TCMD con contraste intravenoso, reconstrucciones multiplanares, planos axiales, lesión multiquística, localizada en cabeza y cuerpo pancreáticos, con calcificaciones amorfas y que provoca hidrops vesicular, dilatación de la vía biliar intra y extrahepática y del Wirsung. (c): RM del mismo paciente, axial T1 con gadolinio, lesión multiquística, con loculaciones de pequeño tamaño, hipointenso y con mínimo realce de los tabiques.
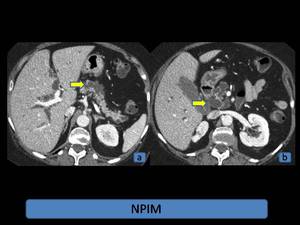
Fig. 10: NPIM. (a) y (b): TCMD con contraste intravenoso, reconstrucciones multiplanares, planos axiales, lesión multiquística, distribuida por la totalidad del parénquima pancreático, con dilatación de la vía biliar intra y extrahepática y del conducto pancreático principal.
En el análisis del líquido de la lesión se encuentran valores elevados de CEA (por encima de 192 ng/ml) y cifras normales o elevadas de amilasa.
Según la Organización Mundial de la Salud,
pueden ser benignos (sin displasia),
borderline (displasia en grado medio-moderado) y malignos.
Las formas malignas se encuentran en aproximadamente el 70% de los casos que afectan al conducto principal y en aproximadamente el 25% de los casos que afectan únicamente a las ramas laterales.
Los criterios de malignidad son: nódulos murales,
componente focal sólido,
dilatación del conducto principal > 18 mm o realce de la pared del conducto pancreático principal.
Así mismo,
un tamaño inferior a 3 cm sin nódulos murales en la variante de las ramas laterales se asocia con bajo grado de malignidad.
OTROS
El tumor neuroendocrino quístico representa únicamente el 17% del total de los tumores neuroendocrinos.
Presenta una frecuencia similar en mujeres y hombres y una edad media de presentación de 53 años.
Sin embargo,
suelen ser más grandes (49 mm vs 23,5),
más frecuentemente sintomáticos (73% vs 45%) y con mayor probabilidad de ser no-funcionantes (80% vs 50%) que los tumores neuroendocrinos sólidos.
Los pacientes con tumores neuroendocrinos quísticos tienen mayor probabilidad (3,5 veces más) de presentar un síndrome MEN I que los pacientes con tumores neuroendocrinos sólidos.
El riesgo de metástasis es igual para ambas variantes.
Se presentan más frecuentemente en el cuerpo y la cola pancreática.
Debido a la naturaleza hipervascular de los tumores neuroendocrinos,
se presentan en los estudios de imagen como masas quísticas con septos en su interior y con un anillo hipervascular periférico.
En la eco-endoscopia sus hallazgos de imagen son inespecíficos: lesiones heterogéneas,
bien delimitadas,
completamente quísticas o sólidas con componentes quísticos.
El líquido del quiste presenta niveles bajos de CEA y de amilasa.
El tumor pseudopapilar sólido es un tumor raro con bajo riesgo de malignidad.
Aproximadamente el 91% de estos tumores se presentan en mujeres,
con una edad media de presentación de 22 años.
Clínicamente cursan con dolor y masa palpable en la exploración.
Puede presentarse en cualquier localización del páncreas,
con una cierta predilección por la cola.
Aproximadamente el 20% presentan metástasis al diagnóstico.
Suelen ser tumores bien circunscritos,
con áreas hiperintensas en secuencias potenciadas en T2 en relación con los componentes quísticos.
También pueden presentan áreas hiperintensas en T1 debido a procesos de degeneración hemorrágica.
Las calcificaciones periféricas están presentes en aproximadamente el 31% de los casos.
En eco-endoscopia se presentan como masas heterogéneas,
bien delimitadas,
predominantemente sólidas con áreas quísticas en su interior.
Los niveles de CEA del líquido de la lesión pueden ser variables y los de amilasa son bajos.
Tratamiento y seguimiento de los pacientes:
La decisión del tratamiento quirúrgico se basa,
tanto en el potencial de malignidad,
como en la presencia de síntomas relacionados con la lesión.
En general,
toda neoplasia quística pancreática sintomática en un paciente operable debería ser valorada para tratamiento quirúrgico resectivo.
En el caso de una neoplasia quística pancreática incidental y asintomática,
es fundamental averiguar si su estirpe es serosa o mucinosa,
para establecer el riesgo de degeneración maligna.
Tras estas valoraciones y dependiendo de la edad y la situación basal del paciente,
se indicará tratamiento quirúrgico o seguimiento mediante pruebas de imagen.
En el caso del cistoadenoma seroso,
la transformación maligna es rara,
por lo que la cirugía solo se recomienda en pacientes sintomáticos.
Sin embargo,
recientes estudios han demostrado la existencia de variantes agresivas,
por lo que se recomienda un seguimiento mediante pruebas de imagen cada 6-12 meses hasta los 2 años,
para demostrar la ausencia de crecimiento.
Para los pacientes intervenidos y con márgenes quirúrgicos libres,
no es necesario el seguimiento mediante pruebas de imagen.
En cuanto al cistoadenoma mucinoso,
debido a su potencial maligno,
la cirugía está recomendada en todos los casos.
No hay riesgo de recurrencia después de la cirugía del cistoadenoma mucinoso benigno con márgenes negativos,
por lo que el seguimiento mediante pruebas de imagen no es necesario.
Sin embargo,
en pacientes operados con anatomía patológica compatible con cistoadenoma mucinoso maligno,
el seguimiento se realizará cada 6 meses debido al riesgo elevado de recurrencia.
En la neoplasia papilar intraductal mucinosa,
todos aquellos casos sintomáticos deben ser intervenidos.
La guías de manejo recomiendan la cirugía para las variantes del conducto pancreático principal y las formas mixtas que presentan un tamaño mayor de los 3 cm.
También se recomienda la resección en las variantes de las ramas laterales o secundarias asintomáticas de tamaño inferior a los 3 cm pero con hallazgos de imagen sospechosos de malignidad o que presenten un crecimiento rápido (más de 2 mm por año).
Aquellas lesiones de pequeño tamaño que deriven de las ramas laterales sin criterios de malignidad requieren seguimiento mediante TCMD o RM.
Se recomienda control anual en tumores inferiores a 1 cm,
cada 6-12 meses en lesiones entre 1 y 2 cm y control cada 3-6 meses en las lesiones mayores de 2 cm.
Debido al riesgo de recurrencia,
se recomienda seguimiento mediante pruebas de imagen después de la cirugía,
cada 6 meses en caso de una NPIM maligna y anual en la NPIM benigna.
Tanto en el tumor neuroendocrino quístico como en el tumor pseudopapilar sólido,
el tratamiento de elección es la cirugía.











