A) EL SÍNDROME DE LA ARTERIA MESENTÉRICA SUPERIOR (SAMS) O SÍNDROME DE WILKIE (SW):
Causa poco frecuente (0.2-1%) de obstrucción duodenal de origen vascular,
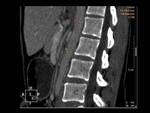
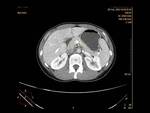
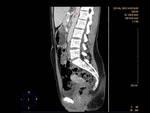
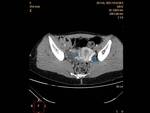
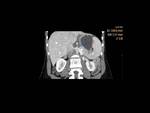
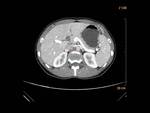
producida por una compresión extrínseca del duodeno por la AMS y la aorta Fig. 2 .
La primera descripción del síndrome de la arteria mesentérica superior (SAMS) parece corresponder a Boener (1754),
y posteriormente (1861) Rokitansky sugirió su mecanismo de producción.
Wilkie en 1921 publicó por la primera serie de casos de compresión duodenal por la AMS y realizó un extenso estudio del tema,
por lo cual se conoce esta entidad como síndrome de Wilkie.
La obstrucción funcional de la tercera porción del duodeno entre la AMS y la aorta abdominal,
se asocia con causas congénitas o adquiridas que disminuyen el ángulo entre ambos vasos,
como son:
- pérdida de grasa retroperitoneal (descenso brusco de peso asociada a trastornos de la alimentación (anorexia nerviosa,
síndromes malabsortivos),
o a estados catabólicos (neoplasias,
quemados...),
- alteraciones restrictivas (deformaciones óseas,
escoliosis,
o hiperlordosis grave)
- procedimientos que determinan hiperextensión dorsal (especialmente en pacientes postquirúrgicos de cirugía correctora de deformaciones óseas (escoliosis..
),
trauma severo...)
- causas congénitas,
incluyen el ligamento de Treitz corto,
lo que provoca que el duodeno quede suspendido más alto de lo normal (casos de SAMS en gemelos idénticos) y el nacimiento anormalmente bajo de la AMS.
Se desconoce la incidencia real del SAMS debido a que se trata de un proceso en muchas ocasiones infradiagnosticado,
que puede presentarse a cualquier edad,
aunque es más frecuente en adolescentes y en adultos jóvenes y que tiene un predominio en el sexo femenino.
Las manifestaciones clínicas características son secundarias a obstrucción intestinal alta y generalmente coexisten con otras enfermedades que enmascaran el diagnóstico en etapas tempranas de su presentación.
Son :
-
Dolor abdominal postpandrial precoz,
epigástrico,
que alivia en posición genupectoral,
en decúbito lateral izdo o prono (59%)
-
Vómitos biliosos (50%) / Nauseas (40%)
-
Distensión abdominal,
saciedad precoz,
sensación de plenitud gástrica (32%)
-
Anorexia (18%).
-
Alteraciones hidroelectrolíticas.
El diagnóstico es clínico,
aunque para ello es necesario un alto índice de sospecha y la confirmación diagnóstica viene dada mediante el uso de estudios radiológicos.
Radiológicamente se usarán consideraciones anatómicas estáticas,
cuyas medidas son difíciles de determinar,
por lo que los aspectos clínicos serán imprescindibles para confirmar o excluir el síndrome.
La AMS se origina en la aorta a nivel de L1,
no obstante la variabilidad es de T12 a L3.
El ángulo aorto-mesentérico normal en adultos (> 25º) contiene la vena renal,
el proceso uncinado del páncreas,
la tercera porción del duodeno y la grasa retroperitoneal.
Fig. 1
El SAMS sólo puede ser confirmado,
teóricamente,
cuando la tercera o cuarta porciones del duodeno son comprimidas por la AMS y la aorta,
la columna o ambos,
y se aceptan los límites del ángulos patológicos los menores de 25º con más de 10 mm de distancia.
Fig. 1
Por otra parte las longitudes mayores o menores del ligamento de Treitz y el nivel del duodeno en la columna (L2 o L3) también parecen ser determinantes en la patogénesis.
Dentro de los estudios de imagen se usarán:
-
Estudio baritado (esófagogastroduodenal) con una sensibilidad del 82%.
Los hallazgos clásicos son la dilatación de la primera y segunda porción del duodeno,
flujo antiperistáltico de bario proximal a la obstrucción,
retardo del tránsito intestinal de 4-6 h y alivio de la obstrucción con los cambios posturales del paciente.
-
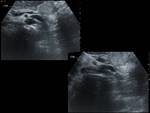
Eco-doppler como estudio inicial en casos sospechosos.
-
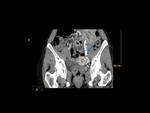
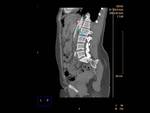
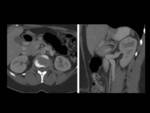
AngioCT: permite la medición precisa del ángulo aorto-mesentérico y de la distancia entre la AMS y la aorta abdominal Fig. 2 Fig. 3 Fig. 4 .
-
Angiografía y arteriografía selectiva de la AMS: reservada para casos dudosos con otros métodos.
Disminución del ángulo aorto-mesentérico,
habitualmente en rango de 6-11º (valor normal > 25º),
con disminución de la distancia aorto-mesentérica entre 2 y 8 mm (valor normal > 10 mm),
siendo éste último más importante que el ángulo.
El diagnóstico diferencial deberá realizarse con procesos como úlcera péptica duodenal,
colelitiasis,
pancreatitis crónica y angina abdominal,
así como con las condiciones que produzcan megaduodeno (enteropatía diabética,
trastornos de la alimentación,
enfermedades del colágeno,
enfermedad de Chagas..)
El tratamiento inicial del síndrome de Wilkie será médico,
para mejorar el estado nutricional y resolver las complicaciones asociadas y si con el tratamiento conservador no se restablece el tránsito intestinal,
se deberá corregir la causa de la obstrucción mediante tratamiento quirúrgico.
El tratamiento definitivo será el etiológico,
siendo generalmente el factor desencadenante más frecuente la pérdida de peso.
B).
SÍNDROME DE CASCANUECES:
El síndrome de cascanueces (SC) consiste en una compresión de la vena renal izda entre la AMS y la aorta,
causando una estenosis funcional de la vena.
Constituye una causa infrecuente de hematuria no glomerular persistente,
procedente del sistema colector izquierdo,
secundario a una compresión extrínseca de la vena renal izquierda,
que traducirá una hiperpresión del sistema venoso renal izdo y el consiguiente desarrollo de varices en la pelvis renal y uréter que podrán comunicarse con la vía excretora y dar lugar a episodios de hematuria.
Fue descrito por primera vez en 1950,
al referirse al hecho de que la aorta y la AMS formarían los dos brazos del cascanueces,
que podría potencialmente comprimir la vena renal produciendo una hiperpresión en su flujo,
y posteriormente en 1972,
fué De Shepper quién dió el nombre a este síndrome.
La etiología no está clara,
aunque existen trabajos en la literatura que postulan una anomalía embriológica en la separación entre la aorta y la AMS,
al igual que sucede en el síndrome de Wilkie,
cuando la misma horquilla vascular comprime el duodeno.
La incidencia exacta es desconocida,
debido a que en múltiples ocasiones es asintomático y frecuentemente el diagnóstico se realiza tras haber descartado otras causas más frecuentes de hematuria y dolor lumbar.
Suele producirse en personas relativamente jóvenes (tercera y cuarta décadas de la vida) y previamente sanas.
Es relativamente más frecuente en mujeres.
Anatomia:En condiciones normales,
la vena renal izquierda se sitúa anterior a la aorta en el ángulo formado entre la aorta y la arteria mesentérica superior (AMS).
La AMS se origina de la aorta abdominal en forma rectangular con un trayecto de 4-5 milímetros en dirección ventral,
para luego iniciar un descenso caudal dando como resultado la configuración de una ”J” invertida.
Esta disposición anatómica previene la compresión de la vena renal izquierda.
Pero existen factores y situaciones que predisponen o asocian una compresión de la vena como son
- la disminución del ángulo entre la aorta y la AMS,
- una rama anormal o un origen diferente de la AMS en la aorta o de la arteria gonadal izquierda,
- la ptosis posterior del riñón izquierdo,
- predisposición anatómica (escasa grasa perirrenal y lordosis lumbar acentuada),
o
- durante el embarazo.
La presencia de fístulas arteriovenosas intrarrenales que se acompañan de un aumento de flujo a nivel de la vena renal,
con hiperpresión de ésta,
pueden originar el llamado “efecto pseudocascanueces”.
FP: La compresión extrínseca de la vena renal izquierda,
presente en este síndrome producirá una hipertensión de la vena con ruptura de su fina pared en el fórnix del cáliz renal,
lo que provocará una hematuria macroscópica intermitente o microhematuria y una dilatación de la zona hiliar de dicha vena,
a su salida del riñón (con desarrollo de una circulación venosa colateral hacia otros territorios,
principalmente la vena gonadal (ovárica o espermática),
pero también los plexos piélicos,
pericaliciales,
periureterales y lumbares).
Este sería el S.C anterior.
Pero cuando la vena renal izquierda tiene un curso retroaórtico entre la aorta abdominal y un cuerpo vertebral,
puede producirse el S.C posterior.
Pueden coexistir ambos síndromes,
anterior y posterior,
por la duplicación de vena renal izquierda,
aunque es raro.
CL:
1.
Pueden permanecer asintomáticos
2.
Manifiestarse como episodios de hematuria macro o microscópica (+/- anemia,
incluso en rango transfusional) que se puede acompañar se dolor en fosa renal izda y/o dolor abdominal.
Característicamente,
la hematuria es más intensa con el ortostatismo (al aumentar la presión sanguínea en la vena renal izda) y con el ejercicio.
3.
También se ha descrito este síndrome como causa de proteinuria ortostática en niños.
4.
Los varones pueden presentar varicocele,
normalmente en el lado izquierdo y las mujeres,
congestión pélvica Fig. 5 Fig. 7 (que se puede traducir como síntomas de dismenorrea,
disuria,
dispareunia y dolor pélvico) y/o varices a nivel vulvar,
glúteos o en miembros inferiores.
En cuanto al diagnóstico,
la mayoría de las ocasiones se diagnóstica tardíamente por la historia natural de la enfermedad.
1.
Debemos tenerlo en cuenta dentro del diagnóstico diferencial,
en pacientes jóvenes y delgados que presenten hematuria y proteinuria y si se presenta como microhematuria aislada,
el diagnóstico será por exclusión de las posibles causas de este síntoma.
2.
Diagnóstico: Las anomalías vasculares del retroperitoneo son poco frecuentes pero cada vez se diagnostican más por el uso de diferentes técnicas de imágen.
A) La técnica de elección es la flebografía retrógrada,
ya que permitirá determinar cálculos de gradiente de presión entre la vena renal en su porción distal y la cava inferior,
definir el punto de compresión y valorar si existen o no vasos colaterales.
El gradiente medio de presión normal entre la vena renal y la vena cava oscila generalmente entre 0 y 1 mm de Hg,
así,
según Takebayashi et al.,
si es <1 será normal,
si es 1-3 será bordeline y si es >3 traducirá hipertensión de la vena renal izda muy sugestivo de pinzamiento Ao-mesentérico; Pero dado que el cálculo de este gradiente no es imprescindible para el diagnóstico,
porque pueden presentarse variaciones del mismo en función del grado de circulación colateral existente y que la flebografía es una prueba invasiva,
en la práctica diaria,
se emplean métodos menos agresivos,
no invasivos,
como son la ECO,
ECO-Doppler,
CT y RM.
B) Mediante ecografía (Fig. 10) se ha postulado (Okada et al.) la obtención de medidas de cálculo de la ratio entre el diámetro de la parte dilatada de la vena renal izda con la parte estrecha de la misma y el diámetro aórtico respectivamente,
así como la diferencia de diámetros entre la vena renal dcha e izda,
estableciendo como valores diagnósticos la elevación de al menos dos de estos parámetros,
estableciendo como puntos de corte 3.7,
0.75 y 1.7 mm respectivamente.
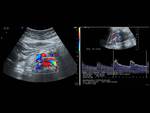
La eco-doppler Fig. 11 permite la medición de diámetro y velocidad máxima de flujo en la vena renal antes y después de su paso por la horquilla Ao-mesentérica,
con una S 78% y una E 100%; Una ratio distal/proximal > 5 es diagnóstica para el S.C.
Dado que es una técnica inocua,
puede ser útil en el screening de proteinuria ortostática.
C) El CT con reconstrucción 3D o volumétrica (VR) Fig. 4, Fig. 6,
Fig. 8,
Fig. 9,
Fig. 12 aportará información sobre la anatomía de los grandes vasos y su relación con la vena renal izda,
la compresión de la vena entre la Ao y la AMS,
la distensión secundaria de la vena,
la evidencia de congestión renal,
y la circulación venosa colateral.
D) Existe menor experiencia con la RM para el diagnóstico de S.C.
La actitud terapéutica está condicionada por la gravedad y forma de presentacíón del cuadro clínico,
es decir dependiendo de la magnitud de la hematuria,
la intensidad de las manifestaciones clínicas y la presencia de circulación venosa importante.
Las opciones varían desde una actitud conservadora (en pacientes con dolor en flanco izdo y/o moderada microhematuria,
así como en pacientes en la pubertad en los que existe una gran posibilidad de remisión tras el desarrollo) hasta un manejo quirúrgico (que va desde deshacer el túnel fibrótico que existe entre la aorta y la mesentérica superior para liberar la vena renal hasta la nefrectomía) o intervencionista (mediante la colocación de stents intra o extravasculares) según el grado de afectación.