Revisión del tema.
Se realiza una revisión actualizada de la literatura acerca de los tumores renales en la infancia,
describiendo la epidemiología,
clínica,
consideraciones histopatológicas y el papel de la imagen en el diagnóstico,
estadiaje y seguimiento de estos tumores.
Ilustramos con nuestra iconografía aquellas masas que en la edad pediátrica afectan con mayor frecuencia al riñón.
Existe una gran variedad de masas renales en la infancia.
En el periodo perinatal las masas renales no suelen tener un origen neoplásico,
siendo la hidronefrosis y el riñón displásico multiquístico las que mayoritariamente las producen (1,
2)
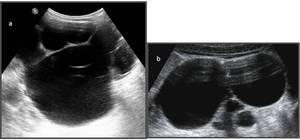
Fig. 2: Figura 1. Imágenes ecográficas a nivel del riñón. a) en el caso de una hidronefrosis gardo IV, b) en el caso de un riñón displásico multiquístico.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
.
Solo un 20% tienen un origen tumoral.
El tumor sólido por excelencia en menores de 2 meses es el nefrona mesoblástico,
otros menos frecuentes serán el tumor de Wilms (TW),
el tumor renal rabdoide,
y el tumor osificante de la infancia (1).
Desde el primer año de vida y durante la primera década,
los tumores son más frecuentes,
aunque mayoritariamente tienen un buen pronóstico,
alcanzando tasas de curación de más del 90% (Tabla 1) (2,3).
Tabla 1
|
Bajo riesgo
|
TW epitelial
Nefroma mesoblástico.
Tumor quístico multilocular
Angiomiolipoma
Tumor renal osificante de la infancia.
Tumor estromal metanéfrico
|
|
Riesgo intermedio
|
TW (no anaplásico)
|
|
Alto riesgo
|
TW (anaplásico)
Carcinoma de células renales.
Sarcoma de células claras.
Tumor rabdoide.
Carcinoma de células renales.
|
El tumor más frecuente es el TW (87%),
aunque pueden desarrollarse otros menos frecuentes,
con los que debemos establecer el diagnóstico diferencial (tabla 2) (3).
Tabla 2.
|
NEOPLASIA
|
Rango de edad (pico)
|
|
Nefrona mesoblástico congénito.
|
0-1 año (1-3 meses)
|
|
Tumor de Wilms.
|
1-11 años (3-4 años)
|
|
Nefroblastomatosis.
|
Cualquier edad (6-18 meses)
|
|
Tumor renal quístico multiloculado.
|
3 meses- 4 años (1-2 años)
|
|
Sarcoma de células claras.
|
1-4 años (2 años)
|
|
Tumor rabdoide
|
6 meses-9 años (6-12 meses)
|
|
Tumor estromal metanéfrico
|
15 meses-83 años (24 meses)
|
|
Tumor renal osificante de la infancia.
|
6 dias-14 meses (1-3 meses)
|
|
Carcinoma de células renales.
|
6 meses- 60 años (10-20 años)
|
|
Angiomiolipoma
|
6 -41 años (10 años)
|
|
Neuroblastoma retroperitoneal.
|
1-10 años (< de 5años 90%; 1año)
|
|
Teratoma retroperitoneal.
|
Cualquier Edad
|
|
Linfoma
|
>de 10 años
|
No debemos olvidar que en ocasiones el riñón se ve infiltrado por tumores de origen extrarenal,
bien por contigüidad como en el caso los tumores retroperitoneales más frecuentes,
neuroblastoma y teratoma o bien,
por diseminación hematógena,
como en el caso de las leucemias/linfomas o las metástasis (1).
El diagnóstico de una neoplasia renal en el niño es sugerido por la historia clínica,
la edad de presentación y las características propias de la imagen,
sin embargo,
a menudo no es posible diferenciar un tumor de otro basándonos únicamente en la semiología radiológica y el diagnóstico final precisa del examen histológico de la pieza quirúrgica (1-4).
La técnica de estudio inicial será habitualmente la ecografía (US),
seguida de la tomografía computarizada (TC) o la resonancia magnética (RM) de abdomen,
para completar el estudio y su estadiaje (1-3).
TUMOR DE WILMS O NEFROBLASTOMA (TW).
El TW es el tumor abdominal más común y el más frecuente en el riñón del niño.
Muchos tumores renales pediátricos en el pasado,
se clasificaron como TW,
siendo en la actualidad reconocidos como entidades independientes. Constituye el 87% de las masas renales tumorales en la infancia,
afectando a 7,8 por millón de niños menores de 15 años.
Su pico de incidencia es máximo en torno a los 3-4 años.
Su afectación es bilateral hasta en un 5-7% de los niños,
por lo general como tumores sincrónicos; estos se presentan a edades más tempranas y se asocian a anomalías congénitas y a focos de nefroblastomatosis con más frecuencia que los unilaterales.
Los niños con TW asocian anomalías congénitas (1,
5) en aproximadamente un 12% de los casos,
entre las que destacan:
- Anomalías genitourinarias (5%) (criptorquidia en 2,5% e hipospadias en 1,8%,…).
- Malformaciones musculoesqueléticas (3%) (pie equinovaro,
fusión costal,
displasia de cadera).
- Hemihipertrofia (2,5%)
- Aniridia (1%)
Por otro lado existen anomalías que asocian un riesgo aumentado de desarrollar TW (1,
5),
como por ejemplo:
- El riñón en herradura (riesgo aumentado 1.96 veces más que en la población normal).
- Riñón displásico multiquístico,
hemihipertrofia (3%).
- Sd.
Beckwith-Wiedemann,
que en un 10% presentan este tipo de tumor y/o un hepatoblastoma y/o un carcinoma suprarrenal; otros posibles hallazgos son macroglosia,
hemihipertrofia,
visceromegalias.
- Aniridia esporádica (33%).
- Sd.
WARG (Wilms,
aniridia,
malformaciones genitourinarias,
retraso mental).
- Síndrome de Denys-Drash (seudohermafroditismo masculino,
insuficiencia renal de inicio precoz con esclerosis mesangial y riesgo alto de TW).
- Sd.
de Bloom (dismunición del crecimiento y la inmunidad,
telangiectasias faciales).
- Trisomías.
- Ano imperforado con fístula rectouretral.
Los casos de tumores familiares se ven asociados a mutaciones de los genes (WT1: 11p13 y WT2: 11p15) ,
así como otros loci en los cromosomas 1,
8 y 12 ,
y suponen una minoría de los casos (1%)(1-3)
El control y seguimiento de estos niños se hará mediante ecografía abdominal cada 3-6 meses durante 7-10 años (5).
El TW se origina del blastema metanéfrico primitivo.
Este suele desaparecer en la maduración fetal y no debe persistir más allá de las 36 semanas de gestación.
Cuando lo hace origina focos de nefroblastomatosis,
sobre los que puede desarrollarse el TW.
La existencia de estos focos es el principal factor de riesgo para su desarrollo (1,
2).
El TW extrarrenal es raro,
las localizaciones más frecuentes son el retroperitoneo,
la región inguinal,
la pelvis y el tórax.
Histológicamente,el TW clásico es trifásico,
está compuesto por blastema,
estroma y epitelio.
Se trata de un tumor sólido grande y voluminoso con una pseudocápsula que comprime el parénquima renal.
Suele tener focos de hemorragia,
necrosis y quistes en su interior.
Tiende a surgir de la periferia del riñón respetando el sistema colector al que puede desplazar o dilatar parcial o totalmente por compresión del mismo (1).
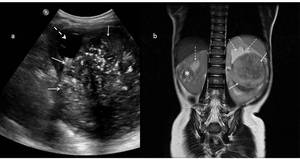
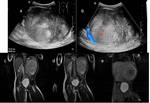
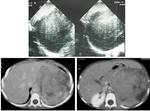
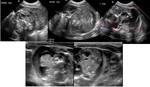
Fig. 3: Figura 2. Niño de 2 años con masa abdominal palpable en el flanco izquierdo. a) Imagen de ecografía sobre el flanco izquierdo donde observamos una masa (flechas continuas) redondeada, de ecoestructura heterogénea, de márgenes precisos que parece depender del riñón izquierdo. b. RM secuencia T2 plano coronal del mismo paciente. En ambas técnicas se identifica la dilatación del cáliz superior por el tumor (flechas discontinuas) . En este caso identificamos un segundo tumor de menor tamaño en el riñón derecho contralateral (*).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
El pronóstico de los niños con TW depende fundamentalmente del grado de anaplasia,
focal o difusa,
que es el indicador mas sensible y que condicionará una escasa respuesta a la quimioterapia y una mayor tasa de recidivas,
sobre todo si es difusa (4% de casos).
Afectan a un grupo de mayor edad y tienen una alta tasa de metástasis linfáticas al diagnóstico.
Metastatiza habitualmente al pulmón (85%),
al hígado y ganglios regionales (1).
Clínicamente,
el niño se presenta con una masa abdominal palpable (75-95%). El 25% de los niños presentan microhematuria ,
siendo la macrohematuria poco común y generándose por invasión del sistema colector.
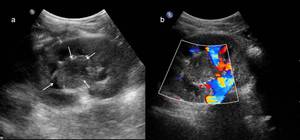
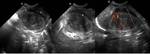
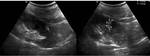
Fig. 4: Figura 3. Niño de 11 años que debutó con macrohematuria, se realiza estudio ecográfico y urografía iv. a y b) muestran imágenes de ecografía a nivel del riñón izquierdo en el que se identifica una masa (flechas) hipovascularizada a nivel del seno renal de un diámetro máximo de 3,3 cm).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
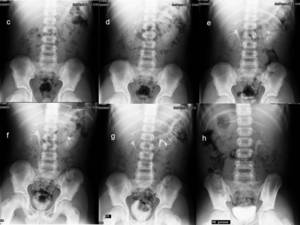
Fig. 5: Figura 4. c, d, e, f, g, h) muestran las imágenes seriadas habituales de un estudio urográfico, en las que se observa la una amputación del grupo calicial superior del riñón izquierdo. Se comprobó con biopsia y posterior exéresis que se trataba de un TW estadio I.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
La hipertensión debido a la producción de renina por el tumor se observa en aproximadamente 25% de los casos.
En el diagnóstico por la imagen encontramos hallazgos inespecíficos que incluyen la existencia de una gran masa en el flanco,
que oblitera los planos de separación grasa del psoas y desplaza el gas de las asas intestinales en la radiografía simple de abdomen.
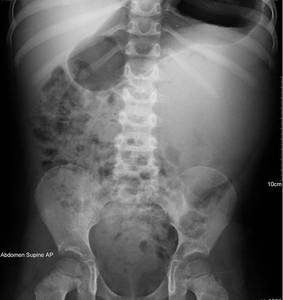
Fig. 6: Figura 5. Rx simple de abdomen donde se observa la existencia de un aumento de
densidad parcialmente bien definido, en el hemiabdomen izquierdo, que desplaza las
asas intestinales a la derecha y que sugiere la existencia de una masa a dicho nivel.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
Se pueden observar calcificaciones en el 9% de estos tumores (2).
En el estudio ecográficose visualiza una gran masa,
de márgenes bien delimitados y de ecogenicidad homogénea interrumpida por áreas hipoecogénicas y otras ecogénicas,
que se corresponden con focos de necrosis,
calcio o grasa
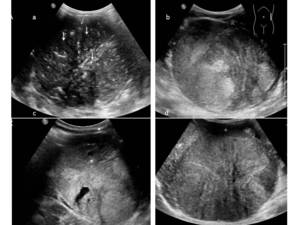
Fig. 7: Figura 6. Imágenes de ecografía de 4 TW diferentes. En todas ellas (a,b,c,d) se observan grandes masas bien definidas y heterogéneas. En a) vemos focos puntiformes ecogénicos (flechas) probablemente por depósitos cálcicos, en c) existen dos zonas quísticas (* ).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
En ocasiones se identifica un límite ecogénico bien definido que corresponde a la pseudocápsula y/o una banda hipoecogénica por el parénquima renal comprimido.
El TW se puede exterder a las estructuras vasculares contiguas,
venas renales ipsi y contralaterales,
vena cava inferior y aurícula derecha.
Por ello es fundamental su valoración durante la exploración ya que este dato puede ser decisivo en la instauración de quimioterapia antes de la cirugía (1-3)
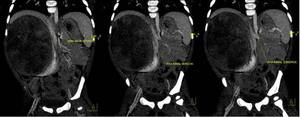
Fig. 8: Figura 7. Reconstrucciones coronales MIP de TC de abdomen con contraste iv en fase portal,
en las que se aprecia compresión de los vasos sin ocupación de los mismos. No hay trombosis
de la vena cava inferior (a), vena renal derecha (b), ni vena renal izquierda (c).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
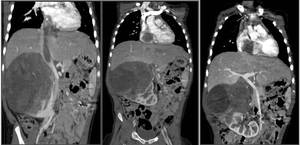
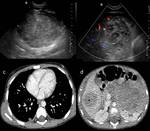
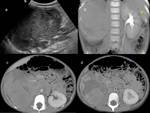
Fig. 9: Figura 8. Reconstrucciones en plano coronal de TC de abdomen con contraste iv. donde se observa la existencia de una gran masa dependiente del polo superior del riñón derecho de limites bien definidos, heterogénea, con áreas pseudoquísticas o necróticas en su interior, y (a), trombosis de la vena cava inferior (*) y (b y c) de la aurícula derecha (flechas).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
.
También debe revisarse exhaustivamente el riñón contralateral para descartar la existencia de tumor sincrónico,
o anómala congénita.
Con el estudio de TC igualmente detectamos una masa de densidad heterogénea,
y se definen muy bien las áreas intratumorales de grasa o calcificación (1,
3).
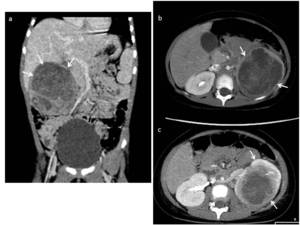
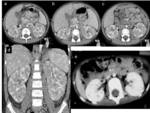
Fig. 10: Figura 9. Reconstrución coronal a) y cortes axiales b y c) de TC abdominal con contraste iv. donde se aprecia la existencia de masas (flechas) de márgenes bien definidos y un interior muy heterogéneo.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
La administración de contraste en estos estudios es fundamental para detectar metástasis a distancia,
extensión del tumor a la vena renal o a la cava,
la existencia de tumores sincrónicos o la existencia de restos nefrogénicos.
El tumor realzará menos que el parénquima renal adyacente.
Se pueden encontrar niveles liquido-liquido.
El estudio de TC debe ampliarse al tórax para descartar metástasis pulmonares,
siendo más sensible que la radiografía simple de tórax en su detección.
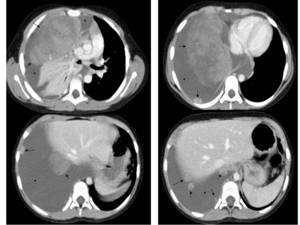
Fig. 11: Figura 10. Niño de 6 años con antecedente de TW intervenido hace 1 año, que presenta fiebre y dolor torácico. Imágenes axiales de TC de tórax con contraste iv. en las que se observa desplazamiento mediastínico a la izquierda, un importante derrame pleural derecho (*), y múltiples metástasis pleurales (flechas negras). Pulmón colapsado (flechas blancas).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
Es también la técnica de elección para el seguimiento de aquellos TW intervenidos (3 al año los 2 primeros años después del diagnóstico).
En RM observaremos una intensidad de señal heterogénea por la existencia de necrosis,
grasa,
sangre y quistes,
aunque es fundamentalmente baja en las secuencias T1 y elevada en las T2
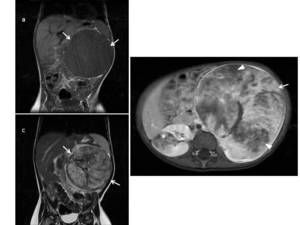
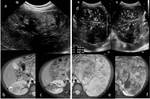
Fig. 12: Figura 11. Imágenes de RM, a) plano coronal secuencia T1, en la que se observa una gran masa (flechas) de señal heterogénea, fundamentalmente hipointensa. b) plano coronal, secuencia T2 en la que se aprecia una gran heterogeneidad en la intensidad de señal. c) plano axial, secuencia T1 con supresión grasa y contraste iv. donde se observa una señal muy heterogénea con áreas hipointensas correspondientes a zonas de necrosis (puntas de flecha) que realzan menos que el parénquima renal sano. Se visualiza un segundo tumor, de menor tamaño en el riñón derecho (*)
References: Hospital Universitario Virgen de la Arrixaca. Murcia
Los bordes del tumor se definen mejor tras la administración del gadolinio,
permaneciendo con un realce menor que el parénquima renal sano contigüo,
del mismo modo que ocurría en el TC.
Permite detectar focos metastásicos y la afectación vascular,
siendo la técnica más sensible para determinar la invasión de estructuras vecinas,
en ocasiones tarea extremadamente difícil.
Existen variedades quísticas de este tumor con lo que tendremos que realizar diagnóstico diferencial con otros tumores como nefroblastoma quístico parcialmente diferenciado o el nefroma quístico multiloculado 1,3)
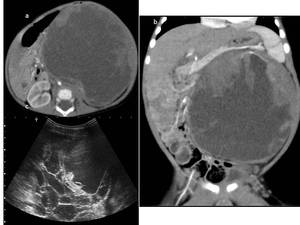
Fig. 13: Figura 12. TW variante quística, indistinguible de tumor con extensas áreas de necrosis
que no realzan con el contraste iv. a) imagen de TC de abdomen con contraste iv, plano axial, b) imagen de TC de abdomen con contraste iv, reconstrucción coronal c) imagen ecográfica en la que se confirma su naturaleza quística.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
ESTADIAJE DEL TW (1-3,
5,
6).
- Tumor limitado al riñón.
Completamente resecable,
con capsula renal intacta.
El seno renal puede estar infiltrado (no mas allá de 2 mm),
pero no afecta a los vasos del hilio
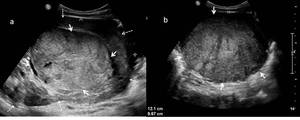
Fig. 14: Figura 13. Niño de 5 años que debuta con masa abdominal palpable. a y b)Imagenes de ecografía en las que se identifica una tumoración bien definida (flechas), de ecogenicidad heterogénea, que a pesar de sus grandes dimensiones permanecía rodeada de parénquima renal (flechas discontinuas). Tras resección quirúrgica se confirmó que se trataba de un TW estadio I.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
- El tumor infiltra tejidos perirrenales (grasa perirrenal,
vasos del hilio). Completamente resecable.
Invasión local confinada al flanco
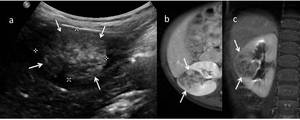
Fig. 15: Figura 14. Niño de 2 años con TW bilateral (estadio V). La tumoración del riñón derecho (flechas) presentaba unos márgenes bien definidos, era heterogénea, y parecia limitarse al riñón, con probable afectación del seno renal, sin invasión de los vasos del hilio renal ni de la cava inferior. El estudio histológico tras su exéresis, determinó que se trataba de un estadio II.
a) imagen de ecografía a nivel del riñón derecho, donde el parénquima renal rodea la
tumoración. b) Imagen RM secuencia T1 con saturación grasa y contrate iv, plano axial y
c) en plano coronal.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
- Tumor residual confinado al abdomen: nódulos a distancia abdominales,
afectación peritoneal,
márgenes de resección positivos.
Tumor biopsiado
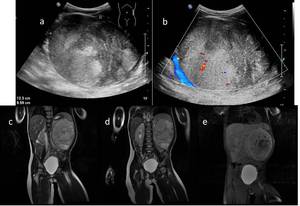
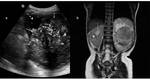
Fig. 16: Figura 15. Niña de 6 años con TW en riñón izquierdo, diagnosticado por biopsia, lo cual convierte a cualquier TW al menos en un estadio III. a y b) imágenes de ecografía; c, d y e) Imágenes de RM, secuencias T2 en plano coronal. No presentaba enfermedad extraabdominal.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
- Diseminación hematógena (en pulmón o hígado fundamentalmente) o linfática a distancia fuera de la cavidad abdomino-pélvica
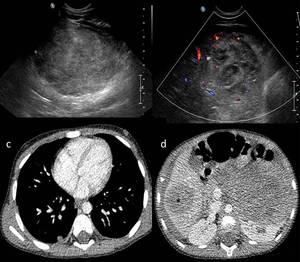
Fig. 17: Figura 16. Niño de 6 años que debutó como abdomen agudo por hemoperitoneo secundario
a la rotura de una metástasis hepática de TW. a y b) son imágenes de ecografía que muestran
la existencia de un tumor renal izquierdo, de ecogenicidad heterogénea y márgenes bien definidos. c y d) son cortes axiales de TC de abdomen con contraste iv. en los que se observa una metástasis pulmonar (flecha) y una hepática (asterisco). Estadio IV.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
- Enfermedad bilateral.
Deben estadiarse por separado y considerar el de peor pronóstico
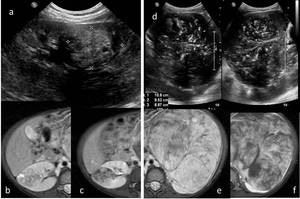
Fig. 18: Figura 17. TW bilateral tipo teratoide. Estadio V. a) Imagen de ecografía del tumor del riñón derecho de menor tamaño. b y c) Imágenes de RM, plano axial, secuencias T2 y T1 con saturación grasa y contraste iv. respectivamente. e) Imagen ecográfica del tumor del riñón izquierdo de mayor tamaño, e y f) las mismas secuencias de RM en este riñón.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
El estadio lo determina el resultado histopatológico tras la exéresis quirúrgica.
El tratamiento comprende la cirugía y la quimioterapia (QT) sobre todo y la radioterapia (RT) ocasionalmente,
en función del estadio del tumor y de sus características anatomopatológicas.
NEFROBLASTOMATOSIS.
Se trata de restos de tejido nefrogénico,
múltiples o difusos en los riñones de niños de más de 36 semanas de gestación.
Tienen un alto potencial de trasformación maligna y se identifican hasta en un 1% de los niños.
Habitualmente se detectan en el recién nacido y hasta los 7 años.
Pueden regresar espontáneamente,
pero un 30 o 40% de los casos desarrollan un TW.
Los restos se clasifican en perilobares (90%) e intralobares (10%) en función de su localización.
Los intralobares se asocian especialmente con un riesgo alto de TW.
Se asocia a algunos síndromes como el de Beckwith-Wiedemann,
Perlman y la trisomía 18.
En TC se observan como focos periféricos de baja atenuación con pobre realce,
adyacentes al parénquima renal normal.
En la RM se identifican como nódulos de baja intensidad de señal en T1 y T2.
En US se visualizan como focos hipoecogénicos pero es menos sensible que el TC y la RM (3)
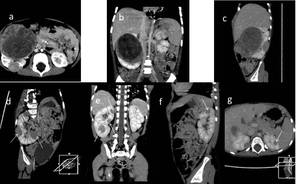
Fig. 19: Figura 18. a, b, c) reconstrucciones axial, coronal y sagital de Tc de abdomen con cte iv de TW. d, e ) reconstrucciones oblicua y coronal que muestran focos de nefroblastomatosis en el riñón derecho del mismo paciente (flechas); f y g) sagital y axial con otros focos de nefroblastomatosis en el riñón izquierdo (flechas).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
Recordar que el linfoma puede tener una apariencia similar.
SARCOMA DE CELULAS CLARAS.
Supone un 4-5% de los tumores renales (1).
Pico de incidencia en torno a los 1-4 años,
con predilección por los varones.
Por imagen se trata de una masa bien definida no claramente distinguible de un TW.
No suele producir invasión vascular y es unilateral.
Es un tumor más agresivo que el TW con una tasa de mortalidad mayor.
Su tratamiento se basa en la nefrectomía y quimioterapia,
con unas tasas de supervivencia de 60-70% (1,3)
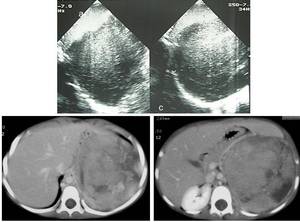
Fig. 20: Figura 19. Niña de 18 meses con masa abdominal palpable (sarcoma de células claras) a) imágenes de ecografía y b y c) imágenes de TC de abdomen con contraste iv. se trata de una masa bien definida, muy heterogénea, con menor realce que el parénquima renal sano contralateral, indistinguible por imagen de un TW.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
NEFROMA MESOBLÁSTICO.
Es el tumor renal sólido más frecuente en el neonato.
Suele aparecer en menores de 3 meses y el 90% de los casos afectan a menores de 1 año.
Predomina discretamente en los varones.
Se diagnostica habitualmente por la existencia de una masa palpable,
menos frecuentemente por hematuria.
En la ecografía prenatal puede presentar polihidramnios,
hidrops y aumento de los niveles de renina.
El tumor tiene un aspecto similar al de un mioma uterino.
Suele ser una masa mal definida,
no encapsulada,
con márgenes infiltrativos.
En la imagen se trata de un tumor de gran tamaño,
intrarrenal que infiltra el seno renal,
y puede tener componente quístico,
hemorrágico y necrótico en su interior
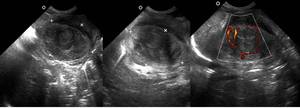
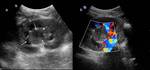
Fig. 21: Figura 20. Imágenes de ecografía de un neonato, que muestran una masa sólida heterogénea, vascularizada, que depende del riñón izquierdo y que resultó ser un nefroma mesoblástico.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
Es habitual la infiltración de los tejidos perinéfricos.
El tratamiento es quirúrgico,
asegurando que los márgenes estén libres de tumor.
Es rara la recidiva local y las metástasis a nivel pulmonar,
cerebral o en huesos.
El pronóstico es mejor en aquellos diagnosticados y resecados en los primeros 6 meses de vida.
TUMOR RENAL QUÍSTICO MULTILOCULADO.
Los septos son los únicos componentes sólidos de estos tumores y es indistinguible del TW quístico pero con ausencia de masas sólidas de nefroblastomosis.
Tiene dos picos de máxima incidencia: uno entre los 3 meses y los 4 años (más en varones) y el segundo,
en la edad adulta (más en mujeres).
Se manifiesta como masa abdominal palpable y los síntomas sistémicos son raros.
Por imagen se presenta como una masa bien definida,
encapsulada con múltiples quistes de escasos milímetros hasta 4 cm de diámetro,
con realce de los septos y sin salida de contraste al interior de los lóculos.
Cuando los espacios quísticos son pequeños,
el tumor puede parece sólido,
siendo el US el que mejor demuestra la naturaleza microquística de la lesión
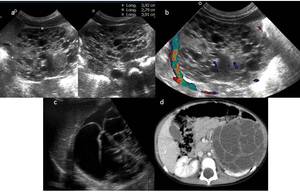
Fig. 22: Figura 21. a y b ) son imágenes ecográficas de una lesión renal con múltiples quistes que
resultó ser una displasia renal c) y d) son imágenes de ecografía y TC respectivamente que
muestran una lesión renal multiquística que fue un nefroma quístico multiloculado. Ambas
lesiones así como el TW quístico pueden ser indistinguibles por imagen.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
Puede o no extendense a estructuras adyacentes al riñón.
Su tratamiento es quirúrgico y el pronóstico es excelente si se extirpa totalmente.
Si se produce recurrencia local se puede tratar con RT o QT.
No se han descrito casos de metástasis a distancia (3,
7)
NEUROBLASTOMA.
El neuroblastoma es la segunda neoplasia abdominal en los niños después del TW y ambos constituyen la tercera causa de enfermedad maligna detrás de la leucemia y los tumores del sistema nervioso central.
El 90% de estos tumores se diagnostican en menores de 5 años (1,
8).
Histológicamente los neuroblastomas derivan de los neuroblastos simpáticos primitivos de la cresta neural embrionaria,
pertenecen al grupo de los tumores de células pequeñas,
redondas y azules de la infancia (como sarcoma de Ewing,
rabdomiosarcomas y linfomas).
Se presenta como una masa abdominal palpable,
que puede asociar hipertensión y elevación de catecolaminas,
de ácido vanilmandélico y homovanílico en sangre y orina.
Los sitios mas comunes donde asientan son: el retroperitoneo,
en la médula adrenal (35%) y el tejido extraadrenal de los ganglios paraespinales (35-40%),
seguido del mediastino (20%),
pelvis (2-3%) y el cuello (1-5%).
Ocasionalmente se encuentran metástasis sin un primario de localización conocida.
Dado que tanto el neuroblastoma como el TW suelen presentarse como masas asintomáticas o con sintomatología inespecífica,
el diagnóstico por imagen resulta imprescindible para una adecuada caracterización de las mismas.
A pesar de que la apariencia radiológica del Neuroblastoma y del TW puede ser muy variable y de que en ocasiones puede ser muy difícil distinguirlos entre sí o de otros tipos de tumores retroperitoneales,
en la mayor parte de los casos es posible llegar a un diagnóstico de certeza si se analizan las variables adecuadas.
El neuroblastoma suele ser irregular,
mal definido y sin cápsula identificable. Se trata de masas extrarenales,
evidenciándose su origen claramente extrarenal en la mayoría de los casos (el 81% de algunas series). En el resto de los pacientes la invasión renal dificulta el poder precisar el origen de la masa.
Habitualmente el neuroblastoma,
por ser de origen extrarenal,
no distorsiona el sistema pielocalicial.
Su tamaño es mayor que el del TW,
siendo común que cruce la línea media
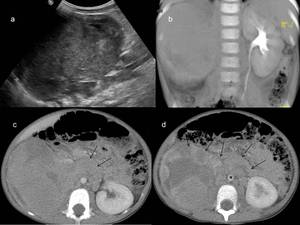
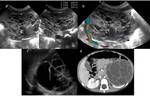
Fig. 23: Figura 22. Niño de 4 años que acude por fiebre y refiere cuadro de diarrea y algún vómito en las últimas 3 semanas, algunos familiares presentan un cuadro de gastroenteritis aguda.
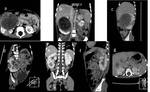
a) Imagen de la ecografía inicial en la que se identifica una masa heterogénea que parece depender del riñón derecho. b) reconstrucción coronal del TC de abdomen con contraste iv realizado posteriormente, en el que se observa una gran masa retroperitoneal sin que se identifique el riñón derecho; esto surgiría que se trataba de un TW. Sin embargo, en las imágenes c) y d) observamos que el tumor cruza la línea media (flechas), y envuelve los vasos (aorta abdominal rodeada de tumor *), dato que orientaba a que se tratara de un neuroblastoma, como confirmó el estudio histológico de la pieza quirúrgica.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
A pesar de que al neuroblastoma se le suele atribuir una apariencia más heterogénea que al TW,
ésta no puede ser achacable a la presencia de necrosis y/o hemorragia,
dado que éstas se encuentran con una frecuencia algo menor que en el TW.
Probablemente la heterogeneidad que tradicionalmente se asigna al neuroblastoma sea resultado de la gran frecuencia con la que calcifica (81% frente al 11% del TW).
Cuando el TW es lo suficientemente grande como para provocar algún tipo de efecto sobre los vasos,
ocasiona desplazamiento y/o compresión de los mismos.
El neuroblastoma puede provocar desplazamiento de los vasos,
pero característicamente engloba las estructuras vasculares,
comportamiento que resulta muy útil para distinguir ambas entidades,
ya que el TW no atrapa los vasos y nunca se extiende por detrás de la aorta.
Con US se debe evaluar el flujo doppler de los principales vasos abdominales así como la afectación metastásica o por continuidad del hígado.
También son de utilidad la TC y la RM; con esta última se valora mejor la infiltración y la diseminación intraespinal del mismo.
La presencia de adenopatías retroperitoneales y retrocrurales resulta más frecuente en los casos de neuroblastoma que en los de TW,
por lo que apoyaría el primer diagnóstico.
En el caso de TW toda la literatura publicada coincide en señalar al pulmón como el asiento más frecuente de metástasis a distancia (85%),
mientras que las localizaciones preferentes en el caso del neuroblastoma serían el hueso y la médula ósea.
El neuroblastoma intrarrenal es una tumoración renal muy infrecuente cuyo probable origen son restos de tejido adrenal que quedan atrapados en el tejido renal,
o de ganglios simpáticos intrarrenales.Se muestra en los estudios de imagen como una masa renal que puede presentar calcificaciones y que puede ser indistinguible del TW en los casos histológicamente más indiferenciados y,
por lo tanto,
de peor pronóstico.
Estos tumores metastatizan y el pronóstico es muy malo.
(8)
TERATOMA.
Los teratomas son tumores que contienen una mezcla de tejidos derivados de dos capas germinales del embrión; deben contener tejido ajeno al sitio anatómico en el que se encuentran.
Los tejidos que los componen son: piel,
dientes,
tejido del sistema nervioso central,
mucosa respiratoria y digestiva,
cartílago y hueso.
La localización más frecuente es las gónadas,
especialmente los ovarios,
seguido de la región sacrocoxígea,
presacra; esto se explica por la relación cercana de estos lugares al paso de la migración de las células germinales; menos frecuente es el retroperitoneo (constituye el 5-10% de todos los teratomas),
la región cervical,
mediastino y testículo.
Existe predominio del sexo femenino sobre el masculino.
Al igual que sucede con el neuroblastoma,
originándose en el retroperitoneo puede infiltrar el riñón por lo que debemos tenerlo presente entre las masas renales de los niños.
En el estudio de US se manifiestan como grandes masas muy heterogéneas en cuyo interior se identifica componentes cálcicos groseros (a veces dientes o falanges) quísticos y grasos
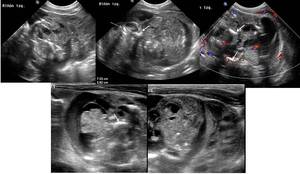
Fig. 24: Figura 23. Imágenes ecográficas de masa en fosa renal izquierda, bien delimitada, muy heterogénea, con áreas quísticas y calcificaciones groseras en su interior (flechas), que dejan sombra acústica posterior. No invadía estructuras vecinas y vasos.La anatomía patológica del tumor confirmó que se trataba de un teratoma.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
En la TC igualmente se confirma el componente óseo,
graso o quístico,
y se valora la extensión retroperitoneal y la posible afectación de los vasos,
si estuviese presente.
La escisión quirúrgica completa es el tratamiento de curativo de elección.
(10,
11)
ANGIOMIOLIPOMA.
Es un tumor infrecuente con una histología similar a la de un hamartoma compuesto por elementos vasculares,
de musculo liso y grasa.
Pueden ser esporádicos pero se asocian especialmente a los pacientes con esclerosis tuberosa,
y a neurofibromatosis y Sd.
de von Hippel-Lindau.
Su pico de incidencia se da en torno a los 41 años.
En los niños son raros salvo asociado a una esclerosis tuberosa.
El 8% de los niños con esta enfermedad presentaran este tipo de tumor hacia los 10 años (1,3)
Los síntomas se relacionan con la existencia de sangrado.
Los que son menores de 4 cm son típicamente asintomáticos,
y aquellos que superan los 4 cm pueden sangrar.
En el caso de que el sangrado sea intenso y retroperitoneal se le conoce como sd Wunderlich (3)
La apariencia por imagen de este tipo de tumor se basa en la presencia de grasa intratumoral en TC y MR. En el caso de US observaremos focos hiperecogénicos,
sin sombra acústica posterior relacionados con los focos grasos
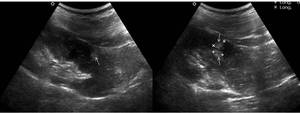
Fig. 25: Figura 24. Los angiomiolipomas se observan como imágenes nodulares dependientes del parénquima renal, que característicamente contienen grasa, esta se identifica en ecografía como focos hiperecogénicos (flechas).
References: Hospital Universitario Virgen de la Arrixaca. Murcia
La angiografía pone de manifiesto su naturaleza vascular con vasos tortuosos y dilatados y la formación de aneurismas en su interior.
Pese a ello algunos son hipovasculares.
Aunque la grasa puede verse ocasionalmente en el TW y en el carcinoma de células renales,
el contexto clínico y la apariencia localmente no agresivo,
sin invasión de vasos ni linfadenopatías sugiere se trata de este tipo de tumor.
Se tratan con nefrectomía parcial o embolización aquellos de mas de 4 cm de tamaño para evitar el sangrado (1,3).
LINFOMA.
El linfoma afecta al riñón de forma secundaria por extensión directa retroperitoneal o por metástasis hematógena.
En los niños el linfoma no Hodgkin,
especialmente el Burkitt,
es el que mas frecuentemente afecta al riñón.
Un 62 % de los pacientes con linfoma tienen afectación renal en las autopsias,
pero solo un 3-8% de los pacientes demuestran esa afectación en el TC.
La infiltración linfomatosa del riñón no produce síntomas hasta estadios avanzados de la enfermedad.
Dolor abdominal o en flanco,
hematuria,
anemia,
pérdida de peso,
masa palpable son algunos de los más frecuentes.
La HTA es rara.
Los hallazgos en imagen son variables e incluyen: la existencia de nódulos o masas únicas o múltiples,
la infiltración difusa parenquimatosa,
afectación por contigüidad del espacio retroperitoneal y la de los tejidos perinéfricos.
Lo más frecuente es que aparezca como múltiples nódulos
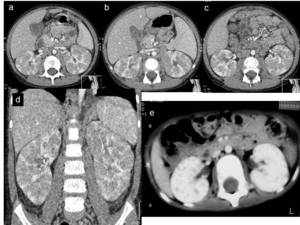
Fig. 26: Figura 25. a, b, c) Imágenes axiales y d) en reconstrucción coronal, de TC de abdomen con contraste renal de linfoma. Se observa una infiltración parcheada difusa y bilateral de ambos riñónes. e) Imagen axial de TC con contraste iv, de otro paciente con linfoma, en el que la afectación renal es también difusa con focos de menor tamaño.
References: Hospital Universitario Virgen de la Arrixaca. Murcia
que rectifican el contorno renal y distorsionan o desplazan el sistema colector.
Las imágenes pueden ser homogéneas,
hipodensas,
sin realce simulando múltiples quistes renales.
Por US se presentan como focos hipoecogénicos y pueden presentar aumento de la trasmisión sónica (1,3,
8).