INTRODUCCIÓN
Los abscesos hepáticos son el tipo mas común de abscesos viscerales y en su valoración juegan un importante papel las diferentes técnicas de imagen,
tanto como método diagnóstico como para su abordaje terapéutico.
Las distintas técnicas de imagen participan de forma complementaria en muchas ocasiones en la caracterización lesional.
La utilidad de la ecografía como técnica de estudio inicial se basa en su sensibilidad en la detección,
su accesibilidad y su bajo coste.
La tomografía computarizada (TC) permite una valoración más precisa del grado de extensión lesional,
cambios en la atenuación y realce del parénquima,
confirmando en ocasiones la presencia de aire o calcio y detectando posibles lesiones sincrónicas en otros órganos.
La mayor capacidad de caracterización tisular de la resonancia magnética (RM) permite visualizar mejor los cambios inflamatorios perihepáticos / edema,
pudiendo incrementar la especificidad para ciertas infecciones.
Aunque los hallazgos radiológicos resulten muy orientativos suelen ser necesarias las técnicas invasivas (punción aspiración con aguja fina (PAAF),
biopsia y/o drenaje ) para precisar el agente causal.
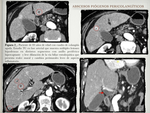
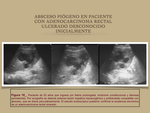
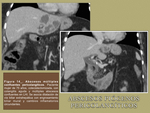
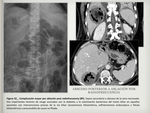
La ecografía y la TC se utilizan como guía en la realización de la mayoría de estos procedimientos ( Fig. 1 ).
Infecciones Piógenas
- Las infecciones hepáticas piógenas se producen por múltiples mecanismos fisiopatológicos,
entre los cuales,
el más usual es la afectación secundaria a la fuga intraabdominal del contenido intestinal,
que se disemina al hígado a través de la circulación portal.
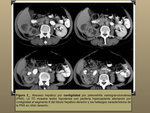
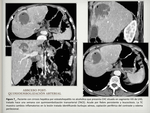
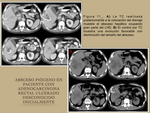
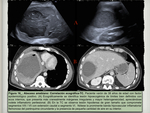
- Otras vías conocidas de acceso de los patógenos incluyen la infección a través de la vía biliar (colangitis ascendente) ( Fig. 2 ),
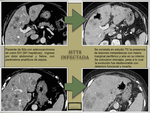
la sobreinfección de tejido necrótico (postquirúrgico / post-ablación),
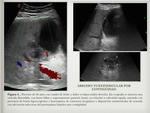
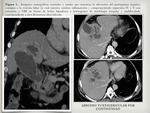
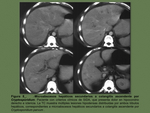
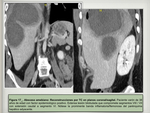
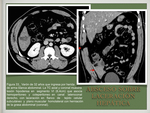
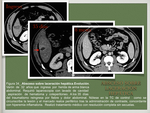
la afectación hepática secundaria y por contigüidad por infección de órganos adyacentes ( Fig. 3 / Fig. 4 / Fig. 5 ),
el traumatismo o la siembra hematógena en el contexto de una infección sistémica,
destacando por último que un número considerable de casos no tendrá una causa identificable (criptogenético).
Epidemiología.
- La incidencia anual ha sido estimada en 2.3 casos por cada 100.000 habitantes y es mayor en hombres que en mujeres (3.3 versus 1.3 por 100.000) [1-3]; aunque se ha reportado una mayor tasa de incidencia en Taiwan que alcanza hasta 17.6 casos por cada 100.000 habitantes [4].
- La tasa de mortalidad en países desarrollados oscila entre el 2 y el 12% [5,6].
Microbiología.
- La mayor parte de la infecciones piógenas hepáticas son polimicrobianas estando formadas por una mezcla de flora entérica y especies de anaerobios como patógenos más comunes,
siendo el gérmen más frecuentemente implicado la Escherichia coli.
- Cuando se identifican Streptococo milleri y S.
anginosus, debemos buscar infecciones metastásicas en otras localizaciones.
- S.
aureus,
S.
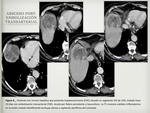
pyogenes y otros Gram positivos están reconocidos como gérmenes frecuentemente vinculados a procedimientos de embolización transarterial de hepatocarcinomas ( Fig. 6 / Fig. 7 ).
- Gérmenes oportunistas tales como Citomegalovirus y Cryptosporidium,
son patógenos presentes en pacientes inmunodeprimidos con colangiopatía por VIH ( Fig. 8 ).
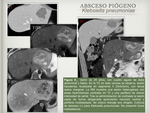
- Klebsiella pneumoniae es un importante patógeno emergente que ha dado lugar a la descripción del denominado “Sindrome del absceso hepático secundario a Klebsiella pneumoniae (SAHK)” que se caracteriza por abscesos hepáticos monomicrobianos ,
bacteriemia e infección metastásica tales como endoftalmitis,
meningitis o abscesos cerebrales.
Si bien puede afectar a pacientes sin comorbilidades se ha identificado que la diabetes mellitus así como la tolerancia disminuida a la glucosa son factores de riesgo [7,8]; asimismo no se ha reconocido una relación con enfermedades hepatobiliares subyacentes ( Fig. 9 ).
- La aparición de un absceso hepático piógeno de etiología desconocida hace necesario descartar la existencia de una neoplasia colorrectal silente como posible puerta de entrada digestiva ( Fig. 10 / Fig. 11 ).
Manifestaciones clínicas.
- La fiebre es el síntoma más frecuente,
presente en hasta el 90% de los pacientes.
Síntomas abdominales se encuentran en el 50-75% de los enfermos y suelen ser referidos al hipocondrio derecho incluyendo desde molestias vagas a dolor franco.
La ausencia de síntomas relacionados con el hipocondrio derecho no excluye la posibilidad diagnóstica.
- Los síntomas acompañantes son variables e incluyen náuseas,
vómitos,
anorexia y pérdida de peso.
- El patrón de afectación bioquímica consiste en un aumento de reactantes de fase aguda asociado a alteración inespecífica del perfil hepático que va desde citolisis hasta cierto componente de colestasis.
Técnicas diagnósticas.
El correcto diagnóstico de los abscesos hepáticos es el resultado de combinar los hallazgos radiológicos con el cuadro clínico del paciente.
A veces métodos diagnósticos más sencillos pueden constituir la clave para profundizar en la investigación diagnóstica,
como podría ser el hallazgo de un derrame pleural o la elevación del hemidiafragma derecho presentes en hasta un 25-35% de los casos.
Los abscesos pueden presentar diferentes características ecográficas dependiendo del estadio evolutivo en el que se encuentren.
Podemos ver inicialmente una lesión focal tenuemente hipoecoica y de límites imprecisos,
de aspecto flemonoso,
que en su evolución adquiere mayor delimitación e hipoecogenicidad en concordancia con el mayor grado de licuefacción tisular.
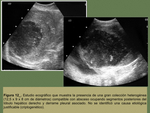
También es frecuente que en fase francamente purulenta tengan una ecoestructura heterogénea presentando un aspecto sólido o quístico con presencia de ecos en su interior correspondientes a detritos y artefacto de reverberación en relación a la producción de gas ( Fig. 12 ).
En cuanto al tamaño estos pueden ser pequeños ,
microabscesos (< 2cm) o macroabscesos (> 2cm).
Los microabscesos pueden aparecer como múltiples lesiones,
como es el caso del patrón miliar de infecciones piógenas ocasionadas por estafilocococemia,
que suelen comprometer también al bazo,
teniendo cierta similitud con los abscesos fúngicos en pacientes inmunodeprimidos.
Otro patrón de afectación es la tendencia a la coalescencia en una lesión focal de mayor tamaño,
siendo esto más característico de lesiones por bacterias coliformes y microorganismos entéricos ( Fig. 13 / Fig. 14 ).
La variabilidad de la apariencia puede plantear dificultades a la hora de realizar una correcta valoración ecográfica,
con lo cual la administración de contraste ecográfico mejora el rendimiento del estudio basal.
Se han descrito tres patrones en ecografía con contraste ( Fig. 15 ),
los cuales son concordantes con los hallazgos en TC y RM [9].
Esta técnica presenta la ventaja de que realiza una valoración en tiempo real permitiendo definir la arquitectura interna de la lesión y de este modo elegir el tratamiento adecuado.
La TC nos permite realizar una mejor valoración de la extensión de la lesión/lesiones.
También resulta muy útil en la identificación de la presencia de gas y en la detección de realce marginal tras la administración de contraste ya que cuando las colecciones son muy homogéneas puede resultar difícil diferenciarlas de lesiones quísticas.
Por último los abscesos por RM tienen una amplia variedad de intensidad de señal ponderada en T1 y T2 dependiendo del contenido proteico,
la presencia de edema,
los cambios necróticos/hemorrágicos y las alteraciones perfusionales durante el estudio dinámico.
El edema perilesional se mostrará como hiperintenso en T2 e hipointenso en T1.
Manejo terapéutico.
El diagnóstico precoz y el drenaje percutáneo han disminuido tanto la mortalidad (de un 40% a un 2%) como la necesidad de cirugía.
Sin embargo,
el drenaje percutáneo solo suele ser necesario en las colecciones de mayor tamaño (>5 cm de diámetro).
La antibioticoterapia debe basarse en la probable causa de infección y debe incluir inicialmente metronidazol hasta que se descarte por serología el origen amebiano del mismo.
Las técnicas de drenaje incluyen el drenaje percutáneo guiado por ecografía o por TC (con o sin colocación de catéter),
el drenaje quirúrgico o el endoscópico a través de colangiografía endoscópica retrógrada (en aquellos que presentan íntimo contacto con la vía biliar).
Para abscesos únicos con un diámetro menor o igual a 5 cm,
tanto el drenaje percutáneo con catéter como la aspiración con aguja están aceptados [10-13].
En las lesiones mayores de 5 cm de diámetro se prefiere el drenaje con catéter antes que la simple aspiración con aguja [14].
Aunque la opción quirúrgica también es posible en estos casos ya que si bien no ha mostrado diferencias significativas,
en cuanto a morbimortalidad y complicaciones,
la tasa de fallo terapéutico parece ser menor que con las técnicas percutáneas [15,16].
Asimismo algunas situaciones son claramente apropiadas para el manejo quirúrgico,
tales como:
- Abscesos múltiples.
- Abscesos loculados.
- Abscesos con contenido espeso.
- Pacientes con enfermedades subyacentes que requieren un manejo quirúrgico primario.
- Inadecuada respuesta al drenaje percutáneo después de 7 días.
Los abscesos múltiples y los multiloculados han sido igualmente tratados con éxito de forma percutánea [17].
------------------------------
Infecciones Parasitarias.
- Amebiasis
Fisiopatologia.
La amebiasis está causada por el protozoo Entamoeba histolytica.
La mayor parte de las infecciones son asintomáticas y la forma sintomática puede manifestarse como amebiasis intestinal o extraintestinal,
siendo el absceso hepático la forma extraintestinal más frecuente.
El parásito existe en dos formas ,
quística (forma infectiva) y trofozoíto (forma responsable de la enfermedad invasiva).
La infección se contrae al ingerir alimentos o agua contaminada con formas quísticas pero también se ha asociado con transmisión venérea a través de contacto fecal oral.
Estos llegan al intestino delgado donde se transforman en trofozoítos,
los cuales pueden invadir la barrera mucosa del colon (ciego y con menor frecuencia recto-sigma ) causar destrucción tisular y alcanzar la circulación portal.
Epidemiología.
Es una infección ampliamente distribuida en el mundo,
habiendo aumentado la la prevalencia de forma desproporcionada en países en vías de desarrollo debido a las pobres condiciones socioeconómicas.
Áreas con altas tasas de incidencia son India,
África,
México y regiones de América central y Sudamérica.
En países desarrollados ,
la amebiasis se presenta en inmigrantes o en viajeros a áreas endémicas y se debería considerar su diagnóstico en personas que han estado o han viajado a dichas regiones en los últimos 6 meses.
Manifestaciones clínicas.
- Entre los factores de riesgo para que la enfermedad sea invasiva se encuentra la susceptibilidad genética,
la edad y el estado inmunológico.
Asimismo son factores de riesgo de enfermedad severa e incremento en la mortalidad el embarazo,
la corticoterapia ,
neoplasias,
malnutrición y alcoholismo.
- Suele tener un presentación subaguda en un período de una a tres semanas de fiebre,
pérdida de peso y dolor en hipocondrio derecho.
La diarrea concomitante está presente en menos de un tercio de los pacientes,
aunque algunos pacientes refieren historia de disentería en los meses previos.
La afectación intestinal cuando está presente puede variar desde diarrea con productos patológicos a colitis fulminante con perforación y peritonitis,
o más raramente la presencia de una masa de tejido de granulación (ameboma) simulando una neoplasia.
Técnicas diagnósticas.
Las técnicas diagnósticas incluyen la microscopía,
la detección serológica,
técnicas moleculares y colonoscopia con examen histológico.
La mejor combinación diagnóstica resulta de la combinación de serología o presencia de Ag,
junto con la identificación del parásito en materia fecal o sitios extraintestinales (pus de absceso hepático).
Si bien los abscesos amebianos ecográficamente suelen ser mas redondeados y homogéneos que los piógenos,
estas no son características relevantes a la hora de distinguir unos de otros [18],
con lo cual,
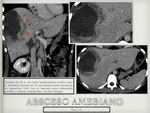
los hallazgos epidemiológicos y la información clínica pueden contribuir al diagnóstico ( Fig. 16 / Fig. 17 ).
Tomográficamente las lesiones suelen localizarse subcapsularmente,
con una pared bien definida con edema periférico,
pueden tener múltiples septos o niveles hidroaéreos.
Es característico el realce de la pared configurando un “anillo inflamatorio” tras la administración de contraste que denota los cambios inflamatorios/flemonosos del parénquima adyacente ( Fig. 18 / Fig. 19 ).
La extensión extrahepática es común haciéndolo hacia la pared torácica,
la cavidad pleural,
el pericardio (cuando compromete el lóbulo izquierdo),
el peritoneo o causando trombosis de venas hepáticas y/o VCI y/o vísceras adyacentes.
Manejo terapéutico.
La terapéutica de elección es con metronidazol (500-750 mg oral tres tomas diarias durante 7 a 10 días).
La tasa de curación con esta terapia es mayor al 90% [19].
Alternativas al Metronidazol incluyen al tinidazol,
ornidazol y nitazoxanida.
Seguidamente a la terapia de la amebiasis invasiva (hepática),
el tratamiento debe incluir un agente luminal (paromomicina),
para eliminar los quistes ,
inclusive si la microscopia de la materia fecal es negativa.
La terapia amebicida es altamente efectiva,
con lo cual el drenaje con catéter es raramente necesario [20]. Podría tener utilidad si hay riesgo de ruptura sobre todo en lesiones de lóbulo hepático izquierdo,
por la posibilidad de extensión a pericardio,
también si hay deterioro clínico o ausencia de respuesta al tratamiento médico.
Los trofozoítos se pueden ver en el 20% de los casos en el contenido aspirado.
El contenido consiste en hepatocitos muertos con algo de hemorragia lo cual le da el nombre de líquido en “pasta de anchoas”.
------------------------------
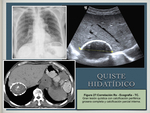
- Quiste hidatídico hepático
La enfermedad hidatídica tiene 4 especies de parásitos que pueden afectar al hombre,
siendo Echinococcus granulosus y Echinococcus multilocularis las más comunes,
responsables de la equincocosis quística y alveolar respectivamente.
Las otras dos especies,
E.
vogeli y E.
oligarthrus raramente se asocian a infecciones humanas.
El hígado es el órgano mas frecuentemente afectado (75%) especialmente el lóbulo hepático derecho,
seguido del pulmón (15%),
pudiendo alcanzar otras localizaciones anatómicas.
Aunque tiene una distribución mundial es endémico en la cuenca mediterránea.
Es una enfermedad que suele cursar de forma asintomática,
en ocasiones se puede adquirir en la infancia y no manifestarse hasta la edad adulta habiéndose descrito períodos de latencia de hasta 50 años.
Si bien suele ser una enfermedad indolente,
tiene múltiples potenciales complicaciones y las manifestaciones clínicas pueden ser diversas:
- Crecimiento exofítico transdiafragmático invadiendo el tórax suele ser a través del área desnuda del hígado por ser una zona desprovista de peritoneo.
- Perforación en víscera hueca y evacuación con hydatidemesis e hydatidorrea.
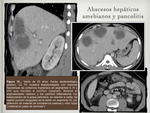
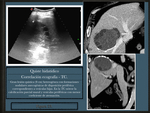
- Sobreinfección,
tras la ruptura conjunta de la periquística y el endoquiste lo cual permite el paso de bacterias al interior del quiste ( Fig. 20 / Fig. 21 ).
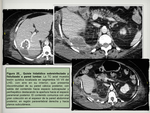
- Ruptura,
la cual puede ser contenida (la periquística permanece intacta visualizándose el endoquiste como membranas flotando dentro del quiste),
comunicante (paso del contenido del quiste a los radicales biliares incorporados en la periquística) o ruptura directa (ruptura de periquística y endoquiste con vertido de material hidatídico a cavidad peritoneal,
cavidad pleural,
víscera hueca,
pared abdominal) ( Fig. 22 ).
La ruptura quística como tal puede dar fiebre y reacciones de hipersensibilidad incluyendo anafilaxia.
Las reacciones de hipersensibilidad están relacionadas con la liberación de una gran carga de material antigénico.
- Comunicación o compresión de la vía biliar,
manifestándose como ictericia obstructiva,
colangitis ,
cólico biliar o pancreatitis.
- Compresión vascular ,
de la vena porta con hipertensión portal o más raramente de la vena cava inferior.
- Diseminación hematógena con afectación de otros órganos como cerebro,
pulmón (15-20%) ,
riñón y hueso.
El parásito es una tenia de 3 a 6 mm de longitud que vive en el intestino del perro que suele ser el huésped definitivo.
Este elimina huevos de parásito en heces,
pudiendo contaminar los alimentos y el agua,
afectando de esta manera al hombre quien suele ser un huésped intermedio.
El análisis histopatológico muestra tres capas:
- Externa periquístca o adventicia correspondiente a un rodete de fibrosis hepática.
- Intermedia o ectoquística constituida por una fina membrana de 1 mm y que es la que suele calcificar.
- Interna o germinal que da lugar a quistes hijos.
La maduración del quiste implica el desarrollo de vesículas hijas como resultado de invaginación endoquística ( Fig. 23 ).
Una vez en el hígado el quiste crece a razón de 2-3 cm/año dependiendo de la resistencia tisular.
Las calcificaciones periféricas (implican un quiste de 5 a 10 años de evolución),
pueden ser nodulares o curvilíneas,
y son comunes tanto en quistes viables como en los no viables,
por tanto la presencia de calcificaciones no implica necesariamente la muerte del parásito,
salvo en el caso de que sean densas y ocupen la casi totalidad del quiste.
Técnicas diagnósticas.
El diagnóstico se basa fundamentalmente en técnicas de imagen y pruebas serológicas.
El test serológico de primera línea es la detección de antígenos e inmunocomplejos del quiste mediante la técnica de enzimoinmunoanálisis (ELISA) siendo la inmunofluorescencia (IFA) (detecta anticuerpos IgG contra protoexcólices de E.
Granulosus) otro test disponible de segunda línea.
A veces las lesiones quísticas calcificadas suelen ser hallazgos incidentales en controles radiológicos por otros motivos ( Fig. 24 ).
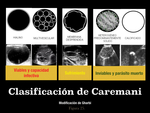
La ecografía es la primera técnica a emplear ante la sospecha de un quiste hidatídico hepático con una sensibilidad próxima al 100%.
Existen varios patrones ecográficos establecidos en la clasificación de Caremani ( Fig. 25 ).
La PAAF también puede realizarse con finalidad diagnóstica pudiendo llegar a demostrar partículas de escólex en el material aspirado.
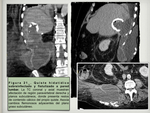
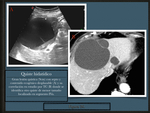
La TC es muy útil en la valoración del quiste,
el contenido del quiste presenta densidad agua (3-30 UH),
se pueden apreciar perfectamente las calcificaciones,
los septos internos o las vesículas y la pared del quiste suele ser hiperdensa incluso sin contraste ( Fig. 26 / Fig. 27 ).
La RM tiene una especificidad y sensibilidad similares a las de la TC aunque en caso de ruptura quística permite detectar alteraciones en la periquística que la TC no es capaz de discriminar.
En los casos de rotura a vía biliar,
la colangio-RM es de gran utilidad.
La afectación hepática por E.
multilocularis,
presenta un patrón ecográfico característico con múltiples nódulos ecogénicos con márgenes irregulares y difusos,
denominado “en granizada”.
Las lesiones con mayor licuefacción central aparecen hipoecoicas con algunos ecos internos y bordes hiperecoicos irregulares [21].
En TC y RM suelen ser lesiones múltiples,
irregulares,
envueltas por un parénquima que es de baja atenuación en la TC e hipertenso en T2 por RM.
Estos hallazgos pueden simular metástasis o abscesos piógenos,
sin embargo no suelen tener realce tras la administración de contraste lo que enfatiza la pobre vascularización de la lesiones parasitarias.
El compromiso hiliar es frecuente (hasta el 50% de los casos) lo cual genera en ocasiones una dilatación de vía biliar intrahepática ,
invasión portal y de venas hepáticas condicionando atrofia por hipoperfusión [22].
En estadios avanzados se pueden encontrar calcificaciones irregulares.
Manejo terapéutico
Los quistes de pequeño tamaño (inferiores a 4 cm),
que no afloren a la superficie y no compriman estructuras vasculares ni biliares podrán ser controlados o tratados de forma conservadora.
El tratamiento médico recomendado es albendazol (10-15 mg/Kg/día repartido en dos dosis durante 1 mes).
Esta pauta puede repetirse según respuesta ecográfica y serológica.
Punción,
aspiración,
inyección y reaspiración (PAIR). La punción con control ecográfico (o TC) del quiste hidatídico hepático,
con aspiración del contenido,
inyección de un escolicida (alcohol absoluto y polidocanol o suero salino hipertónico al 20% en un volumen igual al 50% del volumen extraído) y reaspiración de este,
parece una técnica eficaz y segura en el tratamiento de la hidatidosis hepática.
La tasa de recidivas se sitúa en el 3%.
Las indicaciones de la PAIR son: enfermo inoperable o que rechaza la cirugía,
quistes múltiples,
QHs tipos 1,2 y 3.
El tratamiento quirúrgico está indicado en quistes grandes (> de 10 cm),
situados en la superficie,
infectados o comunicados con la vía biliar.
- Esquistosomiasis
La esquistosomiasis es una enfermedad parasitaria crónica causada por duelas sanguíneas (tremátodos) del género Schistosoma.
Hay dos formas principales,
la intestinal y la urogenital.
Dentro de las que afectan a nivel digestivo,
las especies mas importantes son S.
mansoni,
S. japonicum,
S.
mekongi,
S.
intercalatum y S.
guineansis.
El S.
haematobium es el responsable de la afectación urogenital.
Es prevalente en regiones tropicales y subtropicales,
especialmente en comunidades pobres sin acceso a agua potable ni a saneamiento adecuado.
La infección se adquiere cuando las formas larvarias del parásito,
liberadas por caracoles de agua dulce,
penetran en la piel durante el contacto con aguas infestadas.
Las formas adultas del parásito permanecen viables durante meses en los vasos sanguíneos mesentéricos y la producción de huevos por estas,
seria el mecanismo por el cual afectan al hígado.
Una vez allí,
provocan una reacción fibrosa granulomatosa que eventualmente conduce al bloqueo del flujo venoso.
La hipertensión portal resultante genera colaterales portosistémicas y daño hepático progresivo.
Para el diagnóstico se utilizan,
la serología,
la presencia de huevos en materia fecal,
siendo el foco epidemiológico con eosinofilia periférica de gran ayuda para la sospecha.
Es una infección que en fase aguda puede producir dolor abdominal,
diarrea y sangre en las heces y que en este estadio no tiene hallazgos específicos en cuanto a las técnicas de imagen.
En cambio en un estadio avanzado están descriptos algunos patrones característicos.
En la infección por Schistosoma japonicum puede encontrarse un patrón ecográfico en mosaico con septos ecogénicos,
que determinan áreas poligonales,
con áreas preservadas,
siendo menos común imágenes de calcificaciones o cirrosis [23,24].
En la TCMD el patrón patognomónico es la presencia de septos calcificados,
generalmente alineados perpendicularmente a la cápsula hepática, con apariencia de “caparazón de tortuga”.
Otros hallazgos menos específicos serian calcificaciones capsulares,
retracción de parénquima hepático o contorno hepático irregular en contexto de degeneración a cirrosis.
En la infección por Schistomoa mansoni se suele hallar un engrosamiento de la porta y de sus ramas asociado a incremento de la ecogenicidad,
esto da la apariencia de “ojo de buey” con una imagen anecoica de la vena porta rodeada de tejido fibrótico. En la TC esto se traduce como anillos hipodensos rodeando a la porta y sus ramas con refuerzo postcontraste [24].
------------------------------
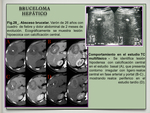
Brucelosis hepática
La brucelosis es una zoonosis transmitida a humanos por contacto con fluidos de animale,s infectados (ovejas,
cabras,
cerdos,
etc) o por ingesta de productos como leche o quesos no pasteurizados.
En los países mediterráneos la brucelosis es causada por Brucella melitensis.
Su alta afinidad por el sistema reticuloendotelial hace que la afectación hepática sea frecuente aunque en la mayor parte de los casos de forma subclínica,
siendo manifiesta solo en un bajo porcentaje de casos en forma de hepatitis.
La producción de necrosis y la supuración en forma de abscesos hepáticos únicos o múltiples (“bruceloma hepático”) se ha descrito en raras ocasiones.
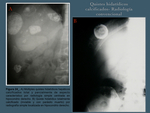
Por ecografía abdominal y TC el “bruceloma hepático” suele presentarse como una lesión ocupante de espacio,
de bordes mal definidos,
casi siempre única,
hipoecoica en el estudio ecográfico e hipodensa por TC,
de tamaño variable (3-8 cm) y frecuentemente con una calcificación central grosera ( Fig. 28 ).
El diagnóstico se establece en la mayoría de casos en base a un cuadro clínico y test de laboratorio que incluyen cultivos,
serologías (aglutinación de Rosa de Bengala,
ELISA,
aglutinaciones y Coombs) y PCR.
El tratamiento inicial puede ser conservador,
utilizando la combinación de 2 antibióticos (doxiciclina mas estreptomicina o rifampicina) durante 2 ó 3 meses,
reservando el drenaje,
preferiblemente percutáneo,
para los casos con mayor afectación clínica,
mala evolución o recidiva.
La tasa de recidiva de la enfermedad que sigue al tratamiento es del 5-15% y usualmente ocurre en los siguientes 6 meses tras completar la terapéutica aunque puede ocurrir hasta 12 meses después.
------------------------------
Infecciones fúngicas
La infección fúngica que afecta al hígado suele ocurrir en el contexto de inmunosupresión,
como complicación de una prolongada neutropenia en pacientes sometidos a tratamientos de quimioterapia por neoplasias hematológicas,
principalmente leucemias.
La especies más prevalentes son Candida albicans,
aunque también criptococo,
histoplasma y mucormicosis afectan al hígado,
presentando hallazgos de imagen similares entre ellos.
En general la afectación se produce en el contexto de diseminación sistémica con afectación no solo hepática sino también esplénica y renal.
Es conocida la importancia de la respuesta inflamatoria del huésped en la identificación y la apariencia en imagen de las lesiones.
Ha sido descrito que las lesiones fúngicas podrían no ser visibles hasta que el paciente se recupere de la neutropenia [25-27].
La ecografía es una gran herramienta en la valoración de la candidiasis ,
y se han determinado algunos patrones:
- “Ojo de buey”: imagen con centro hiperecogénico con un anillo hipoecoico.
Suele presentarse en pacientes con recuento leucocitario relativamente normal.
- “Rueda dentro de una rueda”: lesión hipoecoica periférica (fibrosis),
rueda ecogénica central (tejido inflamatorio) y nido hipoecoico (necrosis con contenido de hongos) central.
- Uniformemente hipoecogénico con múltiples lesiones hipoecoicas.
Es el más frecuente aunque el menos específico ya que se puede confundir con metástasis o con infiltración por un linfoma.
- Ecogénico,
representando la calcificación en relación a la formación de cicatriz,
que indica resolución.
Estos patrones ecográficos tienen poca correlación con la TC,
el patrón en “ojo de buey” ocasionalmente puede detectarse en estadios agudos de la enfermedad.
Se ha sugerido sin embargo que la TC es superior a la ecografía en la identificación de los microabscesos [28] y lo es aun más el estudio por RM [29].
Basados en el conocimiento del realce transitorio en fase arterial en lesiones inflamatorias hepáticas,
hay publicaciones que han sugerido que el estudio multifásico del hígado incrementa la sensibilidad en la detección de las lesiones hepatoesplénicas fúngicas [30].
------------------------------
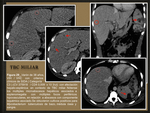
Infecciones por micobacterias (Mycobacterium tuberculosis).
La afectación tuberculosa hepática más frecuentemente reportada,
es aquella que se produce en el contexto de la diseminación hematógena o tuberculosis (TBC) miliar del Mycobacterium tuberculosis.
Existen además otras formas con compromiso principalmente de los ductos biliares intrahepáticos (TBC hepatobiliar) [31], o que se manifiestan en forma de abscesos y tuberculomas.
La presentación clínica de la TBC miliar es altamente variable y esta puede ser aguda aunque más frecuentemente suele tener un curso subagudo o crónico.
El desarrollo de TBC miliar durante la infección primaria puede manifestarse de forma aguda y con un curso clínico rápido.
Esta presentación puede ser fulminante,
en forma de fallo multiorgánico,
shock séptico o distress respiratorio.
La presentación subaguda o crónica es más común,
con cuadros como fiebre de origen desconocido o disfunción progresiva de uno o más órganos .
Los signos y síntomas de la afectación hepática incluyen el dolor abdominal difuso o localizado en hipocondrio derecho,
náuseas,
vómitos y diarrea.
Los hallazgos histopatológicos muestran lesiones granulomatosas dispersas que en el examen macroscópico semejan semillas de mijo.
Las anormalidades del perfil hepático son comunes,
incluyen elevación de fosfatasa alcalina y transaminasas aunque el patrón también pueden ser colestásico predominante.
La insuficiencia hepática raramente ocurre.
Los pacientes con síndrome de inmunodeficiencia adquirida (SIDA) tienen tendencia a desarrollar abscesos,
que suelen ser microabscesos.
La combinación de factores tales como el importante deterioro de la inmunidad celular y la gran carga bacilar llevan a la pobre formación de granulomas defensivos,
favoreciendo de esta forma la necrosis tisular,
viéndose dificultada la reabsorción del material necrótico por déficit de la función macrofágica.
La afectación hepática tuberculosa es inespecífica en cuanto a hallazgos de imagen,
pueden hallarse tuberculomas,
los cuales ecográficamente tienen aspecto de masas redondeadas hipoecoicas,
aunque también pueden ser hiperecogénicas.
Una discreta hepatomegalia puede aparecer en los casos de diseminación miliar,
que puede dejar de forma secuelar granulomas calcificados.
Las lesiones en la TC suelen mostrarse con atenuación disminuida sin realce tras la administración de contraste y en RM suelen ser hipointensas en T1 e hipo o isointensas en T2 ( Fig. 29 ).
Por lo tanto,
debido a esta inespecificidad,
el diagnóstico se establece a través de la obtención de una muestra de tejido,
identificando granulomas caseosos,
el microorganismo (tinción ácido alcohol resistente ),
además del cultivo y PCR para micobacteria.
------------------------------
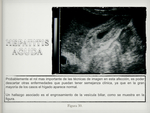
Hepatitis aguda
La hepatitis aguda es un proceso inflamatorio agudo con afectación difusa hepática.
Las causas etiológicas pueden ser muy variadas:
- Infecciones por virus (causa más frecuente),
bacterias o parásitos.
- Trastornos de tipo autoinmune.
- Lesiones debidas a la interrupción de la irrigación sanguínea normal del hígado.
- Traumatismos.
- Drogas,
toxinas y medicamentos.
- Trastornos de tipo hereditario como fibrosis quística o enfermedad de Wilson.
Los cambios patológicos consisten en hinchazón difusa de los hepatocitos,
proliferación de las células de Kupffer que revisten los sinusoides e infiltración de las áreas portales por linfocitos y monocitos,
llegándose a producir necrosis hepatocelular.
Probablemente el rol más importante de las técnicas de imagen en esta afección,
es poder descartar otras enfermedades que puedan tener semejanza clínica,
ya que en la gran mayoría de los casos el hígado aparece normal.
Las características ecográficas son paralelas a los hallazgos histológicos.
El parénquima hepático puede tener una ecogenicidad difusamente disminuida con acentuación del brillo de las tríadas portales,
los manguitos periportales dando un patrón denominado “en cielo estrellado”.
Hallazgos asociados son la hepatomegalia y el engrosamiento de la vesícula biliar ( Fig. 30 ).
Los hallazgos por TC igualmente resultan inespecíficos,
pudiendo encontrar hepatomegalia, disminución difusa de la atenuación,
traducción de infiltración grasa con claridad periportal debido al edema y engrosamiento de la pared de la vesícula biliar.
Después de una insuficiencia hepatocelular grave / hepatitis fulminante,
existen unos patrones morfológicos de necrosis y regeneración del parénquima hepático que son característicos por TC y RM.
Las áreas de necrosis muestran baja atenuación en los estudios de TC sin contraste haciéndose isodensas o hiperdensas respecto al parénquima hepático regenerado después de la administración de contraste.
Por el contrario,
la regeneración hepática nodular es hiperdensa en el estudio sin contraste e hipodensa después de la administración del contraste endovenoso,
pudiendo simular lesión neoplásica.
------------------------------
Peliosis hepática
Peliosis hepática no es mas que la proliferación de capilares rodeados de material granular e infiltrado inflamatorio.
Una forma importante es causada por Bartonella henselae y menos frecuentemente por Bartonella quintana. Si bien se ha asociado mas comúnmente a pacientes con SIDA y a transplantados renales,
también se ha descripto en pacientes con cáncer,
embarazadas,
después de transplante de otros órganos sólidos y raramente en inmumocompetentes. El mecanismo de transmisión es desconocido
Los hallazgos ecográficos son inespecíficos,
múltiples pequeñas lesiones hipoecoicas que usualmente comprometen el hígado y el bazo.
En la TC son nódulos menores de 1 cm hipo o hiperdensos distribuidos por el parénquima hepático [32,33].
Asimismo B.
henselae produce otra afección denominada enfermedad por arañazo de gato,
que afecta a niños o adolescentes inmunocompetentes.
Afecta de dos formas habitualmente,
regional con compromiso de linfadenitis o en forma de infección diseminada.
Esta última ocurre en el 5-10% de los casos y es la forma que provoca compromiso del hígado ocasionando granulomas hepatoesplénicos sin hepatoesplenomegalia.
En ecografía se identifican lesiones hipoecoicas múltiples y en TC son hipodensas que pueden tener un comportamiento variable con contraste en forma de leve realce difuso,
realce marginal o no captante.
------------------------------
Abscesos sobre lesiones hepáticas subyacentes
Las lesiones hepáticas subyacentes pueden proporcionar condiciones adecuadas para la formación de abscesos.
Su mecanismo puede ser variado.
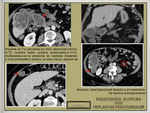
Las metástasis hepáticas tienen cierta tendencia a infectarse,
sobretodo cuando son de gran tamaño y con componente necrótico,
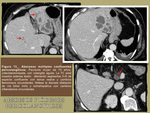
dado que se generan áreas de hipoxia tisular provocando de esta manera un ambiente propicio para el desarrollo de gérmenes anaerobios ( Fig. 31 ).
El mismo mecanismo se aplica a las lesiones posteriores a procedimientos de ablación o de alcoholización ( Fig. 32 ).
Asimismo la cirugía abdominal en general y la cirugía hepática o los traumatismos pueden producir como complicación abscesos,
sea por la presencia de hematomas que pueden sobreinfectarse en el mismo parénquima,
por procesos ascendentes de la vía biliar secundarios a colangitis por cirugía biliar o por diseminación de gérmenes vía portal secundaria a lesiones localizadas en otras vísceras ( Fig. 33 / Fig. 34/ Fig. 35 ).