La médula ósea (MO) es un tejido esponjoso que se encuentra en el interior de la mayoría de los huesos y es responsable de la hematopoyesis normal,
representando aproximadamente el 5% del peso corporal en el adulto.
Su microestructura celular es compleja y sus componentes determinan su aspecto macroscópico en la resonancia magnética,
dando lugar a los términos comúnmente utilizados como médula ósea roja y amarilla.
La médula ósea roja es más celular y contiene aproximadamente un 40% de grasa,
mientras que la médula amarilla contiene un 80% de grasa. Esta diferencia es importante para entender las variaciones en la intensidad de la señal en las distintas secuencias de resonancia magnética (RM),
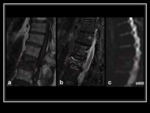
en situaciones normales y patológicas. Fig. 2
En su estudio rutinario se incluyen secuencias potenciadas en T1,
T2 y STIR,
sin embargo existen otras secuencias que nos pueden aportar más información,
dentro de ellas la técnica de difusión.
En esta,
la intensidad de la señal está determinada por el movimiento browniano de las moléculas de agua en los tejidos en función de su composición.
Así,
los tejidos muy celulares tendrán una restricción de la difusión que resultará en una hiperintensidad de la señal en la imagen potenciada en difusión con un determinado valor de b y en una hipointensidad de la señal en el mapa del coeficiente de difusión aparente,
mientras que los tejidos hipocelulares permitirán la difusión de las moléculas de agua.
Se han estudiado una serie de enfermedades musculoesqueléticas con esta técnica.
En nuestra práctica diaria,
la técnica de difusión ha sido de utilidad sobre todo para diferenciar entre fracturas benignas y patológicas,
distinguir la naturaleza de las metástasis óseas y diferenciarlas de entidades simuladoras,
así como para el diagnóstico y seguimiento de las enfermedades hematológicas comunes.
Principios de la técnica de difusión
La secuencia de difusión es una técnica de imagen funcional que permite un análisis cualitativo y cuantitativo de los tejidos a nivel celular.
La intensidad de señal está determinada por el movimiento microscópico de las moléculas de agua en los distintos tejidos,
que no es completamente libre ni aleatorio,
sino que se encuentra relacionado con la estructura microscópica de los mismos.
Así,
los tejidos muy celulares muestran una mayor restricción de la difusión,
es decir,
un impedimento al movimiento de las moléculas de agua.
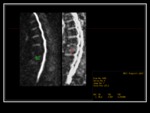
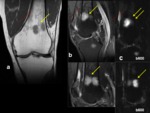
La literaruta sugiere que la correlación entre la celularidad de la MO y el valor del ADC es bifásica1.
Fig. 3
Con la aplicación de gradientes de difusión a las secuencias potenciadas en T2 espin-eco (T2 EE) se puede medir la difusión del agua en los tejidos.
Estos gradientes se pueden aplicar a diferentes secuencias estándar de RM con el inconveniente de que las imágenes tienden a presentar artefactos.
Actualmente,
la técnica más utilizada para obtener imágenes potenciadas en difusión es la single shot eco planar imaging (SS-EPI),
que requiere un menor tiempo de adquisición,
lo que la hace menos susceptible a los artefactos de movimiento,
conservando una relación señal-ruido relativamente alta.
Estas secuencias son más propensas a los artefactos de susceptibilidad en las interfases entre distintos tejidos,
por lo que se tratan imágenes con una baja calidad y detalle anatómico1.
La potencia y duración de la aplicación de los gradientes de difusión viene determinada por su valor b.
En la RM-D generalmente se utiliza un rango de valores b (dos o más) para estudiar la propiedad de difusión de los tejidos.
En ausencia de gradientes de difusión (valor b=0 mm2/s) el agua libre aparece brillante por el efecto intrínseco T2,
que se atenúa a medida que incrementamos el valor b,
es decir,
a medida que potenciamos la imagen en difusión.
Mediante transformaciones matemáticas en nuestra estación de trabajo,
a partir del b calculamos el coeficiente de difusión aparente.
Como el movimiento de las moléculas de agua se encuentra restringido en tejidos muy celulares,
a mayor valor b estos permanecen brillantes,
contrario a lo que ocurre en los tejidos normales de fondo.
La Fig. 4 resume los parámetros técnicos que utilizamos para obtener las imágenes potenciadas en difusión de la columna. .
Aplicaciones clínicas
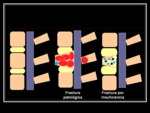
Distinción entre fracturas benignas y fracturas malignas
Las fracturas vertebrales son una complicación frecuente en pacientes con osteoporosis,
y a menudo se observan en pacientes con cáncer,
siendo difícil a veces distinguirlas de las patológicas.
En pacientes con antecedentes de neoplasia la RM se ha convertido en la técnica diagnóstica de elección en la detección de metástasis,
debido a su alta sensibilidad conferida por el excelente contraste entre los tejidos.
Sin embargo,
su especificidad se encuentra limitada,
ya que otras alteraciones de la médula ósea como el edema y la inflamación pueden mostrar una intensidad de señal similar.
En estos casos la especificidad se puede incrementar utilizando las secuencias de difusión,
entre otras.
En tejidos muy celulares,
como el tejido tumoral,
la difusión se encuentra restringida,
resultando en una hiperintensidad de la señal.
Esta hiperintensidad se encuentra influenciada también por el efecto T2 y depende además del valor b,
que se encuentra muy influenciado a su vez por el hardware del equipo,
por lo que un análisis cuantitativo con la medición del ADC es obligatorio para una correcta evaluación.
Se puede considerar que la MO normal en el adulto tiene una celularidad baja y unos valores bajos de ADC,
entre 0,2 – 0,5 x 10 -3 mm2/s2.
En un estudio realizado por Herneth et.
al.
encontraron que el valor medio del ADC en las fracturas patológicas fue de 0,7 x 10 -3 mm2/s ± 0,27 (P<0,03),
significativamente menor que en las fracturas por insuficiencia,
que fue de 1,61 x 10 -3 mm2/s ± 0,373.
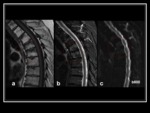
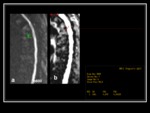
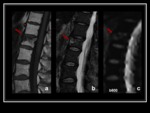
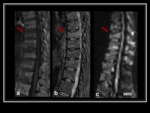
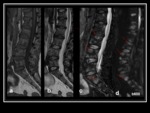
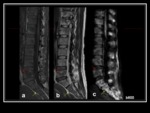
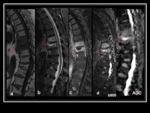
Fig. 5 Es importante el tiempo de evolución de las lesiones,
ya que una fractura aguda benigna,
debido al edema,
presentará un valor de ADC mayor,
que disminuye progresivamente hasta hacerse normal,
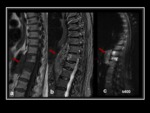
debido a la celularidad inflamatoria como elemento restrictivo al libre movimiento de las moléculas de agua. Fig. 6 Fig. 7 Fig. 8 Fig. 9 Fig. 10 Fig. 11 Fig. 12 Fig. 13 Fig. 14 Fig. 15
Trastornos neoplásicos
Metástasis óseas
Las metástasis óseas son el tumor maligno más frecuente del hueso y siempre debe ser tomado en cuenta en el diagnóstico diferencial de las lesiones malignas,
sobre todo en pacientes mayores.
La mayoría afectan al esqueleto axial – cráneo,
columna y pelvis -,
así como a los segmentos proximales de los huesos largos.
Debido a su alta frecuencia,
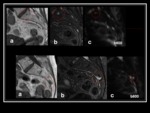
los cánceres de mama Fig. 16 Fig. 17 ,
pulmón Fig. 18 Fig. 19 y próstata son los responsables de la mayoría de las metástasis óseas,
aunque el tumor renal primario,
el cáncer de colon,
intestino delgado,
estómago Fig. 20 y el cáncer de tiroides también pueden metastatizar al hueso.
El cáncer de próstata representa un 60% de todas las metástasis óseas en hombres,
mientras que el cáncer de mama es el responsable del 70% en las mujeres.
Pueden ser solitarias o múltiples,
y se dividen en lesiones líticas puras,
blásticas puras o mixtas. Los tumores primarios que suelen dar metástasis líticas puras usualmente son el tumor renal,
de pulmón,
de mama,
de tiroides y del tracto gastrointesntinal.
Las metástasis blásticas puras más frecuentes provienen del cáncer de próstata,
aunque otros tumores pueden darlas.
La detección no siempre es posible con radiografía simple,
ya que la destrucción ósea a veces no es evidente.
La gammagrafía ósea y el PET se han utilizado ampliamente como pruebas de screening.
Comparado con ellos,
la RM-D ha demostrado ser igual o superior en la detección de metástasis óseas4.
Su capacidad para detectar lesiones extraóseas es otra ventaja de la RM-D sobre la gammagrafía. Una limitación de la RM-CC-D en la evaluación de la médula ósea son las lesiones osteoblásticas,
que aparecen como hipointensas con valores b altos por su bajo contenido en agua.
La caída de la señal en las secuencias de difusión permite diferenciar entre tejidos viables y necróticos.
La mayor difusión en el tejido necrótico se puede evidenciar con las secuencias SSFP (steady state free precesion).
Así,
la difusión se puede convertir en un método no invasivo para evaluar la respuesta al tratamiento. Además,
podría ser útil en la diferenciación entre la recurrencia tumoral y los cambios postquirúrgicos y secundarios a la radioterapia,
aunque se necesitarían estudios que lo confirmen5.
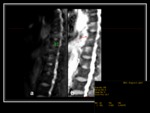
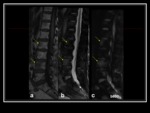
Infiltración por mieloma múltiple
El mieloma múltiple (MM) es una neoplasia clonal de células plasmáticas. Los patrones medulares de afectación en la RM,
en orden creciente de gravedad de la enfermedad,
son los siguientes: patrón medular normal,
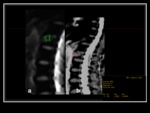
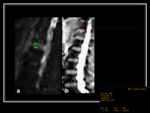
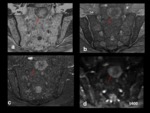
lesiones focales Fig. 21 Fig. 22 ,
patrón abigarrado y patrón difuso Fig. 14 Fig. 23 Fig. 24 .
Los criterios claves de imagen para el estadiaje del mieloma múltiple según la clasificación de Durie-Salmon que se basa en el número de lesiones focales detectadas en el esqueleto.
Aunque la radiografía simple sigue siendo la técnica estándar para el estadiaje de pacientes con MM de reciente diagnóstico,
existe evidencia de las ventajas que ofrece la RM potenciada en T1 y T2 con contraste intravenoso.
La osteopenia puede ser un signo incipiente de infiltración tumoral,
pero es difícil de diferenciar de la osteopenia senil con la radiografía convencional.
Además la extensión extramedular puede pasar desapercibida en la radiografía simple,
pero ser detectada con mucha facilidad en la RM.
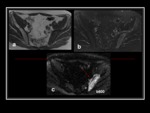
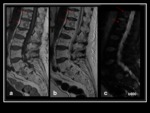
La RM de cuerpo entero se recomienda al menos en pacientes con MM y radiografías simples normales y en aquellos con plasmocitoma óseo solitario Fig. 25 .
La RM-D con supresión de la señal fondo es una técnica no invasiva capaz de detectar tejidos con celularidad alta.
En un estudio realizado por Sommer et.
al. para analizar el potencial de la RM-DSF en el diagnóstico del MM,
encontraron que la intensidad de las lesiones focales en las imágenes potenciadas en T2-STIR,
así como el ADC de las lesiones se correlaciona con la concentración sérica del componente M.
Las lesiones focales tienden a estar peor definidas en pacientes con niveles altos de paraproteína que en aquellos con bajo componente M,
lo que influye de forma negativa en la sensibilidad de la RM.
La RM-DFS aporta un alto contraste entre la lesión y el tejido de fondo,
que es independiente de los niveles de paraproteína. Además,
la monitorización de los niveles de ADC durante el seguimiento puede ser de utilidad en la evaluación de la actividad de la enfermedad junto a los parámetros clínicos6.
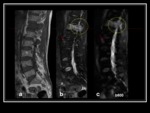
Linfoma
En la estadificación inicial del linfoma,
las secuencias de RM-D de cuerpo completo incrementan la tasa de detección de lesiones sobre los protocolos de RM solo con secuencias morfológicas. Fig. 26 Además,
en los ganglios aumentados de tamaño,
la cuantificación del ADC permite la diferenciación entre los inflamatorios y los que presentan infiltración linfomatosa7.
En un estudio realizado por Yasumoto et al.
encontraron que,
las secuencias espin-eco potenciadas en T1 tienen una mayor sensibilidad que la biopsia de médula ósea (92%),
mientras que las secuencias EPI potenciadas en difusión y STIR tienen una mayor especificidad (92%).
Alteraciones no neoplásicas
La médula ósea se puede encontrar afectada por otras patologías de naturaleza benigna. Tanto la espondilodiscitis piógena como la espondilodiscitis tuberculosa pueden mostrar una hiperintensidad en la señal tanto en las secuencias habituales como en la difusión,
siendo difícil de diferenciar de una afectación maligna.
Esto se explica porque los fluidos con alta concentración de proteínas son muy viscosos y pueden causar una restricción al movimiento libre del agua,
por lo tanto obtendríamos una restricción de la difusión en la infección indistinguible a la tumoral.
Buyn et al.
concluyeron que el valor medio de ADC en 2 pacientes con espondilitis tuberculosa fue de 0,98 x 10 -3 mm2/s,
cercano al valor en las fracturas patológicas.
En estos casos no hay evidencia aún de la utilidad de la difusión. Fig. 27