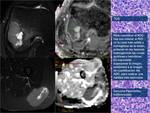
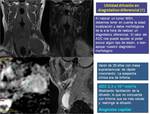
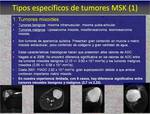
Los tumores musculoesqueléticos son muy heterogéneos,
aunque se pueden establecer unos valores orientativos de ADC para cada grupo de tumores que pueden ayudar en el diagnóstico diferencial: tumores mixoides,
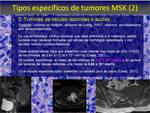
tumores de células redondas,
tumores de células gigantes,
tumores de células fusiformes,
tumores condrales de bajo grado…
Los valores de ADC pueden orientar sobre si se trata de un tumor benigno o maligno.
El ADC sirve para valorar la eficacia del tratamiento QT del osteosarcoma al estimar el grado de necrosis tumoral previo a la cirugía y del sarcoma de Ewing.
1 Introducción
La resonancia magnética (RM) debido a su alta resolución espacial,
gran contraste tisular y a su capacidad multiplanar,
es la técnica de imagen de elección para el diagnóstico,
estadificación preoperatoria,
y seguimiento,
tanto de los tumores óseos como de los de partes blandas.
La radiología simple sigue siendo la modalidad de estudio inicial en los tumores óseos,
y permite valorar la necesidad de realizar otras pruebas diagnósticas.
Hay nuevas secuencias de RM que facilitan el diagnóstico de la patología tumoral: estudio dinámico tras contraste intravenoso (CIV),
las secuencias en fase y fase opuesta (FFO),
espectroscopia y la secuencia de difusión en RM (RM-D).
La imagen de difusión (RM-D) es una técnica de imagen funcional no invasiva,
capaz de aportar información cualitativa y cuantitativa que complementa la información obtenida con las secuencias convencionales de RM.
La RM-D ha demostrado su utilidad en la diferenciación de fracturas vertebrales benignas y malignas y en la monitorización del tratamiento en pacientes con sarcomas.
(Bley,
2009 ;Costa,
2011;Khoo,
2011;Vilanova JC,
2012).
Aunque hasta el momento hay pocos estudios para valorar la utilidad de la RM-D en los tumores óseos y de partes blandas,
parece necesaria su inclusión en los protocolos convencionales morfológicos de RM,
tanto en el diagnóstico como en el seguimiento,
al ofrecer diferente contraste tisular y permitir realizar una cuantificación.
2 Aspectos técnicos
La imagen de difusión es una técnica no invasiva de RM que permite detectar el movimiento aleatorio o Browniano de las moléculas de agua,
dentro de los tejidos.
Se utilizan diferentes secuencias de difusión,
siendo las más empleadas las secuencias EPI (Echo Planar Imaging),
cuya mayor ventaja es la rapidez,
lo que las hace menos sensibles a los artefactos de movimiento,
permitiendo estudiar un amplio volumen.
La adquisición de la secuencia de difusión suele utilizar al menos 2 valores b (0 s/mm2 y otro entre 1 y 1.000 s/mm2),
obteniendo simultáneamente 2 imágenes con esos 2 valores b.
La RM-D permite realizar un estudio cualitativo y cuantitativo.
El estudio cualitativo se basa en la señal que presentan las lesiones.
La intensidad de señal no solo depende de la difusión del agua sino también del tiempo de relajación T2,
así una lesión con tiempo de relajación muy largo en T2 puede aparecer hiperintensa en las imágenes de difusión simulando una difusión restringida,
es lo que se denomina “efecto T2” (T2 shine through effect).
El efecto T2 se puede eliminar parcialmente aumentando el valor b y la posibilidad de realizar una cuantificación mediante el cálculo del ADC (Apparent Diffusion Coefficient,
o coeficiente de difusión aparente).
El ADC es independiente del campo magnético,
no se ve afectado por el efecto T2 y no varía con el valor b,
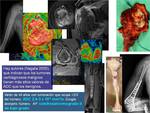
aunque hay autores (Padhani,
2011) que afirman que por razones técnicas sí hay variaciones del valor de ADC debido al campo magnético,
habiendo comprobado en nuestra experiencia personal un ligero aumento de los valores de ADC en equipos 3T comparándolos con los de 1.5T.
Algunos autores (Costa,
201) han propuesto minimizar el efecto de la perfusión del ADC,
no utilizando valores menores de 150 s/mm2,
utilizando únicamente valores b altos (300,450,
o 600 s/mm2).
como un indicador más fiable de la difusión,
denominándole ADC no sensible a la perfusión,
PIDC (perfusion-insensitive diffusion coefficient).
En nuestro protocolo utilizamos un factor b de 0 y 600 mm2/s,
supresión grasa,
matriz de 128 x 128 y 8 NEX (número de adquisiciones).
El resto de parámetros depende de la extensión del tumor y amplitud de la región anatómica que hay que estudiar,
el tipo de antena,
equipo de RM si es 1.5 o 3T.
Los parámetros orientativos son: TR >3000ms (normalmente entre 3000-5000ms,
aunque puede ser mayor si la zona a estudiar es muy amplia y hay mayor número de cortes); TE mínimo 75-90ms; grosor de corte: 3-6 mm; GAP (separación): <1mm La utilización de las técnicas de imagen en paralelo y el empleo de antenas multicanales mejora el tiempo de adquisición e incrementa la resolución espacial .
El tiempo de adquisición es de 3-4 minutos.
Para cuantificar el ADC,
hay que colocar el ROI en la zona más sólida y homogénea de la lesión,
evitando en las lesiones heterogéneas las zonas quísticas o necróticas.
Por eso es importante superponer la imagen anatómica a la imagen de cuantificación del ADC,
para realizar una medida más adecuada.
Fig. 2
3 Valoración de la difusión en los tumores musculoesqueléticos
La RM-D complementa la información obtenida con las secuencias morfológicas convencionales,
que dada la heterogeneidad y variabilidad de los tumores,
muchas veces no permite establecer un diagnóstico específico sin biopsia.
El contraste tisular obtenido con la RM-D es diferente del obtenido con las secuencias convencionales,
lo que facilita la detección de tumores de partes blandas,
óseos y metástasis.
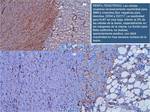
Con la RM-D podemos realizar un análisis cualitativo y cuantitativo y con ello intentar caracterizar el tumor,
al poder estimar los parámetros que influyen en la difusión como son:
celularidad tisular (densidad celular,
ratio núcleo-citoplasma),
-integridad de la membrana celular,
-espacio extracelular (estroma) del tumor y
-perfusión tisular.
Hay mayor restricción al movimiento de las moléculas de agua en tejidos con alta celularidad,
membranas celulares intactas y reducción del espacio extracelular o estroma.
Por el contrario hay una menor restricción o facilitación al movimiento de las moléculas del agua,
en tejidos con menor celularidad,
daño en las membranas celulares y mayor espacio extracelular.
El grado de restricción a la difusión es directamente proporcional a la celularidad tisular y a la integridad de las membranas e inversamente proporcional al espacio extracelular.
Estas diferencias pueden ser útiles para poner estimar la composición histológica de los tumores y establecer unos valores aproximados de ADC en algunos tumores.
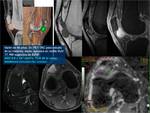
En general los tumores malignos son más celulares que los tumores benignos y presentan una mayor restricción a la difusión Fig. 3
,
y al revés,
en general,
los tumores benignos son menos celulares que los malignos y presentan una menor restricción a la difusión Fig. 4,
sin embargo no todos los tumores malignos tienen más celularidad que los benignos Fig. 5,
ni todos los tumores benignos tienen mayor espacio extracelular ni menor celularidad que los malignos Fig. 6.
Esta variabilidad en la histología de los tumores hace que en general no pueda usarse aisladamente la secuencia en difusión para valorar si un tumor es benigno o maligno o especificar el tipo concreto de tumor,
debido a la superposición en cuanto a los valores de ADC que presentan.
Ante un paciente con un tumor hay que tener en cuenta la edad,
localización de la lesión y los datos morfológicos de la rx,
RM….
Mediante la RM-D habría que comprobar si el valor de ADC se correlaciona con el tumor que pensamos,
lo que apoyaría nuestro diagnóstico o si bien nos permite descartar alguno de los posibles diagnósticos diferenciales,
para con ello acotar más el posible diagnóstico.
Fig. 7,
Fig. 8,
Fig. 9.
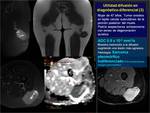
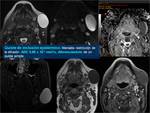
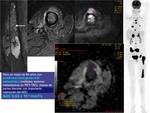
La RM-D diferencia el quiste de inclusión epidermoide,
del quiste simple,
algo que no nos lo permitiría ninguna otra secuencia.
Fig. 10.
4 Diferenciación entre tumores benignos y malignos.
Cuantificación DW.
En base a los valores de ADC,
hay autores que intentan establecer un valor de corte entre benignidad y malignidad,
similar a lo descrito en otros tipos de tumores no musculoesqueléticos.
Hay autores que no encuentran una diferencia significativa entre tumores benignos y malignos (Einarsdottir,
2004;Qi,
2012),
sin embargo otros autores si encuentran una diferencia significativa (Costa,
2011;Khedr SA,
2012;Khoo,
2011;Nagata,
2008;Neubauer,
2012),
e incluso algunos establecen un valor de corte para malignidad (Costa,
2011 y Neubauer,
2012) Table 1.
Todos estos datos deben ser refrendados con series más amplias y además habría que homogeneizar la técnica utilizada.
Como sugiere Nagata (Nagata,
2008),
al examinar histológicamente 88 tumores de partes blandas,
hay que diferenciar inicialmente los tumores mixoides de los no mixoides,
dado que ambos grupos presentan una diferencia significativa en cuanto a los valores de ADC.
No encuentra diferencia significativa entre los tumores mixoides benignos y malignos.
Los dos artículos que no encuentran diferencia entre tumores benignos y malignos no establecen la diferenciación inicial entre tumores mixoides y no mixoides.
Experiencia Hospital Universitario Quirón Madrid:
Hemos estudiado 100 tumores,
32 malignos y 68 benignos.
Los tumores se han dividido en tumores no mixoides (93) y mixoides (7),
como recomendó Nagata et al en 2008.
Ninguno de los tumores tiene tratamiento quirúrgico previo o terapia adyuvante,
quimio o radioterápica previa.
64 de los tumores tienen comprobación histológica,
todos los malignos (32) y 32 de los benignos.
El resto de los tumores presentan un seguimiento de al menos un año.
Se han excluido los tumores benignos con apariencia típica en las imágenes de RM como los lipomas,
gangliones o quistes sinoviales.
Comparamos nuestros datos con los de la literatura.
Se ha llevado a cabo una estadística no paramétrica.
En nuestra serie,
hay diferencia estadísticamente significativa entre los tumores benignos no mixoides y los tumores malignos no mixoides: (2,12;1,07 vs 0,94;0,29 P< 0,001):
– Tumores benignos no mixoides: mediana 2,12 x 10-3 mm2/s; IQR 1,07(IQR Amplitud intercuartil).
– Tumores malignos no mixoides: mediana 0,94 x 10-3 mm2/s ; IQR 0,29
Fig. 11.
Dentro de los tumores malignos no mixoides,
hay algunos tumores malignos que presentan unos valores más altos de ADC de los esperados,
como son los osteosarcomas y dos de los condrosarcomas,
debido a la presencia de abundante matriz extracelular.
Además uno de los liposarcomas convencionales y uno de los cordomas (debido a la presencia de estroma mixoide abundante),
presentan unos valores más elevados de ADC.
Estos hallazgos coinciden con los de trabajos previos (Costa,
2011; Khedr SA,
2012; Khoo,
2011; Nagata,
2008;Neubauer,
2012).
Como posible factor de sesgo podría influir la presencia de la alta prevalencia en nuestra serie de tumores condrales de bajo grado (19),
todos ellos con unos valores de alrededor de 2,2-2,5.
Si se eliminasen estos tumores del análisis estadístico,
también habría una diferencia estadísticamente significativa entre los tumores benignos no mixoides y los tumores malignos no mixoides: (1,7 vs 0,09 p< 0,001).
En estudios previos no hay diferencia estadísticamente significativa entre tumores mixoides benignos y malignos (Nagata 2008).
En nuestra limitada experiencia con únicamente 7 casos,
hay una diferencia entre tumores benignos mixoides y tumores malignos mixoides: (2,39 vs 1,89),
aunque no estadísticamente significativa.
Mostramos nuestros valores de ADC tanto de los tumores benignos como de los malignos y los comparamos con los datos de la literatura.Table 2,
Table 3.
5.
Tipos específicos de tumores MSK.
Es útil esta diferenciación inicial,
aunque después habría que establecer unos grupos de tumores que presenten unas características histologías comunes,
con unos valores de ADC similares,
siempre orientativos y teniendo en cuenta que hay tumores que no es posible encuadrarlos en ningún grupo debido a su heterogeneidad histológica.
Se podrían agrupar en: tumores mixoides,
tumores de células redondas,
tumores de células gigantes,
tumores de células fusiformes,
tumores con estroma especializado y abscesos-hematomas.
5.1.
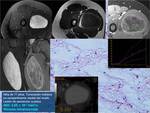
Tumores mixoides.
Fig. 12 ,
Fig. 13 ,Fig. 14 ,Fig. 15.
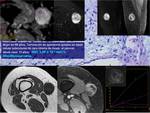
5.2.
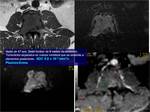
Tumores de células redondas o azules Fig. 16,
Fig. 17.
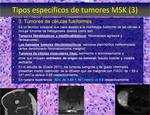
5.3.
Tumores de células fusiformes.
Fig. 18 ,Fig. 19 ,Fig. 20 ,Fig. 21 ,Fig. 22.
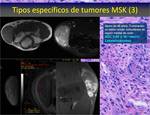
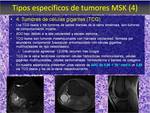
5.4.
Tumores de células gigantes (TCG).Fig. 23 ,Fig. 24 ,Fig. 25 .
5.5.
Tumores con estroma especializado. Son tumores con un estroma abundante característico relacionado con su histogénesis,
estando agrupados en tumores condrales (osteocondromas,
condroblastomas,
encondromas,
y condrosarcomas) y óseos (osteosarcoma o sarcoma osteogénico).
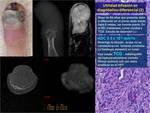
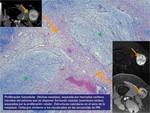
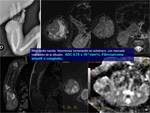
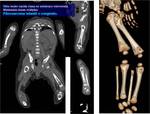
Con respecto a los tumores condrales,
Fig. 26 surge un problema al intentar diferenciar encondroma de condrosarcoma de bajo grado en los huesos largos.
Normalmente se diagnostican incidentalmente mediante radiología simple al presentar dolor en articulación adyacente o bien en un estudio gammagráfico realizado para detectar metástasis.
Se han establecido unos criterios para diferenciarlos,
sugiriendo más condrosarcoma de bajo grado cuando la edad es mayor de 40 años,
el diámetro mayor de la tumoración > 5 cm,
si provoca dolor el propio tumor y rebaje endostal mayor de dos tercios del grosor de la cortical (aunque el rebaje endostal suele verse en ambos),
sin embargo en la mayoría de los casos no es posible diferenciarlos,
teniendo que hablar de tumores condrales de bajo grado.
A veces incluso después de biopsia o cirugía no es fácil diferenciarlos entre patólogos expertos.
Hay autores (Costa,
2011;De,Coninck,
2013;Geirnaerdt,
2000).
que mediante el estudio dinámico tras CIV,
diferencian condrosarcomas de bajo grado de los encondromas “inactivos”,
al presentar intenso realce precoz.
En nuestra experiencia no es posible diferenciarlos,
al tener unas curvas similares,
en general progresivas.
Con la secuencia de la difusión se abría la posibilidad de poder diferenciarlos,
pero en nuestra experiencia tampoco es posible,
pues ambos presentan unos altos valores de ADC de alrededor de 2,2-2,5 x 10-3 mm2/s,
por la presencia de importante cantidad de matriz condroide o estroma.
Nuestra actitud y lo refrendado en la literatura consiste en un manejo multidisciplinario,
basándose en la clínica y en los hallazgos de imagen y tratarlos en general conservadoramente.
Hay autores (Nagata 2005),
que indican que los tumores cartilaginosos malignos tienen más altos valores de ADC que los benignos,
lo cual se cumple en algunos casos Fig. 27 , pero no en todos Fig. 28.
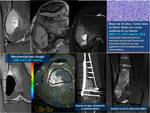
6 Respuesta al tratamiento
La efectividad del tratamiento quimioterápico o quimioradioterápico se basa tradicionalmente en una aproximación anatómica mediante la medición del tamaño tumoral,
utilizando los criterios RECIST,
aunque no puede aplicarse a todos los tumores.
La resonancia magnética con secuencias convencionales junto con la secuencia de difusión es útil para valorar la recidiva y eficacia del tratamiento quimioterápico,
al poder detectar la necrosis tumoral inducida por el tratamiento.
Fig. 29.
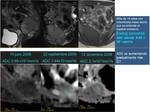
Una de las primeras aplicaciones de la difusión en los tumores musculoesqueléticos fue para valorar la eficacia del tratamiento quimioterápico neoadyuvante en osteosarcomas {Hayashida,
2006;Uhl,
2006}.
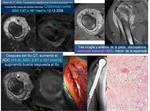
El osteosarcoma,
a pesar de que el tratamiento quimioterápico sea satisfactorio,
no disminuye significativamente de tamaño,
ya que el tratamiento no afecta a la matriz mineralizada del tumor.
Por otra parte,
la efectividad del tratamiento quimioterápico neoadyuvante tiene un valor pronóstico pues indica mayor supervivencia libre de enfermedad.
La respuesta se considera favorable si histológicamente hay una necrosis celular mayor del 90%,
para lo que es necesario realizar biopsias.
La difusión permite estimar la muerte celular y con ello el daño de las membranas,
la disminución de la densidad celular y el aumento del espacio extracelular,
sin necesidad de biopsia (Hayashida,
2006;Oka,
2010 ;Padhani,
2011;Uhl,
2006),
pudiendo evitar seguir con tratamientos ineficaces,
y con ello poder modificar la línea de tratamiento.
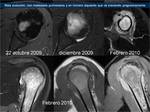
Hay que realizar el estudio de RM antes de comenzar el tratamiento,
a mitad de tratamiento y a los 10-14 días de haber finalizado el mismo Fig. 30 ,
Fig. 31,
Fig. 32. En la serie de Uhl et al 2006,
tras estudiar 8 osteosarcomas,
estimó que los pacientes que responden,
en los que se constató tras la cirugía una necrosis mayor del 90%,
presentan un aumento de los valores de ADC de 0,4-0,7×10−3 mm2/s,
(ADC inicial antes del tratamiento 2,1±0.4×10−3 mm2/s),
mientras que los pacientes con necrosis tumoral < 90%,
presentan un aumento solo del 0-0,3% ×10−3 mm2/s.
En el estudio de Hayashida et al 2006,
los pacientes con necrosis <90%,
aumentaron el ADC del 1,35 a 1,64×10−3 mm2/s,
siendo este aumento mayor en los pacientes con necrosis >90%,
con un aumento del ADC del 95% de 1,09 a 2,01×10−3 mm2/s.
El resto de los estudios también concluyen que hay diferencia en los valores de difusión entre los pacientes que responden y los que presentan una baja respuesta,
aunque la técnica utilizada y la forma del medir el ADC es diferente en todos los estudios.
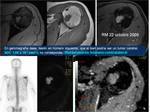
En el estudio Oka et al 2010,
con 22 osteosarcomas,
propone medir el ADC “mínimo”,
el cual está presente en las zonas más sólidas,
no realizando una media de los valores de ADC,
lo cual parece lógico para con ello medir las zonas más celulares del tumor.
Habría que realizar series más amplias y estandarizar la técnica de adquisición y la forma de medir el ADC para con ello ofrecer una mayor reproducibilidad de los resultados.