2.
MATERIAL Y MÉTODOS
Estudio prospectivo transversal,
cuyo protocolo fue aprobado por el Comité Ético de Investigación Clínica de Aragón (CEICA).
Los pacientes incluidos en el estudio fueron prospectivamente preseleccionados desde El Programa de Diagnóstico Precoz de Glaucoma del Servicio de Oftalmología del Hospital Universitario Miguel Servet de Zaragoza.
Se trata de un estudio longitudinal prospectivo diseñado para evaluar la estructura del NO y la función visual en el glaucoma llevado a cabo en la Unidad de Glaucoma de dicho Hospital.
Todos los pacientes del programa Programa de Diagnóstico Precoz de Glaucoma que,
desde enero de 2006 a julio de 2008,
cumplieron con los criterios de inclusión descritos a continuación,
fueron consecutivamente incluidos en el estudio.
Sólo se consideró un ojo de cada sujeto,
de modo que si los dos ojos eran candidatos,
se eligió uno de forma aleatoria,
aunque todas las exploraciones y pruebas fueron realizadas de forma bilateral.
Cada uno de los sujetos preseleccionados debía cumplir los siguientes criterios de inclusión:
- Edad mayor de 18 años
- Agudeza visual corregida igual o superior a 20/40
- Defecto de refracción menor de 5 dioptrías de equivalente esférico y/ o un cilindro menor de 2 dioptrías
- Medios ópticos transparentes: opacificaciones del cristalino <1 según la Lens Opacities Classification System III
- Ángulo de cámara anterior abierto grado IV en la escala de Scheffe
- Ausencia de enfermedades oculares o sistémicas que pudieran afectar al nervio óptico o al campo visual
- Disponibilidad y colaboración para la realización de las pruebas del protocolo exploratorio
- Aceptación del consentimiento informado
Se excluyeron del estudio los sujetos que cumplieran cualquiera de los siguientes criterios de exclusión:
- Cirugía ocular previa
- Malformaciones oculares,
anomalías angulares o del nervio óptico
- Ángulo no abierto,
valorado mediante gonioscopía con lente de Goldmann (grado <III).
- Ametropías esféricas elevadas > 5 dioptrías (D) y astigmatismos > 3 D
- Antecedentes de patología neurooftalmológica (neuritis óptica,
esclerosis múltiple,
etc.).
- Retinopatías o maculopatías
- Uso de medicación que pudiera afectar la sensibilidad del campo visual
- Imposibilidad para realizar una midriasis superior a 5 mm
2.1.
TIPOS DE PACIENTES INCLUIDOS EN LA MUESTRA:
La muestra estaba formada por sujetos control,
pacientes sospechosos de glaucoma y pacientes con daño perimétrico glaucomatoso incipiente.
Pacientes control:
Aquellos que presentaban unas cifras de PIO menores o iguales a 21 mm de Hg,
un estudio de perimetría automatizada normal,
una papila de morfología normal,
así como una exploración oftalmológica sin alteraciones.
Pacientes sospechosos de glaucoma:
Aquellos que presentaban una papila óptica de morfología sospechosa de glaucoma (según una evaluación subjetiva) y/o una PIO mayor de 21 mmHg.
A su vez todos los pacientes presentaban una perimetría automatizada convencional al inicio fiable que mostrase un campo visual normal.
Pacientes con glaucoma perimétrico:
Aquellos pacientes con una papila óptica de morfología sospechosa de glaucoma (según una evaluación subjetiva) y/o una PIO mayor de 21 mmHg,
al igual que en el grupo de sospechosos,
pero en este caso todos presentaban una perimetría automatizada convencional al inicio fiable que mostrase un campo visual con daño glaucomatoso leve o moderado.
2.2.
PROTOCOLO EXPLORATORIO:
A todos los sujetos del estudio se les realizó un mismo protocolo exploratorio completo,
que incluía los siguientes estudios clínicos y pruebas complementarias:
· Historia clínica y Oftalmológica en la que se recogió la siguiente información:
- Datos epidemiológicos: edad,
sexo.
- Antecedentes personales: tensión arterial,
enfermedades generales (especialmente enfermedades cardiovasculares,
hematológicas y neurológicas),
tratamientos generales actuales y previos.
- Antecedentes familiares de patología ocular: especialmente existencia de glaucoma en familiares de primer grado.
- Antecedentes personales oftalmológicos: cirugías oculares,
traumatismos,
uveítis,
tratamientos tópicos oculares previos o actuales.
· Exploración oftalmológica completa,
que incluyó:
- Agudeza visual
- Biomicroscopía de polo anterior usando lámpara de hendidura
- Gonioscopia
- Tonometría de aplanación Goldmann
- Oftalmoscopia de segmento posterior
- Paquimetría ultrasónica corneal central
- Perimetría automatizada convencional
- Estereofotografías papilares
- Oftalmoscopio láser confocal de barrido (HRT)
- Estudio ecográfico Doppler de la vascularización orbitaria
Todas las exploraciones oftalmológicas,
test perimétricos,
análisis topográficos y estudios de flujo,
se realizaron en un plazo máximo de ocho semanas desde la inclusión del sujeto en el estudio.
2.3.
OFTALMOSCOPIO LASER CONFOCAL DE BARRIDO
El análisis topográfico de la cabeza del NO fue realizado utilizando un oftalmoscopio láser confocal de barrido,
el Heidelberg Retina Tomograph,
concretamente su tercera versión o HRT3 (Heidelberg Engineering,
Heidelberg,
Germany).
Automáticamente el HRT-3 obtiene varias series de cortes topográficos papilares de 64 planos focales cada una.
A partir de estas series,
el instrumento calcula la media y proporciona una imagen topográfica papilar final.
El software del HRT ofrece múltiples ventanas que detallan diferentes parámetros topográficos: parámetros estereométricos,
funciones discriminantes,
la clasificación de Moorfield o “Moorfields Rregression analysis” (MRA) y el Glaucoma Probability Score (GPS).
Éste último es el que se utilizó como criterio para la clasificación de nuestra muestra.
El GPS permite una clasificación automática de los pacientes,
basándose en la comparación de la morfología de su capa de fibras neurorretiniana peripapilar y la morfología de la excavación,
con unos modelos de normalidad y de aspecto glaucomatoso.
Con ello establece un valor numérico de probabilidad de glaucoma.
CLASIFICACIÓN DE LA MUESTRA SEGÚN EL GPS
Los resultados del GPS final se dividieron atendiendo a los puntos de corte recomendados por el fabricante.
De este modo los ojos se clasificaron de la siguiente manera:
- Pacientes con valores de GPS comprendidos entre 0 y 0.27 se clasificaron como dentro de los límites normales.
- Pacientes con valores de GPS comprendidos entre 0.28 y 0.64 se clasificaron como borderline.
- Pacientes con valores de GPS entre 0.65 y 1 se clasificaron como fuera de los límites normales.
2.4.
ESTUDIO CON ECOGRAFIA DOPPLER DE LA VASCULARIZACIÓN ORBITARIA
Todos los estudios ecográficos fueron realizados con un mismo equipo de ultrasonidos,
un ecógrafo Siemens Acuson Antares®,
usando un transductor lineal multifrecuencia (VF 10-5) a una frecuencia preseleccionada de 7.3 MHz.
Todas las exploraciones fueron realizadas por un único explorador,
que desconocía la historia clínica del paciente o la asimetría de la enfermedad,
estudiando ambos ojos en todos los pacientes,
comenzando siempre por el ojo derecho.
El tiempo de realización de la prueba osciló entre 15 y 20 min.
PROTOCOLO EXPLORATORIO
Para la realización de la prueba,
el paciente se colocaba en decúbito supino,
tumbado sobre una camilla de exploración médica,
con los brazos situados a ambos lados del cuerpo. El examinador se colocaba a la derecha del paciente.
El estudio se realizaba con los ojos del paciente cerrados,
apoyando suavemente el transductor,
en el plano transversal ó ligeramente oblicuo,
sobre el párpado superior.
En todo momento se intentaba minimizar la presión aplicada sobre el ojo,
lo que podría alterar la PIO y modificar erróneamente la hemodinámica retrobulbar,
para lo cual se apoyaba suavemente la mano del explorador sobre el reborde orbitario del paciente.
El protocolo de estudio estaba compuesto por tres fases:
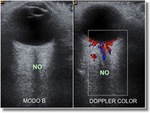
a) Exploración de la órbita en modo B: con el objetivo de realizar una valoración morfológica del globo ocular y de las estructuras retrobulbares,
así como descartar patología concomitante. En esta fase se identificaba el nervio óptico (banda hipoecogénica en el seno de la grasa retrobulbar hiperecoica) como referencia anatómica para localizar las estructuras vasculares a estudiar (Figura1).
b) Estudio Doppler color: para identificar y seleccionar el vaso a valorar. Los vasos que se estudiaron fueron la arteria oftálmica,
la arteria y vena central de la retina,
arterias ciliares posteriores cortas y vena oftálmica superior.
c)Estudio Doppler pulsado: para la valoración espectral y de los diversos parámetros hemodinámicos de cada vaso.
Para ello,
una vez que el vaso se había seleccionado en la modalidad Doppler color,
se colocaba el volumen de la muestra en el centro del mismo,
del menor tamaño posible dentro de las posibilidades del equipo.
En todos los casos se hizo un ajuste del ángulo,
paralelo al eje del vaso,
aunque en la ACR y la AO no se requirió hacer un ajuste del ángulo en la mayoría de los casos,
ya que su recorrido es paralelo al eje del transductor.
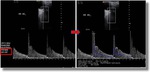
Seguidamente se obtenía la onda velocimétrica y se seleccionaban sobre ella el máximo número de ciclos consecutivos y uniformes posibles,
con un mínimo de 2 (Figura2).
La siguiente tabla muestra los vasos estudiados y los parámetros analizados en cada uno de ellos (Tabla1).
|
Vaso retrobulbar
|
Parámetro hemodinámico
|
|
AO(Arteria Oftálmica)
ACR(Arteria central de la retina)
ACPC N(Arterias ciliares posteriores cortas nasales)
ACPC T(Arterias ciliares posteriores cortas temporales)
|
VPS (Velocidad pico sistólica)
|
|
VFD (Velocidad final diastólica)
|
|
VM (Velocidad media)
|
|
IR (Índice de resistencia)
|
|
IP (Índice de pulsatilidad)
|
|
S/D (Cociente sístole-diástole)
|
|
|
|
|
VCR(Vena central de la retina)
VOS(Vena oftálmica superior)
|
V max (Velocidad Máxima)
|
|
V min (Velocidad mínima)
|
|
V med (Velocidad media)
|
|
IP (Índice de pulsatilidad)
|
Para obtener unas medidas lo más reproducibles posibles,
estas determinaciones se realizaron en una serie de localizaciones específicas para cada vaso,
elegidas en base a la bibliografía disponible (Figura3):
- La arteria y vena centrales de la retina, se identificaron en el espesor del nervio óptico realizando las medidas por detrás de la lámina cribosa,
obteniendo sus registros conjuntamente separados por la línea de base.
- La arteria oftálmica se midió en el lado nasal al nervio óptico,
justo después de cruzar el mismo.
- Las arterias ciliares posteriores cortas,
nasales y temporales,
se identificaron a ambos lados del nervio óptico,
realizando los registros próximos al NO y tan anterior como fue posible.
Las arterias ciliares posteriores cortas no pueden ser medidas de forma individual por esta técnica,
sino que su registro es en realidad una suma de las ondas de varias de ellas.
De manera sistemática se realizaron dos determinaciones en cada uno de los vasos estudiados.
Si no había disparidad entre ambas se seleccionó la de mejor calidad.
En los casos de disparidad de resultados se realizó una tercera medición,
seleccionando en este caso la mediana de las determinaciones realizadas (o la media si no existía una clara mediana).
2.5.
ANÁLISIS ESTADÍSTICO
Para describir las características de los sujetos incluidos en el estudio,
así como los parámetros obtenidos en las diferentes pruebas se utilizaron la media y la desviación estándar.
Los valores medios de las variables demográficas,
clínicas y oftalmológicas,
en cada uno de los grupos de pacientes definidos por el GPS se compararon mediante el test de ANOVA,
previa comprobación de homogeneidad de varianzas mediante el test de Levene.
En las variables que se obtuvieron diferencias significativas se aplicó posteriormente un análisis POST-HOC mediante el test de Bonferroni.
La comparación de medias de los distintos parámetros hemodinámicos medidos por ecografía Doppler ocular de los dos grupos en función de los datos del GPS (normal,
borderline o glaucoma) se llevó a cabo mediante el test de ANOVA para muestras independientes,
considerando una p ≤ 0,05 como nivel de significación estadística.
Previamente se analizó la homogeneidad de las varianzas con el test de Leaven.
Posteriormente se realizó para los parámetros en los que se habían encontrado diferencias significativas un análisis post-Hoc mediante el test de Bonferroni (para variables con varianzas homogéneas) o el test T3 de Dunnett (para los casos en los que no se demostró homogeneidad de las varianzas).