INTRODUCCIÓN
La patología benigna uterina y las malformaciones uterinas pueden detectarse inicialmente en los controles rutinarios ecográficos de las pacientes en edad fértil,
en los estudios de clínica ginecológica inespecífica como metrorragia y dismenorrea,
y también los estudios de infertilidad.
En la mayoría de los casos requerirán un estudio RM ya sea para su confirmación diagnóstica,
valoración del pronóstico de fertilidad,
enfoque terapéutico o planificación quirúrgica.
REVISIÓN ANATÓMICA
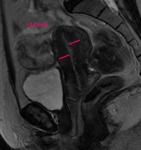
Anatómicamente el útero se divide en: cuerpo y cérvix,
separados por el istmo.
Histológicamente en la pared del cuerpo uterino se distinguen tres capas: la serosa,
el miometrio y el endometrio.
En los estudios RM,
el útero aparece de señal homogénea e isointensa a la musculatura en las secuencias potenciadas en T1.
Mientras que en las secuencias potenciadas en T2,
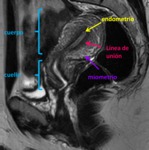
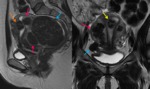
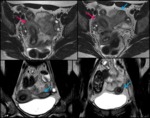
diferenciamos tres zonas en el cuerpo uterino de las mujeres premenopáusicas:
Una zona central hiperintensa,
que se corresponde al endometrio.
Una zona intermedia,
hipointensa llamada línea de unión Ésta corresponde a la parte interna del miometrio,
formada por músculo liso más compacto y menor contenido de agua.
El grosor normal de la línea de unión varía de 2 a 8 mm.
Finalmente una zona externa,
que corresponde a la parte externa del miometrio y muestra una señal intermedia (fig.
1) .
ESTUDIO RM DEL ÚTERO
¿CUÁNDO?
Es mejor realizar el estudio de resonancia magnética evitando la fase menstrual,
para evitar el posible engrosamiento fisiológico de la línea de unión que se produce durante la menstruación,
en especial en aquellos casos que se pretende descartar adenomiosis.
¿CÓMO?
T2: La secuencias potenciadas en T2 son prínceps para la valoración de la pared uterina normal para diferenciar la línea de unión y valorar posible adenomiosis; para la valoración de masas uterinas; y para la valoración de la cavidad endometrial y poder así clasificar las malformaciones uterinas.
T1 y T1 con SUPRESIÓN DE LA GRASA: Es útil para evaluar el componente hemorrágico,
que aparece hiperintenso en las secuencias T1 con supresión de la grasa.
También es útil para descartar posible endometriosis.
CONTRASTE: El contraste será útil en el estudio con patología benigna uterina,
en los caso que se sospeche o se asocie carcinoma endometrial. También se utiliza para el control post-embolización de miomas uterinos.
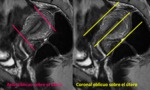
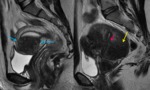
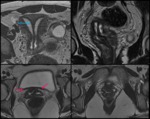
PLANOS: Són imprescindibles los cortes transversales perpendiculares al miometrio o cortes sagitales para valorar el grosor de la línea de unión en el estudio de adenomiosis. El plano coronal oblicuo sobre el útero debe incluirse para valorar el contorno uterino y la morfología de la cavidad endometrial,
para clasificar las malformaciones uterinas ( fig.
2).
CAMBIOS FISIOLÓGICOS
Hay que tener en cuenta cambios fisiológicos que se pueden producir y que pueden alterar la anatomía normal del útero por RM,
debemos conocerlos para evitar falsos positivos.
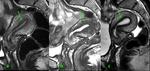
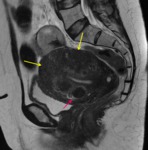
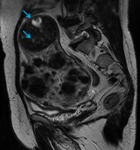
Engrosamiento fisiológico de la línea de unión: Según la fase del ciclo menstrual,
se presentan unos cambios en la línea de unión,
que afectan a su grosor.
Durante la primera fase del ciclo menstrual ,
la fase proliferativa,
aumenta el grosor de la línea de unión de forma fisiológica,
pudiendo ser superior a los 12 mm y valorarse como falso positivo para adenomiosis ( fig.
3).
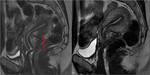
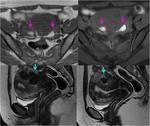
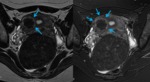
Contracciones uterinas : Las contracciones uterinas pueden producirse también de forma fisiológica,
y son transitorias.
Si se produce durante un estudi RM,
pueden manifestarse como masas miometriales hipointensas en T2 y simular leiomiomas o adenomiomas.
Debido a que las contracciones uterinas son transitorias,
si demostramos su desaparición en las imágenes posteriores,
podemos descartar otras causas de masas uterinas y establecer el diagnóstico de las contracciones (Fig.
4).
ADENOMIOSIS
La adenomiosis es una enfermedad benigna del útero caracterizada por la presencia de tejido endometrial ectópico en el miometrio.
Es una patología relativamente frecuente,
presente en el 25% de las histerectomías.
Por lo general,
la adenomiosis afecta a las mujeres premenopáusicas multíparas.
Los síntomas más frecuentes son metrorragia,
dismenorrea y dispareunia,
pero puede ser asintomática hasta en un 35% de los casos.
El diagnóstico clínico de la adenomiosis es difícil debido a la presentación clínica inespecífica y a la frecuente coexistencia de otras enfermedades pélvicas.
La resonancia magnética es una técnica eficaz para el diagnóstico,
que permite diferenciarla de otras patologías uterinas y ayuda a planificar el tratamiento.
Existen dos tipos de adenomiosis:
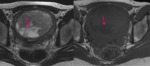
Difusa : Consiste en un engrosamiento difuso de la línea de unión.
El criterio diagnóstico es una engrosamiento > 12mm.
( Fig.
5).
El grosor normal se considera < 8 mm.
Si la línea de unión es de grosor entre 8 y 12 mm debe repetirse el estudio evitando la fase menstrual.
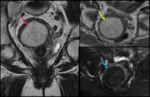
Pueden asociarse pequeños focos de tejido endometrial heterotópico o dilatación quística de las glándulas endometriales ,
estrías lineales que sugieren endometrio dentro de miometrioy pequeños focos hemorrágicos (Fig.
6),
los cuales añaden especificidad para el diagnóstico de adenomiosis.
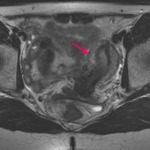
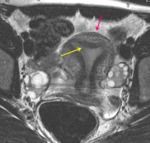
Adenomiosis focal o adenomioma: Se presenta como una masa miometrial de márgenes mal definidos ,
generalmente ovoidea no encapsulada y que puede hallarse en continuidad de la zona de unión o no ( fig.
7) .
Por su señal hipointensa en T2 el principal diagnóstico diferencial es el leiomioma.
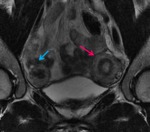
Entre el 60-80% de las pacientes con adenomiosis tiene enfermedad pélvica adicional ,
la más frecuente el leiomioma (fig.
8 ) . También pueden coexistir la adenomiosis y endometriosis.
La endometriosis consiste en la presencia de tejido endometrial ectópico,
fuera del propio útero,
la localización más frecuente es el ovario ( fig.
9)
LEIOMIOMA
El leiomioma es el tumor ginecológico más común,
afecta a un 20-30% de las mujeres en edad fértil.
La mayoría de los pacientes son asintomáticas,
y cuando se acompañan de clínica,
suele ser la metrorragia.
Son tumores benignos compuestos fundamentalmente por células musculares lisas separadas por cantidades variables de tejido conectivo fibroso.
Aunque no tienen una verdadera cápsula,
están bien circunscritos y rodeados por una pseudocápsula.
La manifestación típica por RM es una masa de origen miometrial bien delimitada,
hipointensa en T1 y en T2.
Un 4% de los leiomiomas pueden presentar calcificación,
en TC o RX suele apreciarse un patrón de calcificación densa y amorfa,
pero la sensibilidad de la RM para la calcificación es baja.
Según su localización se clasifican en submucosos,
intramurales o subserosos ( fig 10.)
- Submucosos: Son los menos frecuentes pero los más sintomáticos y pueden ser causa de infertilidad.
Se proyectan hacia la cavidad endometrial y en algunos casos pueden protruir hacia el canal cervical o la vagina.
La señal hipointensa de los miomas y su origen miometrial permite diferenciarlos de los pólipos,
hiperplasia o carcinoma endometrial.
En caso de sospecha se realiza biopsia para confirmar el diagnóstico.
- Intramurales: Son los más frecuentes,
y los que plantean el diagnóstico diferencial con el adenomioma.
Pueden distinguirse por los márgenes: los leiomiomas tienen márgenes bien definidos,
mientras que la interfase entre la adenomiosis focal y el miometrio es irregular.
Además los leiomiomas puede presentar un anillo hiperintenso,
debido a la dilatación de los vasos linfáticos,
venas dilatadas y edema(fig.
11 ) También los leiomiomas,
a igual tamaño condicionan mayor efecto de masa o distorsión del miometrio que los adenomiomas.
- Subserosos: Suelen ser asintomáticos,
aunque los pediculados si se torsionan pueden sufrir infarto y causar dolor.
En algunos casos puede extenderse entre las capas del ligamento ancho,
simulando una masa ovárica y deberá hacerse el diagnóstico diferencial con el fibroma ovárico.
Los leiomiomas también pueden presentar degeneración debido a un crecimiento mayor y más rápido que el de su aporte sanguíneo.
El tipo de degeneración más frecuente es la degeneración hialina (fig.
12).
Un 4% presentan degeneración quística (fig.13),
que consistente en formación de espacios quísticos como secuela del edema. La degeneración mixoide se presenta como masas rellenas de material gelatinoso.
Esta degeneración también puede presentarse en los leiomiosarcomas y otros tumores malignos.
En algunos casos puede producirse un infarto masivo de un leiomioma por la obstrucción de las venas de drenaje en la periferia de la lesión y condicionar degeneración roja.
También existe la degeneración grasa,
habitualmente sobre un mioma que presenta degeneración hialina.
No debe confundirse con LIPOLEIOMIOMA. El lipoleiomioma (fig 14) representa una metamorfosis grasa del mioma,
aunque algunos tumores no tienen componente muscular liso.
Su prevalencia es del 0.8%,
típicamente se produce en la perimenopausa.
En RM se presenta como una masa habitualmente de localización subserosa,
y muestra una intensidad de señal similar a la grasa en todas las secuencias.
Existen diferentes opciones de tratamiento de los miomas.
En el tratamiento con ultrasonido focalizado de alta intensidad ( HIFU),
la RM tiene un papel clave para realizar el tratamiento guiado por RM así como para el seguimiento.
También será útil la RM en el control postembolización de los miomas.
MALFORMACIONES UTERINAS
La prevalencia de malformaciones uterinas varía entre el 3 y el 10% según la bibliografía.
Esta discrepancias pueden deberse a las diferentes técnicas utilizadas en el diagnóstico,
así como en las diferentes sistemas de clasificación utilizados para definir las malformaciones.
Entre las mujeres con antecedentes de abortos de repetición la prevalencia pueden aumentar hasta el 30%.
La histerosalpingografía suele realizarse en las fases inciales del estudio de infertildad.
Ésta aporta información sobre el canal endocervical,
endometrial y permeabilidad tubárica,
sin embargo la caracterización de malformaciones uterinas es difícil y se pueden superponer hallazgos,
no pudiendo diferenciar entre útero bicorne y septado.
En cuanto a la ecografía ha demostrado una precisión diagnóstica del 90-92% en el diagnóstico de las malformaciones uterinas,
frente al 100% de la RM.
Las malformaciones uterinas pueden ser secundarias a trastornos del desarrollo,
de no fusión de los conductos de Müller y de no degeneración.
Estos transtornos se dividen en distintos tipos según características clínicas,
pronósticos y tratamientos similares.
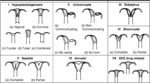
La clasificación más ampliamente aceptada,
es la clasificación de Buttram y Gibbons modificada en 1988 por la Sociedad Americana de Fertilidad,
actualmente la Medicina Reproductiva ( fig.
15).
Debido a que las opciones de tratamiento varían considerablemente ,
es fundamental una caracterización precisa preoperatoria.
La RM permite la valoración del contorno externo y la presencia de cavidades endometriales no comunicantes información clave para la clasificación de las malformaciones.
También permite valorar la existencia de tabiques muscular y fibroso en el canal de endometrio.
En los transtornos del desarrollo de los conductos de Müller se incluyen las hipoplasias y agenesias segmentarias ( clase I) y los úteros unicorne ( clase II).
Agenesias / hipoplasias: La RM demuestra la absencia de útero,
cérvix o vagina.
La forma más frecuente es el síndrome de Mayer-Rokitansky-Küster-Hauser,
que incluye agenesia o hipoplasia vaginal,
ovarios y trompas de Falopio intactas y malformación uterina,
de tracto urinario y esqueleto.
Unicorne: Se produce por la falta de desarrollo de uno de los conductos de Müller.
Puede ser completa,
con un solo cuerno uterino (fig 16) o puede existir un desarrollo incompleto,
existiendo un cuerno rudimentario que puede contener o no endometrio ( fig.
17).
Esta cavidad endometrial puede tener comunicación con la cavidad principal o estar aislada (fig 18).
Es importante la detección de estas cavidades endometriales,
ya que en ocasiones se resecan quirúrgicamente para evitar complicaciones.
Los defectos de no fusión de los conductos de Müller pueden dar a lugar a útero didelfo ( clase III) y a útero bicorne ( clase IV).
En los defectos de fusión existe una indentación del contorno.
El útero didelfo se presenta en RM como dos úteros y cuellos normalmente divergentes (fig.
19)A pesar que el septo vaginal puede asociarse a cualquier malformación uterina,
se asocia más frecuentemente al útero didelfo.
En ocasiones el septo puede ser obstructivo y condicionar hematocolpos ( fig.
20).
El útero bicorne se caracteriza por la presencia de un septo muscular y fibroso que separa los dos cuernos,
la presencia de una indentación del contorno en el plano coronal mayor de 1 cm,
lo diferencia del útero septado.
Los defectos de no degeneración,
condicionaran la existencia de un septo,
útero septado ( clase V) o una pequeña indentación,
útero arcuado (clase VI).
El útero septado es la malformación uterina más frecuente y tiene una elevada asociación con infertilidad.
A diferencia del útero bicorne,
el contorno del útero es convexo o muestra una concavidad inferior a 1 cm.
Además el septo que separa los dos cuernos uterinos suele ser inferior a 4 cm.
( fig.
21,
22) La diferenciación correcta del útero bicorne y septado es importante porque en caso de cirugía,
el abordage quirúrgico del útero bicorne es transabdominal,
mientras que el útero septado se puede tratar por histeroscopia.
El útero arcuado se define cuando existe una mínima indentación del contorno de la cavidad endometrial en el fundus uterino (fig.
22)Esta malformación no representa un riesgo sobre la fertilidad.
Finalmente,
la clase VII de la clasificación,
corresponde a las malformaciones secundarias a DES.