En 1992 tuvo lugar en Atlanta el Simposium Internacional sobre la pancreatitis aguda (PA),
una reunión de 40 expertos internacionalmente reconocidos en la enfermedad inflamatoria aguda pancreática especialistas en Anatomía,
Gastroenterología,
Medicina Interna,
Anatomía Patológica,
Radiología y Cirugía en un intento de llegar a un consenso global multidisciplinar y a una clasificación aplicable universalmente en la PA.
Anteriormente la mayoría de los términos utilizados para describir las entidades morfológicas observadas en las distintas pruebas de imagen o en el quirófano en la PA eran entendidas o interpretadas de distinta manera entre los distintos expertos en páncreas,
sobre todo en lo que se refería a colecciones pancreáticas y peripancreáticas.
Aunque dicha clasificación de Atlanta se utilizó durante años,
muchos de sus términos siguieron sin ser aceptados o utilizados de igual manera por digestivos,
cirujanos y radiólogos,
lo cual,
unido al mejor conocimiento con el paso del tiempo de la fisiopatología de la PA,
a la mejora en las técnicas de imagen y al desarrollo de terapias mínimamente invasivas radiológicas,
endoscópicas y quirúrgicas para el manejo de sus complicaciones hicieron necesario revisar dicha clasificación inicial.
Desde entonces han tenido lugar diversas reuniones y revisiones de la clasificación de Atlanta lideradas por el Acute Pancreatitis Classification Working Group hasta que en 2012,
con la colaboración de miembros de 11 sociedades internacionales de patología pancreática,
se han acuñado las definiciones definitivas por consenso internacional de los distintos tipos clínicos y entidades morfológicas de la PA del adulto (los conceptos sólo son aplicables a pacientes mayores de 18 años) que pasamos a detallar.
*Los comentarios encabezados por un asterisco corresponden bien a reflexiones hechas en revisiones previas al consenso final o nuestras en base a lo leído en la bibliografía aportada,
no recogidas explícitamente en el documento de consenso definitivo.
1.
DEFINICIÓN DE PANCREATITIS AGUDA Y DEL MOMENTO DE INSTAURACIÓN DEL CUADRO
El diagnóstico de PA requiere dos de los tres requisitos siguientes:
- Dolor abdominal sugestivo de PA (dolor de inicio brusco en epigastrio y que a menudo se irradia a la espalda)
- Niveles de lipasa o amilasa sérica al menos tres veces por encima del límite alto de la normalidad
- Hallazgos característicos de PA en las pruebas de imagen,
siendo el TC con contraste la técnica de imagen de elección (menos comúnmente se emplearán la RM o la ecografía transabdominal).
Si el diagnóstico se establece por dolor abdominal y actividad sérica aumentada de las enzimas pancreáticas no suele ser necesario realizar un TC en urgencias o para el ingreso en el hospital.
Si el dolor abdominal es muy sugestivo de PA pero la actividad de las enzimas pancreáticas se encuentra por debajo de tres veces los valores normales,
se requerirán pruebas de imagen para confirmar el diagnóstico.
Hay que tener claro además que el inicio de la pancreatitis aguda se define como el momento en que se instaura el dolor,
y no como el momento de ingreso en el hospital.
2.
CURSO Y SEVERIDAD DE LA PANCREATITIS Y CONCEPTOS QUE HAY QUE TENER CLAROS
La PA ha de ser entendida como un proceso dinámico,
que evoluciona a lo largo del tiempo desde su instauración.
Aunque su fisiopatología aún no se comprende completamente se cree que en la mayoría de los casos (como en pacientes con colelitiasis o abuso de alcohol,
que son sus dos causas más frecuentes) se desencadenan una serie de eventos debido a una obstrucción temporal o permanente del conducto pancreático.
Esto da lugar a nivel local a una activación y liberación de enzimas pancreáticas al intersticio glandular y los tejidos peripancreáticos que,
cuando es importante,
puede conducir a la autodigestión y la necrosis.
Y a nivel sistémico a una liberación de mediadores inflamatorios llamados citoquinas que activan e intensifican la cascada inflamatoria,
conduciendo a un síndrome de respuesta inflamatoria sistémica (SRIS) que puede en último término,
más probablemente cuanto más perdure en el tiempo,
culminar en un fallo (multi)orgánico.
Para determinar la existencia de fallo (multi)orgánico se propone el sistema de puntuación modificado de Marshall por su sencillez y reproducibilidad universal (figura 1) y se considera fallo orgánico transitorio al fallo orgánico que se resuelve en las primeras 48 horas,
fallo orgánico persistente al que persiste más de 48 horas y fallo multiorgánico al que afecta a más de un órgano/sistema.
Otros conceptos que se aclaran son la definición de complicación local,
en la que se incluyen el desarrollo de colecciones peripancreáticas (ya sean colección líquida peripancreática,
pseudoquiste,
colección necrótica o necrosis encapsulada,
que veremos más adelante) y otras como la alteración funcional en el vaciamiento gástrico,
la trombosis esplénica o portal o la necrosis colónica.
Y la de complicación sistémica,
entendiendo por tal la exacerbación de una comorbilidad preexistente (como una enfermedad coronaria o una enfermedad pulmonar crónica) precipitada por la PA.
Y con todo lo anterior el consenso define que dividimos la PA temporalmente en dos fases que responden a los dos principales picos de mortalidad y que pueden solaparse:
- Fase temprana: Comprende en general la primera semana del proceso y en ella la severidad de la pancreatitis va a depender fundamentalmente de parámetros clínicos,
concretamente de si se produce fallo orgánico o no por el SIRS y de la duración del mismo.
Aunque en esta fase se pueden producir complicaciones locales,
no van a ser los principales determinantes de la severidad del cuadro ya que se ha comprobado que la extensión de los cambios morfológicos en la PA no necesariamente se correlacionan con su severidad clínica (y así un paciente puede tener una PA leve con manifestaciones radiológicas severas en la TC o una PA clínicamente severa con mínimos cambios inflamatorios en el páncreas,
como puede ocurrir p.e.
en paciente con comorbilidad importante asociada).
Además,
como ya veremos,
puede no ser fiable la determinación de la necrosis pancreática en el TC (otro conocido factor pronóstico) en los primeros días de la enfermedad.
- Fase tardía: A partir de la primera semana y que puede durar semanas o meses.
Se caracteriza por la persistencia de los datos sistémicos de inflamación o por la presencia de complicaciones locales,
de modo que por definición (lo veremos a continuación) la fase tardía ocurre sólo en pacientes con PA moderada o severa.
Las complicaciones locales evolucionan durante esta fase,
y aunque el principal determinante de la severidad de la PA seguirá siendo el fallo orgánico persistente,
será importante distinguir por imagen las diferentes entidades morfológicas de dichas complicaciones locales porque esto tendrá implicaciones directas en el manejo del paciente.
El manejo se basará así en este momento tanto en criterios clínicos como morfológicos.
Y desde el punto de vista del grado de severidad el consenso habla de PA:
- Leve: En ausencia de fallo orgánico,
de complicaciones locales o sistémicas.
Los pacientes con PA leve suelen ser dados de alta durante la fase temprana,
no suelen requerir pruebas de imagen y la mortalidad asociada es muy rara.
- Moderada: Cuando hay fallo orgánico (o multiorgánico) transitorio o complicaciones locales o sistémicas en ausencia de fallo orgánico persistente.
Puede resolverse sin intervención (como en caso de fallo orgánico transitorio o formación de una colección líquida peripancreática) o requerir cuidados especializados prolongados (como en caso de necrosis estéril extensa sin fallo orgánico) y su mortalidad es mucho menor que en la PA severa.
- Severa: Cuando hay fallo orgánico (o multiorgánico) persistente.
Los pacientes que lo desarrollan a menudo tienen una o varias complicaciones locales y los que lo hacen en los primeros días de la enfermedad tienen un riesgo aumentado de mortalidad que puede alcanzar cifras de hasta el 36-50%.
Si además desarrollan necrosis infectada la mortalidad resulta extremadamente alta.
3.
TIPOS DE PANCREATITIS AGUDA.
CLASIFICACIÓN MORFOLÓGICA.
De todas las técnicas de imagen de las que disponemos,
el consenso reafirma que el TC con contraste es la modalidad de elección en la evaluación inicial y el seguimiento de la PA cuando el curso de la enfermedad lo requiere (pe.
cuando el diagnóstico clínico-analítico es dudoso,
si hay fallo orgánico u otros datos clínico-analíticos sugerentes de PA severa,
en aquellos pacientes en los que se sospecha complicación local severa –una isquemia intestinal o una perforación,
…-,
en el seguimiento de las complicaciones locales,
sobre todo de la infección,
necrosis o hemorragia,
o cuando falla la respuesta clínica al tratamiento).
Además el TC va a ser útil si se contempla intervenir ya que va a servir de guía para la aspiración o drenaje percutáneo,
endoscópico o quirúrgico.
Y subraya que igual que la PA es un proceso dinámico en sus manifestaciones clínicas,
también lo es desde el punto de vista morfológico,
con alteraciones cambiantes en su curso que suelen seguir un desarrollo temporal determinado: sabemos así que la necrosis parenquimatosa,
si se produce,
lo va a hacer pronto en el curso de la enfermedad (normalmente en los primeros 4 días),
que la infección de la necrosis pancreática o peripancreática requiere en cambio varias semanas para aparecer (encontrándose su pico de incidencia entre la segunda y la cuarta),
que la encapsulación completa de las colecciones peripancreáticas suele producirse en torno a la cuarta semana …
*Dichos cambios en la imagen,
dicho orden de aparición temporal,
ya quedaron reflejados en el conocido Índice de Severidad por TC (ISTC) (figura 2) descrito por Balthazar y colaboradores,
un sistema de gradación radiológica compuesto por una escala de 10 puntos que clasifica la PA desde el punto de vista de la imagen en leve,
moderada y severa según los cambios inflamatorios pancreáticos/extrapancreáticos (0-4 puntos) y la extensión de la necrosis glandular (0-6 puntos),
aunque la revisión de la clasificación de Atlanta definitiva no hace mención a dicha gradación.
Y ¿cómo clasifica entonces el consenso la PA desde el punto de vista morfológico? Pues diferencia dos tipos: la pancreatitis edematosa intersticial y la pancreatitis necrotizante,
pudiendo cursar esta última con necrosis parenquimatosa sola,
necrosis peripancreática sola o con necrosis tanto glandular como parenquimatosa.
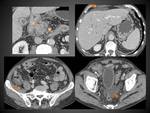
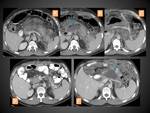
PANCREATITIS EDEMATOSA INTERSTICIAL (PEI)
La mayoría de los pacientes con PEI muestran un aumento difuso (o en algunas ocasiones localizado) del páncreas debido al edema.
En el TC con contraste el paréquima pancreático muestra un realce generalmente homogéneo (aunque también puede ser algo heterogéneo debido a dicho edema,
a la cantidad de líquido intersticial) y la grasa peripancreática suele presentar ciertos cambios inflamatorios a modo de leve borrosidad o estriación.
Puede asociarse también algo de líquido peripancreático (ver apartado de colecciones pancreáticas y peripancreáticas) y sus síntomas normalmente se resuelven durante la primera semana (figura 3).
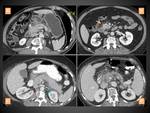
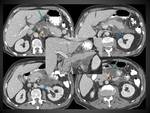
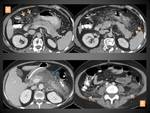
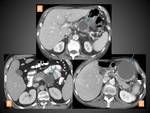
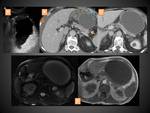
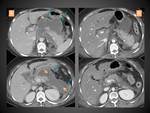
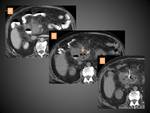
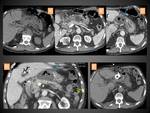
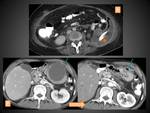
PANCREATITIS NECROTIZANTE (PN)
Aproximadamente el 5-10% de los pacientes desarrollan necrosis que puede ser sólo del parénquima pancreático (lo menos frecuente,
en torno a un 5% de las PN) (figura 4),
sólo de los tejidos peripancreáticos (en torno al 20% de las PN) (figura 5)o de ambos (lo más común) (figura 6).
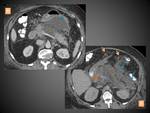
En el TC la necrosis pancreática se manifiesta como una o varias áreas de hipodensidad parenquimatosa,
y la aparición de dichas áreas no realzantes diferencian la PN de la PEI.
En el caso de la necrosis peripancreática el páncreas realza normalmente en el TC con contraste pero los tejidos peripancreáticos desarrollan necrosis (ver apartado de colecciones pancreáticas y peripancreáticas).
No obstante hay que tener en cuenta que la alteración en la perfusión pancreática y los signos de necrosis peripancreática se desarrollan a lo largo de los días,
lo cual explica porqué un TC con contraste realizado demasiado pronto al inicio de la enfermedad puede infraestimar la potencial extensión de la necrosis pancreática y/ó peripancreática.
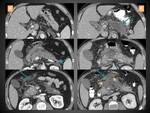
Y así en los primeros días de la PA,
el patrón de captación glandular del contraste puede ser parcheado o heterogéneo antes de que el área de necrosis se demarque mejor o se haga más confluente y podemos tener dudas para clasificar la PA en PEI o PN.
En este caso deberemos de clasificarla inicialmente de indeterminada y dejar su caracterización más precisa para un TC hecho un poco más tardíamente (entre tres y siete días después),
ya que una vez pasada una semana desde la instauración de los síntomas,
un área de parénquima no realzante se podrá considerar finalmente como necrosis parenquimatosa pancreática.
Las mismas dudas podrán plantearse en el caso de la necrosis peripancreática si el TC se ha realizado con demasiada premura (lo veremos más adelante en el apartado de colecciones) (figuras 7 y 8)
Los pacientes con necrosis peripancreática sola tienen una tasa de morbi-mortalidad superior a aquéllos con una PEI,
aunque menor a la de los que tienen necrosis glandular.
La historia natural de la necrosis pancreática y/ó peripancreática es variable,
ya que puede permanecer sólida o licuarse,
permanecer estéril o infectarse,
persistir o desaparecer con el tiempo.
*Tradicionalmente (inclusive en el ISTC) la extensión de la necrosis pancreática se ha cuantificado en tres categorías: con afectación menor del 30% de la glándula,
entre el 30-50% y de más del 50% del páncreas,
siendo precisamente las zonas hipodensas en el TC que afectan a menos del 30% de la glándula las que con más frecuencia pueden plantear la dificultad de clasificarlas en un principio como edema o necrosis.
*En cuanto a la definición de necrosis glandular como “área hipodensa no realzante”,
sólo en la clasificación de Atlanta inicial de 1992 se cuantifica dicha hipodensidad en unidades Hounsfield y se define que hay necrosis en aquellas zonas del páncreas no alcanzan las 50UH con la administración de contraste (el realce glandular normal en fase portal suele oscilar entre las 50 y las 100UH),
aunque nunca se modifican,
nisiquiera se vuelven a mencionar dichos valores de atenuación en las revisiones de Atlanta posteriores.
Balthazar en su artículo sobre el ISTC de 2002 define también que la ausencia de captación glandular de contraste o captación mínima con valores de atenuación por debajo de 30UH indican una perfusión glandular disminuida (una isquemia) que se correlaciona con el desarrollo de necrosis.
*Con todo lo anterior,
tanto de los conocimientos previos como del consenso actual se deduce que el mejor momento para realizar un TC (si es necesario) inicial en la PA es a partir de las 72 horas desde el inicio del cuadro,
para asegurarnos que los datos de necrosis,
si es que la hay,
se han manifestado ya con fiabilidad.
*Y aunque ni Atlanta ni el consenso final la contemplan entre sus definiciones,
sabemos que otra forma de detectar la existencia de necrosis en la grasa peri o extrapancreática es por la presencia en el retroperitoneo o mesenterio de densidades nodulares mal definidas en el contexto de una PA (figura 9).
4.
DEFINICIÓN DE LAS COLECCIONES PANCREÁTICAS Y PERIPANCREÁTICAS
El consenso hace una importante distinción entre las colecciones que pueden presentarse en la PA en función fundamentalmente de su tiempo de evolución,
menor o mayor de 4 semanas,
y de su contenido,
diferenciando las que contienen sólo líquido de las que se desarrollan a partir de la necrosis y contienen componentes sólidos o “semisólidos” (normalmente asociados a mayores o menores cantidades de líquido).
Y así define los siguientes tipos de colecciones:
COLECCIÓN LÍQUIDA PERIPANCREÁTICA AGUDA (CLPA)
Se llaman así a las colecciones que aparecen en la PEI antes de las 4 semanas de evolución de la enfermedad.
Resultan del edema local relacionado con la inflamación pancreática y/ó peripancreática y pueden no tener conexión con el sistema ductal pancreático o surgir de la rotura de alguna pequeña rama secundaria periférica del conducto pancreático principal.
En el TC aparecen como colecciones adyacentes al páncreas,
predominantemente en torno al mismo,
que pueden ser únicas o múltiples y se caracterizan por contener sólo líquido (por definición carecen de componentes sólidos),
de densidad homogénea,
sin pared completamente definida y que se adaptan a los planos fasciales del retroperitoneo (normalmente celda peripancreática,
espacios pararrenales anteriores,
saco menor…) (figuras 10 y 11)
Cuando una CLPA persiste más allá de 4 semanas normalmente evoluciona a un seudoquiste (ver a continuación),
aunque se trata de un evento poco común en la PA.
*Las CLPAs deben ser diferenciadas de la ascitis que puede acumularse en los espacios perihepático y periesplénico,
gotieras parietocólicas y pelvis (figura 12).
PSEUDOQUISTE
Se refiere a la colección líquida peripancreática que aparece en la PEI cuando persiste más de 4 semanas desde el inicio del cuadro,
y se piensa que surge por disrupción del conducto pancreático principal o sus ramas intrapancreáticas,
siendo la consecuente fuga de jugos pancreáticos la que da lugar a que la colección persista todo ese tiempo.
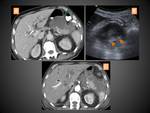
En el escáner aparece como una colección normalmente redondeada u ovalada con pared bien definida (formada por tejido de granulación) que contiene líquido sin elementos sólidos o semisólidos (figura 13),
y aunque el TC con contraste es la modalidad de imagen más empleada en el diagnóstico de los seudoquistes en ocasiones puede ser necesaria una ecografía o una RM para confirmar dicha ausencia de contenido sólido en su interior (figura 14).
Estas características suelen ser suficientes para su diagnóstico,
aunque si se realizara una aspiración del contenido por algún motivo se obtendrían niveles elevados de amilasa y lipasa en el mismo.
El desarrollo de seudoquistes en la PA (en contra de lo que ocurre en la pancreatitis crónica) es un evento muy raro (la mayoría de las colecciones peripancreáticas persistentes en una PA contienen material necrótico),
así que el término en el contexto de PA se cree que posiblemente caerá en desuso.
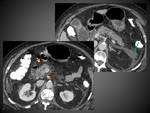
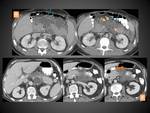
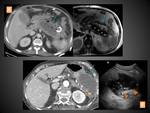
COLECCIÓN NECRÓTICA AGUDA (CNA)
Se llama así a las colecciones que aparecen en la PN durante las primeras 4 semanas de su evolución y por definición contienen cantidades variables de líquido y material necrótico.
La necrosis ya hemos comentado que puede afectar al parénquima pancreático y/ó los tejidos peripancreáticos y que resulta de la liberación de enzimas pancreáticas que ocasiona una digestión,
saponificación de la grasa y finalmente una necrosis de los mismos.
En el TC aparecen como colecciones intra y/o extrapancreáticas que pueden ser múltiples,
con una morfología que a menudo puede ser loculada o septada,
sin pared definida delimitándolas completamente y con densidad heterogénea en su interior por la presencia tanto de líquido como de material sólido o semisólido (figuras 15 y 16).
Como ya hemos comentado anteriormente,
el TC con contraste puede no ser capaz de poner de manifiesto con fiabilidad la presencia de contenido necrótico dentro de las colecciones,
en especial en la primera semana desde la instauración de la enfermedad,
y así ser difícil diferenciar si estamos ante una PEI o PN.
En ese caso las colecciones deberán de catalogarse como indeterminadas y para caracterizarlas será útil realizar un estudio secuencial ya que después de esa primera semana normalmente será más evidente la presencia o no de necrosis en su interior,
a lo que además nos podrán ayudar otras técnicas de imagen (como ya hemos comentado) como son la ecografía o la RM.
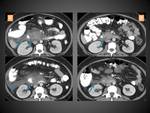
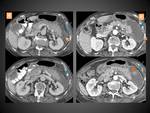
NECROSIS ENCAPSULADA (NE)
Se define como la colección que persiste en la PN más allá de 4 semanas y consiste en tejido necrótico contenido en el interior de una cápsula realzante de tejido inflamatorio reactivo.
En el TC aparecen como colecciones intra y/o extrapancreáticas que pueden ser múltiples,
completamente encapsuladas y con densidad heterogénea en su interior por la presencia tanto de contenido líquido como sólido o semisólido (figura 17).
Pueden en ocasiones ser difíciles de diferenciar de los seudoquistes con las consecuencias y el manejo normalmente opuesto que supone el diagnóstico de unas y otros,
para lo cual el consenso vuelve a considerar útil el empleo de la ecografía o la RM (figuras 18 y 19).
*A esta entidad se hacía referencia previamente en la literatura como “necrosis pancreática organizada”,
“necroma”,
“secuestro pancreático”,
“seudoquiste asociado con necrosis” o “necrosis pancreática subaguda”,
términos que han quedado obsoletos.
PSEUDOQUISTE POSNECROSECTOMÍA (PP)
Es el único caso en el que hablamos de pseudoquiste en el contexto de una PN y se produce como resultado de un “síndrome de desconexión del conducto pancreático”.
Estos pacientes tienen una necrosis de la porción central de la glándula pancreática aunque conservan tejido pancreático viable en la cola y desarrollan una NE que puede potencialmente requerir necrosectomía.
Cuando la cavidad residual libre de material necrótico sigue manteniendo comunicación con dicha cola remanente secretora,
la cavidad se rellena de jugo pancreático y forma un PP.
Se trata de una colección que aparece muy tardíamente (pueden pasar meses o años del episodio de PA) cuyo continente lo forma la cápsula de una NE que se ha rellenado de líquido pancreático y ya no contiene elementos sólidos y es necesaria una historia previa de necrosectomía quirúrgica o endoscópica para su diagnóstico (figuras 20 y 21).
5.
NECROSIS INFECTADA
La necrosis pancreática y/ó peripancreática pueden permanecer estériles o infectarse y la mayoría de las evidencias sugieren que no hay una correlación absoluta entre la extensión de la necrosis y el riesgo de infección y duración de los síntomas.
La infección de la necrosis es rara durante la primera semana de la enfermedad.
El diagnóstico de la infección de la necrosis es importante porque va a tener una historia natural,
un tratamiento (antibiótico y una intervención activa más que probable) y pronóstico diferentes a los de la necrosis estéril.
La presencia de infección se diagnostica cuando hay gas extraluminal en el páncreas o los tejidos peripancreáticos en el TC (hallazgo virtualmente patognomónico de infección y que refleja la presencia de microorganismos productores de gas) (figuras 22 y 23) o cuando una PAAF,
normalmente guiada por imagen,
es positiva para bacterias y/u hongos en la tinción de Gram y el cultivo.
*Aunque el consenso final sólo habla de necrosis infectada,
en las revisiones previas se comenta que cualquiera de las colecciones (incluido el pseudoquiste) pueden infectarse,
y los datos que sirven para diagnosticar la infección son los mismos ya descritos para todas ellas.
Pero también se dice que,
con diferencia,
las colecciones más susceptibles e infección son las que contienen material necrótico,
y probablemente por eso el consenso final habla sólo de la necrosis infectada.
*Ante el hallazgo de burbujas de gas en el TC habremos de tener en cuenta que éstas podrán estar presentes en el interior de colecciones ya drenadas con catéteres o en las que de forma espontánea hayan podido fistulizar a vísceras huecas adyacentes sin que exista necesariamente infección (figura 24).
*Puede haber una cantidad variable de pus asociado a la necrosis pancreática infectada que puede aumentar con el tiempo y la licuefacción.
La clasificación inicial de Atlanta proponía el término “absceso pancreático” para definir una colección localizada de contenido predominantemente purulento sin una cantidad significativa de contenido necrótico.
Este hallazgo es extremadamente poco común y dado que el término es confuso y no ha sido ampliamente adoptado ha quedado fuera de la clasificación definitiva.