Los estudios de imagen por RM se basan en el comportamiento de los nÚcleos de los ÃĄtomos de hidrÃģgeno bajo la influencia de un campo magnÃĐtico.
Sin influencia de un campo magnÃĐtico externo,
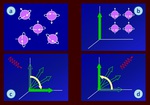
los momentos magnÃĐticos individuales de los protones existentes en un volumen elemental de materia se orientan de forma aleatoria (Figura 1a).
Cuando un paciente es introducido en el interior del imÃĄn de un equipo de RM,
los momentos magnÃĐticos individuales de los protones existentes que se encontraban orientados de forma aleatoria pasan a orientarse en la misma direcciÃģn del campo magnÃĐtico (Figura 1b).
Al aplicar un pulso de radiofrecuencia los protones absorben energÃa y entran en resonancia (todos los protones estÃĄn precesando al unÃsono),
lo que provoca una disminuciÃģn de la magnetizaciÃģn longitudinal y,
paralelamente,
un aumento de la magnetizaciÃģn transversal (Figura 1c).
Cuando cesa el pulso de radiofrecuencia los protones se desprenden de la energÃa que habÃan absorbido cediÃĐndola al medio circundante y dejan de estar en resonancia (todos los protones dejan de precesar al unÃsono),
lo que da lugar a una disminuciÃģn de la magnetizaciÃģn transversal y,
simultÃĄneamente,
a un aumento de la magnetizaciÃģn longitudinal (Figura 1d).
La relajaciÃģn transversal o relajaciÃģn T2 es,
por tanto,
el proceso mediante el cual la magnetizaciÃģn transversal desaparece y se debe a la pÃĐrdida de coherencia de fase de los protones.
A medida que la magnetizaciÃģn transversal se va perdiendo y la magnetizaciÃģn longitudinal se va recuperando se genera una corriente elÃĐctrica,
la cual es recogida por una antena y posteriormente transformada en una imagen.
Este desfase de los protones estÃĄ influido por los microcampos magnÃĐticos de los nÚcleos vecinos y tambiÃĐn por las faltas de homogeneidad del campo magnÃĐtico externo.
De estas dos situaciones,
sÃģlo la falta de homogeneidad del campo magnÃĐtico externo se puede corregir.
En RM existen,
fundamentalmente,
dos grandes familias de secuencias de pulsos:
- Secuencia SPIN â ECO (SE): Se aplica un pulso de excitaciÃģn de 90š seguido de uno o dos pulsos de refase de 180š para obtener uno o dos ecos,
respectivamente.
- Secuencia GRADIENTE â ECO (GE): Se aplica un pulso de excitaciÃģn de menos de 90š y,
posteriormente,
se invierte el gradiente magnÃĐtico para obtener un eco.
El pulso de refase de 180š elimina las inhomogeneidades del campo magnÃĐtico externo,
pero no anula las inhomogeneidades debidas a los microcampos magnÃĐticos de los nÚcleos vecinos.
- En las secuencias SPIN â ECO,
al aplicarse un pulso de 180š,
la relajaciÃģn transversal depende Únicamente de las inhomogeneidades debidas a los microcampos magnÃĐticos de los nÚcleos vecinos.
En este caso se habla de relajaciÃģn T2 (Figura 2a).
- En las secuencias GRADIENTE â ECO,
al no aplicarse un pulso de 180š,
la relajaciÃģn transversal depende de las inhomogeneidades debidas a los microcampos magnÃĐticos de los nÚcleos vecinos y de las inhomogeneidades del campo magnÃĐtico externo.
En este caso se habla de relajaciÃģn T2* (Figura 2b).
Dentro de las secuencias eco de gradiente se incluyen,
entre otras muchas:
- Secuencia GE â T2* (Figura 3a).
- Secuencia SWI (Susceptibility Weighted Imaging) (Figura 3b).
En las imÃĄgenes por RM,
cuando en una zona existen sustancias con diferentes susceptibilidades magnÃĐticas,
el campo magnÃĐtico en esta regiÃģn serÃĄ inhomogÃĐneo.
Estas inhomogeneidades del campo magnÃĐtico se verÃĄn en la imagen final como un VACÃO DE SEÃAL.
Sin embargo,
como la mayor parte de los tejidos del cuerpo humano poseen una susceptibilidad magnÃĐtica parecida,
estas inhomogeneidades son despreciables.
Tanto la secuencia GE â T2* como la secuencia SWI potencian la diferencia de susceptibilidad magnÃĐtica entre los diferentes tejidos,
por lo que son Útiles en la detecciÃģn de:
- Sangre.
- Calcio.
- Hierro.
- Aire.
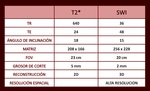
De todos los parÃĄmetros que se tienen en cuenta a la hora de planificar estas secuencias (Tabla 1),
parece ser que el TE es el que mÃĄs influye sobre el efecto de susceptibilidad magnÃĐtica.
Concretamente,
cuanto mayor es el TE,
mayor es el efecto de susceptibilidad magnÃĐtica y mÃĄs evidente es la pÃĐrdida de seÃąal en las imÃĄgenes.
SegÚn esto,
se deduce que la secuencia SWI es mucho mÃĄs sensible que la secuencia GE â T2* convencional para la detecciÃģn de lesiones.
Entre las principales aplicaciones clÃnicas de estas dos secuencias se incluyen el estudio y caracterizaciÃģn de:
- Hemorragia cerebral.
- Microsangrados cerebrales.
- Malformaciones vasculares.
- Tumores cerebrales (arquitectura interna del tumor,
sangrado intratumoral,âĶ).
- Enfermedades neurodegenerativas (Enfermedad de Alzheimer,
enfermedad de Parkinson y enfermedad de Huntington).
- Otras: LesiÃģn axonal difusa,
calcificaciones cerebrales,
siderosis superficial,âĶ
MICROSANGRADOS CEREBRALES
Los microsangrados cerebrales son pequeÃąos depÃģsitos crÃģnicos de hemosiderina de localizaciÃģn perivascular.
Tienen una prevalencia del 5 â 6 % en las personas mayores de 60 aÃąos y son mÃĄs frecuentes en el sexo masculino.
El creciente uso de la RM en la prÃĄctica clÃnica,
asà como el desarrollo exponencial que ha sufrido esta tÃĐcnica en los Últimos aÃąos,
han contribuido a que cada vez sea mÃĄs frecuente la detecciÃģn de estas lesiones.
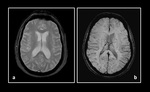
Los principales hallazgos radiolÃģgicos que caracterizan a los microsangrados cerebrales en las imÃĄgenes de RM son (Figura 4):
- TamaÃąo âĪ 5 mm.
- Forma redondeada u ovalada.
- Al menos la mitad de la lesiÃģn estÃĄ rodeada de parÃĐnquima cerebral.
- Hipointensidad de seÃąal en secuencias GE â T2* y SWI.
- Ausencia de hiperintensidad de seÃąal en secuencias SE â T1 y SE â T2.
- âEfecto bloomingâ (se trata de una ampliaciÃģn del ÃĄrea real del depÃģsito de hemosiderina y se debe a la magnificaciÃģn del artefacto de susceptibilidad magnÃĐtica en las secuencias GE â T2* y SWI).
Las principales patologÃas que pueden dar lugar a la apariciÃģn de microsangrados cerebrales son:
- AngiopatÃa cerebral amiloidÃģtica.
- AngiopatÃa cerebral hipertensiva.
- ArteriopatÃa cerebral autosÃģmica dominante con infartos subcorticales y leucoencefalopatÃa (CADASIL).
- Vasculitis cerebrales.
- Otras: Enfermedad de Binswanger,
sÃndrome de Parry â Romberg,âĶ
De entre todas estas,
la angiopatÃa cerebral amiloidÃģtica y la angiopatÃa cerebral hipertensiva son las causas mÃĄs frecuentes de microsangrados cerebrales.
Es importante saber que la distribuciÃģn topogrÃĄfica de los microsangrados cerebrales orienta,
en la mayorÃa de los casos,
hacia su etiologÃa.
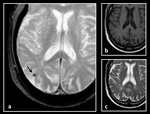
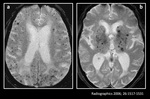
Mientras que en la angiopatÃa cerebral amiloidÃģtica (enfermedad debida al depÃģsito de la proteÃna Îē â amiloide en las capas media y adventicia de los vasos cerebrales de pequeÃąo y mediano tamaÃąo) los microsangrados cerebrales suelen afectar a la regiÃģn cÃģrtico â subcortical de ambos hemisferios cerebrales (Figura 5a),
en la angiopatÃa cerebral hipertensiva estas lesiones se localizan mÃĄs frecuentemente en ganglios basales,
tÃĄlamo,
troncoencÃĐfalo y cerebelo (Figura 5b y 6).
Cuando en un estudio de RM nos encontramos con pequeÃąas lesiones que se comportan como hipointensas en las secuencias eco de gradiente,
ademÃĄs de pensar en microsangrados cerebrales,
debemos tener en cuenta otras entidades con las que hay que hacer el diagnÃģstico diferencial:
1) Calcificaciones cerebrales: Las calcificaciones cerebrales pueden ser de 2 tipos:
a) FisiolÃģgicas:
- Plexos coroideos.
- GlÃĄndula pineal.
- HabÃĐnula.
- Ganglios de la base (globos pÃĄlidos).
- Hoz del cerebro,
tentorio.
b) PatolÃģgicas:
- Calcificaciones vasculares.
- Tumores (oligodendroglioma,
meningioma,
teratoma,âĶ).
- Enfermedades infecciosas (toxoplasmosis,
cisticercosis,
infecciÃģn por CMV,âĶ).
- Enfermedades metabÃģlicas (hipoparatiroidismo,âĶ).
En teorÃa,
el calcio debe aparecer en las imÃĄgenes de RM como una disminuciÃģn o ausencia de seÃąal en todas las secuencias,
como consecuencia de la ausencia de protones mÃģviles en el interior de las calcificaciones.
Sin embargo,
la experiencia nos demuestra que,
dependiendo del tipo de secuencia,
las calcificaciones tienen un comportamiento diferente:
- Secuencias GE: Hipointensas.
- Secuencias SE (T1 y T2): Variable (isointensas,
hipointensas o hiperintensas).
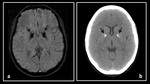
Debido a estas caracterÃsticas inespecÃficas,
la RM no permite confirmar o excluir con seguridad la presencia de calcificaciones.
Por ello,
la TC es la tÃĐcnica de elecciÃģn para el estudio de lesiones calcificadas (Figura 7).
2) LesiÃģn axonal difusa: Se trata de una lesiÃģn cerebral traumÃĄtica que cursa con rotura axonal y formaciÃģn de pequeÃąas hemorragias,
la cual se produce como consecuencia de las fuerzas de aceleraciÃģn â desaceleraciÃģn que sufre el encÃĐfalo tras un TCE.
Esta entidad suele afectar de forma tÃpica a la zona de uniÃģn sustancia gris â sustancia blanca (sobre todo de los lÃģbulos frontales y temporales),
al cuerpo calloso (esplenio) y al troncoencÃĐfalo.
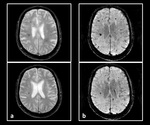
Para distinguir los microsangrados cerebrales de una lesiÃģn axonal difusa podemos valernos de tres herramientas:
- Historia clÃnica: En el caso de la lesiÃģn axonal difusa existe el antecedente de un traumatismo crÃĄneo â encefÃĄlico.
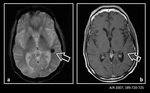
- TC: Inicialmente suele ser normal en la mayorÃa de los casos,
aunque en ocasiones tambiÃĐn pueden verse pequeÃąos focos hipodensos (que se corresponden con zonas de edema) o pequeÃąos focos hiperdensos (que se corresponden con ÃĄreas de hemorragia) (Figura 8a).
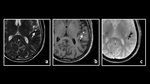
- RM: Lo mÃĄs caracterÃstico es encontrarnos con pequeÃąos focos que se comportan como hiperintensos en las secuencias SE â T2 y FLAIR (Figura 8b,
8c y 8d).
3) Cavernomas: Los cavernomas constituyen un tipo de malformaciÃģn vascular de bajo flujo caracterizada por la presencia de espacios vasculares dilatados sin parÃĐnquima cerebral entre ellos.
Estos espacios vasculares estÃĄn tapizados por un fino y dÃĐbil epitelio que predispone al sangrado,
por lo que los cavernomas suelen contener restos hemÃĄticos en diferentes fases de evoluciÃģn.
En el 80 % de los casos tienen localizaciÃģn supratentorial,
sobre todo a nivel de los lÃģbulos frontales y temporales.
Se diferencian de los microsangrados cerebrales porque los cavernomas presentan una zona central de aspecto heterogÃĐneo tanto en T1 como en T2 (debida a trombosis,
hemorragia,
fibrosis y calcificaciÃģn),
y una zona perifÃĐrica que se comporta como hipointensa en las secuencias potenciadas en T2 (debida a la formaciÃģn de un anillo de hemosiderina) (Figura 9).
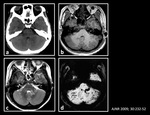
4) MetÃĄstasis cerebrales: El melanoma,
el carcinoma de cÃĐlulas renales y el carcinoma broncogÃĐnico son tumores que pueden dar lugar a micrometÃĄstasis hemorrÃĄgicas.
Este tipo de metÃĄstasis pueden diferenciarse de los microsangrados cerebrales porque de forma tÃpica son hiperintensas en las secuencias potenciadas en T1,
lo que se debe a la tendencia de estos tumores a sangrar y,
en el caso del melanoma,
a la presencia de melanina,
y porque realzan tras la administraciÃģn de contraste (Figura 10).
5) DepÃģsitos de hierro: Es bien sabido que los depÃģsitos cerebrales de hierro aumentan con la edad,
principalmente a nivel de los ganglios basales,
y que los niveles anormales de hierro en el SNC se asocian a varias enfermedades neurodegenerativas (enfermedad de Parkinson,
enfermedad de Huntington,
enfermedad de Alzheimer,
esclerosis mÚltiple y esclerosis lateral amiotrÃģfica).