La Microlitiasis Alveolar Pulmonar,
en adelante MAP,
se trata de una enfermedad crónica infrecuente caracterizada por la presencia de múltiples cálculos formados por calcio y fósforo,
(también llamados calcosferitos,
calcosferas o microlitos),
en el alveolo pulmonar.
ETIOLOGÍA:
Se trata de una patología hereditaria,
autosómica recesiva.
Estudios recientes han confirmado que su causa radica en la mutación del gen SCL34A2,
ubicado en el cromosoma 4,
el cual codifica la proteína que es el transportador de fosfato dependiente de sodio (Fig.
1).
Este transportador de fosfato se encuentra sobre todo en los alveolos tipo II que producen el surfactante pulmonar.
Del surfactante degradado por los macrófagos se producen iones de fósforo que el transportador de fosfato debe eliminar del espacio alveolar.
La proteina resultante del gen mutado no es capaz de eliminar dichos fosfatos y esto conlleva la formación de los microlitos.
DATOS EPIDEMIOLÓGICOS Y CLÍNICA:
Los síntomas comienzan en la 3ª-4ª década,
siendo 35 años la media de edad al diagnóstico.
No se ha constatado predilección por ningún sexo,
siendo igual de prevalente en hombres que en mujeres.
Más de la mitad de los pacientes se encuentran asintomáticos al diagnóstico,
ya que la enfermedad puede ser silente durante un largo periodo de tiempo.
La mayoría de las veces se diagnostica en exámenes rutinarios,
aunque puede ser durante la investigación por la historia familiar.
La ausencia o escasez de síntomas contrasta con las extensas alteraciones visualizadas en las pruebas de imagen.
A la presentación clínica normalmente existe disnea,
tos seca,
patrón restrictivo y disminución de la capacidad de difusión.
La insufienciencia respiratoria finalmente progresa a fibrosis pulmonar y cor pulmonale.
La muerte con frecuencia es debida a la combinación de la disfunción pulmonar y cardiaca consecuente.
Los dos casos expuestos en el presente trabajo se trata de dos hermanas de 22 y 20 años,
diagnosticadas de MAP en otro centro a la edad de 19 y 17 años respectivamente.
Las dos estaban asintómaticas al diagnóstico.
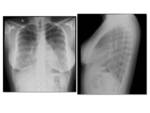
En el caso de la hermana mayor (caso 1) fue un hallazgo en la radiografía de tórax realizada en el contexto de una revisión médica.
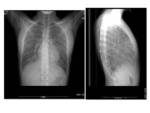
La otra hermana (caso 2) se diagnosticó en base al antecedente familiar.
En la actualidad la dos continuan asintomáticas.
Las pruebas de función pulmonar muestran un patrón restrictivo y disminución de la capacidad de difusión (Figs.
2 y 3).
DIAGNÓSTICO:
Los hallazgos por imagen mediante radiología simple y TC junto con las pruebas pulmonares funcionales y la información extraída de la historia familiar son normalmente suficientes para el diagnóstico.
Sin embargo,
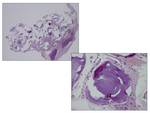
la biopsia pulmonar se realiza con frecuencia para la confirmación diagnóstica,
sobre todo cuando se trata del primer caso conocido de la familia,
como ocurrió con la paciente del caso 1 (Fig.
4).
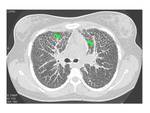
HALLAZGOS POR IMAGEN:
Los ilustramos mediante imágenes de Radiografía simple y TCMC de nuestros dos casos.
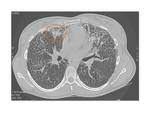
Radiografía de tórax: La MAP se caracteriza por la presencia de múltiples micronódulos calcificados de distribución bilateral difusa que forman un patrón clásicamente llamado “en tormenta de arena” (Figs.
5 y 6).
Con frecuencia existe una predilección por los campos pulmonares inferiores.
Es común el borramiento del borde mediastínico y diafragmático.
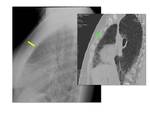
El signo de “la pleura negra” consiste en la visualización de una línea radiolúcida entre las costillas y el parénquima pulmonar y es debido probablemente a la presencia de quistes subpleurales objetivados mediante TC (Fig.
7).
Otro hallazgo típico son las pequeñas bullas apicales y el posible neumotórax asociado.
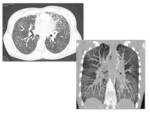
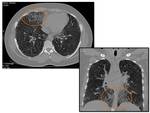
TC multicorte:
En la actualidad la TC multicorte permite una adquisición fina y algoritmos de reconstrucción con alta resolución espacial.
Esto posibilita la detección de cambios mínimos del parénquima que no son adecuadamente evaluados mediante las radiográfias.
Los hallazgos de la MAP en la TC multicorte son los siguientes:
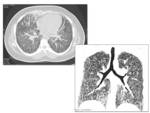
Múltiples micronódulos de densidad calcio: de bordes bien definidos,
distribución difusa y bilateral en el parénquima pulmonar,
con predominio de segmentos posteriores de los lóbulos inferiores y segmentos anteriores del los lóbulos superiores.
La zona medial del pulmón suele estar más afectada que la lateral.
(Figs.
8 y 9).
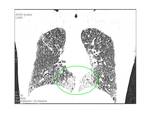
Consolidaciones densas o áreas confluentes de calcificación: Se forman cuando confluyen los micromódulos.
Frecuentemente en regiones póstero-inferiores,
paracardiacas y lóbulos superiores.
Pueden tener broncograma aéreo.
(Fig.
10).
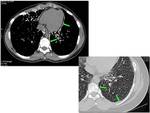
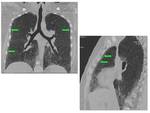
Micronodulación,
engrosamiento y calcificación de los septos interlobulares: es un hallazgo frecuente debido probablemente a la acumulación de los microlitos en la periferia de los lóbulos pulmonares secundarios ya que,
según algunos autores,
no hay confirmación histopatológica de calcificación del septo interlobular o afectación intersticial en las fases iniciales de la enfermedad.
(Fig.
11). Los micronódulos también pueden tener una localización peribronco-vascular (Fig.
12) y subpleural (Fig.
13).
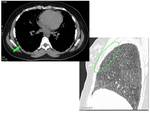
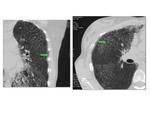
Calcificaciones lineales subpleurales: es frecuente pero controvertido en la literatura.
Algunos autores las describen como calcificaciones pleurales y otros aseguran que no hay confirmación histopatológica y que probablemente la mejor explicación sea que la acumulación de los microlitos en la periferia de los lóbulos pulmonares secundarios demarcan la superficie pleural, produciendo el aspecto de calcificaciones pseudo-pleurales (Fig.
14).
Densidad en vidrio deslustrado: Cuando los micronódulos son < 1 mm producen aumento de densidad del parénquima pulmonar en vidrio deslustrado (Fig 15).
Con una ventana adecuada se pueden identificar con frecuencia discretas calcificaciones.
Atenuación en patrón en empedrado: Se visualiza cuando coexiste el patrón en vidrio deslustrado y el engrosamiento de los septos interlobulares de densidad calcio por el depósito de los microlitos en la periferia del lóbulo pulmonar secundario.
Algunos autores aseguran que este patrón (con densidad calcio de los septos que se puede visualizar con una ventana apropiada) es muy específico de la MAP ya que no se ha descrito en ninguna otra enfermedad,
además de que lo diferencia de la proteinosis alveolar.
(Fig.
16).
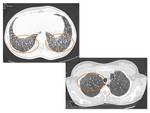
Quistes subpleurales y bullas apicales: Es otro hallazgo frecuente.
Numerosos pequeños quistes < 10 mm,
de localización subpleural,
que probablemente explican el signo de la pleura negra visualizada en las radiográfias,
al formar una banda radiotrasnparente periférica entre las costillas y el parénquima calcificado (Figs.
17 y 18). Las bullas apicales presentan una tamaño >10 mm.
DIAGNÓSTICO DIFERENCIAL POR LOS HALLAZGOS DE IMAGEN:
La MAP debe considerarse en el diagnóstico diferencial de las consolidaciones densas junto con: toxicidad pulmonar por amiodarona,
calcificaciones pulmonares metastásicas,
silicoproteinosis,
talcosis y amiloidosis.
Y en el diagnóstico diferencial de las calcificaciones nodulares en la TBC miliar,
osteosarcoma metastásico,
amiloidosis y silicoproteinosis.
Los hallazgos de las pruebas de imagen y las características clínicas siempre se deben correlacionar.
TRATAMIENTO:
En la actualidad no existe tratamiento efectivo para la MAP con excepción del transplante pulmonar,
que debe ser considerado en casos de fallo respiratorio severo o cor pulmonale.
Los autores que han descubierto la mutación del gen causante de la enfermedad sugieren que la diana del tratamiento debería ser el metabolismo del fosfato más que el del calcio.