Introducción
La afectación renal en las autopsias de los pacientes con linfoma se estima en el 30-60% sin embargo,
en los estudios de extensión mediante Tomografía computarizada de estos pacientes solamente se describen en el 5-8% de los casos.
Esto puede ser debido a la menor sensibilidad de los equipos antiguos para el diagnóstico de lesiones de pequeño tamaño,
a las pocas biopsias necesarias realizadas para su confirmación o a la escasa manifestación clínica que permita sospechar la afectación renal.
Descrito desde 1878 por Sutton y Turner el linfoma renal se suele diagnosticar en el contexto de la enfermedad sistémica consecuencia de su extensión hematógena o por contigüidad retroperitoneal.
La afectación extraganglionar también es más frecuente en los casos de enfermedad recurrente.
El genitourinario es el sistema extraganglionar más frecuente afectado por el linfoma tras el hematológico y el reticuloendotelial; los testículos en primer lugar y los riñones en segundo.
El linfoma es el tumor testicular más frecuente en varones mayores de 60 años.
El linfoma renal primario
El linfoma renal primario es infrecuente o inexistente,
representando menos del 1% de los linfomas extraganglionares.
Por definición el término de linfoma renal primario se aplica a los pacientes con enfermedad localizada en el riñón sin signos de patología en otro órgano,
es decir se debe excluir la posibilidad de linfoma extrarrenal.
Unilateral,
muy raros bilaterales,
suele afectar a adultos de 60 años,
(aunque se han descrito casos infantiles) y ligeramente más frecuente en varones.
Muchos de los casos publicados son cuestionados por un estudio incompleto de extensión extrarrenal o por la ausencia autopsias que lo confirmen.
También existe la controversia sobre si se trata de una enfermedad primaria o realmente de una manifestación inicial de una rápida progresión de la enfermedad sistémica,
de hecho existen casos intervenidos de linfoma renal primario que al cabo de los meses se presentan como enfermedad adenopática diseminada.
Su origen es incierto debido a la ausencia de tejido linfático renal en personas sanas.
Podría originarse desde la cápsula renal rica en tejido linfático o a partir de la infiltración linfocitaria intraparenquimatosa consecuencia de enfermedades inflamatorias crónicas como también ocurre en los linfomas salivales,
tiroideos o gástricos.
También se asocia a otras enfermedades como el síndrome de Sjögren,
lupus eritematoso sistémico o el virus de Epstein-Barr.
Clínica de los pacientes con linfoma renal
La afectación renal se sospecha clínicamente sólo en el 14% de los pacientes con linfoma.
La mayoría de las veces el diagnóstico de la afectación renal ocurre de forma ocasional en el contexto de los estudios de imagen de extensión del linfoma diagnosticado previamente.
Normalmente ocurre en las fases avanzadas de la enfermedad y de forma silente.
No existen diferencias significativas en cuanto a la edad y al sexo de los enfermos.
Los hallazgos clínicos y analíticos que hacen sospechar la afectación renal en los pacientes con linfoma son el dolor o la palpación de masa en el flanco,
hipertensión,
oligoanuria,
hematuria macroscópica o edema generalizado.
Aunque los casos con afectación renal inicial no implican un mal pronóstico,
no ocurre lo mismo cuando el linfoma recidiva en el riñón,
con mayor tasa de mortalidad. Hay casos de insuficiencia renal aguda aunque son infrecuentes, siendo la causa del fallecimiento en el 2.5% de los pacientes.
Anatomía Patológica: mecanismos de crecimiento.
En general,
los linfomas no Hodgkin (LNH) tienen peor pronóstico que los Hodgkin (LH).
A diferencia del LH,
que habitualmente presenta una extensión ganglionar por contigüidad,
el LNH no suele presentar un aspecto localizado en el momento del diagnóstico,
con frecuente extensión extranodal.
En relación con el tipo: el 15% son tipo LH y el 85% LNH; y desde el inicio de la enfermedad en el 1% de los casos de LH y en el 50% de los LNH.
La mayoría de los LNH son de tipo de células B.
Con predominio de las formas difusas frente a las nodulares,
de medio o alto grado,
incluyendo los linfomas de Burkitt (especialmente frecuentes en la edad infantil).
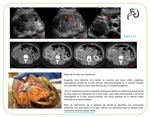
Macroscópicamente las masas linfomatosas renales tienen aspecto carnoso,
amarillo,
gris o marrón,
desde1 cmhasta los 15-20 cmde tamaño.
La vía de llegada de los linfocitos al riñón puede ser: hematógena o por contigüidad desde los ganglios linfáticos del seno,
perirrenales o capsulares.
Con independencia de las formas,
inicialmente existe aumento general del volumen renal,
con proliferación celular intersticial que utilizan a las nefronas,
túbulos colectores y vasos como soporte.
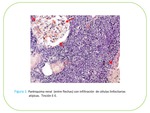
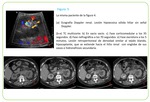
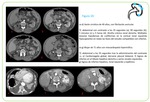
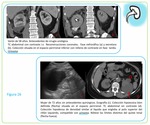
Cuando el tejido linfomatoso crece se comprime y destruye el parénquima subyacente.
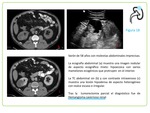
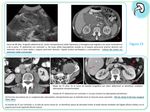
Fig. 1 A veces el crecimiento no suele ser tan uniforme y se forman grandes masas que sobrepasan el contorno renal y distorsionan el sistema colector,
semejando neoplasias renales primarias. La variable proporción y la distribución conducen a los distintos tipos de presentación radiológica.
El seno renal y el sistema pielocalicial no suelen verse infiltrados,
únicamente existe hidronefrosis debido al efecto compresivo de la enfermedad retroperitoneal.
Técnicas de imagen
- Urografía intravenosa (UIV)
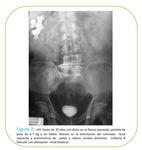
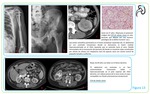
Los hallazgos más frecuentes son el aumento difuso del volumen renal o la sensación de masa con deformidad focal sobre el sistema colector.
Igualmente aporta información sobre la afectación hidronefrótica.
Fig. 2
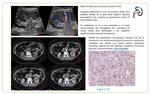
Dado que la ecografía suele ser el primer método de estudio de los pacientes con insuficiencia renal o dolor en el flanco,
es útil el reconocimiento de las sutiles anomalías producidas por el linfoma.
Igualmente representa un método diagnóstico alternativo en los pacientes que no pueden recibir contrastes yodados intravenosos así como guía para la biopsia percutánea.
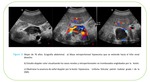
Normalmente las lesiones linfomatosas suelen ser sólidas,
hipoecoicas,
homogéneas con buena transmisión acústica posterior,
sin señal Doppler significativa Fig. 3.
Se describen cambios tras el tratamiento como hemorragias,
transformación quística y calcificaciones.
- Resonancia Magnética (RM)
Fundamentalmente indicada en los casos en los existe la contraindicación de la administración del contraste yodado.
Existen estudios que describen la misma capacidad diagnóstica dela RM que la TCMC (tomografía computarizada multicorte) en el linfoma renal.
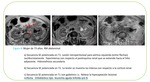
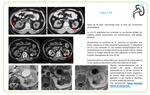
El aspecto en RM del linfoma Fig. 4 es el de una masa homogénea,
sin signos de necrosis, iso- hipointensa en las secuencias potenciadas en T1 e hipointensa o discretamente isointensa en T2 con respecto a la cortical renal.
Tras la administración del contraste intravenoso el tejido linfomatoso muestra menor realce que el resto del parénquima sano aunque algunas lesiones presentan realce progresivo en fases retardadas.
Estos hallazgos se deben a la naturaleza relativamente homogénea de las células linfomatosas con escaso contenido en vasos.
- Tomografía computarizada (TC)
Técnica tradicionalmente más sensible y eficiente en el diagnóstico radiológico de las masas renales incluyendo el linfoma y su estadificación.
No solamente estudia la lesión renal sino que valora la extensión hacia las estructuras anatómicas adyacentes (espacio perirrenal y retroperitoneo),
analiza detalladamente la vasculatura renal y permite el seguimiento y la respuesta al tratamiento de la enfermedad.
Invariablemente el estudio precisa de la administración de contraste intravenoso dinámico Table 1 .
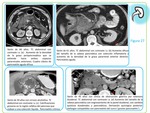
Aunque las fases del estudio pueden ser: arterial (o corticomedular), nefrográfica y excretora la mayoría de las veces se resumen en dos fases: corticomedular/nefrográfica (al cabo de los 90-120 segundos tras la administración del contraste) y excretora (al cabo de los 4 minutos).
La fase nefrográfica (venosa) es esencial en el diagnóstico de pequeñas lesiones nodulares que no deforman el contorno visceral y que pueden ser pasadas por alto si la médula no se encuentra contrastada como ocurre en las fases muy precoces.
El tejido linfomatoso presenta una densidad similar al tejido blando,
homogéneo,
iso-hiperdenso con respecto al parénquima sano en el estudio sin contraste intravenoso.
Tras su administración suele ser hipovascular,
con escaso realce.
Fig. 5
Infrecuentemente pueden tener un aspecto heterogéneo o quístico,
sobre todo con tratamiento quimioterápico indicativo de cierto grado de necrosis o cuando son de gran tamaño.
Extremadamente infrecuente la calcificación.
Fig. 6 A veces tras el tratamiento se produce la disminución del tamaño de las lesiones linfomatosas con retracción capsular secundaria.
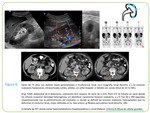
- Tomografía por emisión de positrones. (PET)
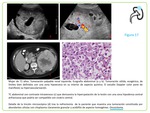
La PETes un método emergente en la estadificación y diagnóstico de recidiva del linfoma.
Debido a la hipercaptación funcional de la fluorodesoxiglucosa,
es un método más sensible y específico que las técnicas de imagen anatómicas convencionales.
La combinación de la PET y la TC aumenta poderosamente la especificidad de la prueba que une la actividad metabólica (no olvidemos que el trazador se acumula fisiológicamente en los riñones) junto con el detalle anatómico de la TC,
así se posibilita la detección temprana de focos de enfermedad adicionales y la diferenciación entre tumor viable,
necrosis o fibrosis.
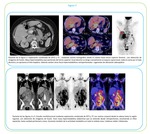
Fig. 7 Fig.
7
Aunque se enfatiza en la realización dela PET antes de la quimioterapia,
realmente la mayor indicación de la PET-TC es la valoración de la respuesta al tratamiento especialmente en los pacientes con masas residuales donde,
mediante técnicas radiológicas convencionales,
no es posible diferenciar la persistencia de tumor viable de la fibrosis residual.
Tampoco se enfatiza el uso de la PET como fin diagnóstico debido a la existencia de falsos positivos en patología inflamatoria (nefritis).
Por sí misma la hipercaptación tras la finalización del tratamiento es un factor de mal pronóstico independientemente de los hallazgos conla TC.
Igualmente la persistencia de PET positivos durante y tras la quimioterapia tiene una alta sensibilidad como predicción de recidiva; inversamente una PET negativa tras el tratamiento tiene una alta capacidad predictiva de supervivencia sin recaída.
Patrones de diseminación
En general el diagnóstico del linfoma renal no suele ser complicado al presentarse en general asociado con adenopatías retroperitoneales en el 73% de los casos y de forma bilateral en el 74%.
En 1962 Richmond et al.
describen clásicamente cuatro patrones de diseminación del linfoma renal (actualmente ampliados a cinco) que se correlacionan con su apariencia en TC: múltiples masas,
masa solitaria,
extensión por contigüidad retroperitoneal,
enfermedad perirrenal y afectación infiltrativa difusa.
Forma de presentación más frecuente en todas las edades (50-60% de los casos),
típicamente de forma bilateral.
Suelen ser masas de densidad similar a las partes blandas,
homogéneas,
entre 1 y5 cm de diámetro,
isodensas o levemente hiperdensas respecto al parénquima sano.
Tras la administración del contraste intravenoso existe mínimo realce,
con aspecto de masas hipodensas.
La mayoría asocian adenopatías retroperitoneales.
Fig. 8
El diagnóstico diferencial fundamental de las masas renales múltiples son las metástasis.
Table 2 Se describen en el 7-13% de las autopsias,
la mayoría de las veces se conoce el antecedente oncológico o se diagnostican incidentalmente al mismo tiempo que la neoplasia primaria,
sin ser necesaria su confirmación mediante biopsia percutánea.
Fig. 9
Las grandes series muestran que el cáncer de pulmón es la primera causa de enfermedad metastásica renal,
seguido del cáncer de mama,
gastrointestinal y del riñón contralateral.
Su aspecto suele ser el de pequeños tumores renales multifocales,
bilaterales en más del 50% de los casos,
de aspecto infiltrante,
hipodensos con realce inferior al resto del parénquima.
Otras entidades neoplásicas múltiples son las asociadas a la enfermedad de von Hippel-Lindau y la esclerosis tuberosa así como las leucemias agudas.
En relación con otros procesos no neoplásicos múltiples se deben de incluir las pielonefritis agudas focales,
los émbolos sépticos renales,
las infecciones fúngicas (habitualmente de pequeño tamaño en pacientes inmunodeprimidos que suelen asociar afectación esplénica y hepática),
los infartos renales Fig. 10 y los abscesos (estos dos últimos de origen embólico).
Probablemente la forma más infrecuente (1-20%) e inespecífica de crecimiento,
que simula al carcinoma de células renales (CCR),
a cualquier neoplasia hipovascular y a las metástasis.
Se describen masas entre 1 y15 cm de diámetro.
A diferencia del realce arterial típico del CCR las masas linfomatosas típicamente son hipovasculares (no obstante una masa linfomatosa única puede presentar mayor realce de lo esperado debido a su vascularización cortical directa) Table 3 y ecográficamente son menos ecogénicos que el CCR.
Fig. 11 Fig.
11
El CCR clásico tiene un aspecto más heterogéneo con imágenes quísticas intratumorales,
crecimiento expansivo,
con realce intenso precoz de predominio periférico y con frecuente invasión de la vasculatura renal que prácticamente nunca ocurre con el linfoma renal. Fig. 12 y Fig. 13 En los escasos estudios realizados sobre la PET y el diagnóstico diferencial con el linfoma renal Xiang-Hua Ye et al.
demuestran en 24 pacientes que la captación es mayor en los casos de linfoma que en el CCR de células claras convencional mientras que es similar que el resto de neoplasias renales y del sistema colector,
por tanto de escasa especificidad diagnóstica.
Más interesante resulta el diagnóstico diferencial de una masa renal hipovascularizada que,
además del linfoma debe incluir al leiomioma hemangioma y ciertos carcinomas de células renales menos frecuentes. En relación con éstos últimos el más significativo es la variedad papilar.
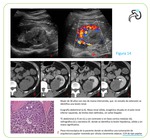
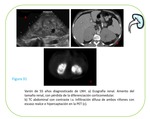
El CCR papilar Fig. 14 es el segundo subtipo histológico más frecuente de CCR (10-15%).
Típicamente se muestra como una masa hipovascular y homogénea en la TC.
Además del menor realce también se diferencia del CCR de células claras en la mayor tendencia a la multifocalidad y bilateralidad.
En casos raros se describe contenido de densidad similar a la grasa en su interior.
El aspecto en RM suele ser hipointenso en las secuencias potenciadas en T2,
debido a su componente papilar (hallazgo diferencial fundamental con el CCR de células claras,
la mayoría de las veces hiperintenso).
Las variedades cromófoba y del conducto colector del CCR también se incluyen en el diagnóstico diferencial debido a la hipocaptación del contraste: el carcinoma cromófobo Fig. 15 suele ser un tumor grande,
homogéneo,
sin necrosis o hemorragia y el carcinoma del conducto colector puede ser sólido,
o sólido complejo o quístico,
se localiza en la porción central del riñón y se presenta como masa palpable o con hematuria macroscópica.
El carcinoma mucinoso tubular de células lisas Fig. 16 es una neoplasia muy infrecuente derivada del asa de Henle,
que afecta predominantemente a mujeres asintomáticas de edad media,
con pronóstico favorable.
Los hallazgos en RM son similares al tumor papilar (isointenso a la cortical en T1,
iso o discretamente hiperintenso en T2 con hipocaptación de gadolinio).
El carcinoma medular renal es muy infrecuente,
de mal pronóstico,
prácticamente siempre asociado a pacientes con anemia drepanocítica.
Se presenta como una masa mal definida asociada a ectasia calicial que,
a diferencia del linfoma,
es heterogénea,
con zonas de hemorragia y necrosis,
hipovascular tras la administración del contraste.
El oncocitoma Fig. 17 es la neoplasia renal benigna más frecuentemente intervenida debido a que es imposible diferenciarlo preoperatoriamente del CCR mediante técnicas de imagen,
mostrándose como una masa renal de márgenes bien definidos con realce homogéneo sin presencia de necrosis o hemorragia y,
a veces,
con una cicatriz central que puede simular la necrosis del CCR.
El hemangioma renal se localiza en las pirámides renales,
se clasifican como capilares o cavernososos,
de pequeño tamaño (inferiores a1 cm),
pueden producir hematuria macroscópica.
Los métodos de imagen muestran una masa sin realce significativo.
Fig. 18
El reninoma renal es un tumor extraglomerular,
dos veces más frecuente en mujeres con hipertensión y niveles elevados de renina.
Ecográficamente pueden ser hipo o hiperecogénicos,
hiporrealzantes tras la administración del contraste en la TC.
El hemangiopericitoma es un tumor renal raro,
con potencial maligno que suele cursar con hipoglucemias debido a la producción de insulina.
En relación con las metástasis renales únicas,
en los pacientes con neoplasia conocida,
la coexistencia de una masa renal es cuatro veces más frecuente que una lesión renal primaria.
Las metástasis aisladas pueden simular un CCR,
sin embargo éste último suele presentar mayor grado de necrosis y límites mejor definidos.
Fig. 19
Otras masas focales no neoplásicas Fig. 20 incluyen la pielonefritis aguda focal,
pielonefritis xantogranulomatosa,
malacoplaquia parenquimatosa,
los abscesos y los infartos renales.
En los procesos inflamatorios el contexto del paciente es distinto y en los estudios de imagen suele afectarse la grasa perirrenal.
En los procesos isquémicos renales no tienen efecto expansivo ni se deforma el contorno visceral.
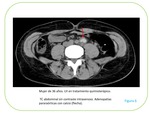
- Extensión por contigüidad retroperitoneal:
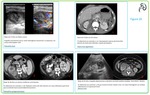
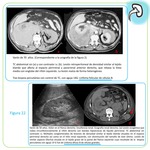
Segunda forma de presentación más común (11-25%). Se suele presentar como una masa retroperitoneal voluminosa hipodensa e hipocaptante que infiltra al parénquima renal a través de la cápsula o del hilio.
Típicamente se identifican los vasos en el interior de la masa,
habitualmente no trombosados,
e hidronefrosis.
Fig 3 y 5 Obligatoriamente coexisten adenopatías retroperitoneales cuyo aspecto en TC y RM es similar al de la masa renal.
Clínicamente muchos de estos pacientes están inmunodeprimidos.
El diagnóstico diferencial incluye el conjunto de patologías que cursan con adenopatías retroperitoneales Table 4 ,
especialmente otros tumores con la misma extensión (metástasis de adenocarcinoma de próstata,
de colon o de origen desconocido).
Las adenopatías metastásicas por adenocarcinoma suelen tener un efecto compresivo superior sobre la vasculatura renal mientras que las linfomatosas rodean a los vasos sin producir obstrucción.
Fig. 21
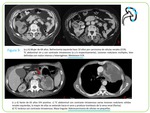
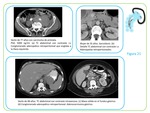
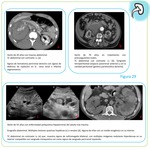
Aunque la extensión perirrenal desde el retroperitoneo o desde el parénquima renal vía transcapsular no es infrecuente,
si que lo es su presentación aislada, probablemente la más atípica y prácticamente patognomónica.
Consiste en la presencia de una placa o corteza de tejido blando que rodea total o parcialmente al riñón sin signos de invasión ni de deformidad.
Normalmente el tejido es iso-hiperdenso con respecto al parénquima renal sin contraste i.v.
e hipodenso tras su administración.
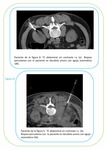
En casos menos llamativos los hallazgos se limitan al discreto engrosamiento de la fascia de Gerota en forma de placas o de nódulos. Fig. 22 y Fig. 23
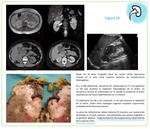
En el diagnóstico diferencial Table 5 de otros procesos neoplásicos que pueden presentar un aspecto similar se incluyen: la extensión local neoplasias de las vísceras retroperitoneales (CCR,
tumores originarios de la cápsula renal Fig. 24 ,
glándula adrenal y páncreas fundamentalmente),
neoplasias primarias retroperitoneales (sobre todo el liposarcoma) y las metástasis del cáncer de pulmón,
de mama o el melanoma en el espacio perirrenal.
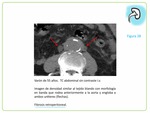
Fig. 25
Otros procesos inflamatorios pueden simular esta afectación (urinomas,
pancreatitis o fibrosis retroperitoneal).
Los urinomas Fig.
Fig. 26 son colecciones irregulares perirrenales de densidad líquida habitualmente asociados a hidronefrosis u obstrucción ureteral,
con extravasación del contraste intravenoso.
En las pancreatitis Fig. 27 el proceso inflamatorio puede extenderse caudalmente hacia el espacio pararrenal con engrosamiento de la fascia de Gerota,
así como al espacio perirrenal; obviamente el contexto clínico del paciente es distinto.
En la fibrosis retroperitoneal Fig. 28 el tejido puede englobar lateralmente a la pelvis renal,
al espacio perirrenal o al riñón.
Enla TC sin contraste las placas de fibrosis suelen ser isodensas con respecto a los músculos vecinos con realce variable tras la administración del contraste i.v.
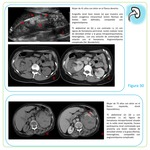
Igualmente hay que incluir las hemorragias del espacio perirrenal Fig. 29 y Fig. 30 bien postraumáticas o espontáneas normalmente asociadas a otras lesiones renales como el CCR o angiomiolipomas o en las alteraciones de la coagulación.
También pueden simular procesos que afectan a la periferia renal la necrosis cortical aguda,
que presenta en la TC con contraste un anillo hipodenso que rodea total o parcialmente al riñón con realce normal de la medular,
o la nefroblastomatosis,
con el riñón agrandado de contornos lobulados con múltiples nódulos hipodensos de diversos tamaños en la periferia.
Igualmente existen artefactos en este espacio producidos por la protrusión del diafragma hacia la grasa perirrenal,
hipertrofia de una de las cruras diafragmáticas o por la respiración del paciente.
Descrito en el 20% de los casos,
la mayoría de las veces bilateral.
El crecimiento tumoral se produce en el intersticio renal,
siendo el único hallazgo morfológico la nefromegalia difusa con preservación de la morfología. Fig. 31 El diagnóstico suele ser dificultoso siendo la clave de sospecha el aumento del tamaño visceral.
Muchas veces el diagnóstico suele ser retrospectivo cuando los riñones disminuyen su tamaño con el tratamiento quimioterápico.
Este aspecto es más común en los linfomas tipo Burkitt (bien diseminado o primario renal) y con escasa respuesta al tratamiento quimioterápico.
Ecográficamente los hallazgos son sutiles: aumento del tamaño renal,
de aspecto globuloso de ecogenicidad heterogénea,
con pérdida de la ecogenicidad normal del seno.
En la TC tras la administración del contraste se identifica escaso realce de forma heterogénea y pérdida de la diferenciación cortical y medular.
En la PET existe una marcada captación.
Es posible la infiltración y destrucción completa del parénquima renal,
con aspecto de riñón no funcionante.
Mediante RM persiste la ausencia de diferenciación corticomedular tras la administración de gadolinio intravenoso a diferencia de otros procesos que cursan con aumento de los niveles de creatinina.
No se suele manifestar clínicamente aunque si ambos riñones presentan infiltración difusa es posible el fallo renal agudo con necesidad de tratamiento médico.
En relación con el diagnóstico diferencial Table 6 el aumento del tamaño renal asociado al tratamiento quimioterápico de los pacientes con linfoma sugiere bien la lisis tumoral de la enfermedad sistémica o bien la presencia de una infección,
más que la infiltración linfomatosa difusa renal.
Linfoma en pacientes inmunodeprimidos
A diferencia del resto,
los linfomas ligados a inmunodeficiencias suelen tener origen extraganglionar.
La afectación renal en este tipo de pacientes es infrecuente aunque se han descrito casos fundamentalmente en pacientes trasplantados o VIH positivos.
El patrón de afectación es similar a los descritos en los inmunocompetentes.
Biopsia renal
Como se ha descrito anteriormente los pacientes con linfoma renal prácticamente siempre presentan enfermedad sistémica,
si los hallazgos de imagen se corresponden con alguno de los patrones descritos,
la diferenciación del CCR no suele ser complicada.
En esta situación el tratamiento quimioterápico se podrá instaurar esperando también la misma respuesta en la enfermedad renal que en la sistémica.
En raras ocasiones el linfoma renal se manifiesta como una masa renal solitaria o con hallazgos de imagen inusuales,
siendo complicada la diferenciación del CCR.
En estos casos,
con el fin de evitar nefrectomías innecesarias,
se indica la biopsia percutánea o quirúrgica.
El procedimiento se realiza bien mediante ecografía o TC,
a elección del radiólogo,
con aguja coaxial 17G o similares.
La información aportada por la biopsia (capacidad de diferenciación entre linfomas B o T) es superior al análisis flujométrico y citológico que aporta la punción espirativa.
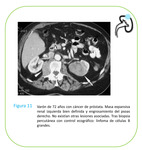
Fig. 32
En general,
las masas renales sólidas tienen mayor probabilidad de malignidad que las quísticas y su manejo conlleva una actitud más agresiva.
Ante una masa sólida mayor de 1 centímetro diagnosticada accidentalmente en la población general hay que descartar mediante la clínica y otras pruebas radiológicas la posibilidad de patología inflamatoria,
vascular o neoplásica tipo angiomiolipoma; en el resto de los casos se recomienda el estudio histológico bien por biopsia o quirúrgicamente.
Si la lesión es menor de1 cm la mejor opción es el seguimiento periódico cada 3-6 meses.
En los pacientes con menor expectativa de vida el diámetro límite de la lesión aumenta hasta los3 cm.
Bibliografía
BA.
Urban y EK.
Fishman.
Renal lymphoma: CT patterns with emphasis on helical CT.
Radiographics 2000;20:197-212.
S.
Sheth,
S. Ali y E. Fishman.
Imaging of renal lymphoma: patterns of disease with pathologic correlation.
Radiographics 2006;26:1151-1168.
J.
Zhang et al.
Masses and pseudomasses of the kidney: imaging spectrum on MR.
J Comput Assist Tomogr 2004;28(5):588-95.
AG.
Thomas et al.
Extranodal lymphoma from head to toe: part 2,
the trunk and extremities.
AJR Am J Roentgenol 2011 Aug;197(2):357-64.
SR.
Sheeran y SK. Sussman.
Renal lymphoma: spectrum of CT findings and potential mimics.
AJR Am J Roentgenol 1998;171:1067-72.
MR.
Sun e I.
Pedrosa.
Magnetic resonance imaging of renal masses.Semin Ultrasound CTMR 2009 Aug;30(4):326-51.
F.
Ferrozzi ,
D.
Bova y F.
Campodonico F.
Computed tomography of renal metastases.
Semin Ultrasound CTMR 1997;18(2):115-21.
RM.
Paspulati y S.
Bhatt.
Sonography in benign and malignant renal masses.
Radiol Clin North Am.
2006;44(6):787-803.
NB.
Chepuri,
PJ.
Strouse y GA. Yanik.
CT of renal lymphoma in children.
AJR Am J Roentgenol 2003;180(2):429-31.
M.
Anis y A.
Irshad.
Imaging of abdominal lymphoma.
Radiol Clin North Am 2008;46(2):265-85.
J.
Rademaker.
Hodgkin's and non-Hodgkin's lymphomas.
Radiol Clin North Am 2007 ;45(1):69-83.
RC.
Semelka et al.
Renal lymphoma: demonstration by MR imaging.
AJR Am J Roentgenol 1996;166(4):823-7.
YH.
Wu et al.
Retroperitoneal neoplasms within the perirenal space in infants and children: differentiation of renal and non-renal origin in enhanced CT images.
Eur J Radiol 2010;75(3):279-86.
XH.
Ye et al. 18F-FDG PET/CT evaluation of lymphoma with renal involvement: comparison with renal carcinoma.
South Med J 2010;103(7):642-9.
F.
Vázquez Alonso et al.
Primary renal lymphoma: report of three new cases and literature review.
Arch Esp Urol.
2009;62(6):461-5.
A.
Tefekli et al.
Lymphoma of the kidney: primary or initial manifestation of rapidly progressive systemic disease?.
Int Urol Nephrol 2006;38:775-8.
S.
Hunter et al.
Diagnosis of renal lymphoma by percutaneous image guided biopsy: experience with 11 cases.
J Urol 2006;176:1952-6.
MA.
Dimopoulos et al.Primary renal lymphoma: a clinical and radiological study.
J Urol 1996;155(6):1865-7.
AH.
Ahmad,
GT.
Maclennan y C.
Listinsky.
Primary renal lymphoma: a rare neoplasm that may present as a primary renal mass.
J Urol.
2005;173:239.
JP.
Heiken et al.
Computed tomography of renal lymphoma with ultrasound correlation.
J Comput Assist Tomogr 1983;7:245-50.
SZ.
Jafri.
CT of renal and perirenal non-Hodgkin lymphoma.
AJR Am J Roentgenol.
1982;138:1101-5.
J.
Richmond et al.
Renal lesions associated with malignant lymphomas.
Am J Med 1962;32:184-207.
SR.
Prasad et al.
Common and uncommon histologic subtypes of renal cell carcinoma: imaging spectrum with pathologic correlation.
Radiographics 2006;26(6):1795-806.
R.
Dyer,
DJ.
DiSantis y BL.
McClennan.
Simplified imaging approach for evaluation of the solid renal mass in adults.
Radiology 2008 May;247:331-43.
SG.
Silverman et al.
Management of the incidental renal mass.
Radiology 2008;249(1):16-31.
P.
Aidan.
Magnetic Resonance Imaging characterization of a mucinous tubular and spindle cell carcinoma of the kidney detected incidentally during an ectopic pregnancy.
Urology 2010;75(2):247-248.
MR. Oliva et al.
Original Research: Renal Cell Carcinoma: T1 and T2 signal intensity characteristics of papillary and clear cell types correlated with pathology .
AJR Am J Roentgenol 2009;192:1524-1530.