La utilización de los agentes de contraste en RM persigue fundamentalmente tres objetivos:
- Mejorar la definición tisular
- Incrementar las diferencias entre el tejido normal y el patológico
- Proporcionar información funcional (grado de realce en función del tiempo transcurrido desde la administración del contraste
Se trata con su admnistración de mejorar el contraste y por tanto la definición de las estructuras (Fig.
1)

Fig. 1: Imagen A sin contraste y B tras aumentar el contraste, permite distinguir con mayor claridad las distintas partes de la fotografía
Un contraste es un medicamento,
es decir,
una sustancia que administrada al organismo es capaz de prevenir,
curar,
paliar o diagnosticar (como es nuestro caso) una enfermedad.
Este tipo de sustancias funcionan modificando el contraste y se objetivan llegando a unos tejidos sí y a otros no,
en una concentración u otra y a un tiempo u otro.
De este modo se modifica la señal que emite el paciente y se mejora el diagnóstico.
La base de los contrastes en resonancia magnética es la susceptibilidad magnética intrínseca del compuesto que incluye el contraste,
es decir,
la disponibilidad de esa sustancia para ser imantada (magnetizada) en un campo magnético externo.
Esta susceptibilidad magnética se debe a la existencia de electrones desapareados,
es decir,
a la existencia de un número másico (suma de protones y neutrones) impar,
por lo que el espin es un número semientero.
Según la susceptibilidad magnética las sustancias pueden clasificarse en:
- Diamagnéticas: Sin momento magnético permanente,
por tanto no se imantan y no tienen interés como contraste en RM
- Paramagnéticas: Con momento magnético permanente y por tanto suceptibles al campo magnético.
Son muy escasas pero muy interesantes para su uso potencial como contraste en RM
- Ferromagnéticas: Son sustancias paramagnéticas en estado cristalino.
Muy susceptibles al campo magnético y muy interesantes como potenciales contrastes en RM.
- Superparamagnéticas: Sustancias paramagnéticas micronizadas.
Muy susceptibles al campo magnético,
resultan así mismo muy interesantes como posibles contrastes en RM.
El efecto de los contrastes sobre la señal en RM puede ocurrir en dos sentidos.
Bien acortan el T1,
es decir,
provocan un aumento de señal en imágenes potenciadas en T1.
(Fig.
2)
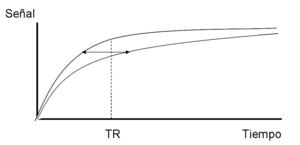
Fig. 2: Acortamiento del T1 tras administración de contraste que provoca un aumento de la señal del tejido en imágenes potenciadas en T1
O acortan el T2 provocando una pérdida de señal en secuencias potenciadas en T2.
(Fig.
3)
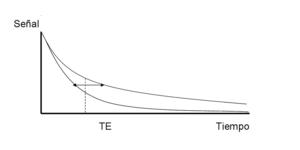
Fig. 3: Acortamiento del T2 tras administración de contraste que provoca un aumento de la señal del tejido en imágenes potenciadas en T2
Cuando se administra contraste,
la diferente captación tisular incrementa la diferencia de señal entre los tejidos,
de forma que es más fácil distinguirlos.
(Figs.
4 y 5)
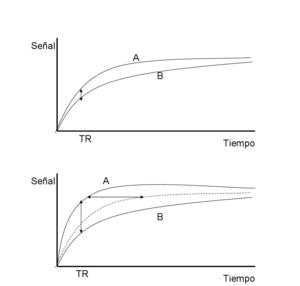
Fig. 4: Escasa diferencia de señal de forma previa a la administración de contraste entre los tejidos A y B, que se incrementa tras la admnistración del mismo, permitiendo distinguir mejor ambos tejidos
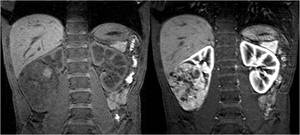
Fig. 5: Mejor diferenciación tisular tras admnistración de contraste (imagen de la derecha)
CONTRASTE IDEAL
El contraste ideal debería cumplir todos aquellos requisitos que caracterizan la acción de un fármaco en su más alto grado:
- Actividad: Máxima influencia sobre los parámetros responsables de la señal en RM (tiempo de relajación T1 y T2)
- Toxicidad: Nula
- Farmacocinética
- Administración: Fácil (preferentemente oral)
- Distribución: Selectiva
- Eliminación: Rápida y completa
- Estabilidad: Alta
- Eficiencia: Buena relación coste/efectividad
CLASIFICACIÓN DE LOS CONTRASTES DE RM
Los medios de contraste en RM podemos clasificarlos atendiendo a diversas características:
- Morfología de la molécula
- Susceptibilidad magnética
- Paramagnético
- Ferromagnético
- Superparamagnético
- Positivo / negativo
- Tejido diana
- Extracelular inespecífico
- Tejido específico
- Características fisicoquímicas
- Iónico – no iónico
- Isoosmolar –hiposomolar…
Los medios de contraste más habitualmente utilizados en la práctica clínica diaria en RM son los medios de contraste basados en gadolinio (Gd),
que es una sustancia paramagnética o ión metálico con electrones no pareados.
Dado que el gadolinio es tóxico si se administra directamente,
todos los medios de contraste cuya base es el gadolinio añaden a su composición una sustancia quelante de morfología lineal o cíclica que “sujeta” el gadolinio y limita su toxicidad en el organismo,
dando origen a la clasificación de los agentes de contraste en RM en lineales o cíclicos.
(Fig.
6)
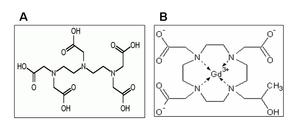
Fig. 6: A. Gadopentato de dimeglumina, medio de contraste lineal. B. Gadoteridol, medio de contraste cíclico
Contrastes intravenosos de gadolinio
Así atendiendo al tejido diana,
los medios de contraste de gadolinio de distribución extracelular son los más comúnmente utilizados y son los que aparecen en la tabla siguiente:
|
Principio activo
|
Nombrecomercial
|
Estructura
|
Carga
|
|
Gadopentato de dimeglumina Gd-DTPA (1983)
|
Magnevist®
|
Lineal
|
Iónico
|
|
Gadodiamida Gd-DTPA-BMA (1986)
|
Omniscan®
|
Lineal
|
No iónico
|
|
Gadoteridol (1992)
|
Prohance®
|
Cíclica
|
No iónico
|
|
Gadoversetamida Gd-DTPA-BMEA
|
Optimark®
|
Lineal
|
No iónico
|
|
Gadoterato de meglumina Gd-DOTA (1988)
|
Dotarem®
|
Cíclica
|
Iónico
|
|
Gadobutrol Gd-BT-DO3A
|
Gadovist®
Gadograf®
|
Cíclica
|
No iónico
|
Todos ellos presentan una concentración 0,5 molar excepto el Gadobutrol que es 1 molar.
Existen tres medios de contraste de gadolinio de distribución hepatobiliar comercializados:
- Mangafodipir trisódico (Teslascan®)
- Gadobenato de dimeglumina (Multihance®) que también puede ser utilizado como contraste extracelular
- Ácido gadoxético (Primovist®) que también puede ser utilizado como contraste extracelular
Y un contraste de gadolinio de distribución intravascular,
el gadofosfoverset trisódico (Vasovist®) de administración intravenosa y distribución intravascular mediante unión reversible a la albúmina plasmática y formado por una molécula de gran tamaño que no difunde al espacio extracelular,
por lo que resulta indicado para la realización de estudios vasculares con RM.
Contrastes intravenosos de manganeso
Además de contrastes de gadolinio,
que son los más habituales,
también podemos encontrar quelatos de manganeso como el Mangafodipir trisodio (Mn-DPDP) o Teslascan® que es un medio de contraste hepatobiliar que se administra por vía intravenosa y es captado fundamentalmente por los hepatocitos y por tanto eliminado fundamentalmente a través de la bilis (una pequeña proporción se elimina vía renal),
por lo que puede utilizarse para valoración de patología hepática o de la vía biliar y en algunos casos de patología pancreática debido a que también el páncreas realza levemente tras su administración.
Contrastes intravenosos de partículas de hierro
Existen también contrastes cuya base es el hierro,
son los conocidos como agentes de partículas de mayor o menor tamaño,
lo que va a condicionar su biodistribución.
Así existen agentes de partículas de mayor tamaño (>200nm) formados por óxido de hierro superparamagnético como el Endorem®,
Feridex®,
Abdoscan®.
Agentes con partículas de menor tamaño como el Resovist® (100-200nm) e incluso menores (<100nm) como el Sinerem® que causan un acortamiento de la señal T2 (señal hipointensa en T2).
Contrastes orales
Poco utilizados por su alto coste,
pueden ser positivos o negativos.
Lo más habitual es emplear como medio de contraste oral una dilución de un contraste de gadolinio extracelular convencional con agua en la proporción de 1:200 que provoca un acortamiento de la señal T2 (hiposeñal en T2) que resulta de utilidad para realizar adecuadamente las colangio-RM al oscurecer las estructuras del tubo digestivo que impiden la adecuada visualización de la vía biliar.
(Fig.
7)
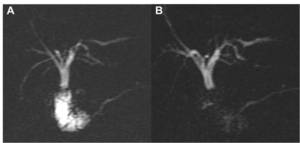
Fig. 7: A. Colangioresonancia. B. Colangioresonancia tras administración de gadolinio diluido en agua y la consiguiente opacificación duodenal
También es habitual emplear distintas soluciones acuosas para la realización de estudios del tubo digestivo con objeto de distender las asas de intestino delgado o el colon.
(Fig.
8)
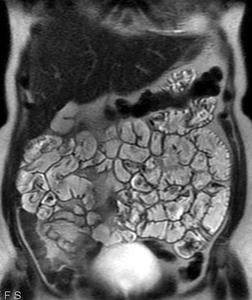
Fig. 8: Imagen T2 coronal en estudio de enteroresonancia . El paciente ha tomado durante la hora previa al estudio una disolución de 30g de sorbitol en 1,5 litros de agua.
FARMACOCINÉTICA
Las características generales de los contrastes de RM de gadolinio extracelulares,
que van a determinar su farmacocinética,
son las siguientes:
- Son hidrosolubles (no se distribuyen en la grasa,
sólo en el agua)
- Moléculas grandes (se moverán con dificultad)
- No unión a la albúmina
- No se metabolizan
- Eliminación lenta
Administración: Todos ellos se administran por vía intravenosa.
Distribución: Todos se distribuyen en el compartimento (parte del organismo en el medicamento se mueve de la misma forma) extracelular.
Eliminación: Todos se eliminan por vía renal de forma prácticamente completa a las 24 horas.
El gadobenato de dimeglumina (Multihance®) presenta la particularidad de que puede ser utilizado como contraste extracelular con las mismas características que los ya mencionados,
pero que se elimina fundamentalmente por la bilis con un pico máximo de concentración hepática a los 60 minutos de su administración,
lo que lo hace útil para su uso como contraste hepatoespecífico.
El Mangafodipir trisódico (Mn-DPDP) o Teslascan® es un quelato de manganeso que actúa como medio de contraste hepatobiliar de administración intravenosa en infusión lenta (15-20 minutos) aumque puede administrarse hasta a 1ml/s.
Es captado fundamentalmente por los hepatocitos (80%) y por tanto eliminado a través de la bilis (una pequeña proporción 15-20% se elimina vía renal en las primeras 24 horas),
por lo que se utiliza para valoración de patología hepática o de la vía biliar y en algunos casos de patología pancreática debido a que también el páncreas realza levemente tras su administración.
El pico máximo de realce (acortamiento del T1) con este tipo de contraste ocurre aproximadamente a los 15-20 minutos de su administración y persiste hasta trascurridas aproximadamente unas 4 horas.
Los contrastes cuya base es el hierro o agentes de partículas deben administrarse en perfusión lenta (aproximadamente 30 minutos) y son captados por el sistema reticuloendotelial (hígado,
bazo,
ganglios linfáticos…) provocando un acortamiento del T2 durante una o dos horas posteriores a su administración y se incorporan a la vía metabólica del hierro en el organismo.
Los de mayor tamaño se utilizan para valoración de patología hepática y los de menor tamaño para valoración ganglionar,
observándose captación a las 24 horas de la administración en los ganglios no patológicos
TOXICIDAD
La toxicidad de los compuestos de gadolinio va a depender directamente de la estabilidad del quelato,
que está definida por el valor de la constante termodinámica de disociación del preparado.
Influirá también en la aparición de efectos adversos,
especialmente náuseas y vómitos en una inyección rápida,
la osmolaridad del preparado.
La introducción de una sustancia hiperosmolar provoca una elevación de la osmolaridad del plasma con deshidratación intracelular y una alteración de los metabolitos de la sangre,
provocando dolor vascular,
lesión endotelial,
vasodilatación con hipotensión y/o hipovolemia por bradicardia.
Lo ideal es que la osmolaridad del preparado se aproxime lo más posible a la osmolaridad del plasma (isoosmolar) que es de 300mOsm.
Del mismo modo,
la viscosidad deberá ser baja para evitar toxicidad.
|
Principio activo
|
Nombre comercial
|
Osmolaridad
(mOsm/Kg)
|
Log cte estabilidad termodinámica
|
Carga
|
Viscosidad a 37º (centipoises)
|
|
Gadopentato de dimeglumina Gd-DTPA (1983)
|
Magnevist®
|
1960
|
22,1
(1% exceso quelante)
|
Iónico
|
2,9
|
|
Gadodiamida Gd-DTPA-BMA (1986)
|
Omniscan®
|
780
|
16,9
(5% exceso quelante)
|
No iónico
|
1,9
|
|
Gadoteridol
|
Prohance®
|
630
|
23,8
|
No iónico
|
1,3
|
|
Gadoversetamida Gd-DTPA-
BMEA
|
Optimark®
|
1110
|
16,6
|
No iónico
|
2
|
|
Gadoterato de meglumina Gd-DOTA (1988)
|
Dotarem®
|
1350
|
25,8
|
Iónico
|
2
|
|
Gadobutrol Gd-BT-DO3A
|
Gadovist®
Gadograf®
|
1603
|
21,8
|
No iónico
|
4,96
|
Las características farmacológicas de todos ellos son similares,
siendo la diferencia principal su estructura y carga iónica.
La estabilidad de los quelatos de gadolinio es muy alta y los compuestos macrocíclicos fijan el ión de gadolinio más fuertemente que los de estructura lineal.
La ionicidad mejora la estabilidad de la molécula.
Los agentes no iónicos tienen una menor osmolaridad y son menos viscosos.
La concentración de las preparaciones de estos quelatos de Gd comercialmente disponibles es de 0.5 molar y a excepción del gadobutrol que es 1 molar.
REACCIONES ADVERSAS
Los medios de contraste radiológicos compuestos de gadolinio son considerados clásicamente muy seguros aunque pueden producir reacciones adversas con prevalencia entre el 0,17 % - 2,4 %.
Los efectos secundarios más frecuentes son leves,
fundamentalmente nauseas-vómitos,
pero también:
- Sensación de calor o frío (velocidad de inyección)
- Dolor en el punto de inyección (velocidad de inyección)
- Mareo,
cefaleas,
náuseas (velocidad de inyección)
- Disgeusia o sabor metálico
- Urticaria (rara,
puede ser aviso de reacción grave)
- Convulsiones (muy raro,
cuidado pacientes epilépticos)
- Reacción anafiláctica (muy rara,
puede ser grave/mortal)
Otro efecto secundario a tener en cuenta y que ha preocupado de forma importante es la fibrosis sistémica nefrogénica (FSN) de la hablaremos de forma separada.
En la última década y fundamentalmente en los últimos 3 años están apareciendo publicadas reacciones alérgicas a estos contrastes,
con prevalencia de 0,04 - 0,07%.
Las reacciones alérgicas de mayor gravedad,
las reacciones anafilácticas,
pueden aparecer en el 0,01%.
Actualmente la mortalidad por reacciones alérgicas con el uso de estos agentes de contraste es mayor que por fibrosis sistémica nefrogénica,
con aproximadamente 7 muertes/año en EEUU en los últimos años,
dado que la FDA tiene registradas 40 muertes por reacciones alérgicas entre los años 2004 y 2009.
|
|
REAC.
ADVERSAS INMEDIATAS
|
MUERTES por R.
Inmediatas
|
|
|
Prince et al.
(2000-9)
/1000 pac
|
FDA
(2004-9)
/millón pac
|
Prince et al.
(2000-9)
/1000 pac
|
FDA
(2004-9)
/millón pac
|
|
GADOTERIDOL
Prohance®
|
3,3
|
49
|
0
|
0.7
|
|
GADOBENATO
Multihance®
|
1,2
|
322
|
1
|
2,7
|
|
GADOPENTETATO
Magnevist ®
|
0.5
|
62
|
0
|
0,97
|
|
GADIDIAMIDA
Omniscan®
|
0.2
|
4.7
|
0
|
0.15
|
Incidencia de reacciones inmediatas a la administración de contraste de gadolinio.
AJR 2011; 196 (2): 138-43
En los contrastes cuya base es el hierro,
los efectos adversos vienen normalmente derivados de la inyección rápida,
habiéndose descrito hipotensión,
disnea,
sofocos,
dolor lumbar…
FIBROSIS SISTÉMICA NEFROGÉNICA
En el año 1997 se describe la fibrosis sistémica nefrogénica como una dermopatía idiopática con aumento de formación de tejido conectivo en la piel y posible afectación sistémica,
en pacientes con insuficiencia renal grave y que puede ser rápidamente progresiva y fulminante en un 5% de los pacientes.
Es en el año 2006 cuando se describe su asociación con la administración de contraste de gadolinio en pacientes con insuficiencia renal.
En el año 2009 la agencia española de medicamentos y EMEA clasifican estos contrastes en función de los datos publicados hasta ese momento y según su riesgo asociado de provocar fibrosis sistémica nefrogénica en:
- Riesgo alto: Magnevist®,
Optimark®,
Omniscan®
- Riesgo medio: Vasovist®,
Primovist®,
Multihance®
- Riesgo bajo: Dotarem®,
Prohance®,
Gadovist®
De esta forma se establecen unas pautas de conducta ante la administración de contraste de gadolinio en los pacientes con insuficiencia renal:
- Contraindicación a la administración de contrastes de riesgo alto en pacientes con insuficiencia renal severa (tasa de filtración glomerular <30ml/min/1.73m2)
- Contraindicación a la administración de contrastes de riesgo alto en pacientes con transplante hepático y/o renal
- Contraindicación a la administración de contrastes de riesgo alto en niños menores de 1 año
- Cuidadosa valoración del riesgo/beneficio en pacientes con tasa de filtración glomerular <30ml/min/1.73m2
- No sobrepasar la dosis de 0,1 mmol/Kg en p.acientes con tasa de filtración glomerular <30ml/min/1.73m2
MANEJO DE LOS CONTRASTES DE GADOLINIO
Después de un pico de incidencia a mediados de la pasada década,
la FSN prácticamente ha desaparecido en nuestros días,
probablemente debido a la toma de conciencia por parte de los radiólogos del problema y a un seguimiento de las normas previamente expuestas.
Incluso en una reciente presentación de los resultados iniciales del estudio prospectivo francés sobre FSN que comenzó en 2008 parece concluirse la no aparición de FSN incluso en pacientes en fallo renal,
sometidos a diálisis.
De hecho la recomendación de septiembre de 2010 de la US Food and drug administration no prohíbe la administración de contrastes de gadolinio en estos pacientes sino que recomienda la inyección de la menor dosis posible de un contraste de bajo o moderado riesgo.
La elección del contraste adecuado debería fundamentarse en la función renal del paciente de forma que en pacientes con función renal alterada es importante considerar el uso de los contrastes que menos frecuentemente producen FSN.
En cambio,
en los pacientes que tengan función renal normal,
en la elección del contraste debería considerarse el riesgo de reacción alérgica con mayor peso al riesgo de FSN.
(Fig.
9)
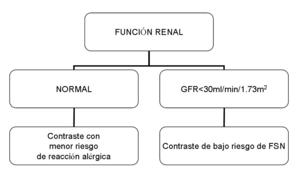
Fig. 9: Algoritmo de elección de contraste
Para determinar la función renal del paciente parece complicado el realizar un análisis de la tasa de filtración glomerular en cada paciente que va a recibir contraste,
por ello se proponen otros métodos como el cuestionario de Choyke et al.
que mediante seis preguntas sencillas detecta con una fiabilidad superior al 99% si el paciente tiene una tasa de filtración glomerular inferior a 30ml/min/1.73m2:
- ¿Alguna vez ha tenido problemas de riñón?
- ¿Alguna vez ha tenido proteinuria?
- ¿Es usted hipertenso?
- ¿Es usted diabético?
- ¿Tiene gota?
- ¿Alguna vez ha sido operado de riñón?
Como hemos visto,
los dos efectos secundarios más graves de los contrastes de gadolinio son la FSN y las reacciones alérgicas.
Por eso,
independientemente de que su incidencia sea baja,
el personal que realiza la RM debe estar entrenado en el reconocimiento precoz y manejo inmediatode las reacciones alérgicas.
Dado que como hemos visto,
este grupo de medicamentos no está exento de afectos secundarios aunque sean poco frecuentes,
debemos siempre preguntarnos antes de su administración y especialmente como hemos visto en pacientes con mal funcionamiento renal,
si podríamos obtener lo mismo,
sin contraste,
con las secuencias de pulso adecuadas.
Debe valorarse siempre también el tiempo de máquina necesario para obtener esas secuencias y el ahorro potencial del mismo si utilizamos contraste.
Es fundamental preguntarse si su administración va a cambiar el diagnóstico/pronóstico.
Por último debemos evaluar cuidadosamente la dosis de contraste que es necesaria para conseguir el realce adecuado para el diagnóstico,
prestando mucha atención al tiempo de realce máximo del contraste.










