1.
Introducción:
1.1 Definición endometriosis invasiva
La endometriosis se define como la presencia de glándulas y estroma endometrial funcional fuera de la cavidad endometrial y miometrio.
Este tejido es tejido hormonodependiente que puede ser responsable de sangrado,
inflamación,
fibrosis y formación adherencias por sangrado e inflamación cíclica,
ocasionando dolor pélvico e infertilidad.
La endometriosis pélvica profunda (EPP) se define por la presencia de lesiones endometriósicas penetrantes en el espacio retroperitoneal o pared de órganos vecinos a una profundidad de al menos 5 mm bajo la superficie peritoneal (1,
2,
3).
El uso frecuente en la práctica clínica del término endometriosis infiltrante como intercambiable respecto a la EPP se basa en conceptos anatómicos erróneos.
El término de EPP debe reservarse a las lesiones que afectan a tejidos retroperitoneales (4).
Por motivos prácticos se incluyen también aquellas lesiones que afectan estructuras vitales como intestino,
uréteres y vejiga,
que deberían definirse como endometriosis infiltrante.
La mayor parte de los autores utiliza estos términos como sinónimos o los engloba dentro del concepto de endometriosis subperitoneal o extraperitoneal (5).
Microscópicamente,
tanto las lesiones endometriósicas superficiales típicas como las profundas contienen glándulas y estroma y pueden acompañarse de hemorragia o fibrosis.
Sin embargo,
los hallazgos de lesiones endometriósicas infiltrantes se caracterizan por hiperplasia fibromuscular que rodea al foco de endometriosis,
presentando en ocasiones pequeñas cavidades hemáticas dentro de los focos endometriósicos (Fig. 1).
En la denominada endometriosis intestinal (EI),
los implantes se adhieren inicialmente a la superficie de la serosa del intestino y pueden invadir posteriormente las capas musculares e incluso alcanzar la mucosa intestinal.
Al infiltrar la muscularis propria,
las glándulas y el estroma endometriósico inducen la proliferación del músculo liso y reacción fibrótica,
dando como resultado la formación de nódulos sólidos (4).
Esta proliferación fibromuscular puede dar como resultado un engrosamiento mural,
estenosis u obstrucción intestinal (4).
En la mayoría de los casos de enfermedad endometriósica infiltrante severa,
también en la EI,
la solución final es quirúrgica.
La valoración prequirúrgica es,
por lo tanto,
crucial estableciendo la distribución precisa de las lesiones endometriósicas infiltrantes,
para asegurar una resección quirúrgica completa.
1.2 Teorías etiopatogénicas.
Las causas de la endometriosis permanecen controvertidas.
Se han propuesto teorías que incluyen la teoría metastásica,
la teoría metaplásica y la teoría de inducción (2,
5,
6,
7).
La más ampliamente aceptada es la teoría metastásica según la cual,
la presencia de células endometriales e implantes estromales en localización ectópica pélvica es probablemente secundaria a menstruación retrógrada,
implantándose células viables en la superficie serosa.
Una teoría alternativa es la teoría metaplásica o celómica que defiende que la endometriosis se desarrolla de la transformación metaplásica de células epiteliales peritoneales dado que ambos tipos celulares derivan del epitelio celómico.
La tercera hipótesis es la teoría de inducción,
propone que las células endometriales pueden liberar sustancias que inducen la transformación de tejido desdiferenciado mesenquimal en tejido endometriósico.
La diseminación a distancia también puede ocurrir por vía linfática o hematógena o iatrogénicamente durante exploración quirúrgica o biopsia.
1.3 a) Prevalencia.
La endometriosis se encuentra predominantemente en mujeres en edad fértil y se estima entre el 5-10% aproximadamente de la población femenina.
La frecuencia es mayor en mujeres con infertilidad y dolor pélvico (2,
7).
En concreto,
la prevalencia de endometriosis entre mujeres con infertilidad se estima entre el 25 y 48% (8,
9).
1.3 b) Localizaciones más frecuentes.
Las localizaciones más frecuentes de EPP son,
en orden descendente,
ovarios,
torus uterino y ligamentos uterosacros,
saco de Douglas,
trompas uterinas,
vagina,
colon rectosigmoideo y vejiga (2,
7,
10).
La frecuencia de afectación del saco de Douglas se estimaque sucede hasta en un 54-56% (11,
12) (Fig. 2).
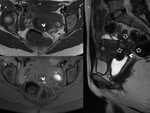
Cuando la endometriosis es infiltrante nodular (sólida) asienta típicamente en el tabique rectovaginal (TRV) y otras estructuras fibromusculares pélvicas como los ligamentos uterinos (69,2%) (Fig. 3,
Fig. 4),
vagina (14,5%) y la pared muscular de órganos pélvicos como recto y vejiga (4,
10).
El tracto gastrointestinal es la localización más frecuente de endometriosis extra-pélvica.
La incidencia referida de la EI es variable según series desde un 5% a un 37% (4,
7,
10,
13,
14,
15),
dependiendo de la población estudiada y el método diagnóstico utilizado.
1.4 a) Presentación clínica.
La EPP es causa de dolor pélvico,
dismenorrea,
dispareunia,
disquecia y síntomas urinarios y se asocia a infertilidad (3,
7),
aunque puede también darse en pacientes asintomáticas.
Se ha demostrado que la extensión de la enfermedad no se correlaciona con la gravedad de los síntomas (4).
La mayoría de pacientes con EI desarrolla en el tiempo una variedad de síntomas gastrointestinales (16,
15).
La EI puede imitar un proceso intestinal primario (17,
18) causando de dolor abdominal,
perforación,
obstrucción y/o sangrado,
retrasando el diagnóstico.
En particular,
puede ser confundida con la enfermedad de Crohn porque ambas pueden afectar de forma parcheada el intestino con lesiones satélites y porque puede existir una extensión transmural e inflamación,
con desarrollo posterior de estenosis,
adherencias y obstrucción (2).
También puede imitar clínicamente el síndrome del colon irritable y,
en casos más graves,
patologías obstructivas intestinales (13),
pudiendo llegar a producir masas y simular una neoplasia primaria intestinal,
particularmente cuando la afectación es anular o circunferencial (2).
La infiltración mucosa puede ocasionar ulceraciones y sangrado.
La presentación con sangrado rectal se relaciona de forma estadísticamente significativa con EI del colon distal (17).
2 Endometriosis Intestinal por Imagen por RM.
2.1 Consideraciones técnicas del estudio de Endometriosis Intestinal por RM
El estudio prequirúrgico de EI requiere de la valoración panorámica de aquellas áreas más frecuentemente afectadas,
incluyendo todo el tracto gastrointestinal en su conjunto.
Nuestro protocolo prequirúrgico incluye la realización de RM pélvica de alta resolución y estudio de Enterografía por RM o Colonografía por RM,
que pueden realizarse en un solo tiempo de estudio o,
mejor tolerado por las pacientes,
en dos sesiones separadas al igual que describen otros autores (9).
2.1.1 RM Pélvica.
El protocolo de RM pélvica para valoración de EPP debe adaptarse a las peculiaridades y características intrínsecas de las lesiones que queremos evaluar.
- En primer lugar,
es necesaria la realización de secuencias T1 sin y con saturación grasa para mejorar la conspicuidad de lesiones con contenido hemático,
que es una característica cardinal de implantes endometriósicos y endometriomas (Fig. 5).
- En segundo lugar,
obtenemos imágenes con distensión vaginal y,
según sospecha,
también rectal mediante gel ecográfico estéril o enema rectal con suero templado al igual que han descrito otros autores (5).
La EI afectando al colon puede ser confundida con materia fecal que presenta frecuentemente elevada señal en secuencias T1 sin y con saturación grasa.
Un enema de agua administrado previo a la RM es de gran utilidad evitando falsas imágenes (10) y mejorando el diagnóstico de lesiones endometriósicas (11).
La opacificación de la vagina y el recto con gel ecográfico mejora de forma significativa la sensibilidad de la RM para la detección de EPP por la distensión de las cavidades,
delimitando mejor las estructuras pélvicas (19) (Fig. 6).
El gel ecográfico tiene una intensidad de señal similar al agua en secuencias ponderadas en T2,
lo que contrasta con la hiposeñal relativa de la pared vaginal y rectal.
Además,
tiene cualidades inherentes beneficiosas para el estudio,
permitiendo una distensión estable de estas cavidades,
previniendo por su naturaleza viscosa la pérdida que ocurriría si se emplease líquido puro (20).
Es especialmente eficaz para detección de las lesiones localizadas en la vagina y tabique rectovaginal (19) (Fig. 7,
Fig. 8) y es una técnica bien tolerada y aceptada por las pacientes que han sido correctamente informadas de su administración previa a la exploración (19).
- Por último,
consideramos ventajosa la realización de estudio dinámico tras la administración de contraste intravenoso.
Algunos autores evitan el uso de contraste intravenoso debido a la falta de consenso definitivo concerniente a su indicación.
Una precisa valoración de la distribución y extensión preoperatoria de la endometriosis,
incluyendo implantes profundos y adherencias ha sido demostrado incluso sin uso de gadolinio (21).
Al contrario,
otros autores achacan el bajo rendimiento de la RM en algunas series a la ausencia de administración de contraste intravenoso y drogas antiperistálticas (10).
Se ha descrito la utilidad del contraste intravenoso para definir la extensión de procesos inflamatorios activos asociados con la endometriosis (4,
7).
El uso de secuencias post-contraste se ha recomendado también para identificar nódulos sólidos captantes en quistes endometriósicos cuando se sospecha transformación maligna (7,
22).
2.1.2 Enterografía por RM/Colonografía por RM.
La técnica de Enterografía-RM aplicada a la valoración de EI no difiere de forma significativa de la valoración en otras patologías (23),
pero también añadimos algunas recomendaciones extraordinarias:
- En primer lugar,
la distensión del marco cólico es un hecho de capital importancia,
lo cual se puede obtener con un relleno anterógrado (que obtiene una distensión colónica irregular pero,
en nuestra experiencia,
casi siempre suficiente para detectar y caracterizar las lesiones parietales) (Fig. 9) o más correctamente aplicando un enema de suero templado con técnicas de Colonografía-RM (24) que han demostrado mejorar el rendimiento diagnóstico (9).
- En segundo lugar,
dado que la presencia de adherencias es un hecho muy común en pacientes con endometriosis y,
en muchas ocasiones,
afecta de forma evidente la función gastrointestinal,
la aplicación de secuencias dinámicas cine es de gran utilidad como ha sido confirmado en estudios dirigidos (25) (Fig. 10).
Nuestra recomendación es realizarlas en los tres planos del espacio,
incluyendo el plano sagital,
dado que en muchas ocasiones las adherencias se forman sobre la superficie peritoneal anterior,
fundamentalmente en aquellos casos con antecedentes quirúrgicos (Fig. 11).
- Por otra parte,
el uso de drogas antiperistálticas es esencial para definir correctamente la pared intestinal.
Es recomendable aunque no imprescindible también su uso en los estudios limitados a pelvis,
mejorando la valoración de asas pélvicas.
- Por último,
la valoración panorámica que aporta el estudio de Enterografía-RM o Colonografía-RM permite también la valoración en un mismo tiempo del tracto urinario gracias a secuencias coronales FIESTA,
secuencias dinámicas cine (permitiendo valorar la dinámica de ambos uréteres) y el estudio de urografía-RM post-contraste,
con secuencias coronales tardías,
sin aumentar de forma significativa el tiempo de realización de la prueba.
2.2 Imagen por RM de implantes endometriósicos intestinales.
Las características por imagen de los implantes endometriósicos dependen fundamentalmente del componente histológico predominante,
así como de otras características de la lesión,
tales como el tipo de lesión (profundidad y localización).
Según el tipo de lesión podremos encontrar pequeños implantes infiltrantes,
lesiones sólidas pélvicas profundas (generalmente en saco de Douglas,
ligamentos uterosacros o torus uterino) (9) o la endometriosis infiltrante visceral (afectando a la vejiga o pared rectal) (4).
Los hallazgos de imagen representan directamente el predominio del componente fibrótico o glandular.
Así podemos encontrar lesiones fibróticas,
glandulares,
fibroglandulares o fibromiomatosas,
acompañadas o no por la presencia de contenido hemorrágico o de endometriomas.
En una serie el 100% de las lesiones contenían componente fibrótico y un 61% de ellos contenía focos hemorrágicos (3).
En implantes profundos,
la RM en ocasiones puede demostrar únicamente pequeños focos puntiformes de hiperseñal en ambas secuencias de pulso,
representativas de pequeños focos de hemorragia (Fig. 12).
El componente fibrótico predominante y ubicuo,
se presenta con hipointensidad de señal franca en imágenes T2 (Fig. 13,
Fig. 14).
La pared vaginal y rectal presentan características de intensidad de señal similares en RM que las lesiones fibróticas,
que pueden incluso ser confundidas con gas luminal (19).
En ausencia de componente inflamatorio asociado estas lesiones fibróticas demuestran nulo o mínimo realce post-contraste en comparación con el miometrio (Fig. 15).
Algunas masas endometriósicas,
localizadas en ligamentos uterosacros,
fórnix vaginal posterior o saco de Douglas,
pueden estar compuestas por una gran proporción de material glandular con escasa reacción fibrótica,
resultando en elevada hiperseñal en T2 (4) y demostrando focos puntiformes de elevada intensidad de señal en secuencias ponderadas en T1,
representativas de hemorragias petequiales.
Este material glandular sólido suele realzar intensamente y de forma precoz tras la administración de contraste intravenoso,
al menos similar al miometrio (Fig. 16),
diferenciándose así de necrosis o hemorragia intratumoral (4,
26).
Las lesiones viscerales sólidas corresponden a implantes fibroglandulares o fibromiomatosos y presentan una intensidad de señal baja o intermedia con focos puntiformes de alta señal en secuencias ponderadas en T1,
demostrando una señal uniforme y baja en imágenes ponderadas en T2,
y pueden demostrar mayor o menor grado de realce en secuencias post-contraste (4) (Fig. 17,
Fig. 18).
Algunos autores han descrito que el realce post-contraste corresponde a la abundante cantidad de tejido fibrótico de estas lesiones (4,
7).
En nuestra experiencia,
sin embargo,
estos implantes profundos fibróticos así como los implantes viscerales fibromusculares se comportan en el estudio dinámico post-contraste como hipocaptantes respecto al miometrio en fases precoces,
con realce progresivo más o menos intenso en fases tardías,
como cabe esperar de estructuras con alto componente fibrótico (Fig. 19). Esta característica ayuda a diferenciarlos de lesiones tumorales o patología inflamatoria intestinal activa que demuestran un realce intenso y precoz.
Estas masas sólidas endometriósicas pueden simular implantes metastásicos de enfermedades malignas intraperitoneales como tumores ováricos (26).
Estos procesos patológicos pueden diferenciarse por la baja intensidad de señal en secuencias ponderadas en T2 de la endometriosis sólida,
muchas veces combinada con la presencia de endometriomas (4).
Entre un 70-85% de los casos de EI afecta al recto y unión rectosigmoidea (13).
Las tres localizaciones de endometriosis rectosigmoidea en orden de frecuencia son la unión rectosigmoidea (Fig. 20,
Fig. 21),
la pared anterior del recto superior (a nivel de la saco de Douglas y asociado frecuentemente a afectación del torus uterino y espacio retrocervical) (Fig. 22),
y el colon sigmoide en fosa iliaca izquierda (Fig. 23) junto al ovario izquierdo (10).
El resto de localizaciones del tracto gastrointestinal afectadas con menor frecuencia incluyen,
en orden descendente,
el apéndice,
el ciego y el ileon distal (Fig. 24),
que rara vez se ve afectado por la endometriosis (6,
7,
13).
Cuando se afecta el intestino delgado los implantes endometriósicos generalmente se localizan en los últimos 10 cm proximales a la válvula ileocecal (10).
Los implantes endometriósicos intestinales se encuentran típicamente localizados en el borde antimesentérico intestinal,
dando una apariencia muy variable por imagen (13).
La EI puede manifestarse en RM mediante formaciones nodulares adheridas a la serosa,
hipointensas en secuencias potenciadas en T2 (Fig. 25),
que ocasionan retracción parietal.
Implantes superficiales serosos o síndromes adherenciales pueden presentarse como distorsión o angulación parietal,
mientras que los infiltrantes podrán ocasionar un engrosamiento parietal focal o circunferencial,
llegando a producir estenosis,
procesos suboclusivos u obstructivos francos,
erosiones mucosas,
e incluso la formación de raros endometriomas intestinales (Fig. 26).
En mujeres con EPP,
la prevalencia de endometriosis apendicular se estima en un 2,8% (27).
Los implantes endometriósicos que afectan al apéndice pueden ocasionar la formación de mucoceles apendiculares o signos de apendicitis aguda o procesos de apendicopatía crónica según el grado de obstrucción luminal y la evolución del proceso inflamatorio asociado (2) (Fig. 27).
Hay que hacer una mención expresa a la invasión del espacio retrocervical,
del Tabique Recto-Vaginal (TRV) y las lesiones del torus uterino,
por la elevada frecuencia en que concurre la afectación endometriósica rectosigmoidea
La afectación endometriósica del TRV puede ser confundida con una afectación masiva confluente de la porción más declive y profunda del saco de Douglas,
cubierto y excluido por adherencias del resto del peritoneo pélvico (4) (Fig. 28).
La afectación de la vagina por endometriosis casi siempre se asocia a la obliteración del saco de Douglas (3).
El área retrocervical es un espacio extraperitoneal situado detrás del cérvix,
situado en el mismo plano que el saco de Douglas y craneal al TRV.
Los fórnix vaginales son la porción más profunda de la vagina y se extienden hacia los recesos creados por la extensión caudal del cérvix al espacio vaginal (5).
Se ha propuesto una clasificación de las lesiones retroperitoneales de EPP que afectan al TRV y espacio retrocervical en 3 grupos.
Las lesiones propias del TRV (tipo I),
las lesiones de la pared posterior del fórnix vaginal (tipo II) y las lesiones en morfología de reloj de arena que se extienden entre ambas (tipo III) (28).
Las lesiones del TRV (tipo I) incluyen aproximadamente un 10% de los casos y generalmente son de pequeño tamaño.
Se sitúan en el tabique entre las capa muscularis propria de la pared anterior del recto y la capa mucosa de la pared posterior de la vagina,
bajo el recubrimiento peritoneal del saco de Douglas (Fig. 13).
Las lesiones parietales posteriores de los fórnix vaginales (tipo II) suman el 65% de los casos y se desarrollan desde el fórnix posterior de la vagina hacia el TRV (Fig. 29).
Las lesiones tipo III con morfología en reloj de arena (25% de los casos) ocurren en la progresión de las lesiones del fórnix vaginal posterior con extensión craneal hacia la pared anterior del recto superior.
Habitualmente son lesiones de gran tamaño (>3 cm) con infiltración importante de la pared rectal.
Estas lesiones siempre ocurren bajo la superficie peritoneal del saco rectouterino de Douglas.
La infiltración de la muscularis propria rectal se observa sistemáticamente en lesiones tipo III (4) (Fig. 30).
El torus uterino es un pequeño engrosamiento transversal que une la inserción original de los ligamentos uterosacros detrás del cérvix posterior,
aunque no es claramente visible por RM en ausencia de engrosamiento patológico (5).
Las lesiones del torus uterino se han descrito como isointensas en T2 al miometrio (10) (Fig. 31).
Cuando tanto los ligamentos uterosacros y el torus uterino se encuentran afectados por endometriosis profunda,
se puede identificar una típica imagen nodular hipointensa arciforme o estrellada que cubre el margen posterior uterino.
La retracción de la pared anterior del recto puede deberse a adherencias entre esta formación nodular del torus uterino y la serosa rectal o extensión directa con invasión de la capa muscular de la unión rectouterina (10),
con formación de un ángulo obtuso con la pared normal,
y algunas veces como un área que contiene focos de hiperintensidad de señal en secuencias ponderadas en T2 o T1 sin y con saturación grasa,
mejor definidas tras la administración de contraste intravenoso (3).
2.3 Diagnóstico diferencial EI vs cuadro adherencial peritoneal.
La presencia de síndromes adherenciales es típica en patología endometriósica florida,
bien por antecedentes quirúrgicos con formación de bridas o bien por el componente fibrótico secundario a implantes peritoneales o restos hemáticos sobre serosa intestinal,
pudiendo ocasionar cuadros suboclusivos intestinales persistentes y severos (Fig. 32).
La valoración de estos cuadros adherenciales en otras técnicas de imagen es improbable.
Los estudios ecográficos transrectales o transvaginales,
aunque permiten una valoración en tiempo real,
no permiten valorar el tracto gastrointestinal en su conjunto.
Los estudios de enema baritado de doble contraste demuestran una baja sensibilidad en la detección de adherencias en pacientes con endometriosis intestinal (29).
Las técnicas de TCMD con enteroclisis rectal pueden aportar la sospecha de este tipo de patología pero no permite estudio dinámico y tiene el serio inconveniente de la exposición a radiaciones ionizantes.
Por otra parte la presencia de extensas adherencias pélvicas,
especialmente en saco de Douglas,
suponen una importante limitación para la laparoscopia exploradora (16).
En RM,
las adherencias generalmente demuestran baja intensidad de señal y oscurece las interfases entre órganos.
El desplazamiento posterior de útero y ovarios,
angulación de asas intestinales,
elevación de los fórnix vaginales y la loculación de colecciones líquidas sugiere la presencia de adherencias (7) (Fig. 15).
La afectación limitada a la serosa puede ser difícil de diferenciar de la invasión de la pared muscular (3).
Además,
las adherencias extensas (entre 3-8 cm) entre la pared anterior del recto y la pared posterior uterina han sido descritas como una fuente potencial de falsos positivos por RM,
a pesar de que son expresiones frecuentes de EPP.
La valoración dinámica con secuencias cine por RM han demostrado ser de gran utilidad en la valoración de estos cuadros adherenciales (25) (Fig. 10,
Fig. 11) en su diagnóstico diferencial con cuadros obstructivos orgánicos (Fig. 33).
2.4 b) Complicaciones de la Endometriosis Intestinal:
Las complicaciones de la EI se desprenden del comportamiento de la afectación intestinal por los implantes infiltrantes.
Estos comienzan con la infiltración serosa con retracción peritoneal que requieren diagnóstico diferencial con la presencia de cuadros adherenciales,
pudiendo ocasionar cuadros de suboclusión intestinal.
La progresión de la infiltración a capas musculares parietales inducen la proliferación muscular y fibrosa con engrosamiento parietal (Fig. 34,
Fig. 35) ,
lo cual ocasiona estenosis más o menos sintomáticas y cuadros obstructivos francos.
Aunque infrecuente,
se han descrito en la literatura algunos casos de obstrucción intestinal debido a endometriosis intestinal afectando al ileon (14,
30,
31) (Fig. 36,
Fig. 37).
Menos frecuente es el diagnóstico de otros procesos obstructivos como invaginación intestinal secundario a endometriosis mesentérica (Fig. 38,
Fig. 39).
En casos excepcionales pueden alcanzar la mucosa intestinal,
con una extensión transparietal completa.
Este hecho puede acarrear el desarrollo de fístulas o incluso perforación intestinal y la formación de abscesos mesentéricos (Fig. 40,
Fig. 41).
La ruptura de endometriomas es una rara entidad con escasos casos descritos en la literatura,
pudiendo ocasionar sangrados intraperitoneales con cuadro de irritación peritoneal y abdomen en tabla,
o menos frecuentemente,
intraluminales.
La transformación maligna,
aunque excepcional,
es bien conocida desde hace mucho tiempo como complicación potencial de la endometriosis.
Fue inicialmente descrita por Sampson en 1925 (32),
estableciendo el criterio de diagnóstico de malignidad sobre endometriosis como sigue: clara evidencia de endometriosis encontrada junto al tumor,
apariencia histopatológica donde el desarrollo del origen tumoral de un foco endometriósico sea plausible y no se encuentre otro foco primario posible del tumor.
La incidencia de malignidad ovárica en endometriosis se estima en torno al 1%.
3 Métodos diagnósticos prequirúrgicos
Las guías clínicas de valoración prequirúrgica de pacientes con sospecha de EI no están claramente establecidas.
La prueba diagnóstica considerada gold standard sigue siendo la laparoscopia,
aunque las pruebas de imagen son cada vez más valoradas para la evaluación prequirúrgica en pacientes con dolor pélvico o infertilidad (2,
7).
Salvo nódulos rectales bajos y del TRV,
la EI no puede ser identificada con examen físico (exploración digital rectovaginal).
La laparoscopia exploradora también presenta serias limitaciones en la demostración de lesiones de EPP ocultas por adherencias o localizadas en el espacio subperitoneal (1,
16).
Además,
la confirmación prequirúrgica de EI repercute de forma importante sobre el tipo de abordaje quirúrgico y pronóstico posterior (17).
La evaluación se realiza usualmente con diversas técnicas radiológicas,
pero la técnica ideal del diagnóstico de endometriosis debe incluir no solo el recto-sigma,
sino también el resto del colon,
el ciego e ileon terminal,
incluso cuando estas localizaciones sean infrecuentes (13).
Numerosas técnicas de imagen han sido propuestas para el diagnóstico de EI.
La ecografía transvaginal,
transrectal y ecoendoscópica transrectal han demostrado un elevado grado de exactitud diagnóstica en la predicción de la afectación rectal.
Sin embargo el campo de visión limitado al recto-sigma y la posibilidad de definir el grado de infiltración en profundidad de la pared rectal sigue siendo un reto para la ecografía.
Recientes estudios con enema de bario de doble contraste enfatizan su capacidad en la predicción de la infiltración colónica,
aunque la experiencia requerida para interpretar esta técnica supone una limitación en su empleo.
Otras limitaciones serias son la exposición a radiaciones ionizantes,
la baja sensibilidad en el diagnóstico de síndromes adherenciales y la necesidad de estudios complementarios para valorar la EPP.
El TC con enteroclisis vía rectal permite estimar la infiltración en profundidad de colon,
pero enfrenta el problema de la exposición a radiaciones ionizantes en mujeres en edad fértil.
La RM ofrece una valoración panorámica de las potenciales localizaciones de EPP,
lo cual es la principal limitación de las técnicas ecográficas anatómicamente dentro del área de la cavidad pélvica y espacio subperitoneal,
no siendo ninguna de ellas capaz de realizar una valoración general de la extensión endometriósica.
Actualmente el estudio pélvico de alta resolución por RM se considera la mejor técnica no invasiva para la valoración de EPP (7,
33,
34),
y ofrece un elevado rendimiento en la demostración de EI.
La RM proporciona una tremenda ventaja respecto a otros métodos diagnósticos debido a la posibilidad de realizar un estudio completo de los compartimentos anterior y posterior de la pelvis en un mismo tiempo (4).
La RM ha demostrado en estudios recientes una elevada exactitud diagnóstica para definir localizaciones específicas de EPP (3).
Teniendo en cuenta todas las localizaciones en su conjunto,
la RM tiene una sensibilidad superior al 90% (19) y concretamente para EI una sensibilidad del 88,3%,
especificidad del 97,8% y exactitud diagnóstica del 94,9% (3).
Estudios de RM de alta resolución pélvica complementados con técnicas de Colonografía-RM se ha demostrado mejoría del rendimiento diagnóstico (9) y recientes estudios han demostrado buena sensibilidad en la detección de pequeños implantes peritoneales (3,
21) (Fig. 42,
Fig. 43).
En general se acepta que la RM es útil,
junto a la exploración física u ecografía transvaginal (o transrectal),
en la evaluación de las pacientes con endometriosis infiltrante o profunda.
Por otra parte,
la mayor parte de los estudios científicos solo consideran la afectación rectosigmoidea,
mientras que una técnica de imagen ideal debería al menos estudiar todo el marco cólico e ileon distal.
Es por ello que proponemos la necesidad de completar la valoración clásica pélvica de alta resolución mediante estudio de enterografía-RM con relleno anterógrado cólico o mediante técnicas de colonografía-RM.
4.
Criterios quirúrgicos de endometriosis intestinal.
Utilidad de la RM.
Aunque las indicaciones de la resección colorrectal son controvertidas,
múltiples estudios recientes demuestran la mejoría en la sintomatología,
ofreciendo un alivio sintomático a largo plazo,
mejorando la calidad de vida así como la fertilidad de las pacientes tras una exhaustiva resección quirúrgica de la enfermedad (8,
16).
Los criterios quirúrgicos fundamentalmente se establecen en función de la clínica,
pero existen algunas indicaciones relativas basadas en imagen diagnóstica.
En nuestro centro se establecen como indicaciones por RM la estenosis luminal >60% de la luz colorrectal distendida,
afectación intestinal de 360º,
lesiones >3 cm que infiltren aunque sea focalmente hasta la muscularis propria y los implantes endometriósicos infiltrantes que alcanzan la subserosa de forma evidente. Además,
lógicamente,
complicaciones como obstrucción intestinal o procesos suboclusivos severos,
sangrado intraluminal o endometriomas de pared intestinal deben ser resueltos quirúrgicamente.
Los nódulos endometriosicos intestinales pueden ser resecados mediante diversas técnicas: resecciones mucosas,
nodulectomías,
resección en disco de espesor completo de la pared o resección de un segmento intestinal (16).
Las lesiones de la EPP son más frecuentemente multifocales y se pueden presentar como masas infiltrantes consitentes en una confluencia de lesiones independientes.
Debido a esta naturaleza multifocal de la EPP,
la valoración de la extensión es esencial con el objetivo de identificar preoperatoriamente su localización exacta dado que se ha establecido que el tratamiento definitivo de la EPP requiere la resección completa de todas sus lesiones sintomáticas (19).
La frecuencia de lesiones de EI aisladas representan menos del 21% de los casos (35),
por ello el método de imagen ideal debe incluir al menos la cobertura del colon completo y el ileon distal.
Así,
la combinación de estudio pélvico e intestinal por RM parece el método de imagen más apropiado en el diagnóstico de todas las localizaciones posibles de extensión de la endometriosis (10).
Para algunos autores el mayor rol de la RM en la valoración de la EPP es diagnosticar y proporcionar un mapa exhaustivo de las lesiones endometriósicas (3,
4,
10,
21,
33).
El diagnóstico preoperatorio de EI favorece una aproximación quirúrgica menos invasiva y mejor evolución clínica (17).
La decisión de realizar cirugía intestinal influye en gran medida en el tipo de preparación intestinal preoperatoria,
la necesidad de cirujano colorrectal,
la aceptación psicológica de la necesidad de proctectomía por parte de la paciente y la recogida de consentimiento informado previo a la intervención (8,
13,
29).
No obstante,
es necesario considerar detenidamente las posibles complicaciones secundarias a cirugía colorrectal como pueden ser,
entre otras,
la relativa frecuencia de fístulas rectovaginales o dehiscencias de sutura (8).
REFERENCIAS.
1.
Koninckx PR,
Meuleman C,
Demeyere S,
Lesaffre E,
and Cornillie FJ.
Suggestive evidence that pelvic endometriosis is a progressive disease,
whereas deeply infiltrating endometriosis is associated with pelvic pain.
Fertil Steril.
1991,
Apr;55(4):759-65.
2.
Bennett GL,
Slywotzky CM,
Cantera M,
and Hecht EM.
Unusual manifestations and complications of endometriosis--spectrum of imaging findings: pictorial review.
AJR Am J Roentgenol.
2010,
Jun;194(6 Suppl):WS34-46.
3.
Bazot M,
Darai E,
Hourani R,
Thomassin I,
Cortez A,
Uzan S,
and Buy JN.
Deep pelvic endometriosis: MR imaging for diagnosis and prediction of extension of disease.
Radiology.
2004,
Aug;232(2):379-89.
4.
Del Frate C,
Girometti R,
Pittino M,
Del Frate G,
Bazzocchi M,
and Zuiani C.
Deep retroperitoneal pelvic endometriosis: MR imaging appearance with laparoscopic correlation.
Radiographics.
2006;26(6):1705-18.
5.
Coutinho A,
Bittencourt LK,
Pires CE,
Junqueira F,
Lima CM,
Coutinho E,
et al.
MR imaging in deep pelvic endometriosis: a pictorial essay.
Radiographics.
2011;31(2):549-67.
6.
Woodward PJ,
Sohaey R,
and Mezzetti TP.
Endometriosis: radiologic-pathologic correlation.
Radiographics.
2001;21(1):193-216; questionnaire 288-94.
7.
Choudhary S,
Fasih N,
Papadatos D,
and Surabhi VR.
Unusual imaging appearances of endometriosis.
AJR Am J Roentgenol.
2009,
Jun;192(6):1632-44.
8.
Stepniewska A,
Pomini P,
Bruni F,
Mereu L,
Ruffo G,
Ceccaroni M,
et al.
Laparoscopic treatment of bowel endometriosis in infertile women.
Hum Reprod.
2009,
Jul;24(7):1619-25.
9.
Scardapane A,
Bettocchi S,
Lorusso F,
Stabile Ianora AA,
Vimercati A,
Ceci O,
et al.
Diagnosis of colorectal endometriosis: contribution of contrast enhanced MR-colonography.
Eur Radiol.
2011,
Jul;21(7):1553-63.
10.
Kinkel K,
Frei KA,
Balleyguier C,
and Chapron C.
Diagnosis of endometriosis with imaging: a review.
Eur Radiol.
2006,
Feb;16(2):285-98.
11.
Hottat N,
Larrousse C,
Anaf V,
Noël JC,
Matos C,
Absil J,
and Metens T.
Endometriosis: contribution of 3.0-T pelvic MR imaging in preoperative assessment--initial results.
Radiology.
2009,
Oct;253(1):126-34.
12.
Kataoka ML,
Togashi K,
Yamaoka T,
Koyama T,
Ueda H,
Kobayashi H,
et al.
Posterior cul-de-sac obliteration associated with endometriosis: MR imaging evaluation.
Radiology.
2005,
Mar;234(3):815-23.
13.
Faccioli N,
Manfredi R,
Mainardi P,
Dalla Chiara E,
Spoto E,
Minelli L,
and Mucelli RP.
Barium enema evaluation of colonic involvement in endometriosis.
AJR Am J Roentgenol.
2008,
Apr;190(4):1050-4.
14.
Alatise OI,
Sabageh D,
Ogunniyi SO,
and Olaofe OO.
Ileal endometriosis presenting as acute small intestinal obstruction: a case report.
West Afr J Med.
2010;29(5):352-5.
15.
Prystowsky JB,
Stryker SJ,
Ujiki GT,
and Poticha SM.
Gastrointestinal endometriosis.
Incidence and indications for resection.
Arch Surg.
1988,
Jul;123(7):855-8.
16.
Remorgida V,
Ferrero S,
Fulcheri E,
Ragni N,
and Martin DC.
Bowel endometriosis: presentation,
diagnosis,
and treatment.
Obstet Gynecol Surv.
2007,
Jul;62(7):461-70.
17.
Kaufman LC,
Smyrk TC,
Levy MJ,
Enders FT,
Oxentenko AS,
Kaufman LC,
et al.
Symptomatic Intestinal Endometriosis Requiring Surgical Resection: Clinical Presentation and Preoperative Diagnosis.
The American Journal of Gastroenterology.
2011,
Apr 4;106(7):1325.
18.
Yantiss RK,
Clement PB,
and Young RH.
Endometriosis of the intestinal tract: a study of 44 cases of a disease that may cause diverse challenges in clinical and pathologic evaluation.
Am J Surg Pathol.
2001,
Apr;25(4):445-54.
19.
Chassang M,
Novellas S,
Bloch-Marcotte C,
Delotte J,
Toullalan O,
Bongain A,
and Chevallier P.
Utility of vaginal and rectal contrast medium in MRI for the detection of deep pelvic endometriosis.
Eur Radiol.
2010,
Apr;20(4):1003-10.
20.
Brown MA,
Mattrey RF,
Stamato S,
and Sirlin CB.
MRI of the female pelvis using vaginal gel.
AJR Am J Roentgenol.
2005,
Nov;185(5):1221-7.
21.
Zanardi R,
Del Frate C,
Zuiani C,
and Bazzocchi M.
Staging of pelvic endometriosis based on MRI findings versus laparoscopic classification according to the American Fertility Society.
Abdom Imaging.
2003;28(5):733-42.
22.
Takeuchi M,
Matsuzaki K,
Uehara H,
and Nishitani H.
Malignant transformation of pelvic endometriosis: MR imaging findings and pathologic correlation.
Radiographics.
2006;26(2):407-17.
23.
Herraiz Hidalgo L,
Alvarez Moreno E,
Carrascoso Arranz J,
Cano Alonso R,
and Martínez de Vega Fernández V.
[Magnetic resonance enterography: review of the technique for the study of Crohn's disease].
Radiologia.
2011;53(5):421-33.
24.
Rimola J,
Rodríguez S,
García-Bosch O,
Ricart E,
Pagès M,
Pellisé M,
et al.
Role of 3.0-T MR colonography in the evaluation of inflammatory bowel disease.
Radiographics.
2009;29(3):701-19.
25.
Buhmann-Kirchhoff S,
Lang R,
Kirchhoff C,
Steitz HO,
Jauch KW,
Reiser M,
and Lienemann A.
Functional cine MR imaging for the detection and mapping of intraabdominal adhesions: method and surgical correlation.
Eur Radiol.
2008,
Jun;18(6):1215-23.
26.
Gougoutas CA,
Siegelman ES,
Hunt J,
and Outwater EK.
Pelvic endometriosis: various manifestations and MR imaging findings.
AJR Am J Roentgenol.
2000,
Aug;175(2):353-8.
27.
Gustofson RL,
Kim N,
Liu S,
and Stratton P.
Endometriosis and the appendix: a case series and comprehensive review of the literature.
Fertil Steril.
2006,
Aug;86(2):298-303.
28.
Donnez J,
and Squifflet J.
Laparoscopic excision of deep endometriosis.
Obstet Gynecol Clin North Am.
2004,
Sep;31(3):567-80,
ix.
29.
Landi S,
Barbieri F,
Fiaccavento A,
Mainardi P,
Ruffo G,
Selvaggi L,
et al.
Preoperative double-contrast barium enema in patients with suspected intestinal endometriosis.
J Am Assoc Gynecol Laparosc.
2004,
May;11(2):223-8.
30.
Payne SP,
Pace RF,
Benjamin IS,
and Clark DM.
Isolated endometriosis of the small bowel presenting as acute small bowel obstruction.
Br J Clin Pract.
1991;45(1):57-8.
31.
Chaâbouni S,
Makni SK,
Kallel RI,
Gouiaa N,
Bahri I,
Mnif L,
et al.
Unusual cause of intestinal obstruction: ileal endometriosis.
Pathologica.
2009,
Jun;101(3):130-2.
32.
Endometrial carcinoma of the ovary arising in endometrial tissue in that organ.
.
Arch Surg 1925; 10:1-72.
33.
Roy C,
Balzan C,
Thoma V,
Sauer B,
Wattiez A,
and Leroy J.
Efficiency of MR imaging to orientate surgical treatment of posterior deep pelvic endometriosis.
Abdom Imaging.
2009;34(2):251-9.
34.
Chamié LP,
Blasbalg R,
Gonçalves MO,
Carvalho FM,
Abrão MS,
and de Oliveira IS.
Accuracy of magnetic resonance imaging for diagnosis and preoperative assessment of deeply infiltrating endometriosis.
Int J Gynaecol Obstet.
2009,
Sep;106(3):198-201.
35.
Chapron C,
Fauconnier A,
Vieira M,
Barakat H,
Dousset B,
Pansini V,
et al.
Anatomical distribution of deeply infiltrating endometriosis: surgical implications and proposition for a classification.
Hum Reprod.
2003,
Jan;18(1):157-61.