El angioTAC cerebral es una herramienta útil en la HSA no traumática ya que permite la detección de la causa (aneurismas,
MAV o FAVD) y la planificación del tratamiento. La sensibilidad es del 90-95% para los aneurismas mayores de 2 mm aunque varia dependiendo de la localización de los mismos.
El angioTAC cerebral precisa de manipulación postproceso,
cuya influencia sobre el grado de detección de aneurismas se desconoce,
aunque se supone que los mismos datos procesados con técnicas y equipos diferentes producirán diferentes grados de detección.
Limitaciones del angioTAC:
- No visualiza los vasos de pequeño calibre
- Dificultad para diferenciar una dilatación infundibular de un aneurisma
- Artefacto de vasos en kissing (fusión de dos vasos que contactan sus paredes)
- Confusión de venas con aneurismas
- Incapacidad para representar las calcificaciones y los trombos en las imágenes 3D
- Artefacto de endurecimiento del rayo producido por clips quirúrgicos.
Estas limitaciones aumentan cuando la técnica no ha sido correctamente realizada (colocación del ROI errónea o fallo en la inyección) y las arterias no alcanzan su máximo grado de realce.
Técnica del angioTAC
El equipo utilizado es un Brilliance TCMD de 64 detectores de Phillips,
parámetros empleados:
- técnica de 120 Kvp, 270 mAs
- colimación de 64 x 0,625,
desplazamiento de 0,9 mm por rotación y un tiempo de rotación de 0,5 segundos
- reconstrucciones con espesor de corte de 1 mm y un incremento 0,5 mm,
el FOV es de 220 mm y la resolución estándar.
El medio de contraste usado es iomeron 350 (iomeprol 71,44 g/100 ml de iodo),
la inyección se realiza mediante inyector para CT Medrad en vía periférica “buena” con 18 G en antebrazo,
revisamos y aseguramos las conexiones para comprobar que soportaran un flujo alto.
Parámetros de la inyección: 80 cc de contraste a un flujo de 5 cc/s seguido de 40 cc de suero salino a 5 cc/s.
Usamos técnica de bolus tracking para alcanzar un grado óptimo de realce de las arterias,
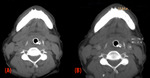
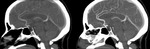
el ROI lo situamos en la arteria carótida común,
el corte de prueba y el tracker están colocados por debajo de la mandíbula,
ya que en esta localización es mas fácil identificar la carótida común.
(Figura 1 y 2)
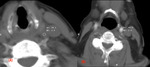
Es más difícil identificar la carótida interna en un estudio sin contraste cuando se realiza de urgencias por el personal de guardia que puede no estar entrenado en esta técnica.
Este es uno de los principales puntos de error que hemos encontrado.
(Figura 3)
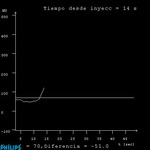
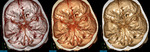
Mediante la técnica bolus tracking el estudio se dispara al alcanzar las 70 UH en el ROI con un retraso postumbral de 4 sg.
(figura 4)
El equipo dispone de un sistema que permite disparar el estudio de forma manual si durante la escopia continua detectamos realce adecuado en el sistema arterial y el ROI no está correctamente colocado,
esto puede “salvar” el estudio.
Los casos en los que la inyección no ha sido correcta volvemos a realizar una segunda adquisición bien elevando el umbral de disparo a 100-150 UH o con disparo manual lanzando el estudio en el cuando identificamos teñido arterial.
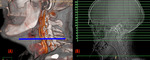
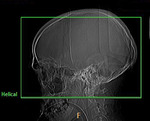
El volumen explorado incluye desde el atlas hasta el vértex,
es importante incluir el atlas para asegurar que se incluye las arterias cerebelosas posteroinferiores que pueden tener origen extracraneal hasta en el 18% de los casos,
y acabar en el vértex para poder detectar las malformaciones vasculares altas.
(figura 5)
Análisis del angioTAC:
El estudio es analizado en las estaciones de trabajo de Phillips con el sofware para análisis vascular.
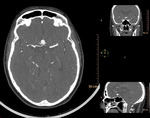
Revisamos las imágenes fuente en el plano axial,
coronal y sagital,
con ventana en la que el vaso pueda ser diferenciado de las partes blandas y del hueso de la base del cráneo (aproximadamente centro de 150 UH y ancho de 500 UH).
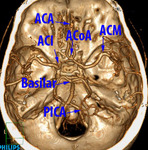
Insistiendo en las zonas donde el estudio sin contraste existe signos localizadores y en las zonas donde son más frecuentes los aneurismas.
(figura 6 y 7).
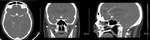
Posteriormente aumentamos el espesor de corte a 3 mm y revisamos nuevamente las reconstrucciones MPR en modalidad MIP.
(figura 8)
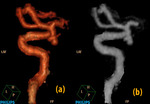
MIP:
La proyección de máxima intensidad usa para crear la imagen los vóxel más brillantes (de mayor atenuación) agrupándolos en un solo plano.
Es útil para diferenciar el hueso y las calcificaciones porque tienen una atenuación mucho mas alta que el contraste.
(figura 8)
Usamos la modalidad MIP en reconstrucciones MPR de 3- 5 mm de espesor.
No lo usamos en el angioTAC cerebral para reconstrucciones 3D porque,
al agrupar todos los vóxel,
a veces no permite diferenciar los aneurismas de los vasos de los que depende y los aneurismas pequeños pueden quedar incluidos o eclipsados por la densidad del vaso y no ser detectados.
(Figura 9)
Este tipo de reconstrucciones son fáciles de realizar ya que no dependen de ningún umbral por lo que las arterias pequeñas se muestra sin interacción del usuario simplemente ajustamos el nivel de ventana deseado.
Es en las reconstrucciones multiplanares donde realizamos las medidas del aneurisma de una manera más fiable,
valoramos los diámetros máximos del aneurisma,
tamaño del cuello y relación cuello/saco.
Aunque en aneurismas pequeños (<5 mm) la medida de la relación del cuello/saco puede no ser fiable.
Esto nos permite cuando van a ser tratados mediante embolización con coils elegir el tamaño del primer coil (framing) y si precisará de remodeling vascular o stent.
Volume rendering
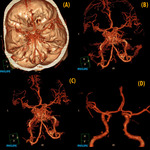
Las imágenes 3D son volume rendering (VR) con asignación automática de colores que por defecto tiene la estación de trabajo para la modalidad vascular cerebral .
Aunque existen varios modelos de reconstrucción en los que se asigna colores diferentes a la densidad hueso y a los vasos,
no se ha descrito que el color escogido determine una mayor sensibilidad en la detección de aneurismas.
Usamos el modelo con las arterias coloreadas en amarillo y el hueso en color ocre.
(figura 10 )
El volume rendering selecciona grupos de vóxel según su atenuación y les asigna un color y un nivel de opacidad.
Cuando se usa para hacer angiografías los vóxel de mayor atenuación que corresponden al hueso se selecciona separadamente de los que tienen una atenuación entre 100-300 UH que contienen información que corresponden a vasos,
esta selección crea imágenes 3D mostrando las arterias en color diferente del hueso.
Primero realizamos un recorte de la calota paralelo a la base del cráneo que permite realizar una inspección desde una vista craneal del interior del cráneo.
Posteriormente eliminamos el hueso bien con recorte manual o recorte automático con umbral de 350 UH,
vigilando que no desaparezcan estructuras de interés.
(Figura 11)
Una vez identificada la lesión realizamos análisis de su morfología,
mediciones de los diámetros y la relación con el cuello aunque confiamos más en las obtenidas en reconstrucciones MPR que el VR.
Posteriormente recortamos el vaso del que depende magnificándolo sin llegar a producir borrosidad o pixelación de la imagen.
(Figura 12)
Si detectamos un aneurisma volvemos a revisar el resto de las áreas donde asientan mas frecuentemente hasta en el 20% de los pacientes con HSA presentan mas de un aneurisma.