| ÍNDICE DE LA SECCIÓN: |
- INDICACIONES DE LA CARDIO-RM
- PECULIARIDADES: PREPARACIÓN DEL PACIENTE
- Planos cardíacos
- Adquisición de los planos específicos
- Formas de sincronización: gating retrospectivo y triggering prospectivo.
- Tipos de secuencias: espín eco y eco de gradiente.
- PROTOCOLOS Y EJEMPLOS (CASOS)
|
- INDICACIONES DE LA CARDIO-RM
Hoy en día,
además de para estudiar la patología isquémica,
la cardio-RM tiene es una indicación aceptada por el colegio americano de la radiología para otros múltiples tipos de patologías cardíacas ,
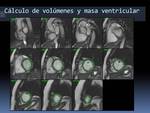
siendo el patrón de referencia para la valoración de dimensiones,
masa y función del ventrículo izquierdo (VI) y ventrículo derecho (VD),
así como para cuantificación de valvulopatías (ver Figura).

Fig. 1
- PECULIARIDADES: PREPARACIÓN DEL PACIENTE
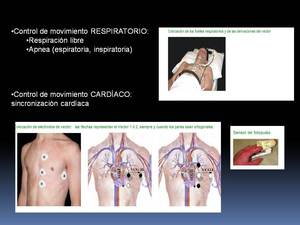
Fig. 2
La peculiaridad que tienen los estudios de RM cardíaca es la dificultad para obtener imágenes de una estructura en continuo movimiento y,
a su vez,
dentro de otra,
la caja torácica,
igualmente en movimiento continuo.
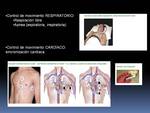
-El control de los movimientos respiratorios se realzará adquiriendo las imágenes en apnea,
generalmente espiratoria,
pero en algún caso será útil la adquisición en apnea inspiratoria,
como veremos.
Algunas secuencias también pueden realizarse en respiración libre,
aunque serán más susceptibles de artefactos por movimiento.
-El "control" de los movimientos cardíacos consiste en una sincronización entre la adquisición y el movimiento cardíaco,
a ser posible mediante el trazado electrocardiográfico y,
en su defecto en caso de un trazado irregular por presencia de arritmias,
con el que no se pueda sincronizar,
con el pulsioxímetro,
pero siempre como segunda opción,
debiéndose emplear el electrocardiograma(ECG) siempre que sea posible.
Sincronización cardíaca:
Fig. 3
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Cuando sincronizamos con el ECG,
nuestro trigger será la onda R.
Por ello,
tras colocar los electrodos a nuestro paciente, hemos de comprobar que nuestra onda R tiene predominancia en el trazado ECG,
debiendo tener una amplitud mayor a 0,5 mV,
asegurándonos así que la sincronización se realizará con la onda R y no con otra onda de ECG.
Los intervalos RR del ECG serán los que determinen nuestro TR (en secuencias espín eco).
A mayor frecuencia cardíaca (FC),
menor duración tendrán los intervalos RR,
siendo la duración del intervalo RR de aproximadamente 1000 ms para una FC de 60 latidos por minuto (lpm).
Cuando sincronizamos con el pulsioxímetro,
nuestro trigger será la onda sistólica.
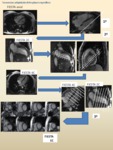
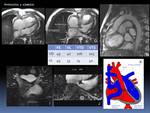
- Planos cardíacos.
Además de los planos ortogonales estrictos axial,
sagital y coronal puros,
los planos intrínsecos cardíacos son:

Fig. 4
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
- Cuatro cámaras (4C)
- Dos cámaras aurícula izquierda (AI)-ventrículo izquierdo (VI)
- Eje corto (EC)
- Dos cámaras aurícula derecha (AD)-ventrículo derecho(VD)
- Tracto de salida del VI (TSVI) o tres cámaras (3C)
- 2 cámaras VI-Aorta (Ao)
- Tracto de salida del VD (TSVD)
- 2 cámaras VD- Arteria pulmonar (AP)
A partir del plano TSVI,
junto con un plano 2C VI-Ao ó bien un plano coronal estricto (localizador ortogonal inicial),
podremos planificar una adquisición completamente perpendicular a la aorta,
bien para realizar una secuencia cine RM a través de la válvula aórtica (planimetría aórtica) ó para una secuencia de flujo un cm por encima de la válvula aórtica (ver Fig. 7,
Fig. 8 y Fig. 9).
Del mismo modo,
a partir del TSVD junto con el 2C VD-AP,
podremos adquirir la secuencia de flujo pulmonar un cm por encima de la válvula pulmonar (Fig. 10 y Fig. 11).
2.
Adquisición de los planos específicos:
- CINE (O FIESTA) 2C,
4C y EC:
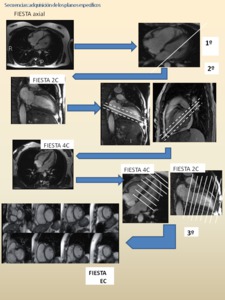
Fig. 5: Ver la descripción en la siguiente figura.
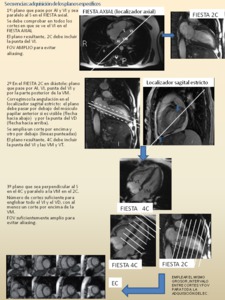
Fig. 6: Abreviaturas: VI: ventrículo izquierdo, AI: aurícula izquierda, VD: ventrículo derecho, AD: aurícula derecha, A: aorta, TP: tronco de la arteria pulmonar, VCS; vena cava superior; VM: válvula mitral; VT: válvula tricúspide; S: septo.
- CINE TSVI O 3C,
2C VI-Ao,
FLUJO AORTA y PLANIMETRÍA AÓRTICA:
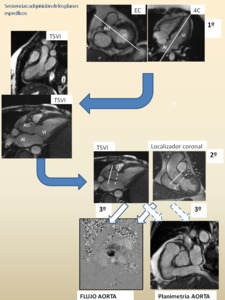
Fig. 7: Ver descripción en siguientes dos imágenes.
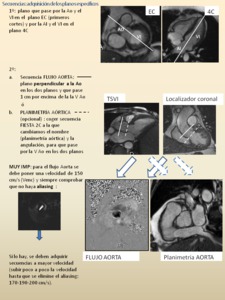
Fig. 8: Abreviaturas: VI: ventrículo izquierdo, AI: aurícula izquierda, VD: ventrículo derecho, AD: aurícula derecha, A: aorta, TP: tronco de la arteria pulmonar, VCS; vena cava superior; VM: válvula mitral; VT: válvula tricúspide; S: septo.
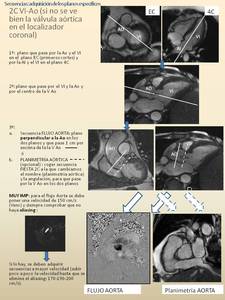
Fig. 9: Abreviaturas: VI: ventrículo izquierdo, AI: aurícula izquierda, VD: ventrículo derecho, AD: aurícula derecha, A: aorta, TP: tronco de la arteria pulmonar, VCS; vena cava superior; VM: válvula mitral; VT: válvula tricúspide; S: septo.
- CINE TSVD y FLUJO PULMONAR:
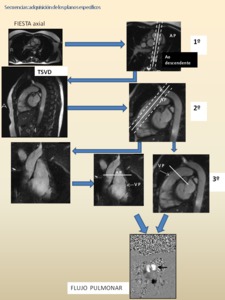
Fig. 10: Abreviaturas: VI: ventrículo izquierdo, AI: aurícula izquierda, VD: ventrículo derecho, AD: aurícula derecha, A: aorta, TP: tronco de la arteria pulmonar, VCS; vena cava superior; VM: válvula mitral; VT: válvula tricúspide; S: septo.
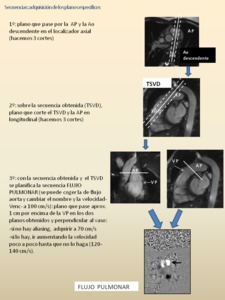
Fig. 11: Abreviaturas: VI: ventrículo izquierdo, AI: aurícula izquierda, VD: ventrículo derecho, AD: aurícula derecha, A: aorta, TP: tronco de la arteria pulmonar, VCS; vena cava superior; VM: válvula mitral; VT: válvula tricúspide; S: septo.
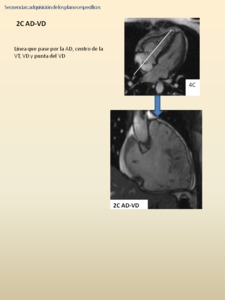
Fig. 12: Abreviaturas: VI: ventrículo izquierdo, AI: aurícula izquierda, VD: ventrículo derecho, AD: aurícula derecha, A: aorta, TP: tronco de la arteria pulmonar, VCS; vena cava superior; VM: válvula mitral; VT: válvula tricúspide; S: septo.
- CINE AXIAL multicorte-multifase:
Fig. 13: La secuencia cine RM SSFP puede adquirirse también en un plano axial (así como sagital ó coronal) estricto, cuya planificación debe incluir el cayado aórtico y la VCS en la parte craneal y las suprahepáticas en la región caudal, para lo cual debe incluirse parte del hígado que vemos en el localizador.
El ejemplo de la figura es un caso de TGA operada mediante la técnica de Mustard.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
3.
Formas de sincronización.
GATING RETROSPECTIVO.
Fig. 14
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
En el gating retrospectivo,
una forma de sincronización de las secuencias eco de gradiente,
la emisión de pulsos de radiofrecuencia (RF) y la adquisición de información se realiza de forma continua durante todo el ciclo cardíaco y durante sucesivos ciclos. Tras realizar una estimación de lo que dura el intervalo RR,
la máquina cambia el incremento de la fase.
Graba el trazado electrocardiográfico y posteriormente redistribuye las señales sobre el espacio K según el momento del ciclo en que las ha adquirido.
Antes eran secuencias más largas porque el intervalo RR se sobreestimaba para asegurar una completa cobertura del latido cardíaco en cada incremento de la codificación de fase,
pero las secuencias actuales no necesitan sobreestimarlo.
Se prefieren a la secuencias con triggering prospectivo,
pues adquieren información de todo el ciclo cardíaco.
Así,
para una secuencia eco de gradiente multifásica,
como es la imagen 4C cine RM multicorte-multifase de la figura anterior,
tanto si se realiza la adquisición retrospectiva como prospectiva (Fig.
15),
en contra de lo que pueda parecer,
las imágenes no son en tiempo real.
Para cada corte de esta secuencia cine RM se obtienen 20 fases del ciclo cardíaco (20 imágenes estáticas) en nuestra máquina,
y cada una de ellas se reconstruirá a partir de la información procedente de varios ciclos cardíacos para ese momento concreto (fase).
No obstante,
ya existen máquinas que permiten adquirir imágenes en tiempo real.
TRIGGERING PROSPECTIVO.

Fig. 15
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Se puede emplear en secuencias monofásicas (en donde se adquiere información en una parte del intervalo RR,como el realce tardío de la figura 15) y multifásicas (en donde se adquiere información de todo o de la mayor parte del intervalo RR ,como la secuencia cine de la figura 15).
La onda R será nuestro desencadenante del pulso de RF.
El ciclo cardíaco se trunca a una longitud constante,
dejando sin leer aproximadamente el 20% final de cada intervalo RR (tiempo conocido como “ventana de rechazo de arritmia”).
Por ello,
serán secuencias más insensibles a las variaciones fisiológicas de la longitud entre intervalos RR y,
por tanto a las arritmias moderadas,
pero desechan aquellos intervalos RR cuya variabilidad en su duración sea mayor al 20%,
por lo que puede que no se puedan realizar en arritmias más severas.
Otro inconveniente obvio es que dejan sin leer parte del ciclo y se pierde información funcional procedente de la telediástole en secuencias multifásicas. En arritmias severas puede ampliarse la “ventana de rechazo de arritmia”,
pero esto disminuye la calidad de la imagen.
Son más rápidas que las que se realizan con gating retrospectivo.
4.
Tipos de secuencias.
CLASIFICACIÓN :
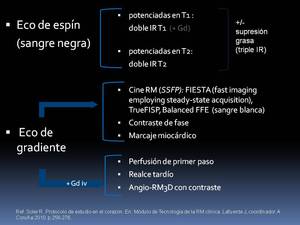
Fig. 16
-Secuencias espín eco (doble IR): nos ofrecen información anatómica y tisular,
con exquisito detalle,
siendo útiles para casos concretos como valoración del grosor y estructura del pericardio,
depósito graso miocárdico ó de la presencia de edema miocárdico.
Su tiempo de adquisición es largo.
Han perdido protagonismo frente a las secuencias eco de gradiente.
Pueden potenciarse en T1 ó T2,
las primeras pueden asociarse a Gd iv,
y todas ellas pueden asociarse a supresión de la grasa,
en cuyo caso se denominarán Triple IR.
Son coloquialmente conocidas como secuencias “sangre negra”.
-Secuencias eco de gradiente: son las más importantes,
pues ofrecen información anatómica pero,
sobre todo,
funcional.
Pueden ser mono o multicorte,
así como mono o multifase.
El grupo de las SSFP son coloquialmente conocidas como secuencias “sangre blanca”.
La adquisición en paralelo puede ser aplicada a la mayor parte de los tipos de secuencias.
Para ello se emplean múltiples antenas alineadas en el eje de la fase y el muestreo de cada una queda limitado a porciones del espacio K en el tiempo.
Supone una mayor velocidad de adquisición,
aunque compromete la señal/ruido y es especialmente susceptible a artefactos.
SECUENCIAS ESPÍN ECO:

Fig. 17
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube

Las imágenes potenciadas en espín eco son realmente imágenes turbo o fast spin eco,
siendo el tren de ecos de 32 en este tipo de secuencias y en nuestra máquina.
-Momento de adquisición: son imágenes monofásicas,
que se adquieren en un momento concreto del trazado ECG.
Generalmente se adquieren en la meso-telediastole,
como muestra la figura (cuadro que contiene los pulsos de RF),
pues es el momento en que el corazón se mantiene estático durante más tiempo y tenemos mayor ventana de adquisición.
No obstante,
como también nos interesa conseguir la máxima supresión de la señal procedente del flujo sanguíneo (de ahí el nombre de la secuencia “sangre negra”),
para una mejor calidad de imagen,
hay autores que recomiendan que esta adquisición se realice durante la sístole,
pues al ser mayor la velocidad del flujo sanguíneo,
tendremos menos artefactos de flujo.
El momento en el que se realiza esta adquisición podremos ajustarlo mediante el trigger delay,
time delay (TD) o retraso tras la onda R.
Ante una elevada FC,
el intervalo RR se acortará.
Así,
para obtener la imagen en sístole,
si la FC es > 75 lpm,
el TD será de 50 mseg y si la FC es < 75 lpm el TD será de 100 mseg.
El TD debe aumentar para realizar la adquisición en meso-telediástole.
-Supresión de la sangre y secuencia de pulsos: se debe conseguir un efecto máximo de sangre negra,
pues tanto la pulsatilidad de los vasos como el flujo lento,
no suprimido,
que brilla y puede mezclarse con las estructuras anatómicas estáticas,
degradan la imagen y limitan su valoración.
Para ello,
además de lo explicado,
se aplica siempre un doble pulso de 180 grados de inversión recuperación (doble IR): el primer pulso no selectivo del corte (azul en la imagen) seguido del segundo,
selectivo del corte que nos interesa (rosa en la imagen) .El efecto neto es que no se modifican los espines de la sección de corte de interés (flechas rosas),
mientras que los que están fuera (flechas azules),
influyendo los del flujo sanguíneo,
que irán entrando a nuestro corte de interés (flechas negras),
se invierten. Con el tiempo,
estos espines de fuera de nuestro corte se van a ir relajando hasta un momento en que,
incluso siendo excitados con subsecuentes pulsos de radiofrecuencia (RF),
generarán muy poca señal.
El tiempo desde el primer pulso de inversión hasta este momento corresponde al tiempo de inversión (TI).
Si aplicamos justo en ese instante el pulso de excitación de 90 grados,
seguido del tren de pulsos de refase de 180,
el flujo de sangre entrante no producirá señal.
La presencia de gadolinio iv puede interferir en la anulación de la señal de la sangre.
Tras cada pulso de refase de 180 grados obtendremos un eco o línea del espacio K.
Fig. 18
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Necesitaremos repetir el ciclo de pulsos en sucesivos intervalos RR hasta rellenar las líneas del espacio K necesarias para obtener una determinada imagen: por ejemplo,
para una matriz de 256 fases,
con un tren de ecos de 32 (32 líneas del espacio K),
necesitaremos 8 intervalos RR para rellenar nuestra matriz.
Si el TR aproximado,
para una imagen potenciada en T1,
es de 1000 ms (con una FC de 60 lpm),
necesitaremos 8000 ms,
es decir 8 segundos por imagen,
en apnea (es decir,
hay que sumar el tiempo que el paciente ventila entre las apneas en las que se realiza la adquisición).
Y así para cada una de las imágenes.
Por tanto,
son secuencias que requieren un largo tiempo de adquisición.
-POTENCIACIÓN EN T1 O T2:

Fig. 19
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Nuestro TR va a estar determinado por el intervalo RR,
y éste por la FC: a mayor FC,
menor duración del intervalo RR.
Para una secuencia potenciada en T1 emplearemos generalmente un intervalo RR y para una secuencia potenciada en T2,
dos intervalos RR,
para una FC de aproximadamente 60.
Si la FC es alta,
el TR disminuye y podríamos necesitar más de uno ó dos intervalos RR respectivamente para adquirir estas dos secuencias.
Hay que tener en cuenta que la potenciación en T1,
debido al TR,
tendrá características de intensidad de señal de densidad protónica,
lo que debe tenerse en cuenta a la hora de su interpretación.
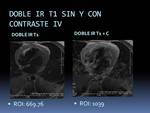
-Ejemplo de DOBLE IR T1:
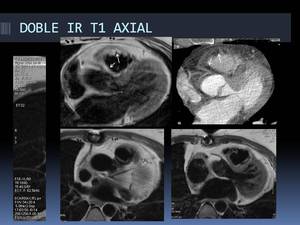
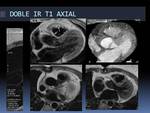
Fig. 20: Ejemplos de imágenes Doble IR T1 en plano axial: presencia de depósito graso en la pared del VD(flechas blancas en la imagen superior izquierda) correlativo con la imagen de TC (flechas blancas en la imagen superior derecha), con exquisito detalle tisular.
Puede verse también de forma muy precisa, el espesor pericárdico, la anatomía de los vasos mamarios internos y las arterias coronarias y la anatomía valvular pulmonar en esta otra paciente operada de atresia valvular (imágenes inferiores).
-Ejemplo de DOBLE IR T1 con contraste iv :
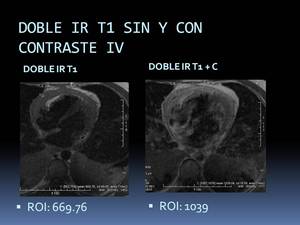
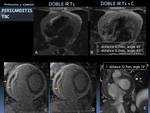
Fig. 21: Ejemplos de imágenes Doble IR T1 en plano axial sin y con contraste (+C) iv en un paciente con un pericardio marcadamente engrosado e hipercaptante, debido a una pericarditis aguda tuberculosa.
Tras administrar el contraste realizaremos la adquisición en el tiempo que esperamos desde la inyección hasta la adquisición del realce tardío, empezando a adquirir el doble IR T1+ C en el primer minuto tras la inyección.
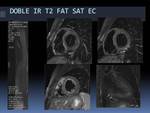
-Ejemplo de DOBLE IR T2:
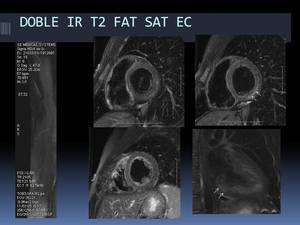
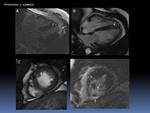
Fig. 22: Ejemplo de imágenes Doble IR T2 con saturación grasa (FAT SAT) en plano eje corto y en plano 2C AI-VI (imagen inferior derecha): presencia de edema subepicárdico-centromiocárdico en la pared lateral del VI (flechas blancas), en un paciente con miocarditis.
SECUENCIAS ECO DE GRADIENTE:
1.
SSFP:

Fig. 23
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
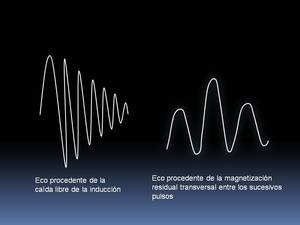
Fig. 24: Significado de los símbolos empleados en la figura anterior.
A diferencia de las secuencias eco de espín,
en lugar de dar un pulso de excitación que dé lugar a una angulación de 90 grados,
se da un pulso cuyo ángulo de basculación (flip angle) es menor a 90 grados,
generalmente en torno a 60 grados,
y en lugar de los pulsos de refase de 180 grados,
usa un gradiente bipolar (dos gradientes de igual magnitud pero de sentido opuesto: G+ y G-),
para obtener los múltiples ecos.
Estas secuencias SSFP (coherentes con refase total) emplean el eco procedente de la caída libre de la inducción,
que se genera tras cada pulso de RF,
sin destruir la magnetización residual transversal entre los sucesivos pulsos,
a diferencia de las antiguas secuencias eco de gradiente (incoherentes o spoiled GRE),
que destruían esta magnetización residual transversal antes de dar el siguiente pulso de RF. Por ello,
las nuevas secuencias SSFP son más independientes de la recuperación de la magnetización longitudinal entre pulsos y,
por tanto,
más independientes del tiempo,
pudiendo emplear TR y TE muy cortos y ganar velocidad de adquisición. Además,
a diferencia de las antiguas secuencias,
su señal no depende tanto de la perpendicularidad entre el plano de adquisición y la dirección del flujo sanguíneo ni de la velocidad del mismo, mejorando así la calidad de las imágenes (alto contraste-señal ruido).
Así,
el contraste miocardio-sangre es bueno en pacientes con disfunción sistólica.
Cuanto mayor es el ángulo alfa,
mayor es la relación contraste-señal ruido.
La intensidad de señal depende del ratio entre las propiedades T2 y T1 de la materia,
predominando las características T2.
Como inconveniente,
son más susceptibles a artefactos,
por ejemplo,
secundarios a inhomogeneidades del campo.
Además de la mejora de la secuencia en sí,
se ha ganado velocidad de adquisición gracias a la segmentación del espacio K: actualmente es posible obtener más de una línea del espacio K por intervalo RR,
generalmente en torno a 7 líneas en estas secuencias eco de gradiente (7 vistas por segmento) lo que multiplica por 7 la velocidad de adquisición.
Para una matriz de,
por ejemplo,
128 fases,
obtendremos 7 líneas del espacio K en un solo intervalo RR.
A mayor número de vistas por segmento se acorta tiempo de adquisición,
pero se pierde resolución temporal.
Puede mejorarse la resolución espacial mediante el relleno diferente del espacio K (echo sharing),
obteniendo dos veces el centro del espacio k.
Ejemplos de secuencias cine RM SSFP en planos 4C,
2C y EC:
Fig. 25
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Las imágenes SSFP nos proporcionarán,
empleando el método de cálculo de volúmenes SIMPSON,
datos de volúmenes ventriculares telediastólico,
telesistólico y fracción de eyección (mediante el trazado de la superficie endocárdica en telediástole y en telesístole),
de masa ventricular (mediante el trazado de la superficie endocárdica y epicárdica en telediástole) y el espesor miocárdico.
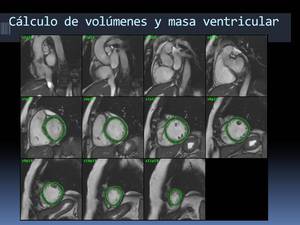
Fig. 26: Fase telediastólica con trazado endocárdico y epicárdico y medida del espesor miocárdico del VI en los 16 segmentos valorables.
Si adquirimos la secuencia cine en un plano transvalvular,
obtendremos información de la morfológica valvular,
como en el ejemplo de válvula Ao cuatricúspide (imágenes superiores de la Fig.
27) y podremos realizar medidas de áreas valvulares (planimetría) como en el caso de la figura (imágenes inferiores de la Fig.
27) importantes,
sobre todo,
en casos de estenosis valvular.
Para esto último se requerirá un grosor de corte fino (5-6 mm) y cortes contiguos o incluso solapados entre sí,
debiéndose englobar,
en la adquisición,
el área de mayor turbulencia valvular que veamos en secuencias cine o flujo sobre la que estemos planificando.
Fig. 27
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
2.
Secuencias tipo FLUJO o CONTRASTE DE FASE:

Fig. 28
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Esta secuencia nos ofrece imágenes implementadas en magnitud (información anatómica) y en fase (información de velocidad).
Gracias a la adquisición de la secuencia, inicialmente con un gradiente positivo y a continuación con un gradiente de igual magnitud y de polaridad inversa ,
podremos realizar una sustracción entre adquisiciones y así eliminar la información procedente de los espines de los tejidos estáticos.
Por tanto,
el cambio de la fase de los protones de los tejidos en movimiento es el que nos va a dar la señal,
es decir,
de los protones del flujo,
en este caso. El cambio en la angulación de estos espines es lo que la máquina va a codificar como velocidad.
La velocidad pico corresponde a un cambio de fase de 180 grados. Esto tendrá su traducción en las imágenes en fase,
de modo que la señal del flujo será hipo o hiperintensa según su dirección y será más o menos brillante según su velocidad.
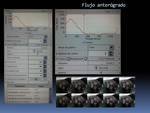
Si dibujamos un ROI rodeando el vaso de interés,
en cada una de las fases que hemos obtenido,
podremos obtener curvas de flujo,
como la de la figura y datos de volumen anterógrado (Fig. 29),
regurgitante (Fig. 30) y de velocidad pico sistólica y gradiente de presión a partir de ésta.
Dibujaremos el ROI en imágenes en magnitud,
recomendándose su rectificación en imágenes en fase para las imágenes sistólicas.
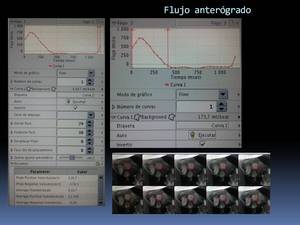
Fig. 29
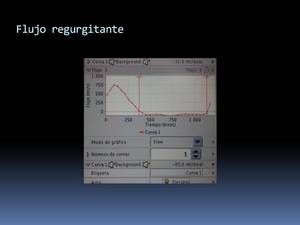
Fig. 30
Los parámetros con que se debe adquirir la secuencia para que la exactitud de las medidas sea máxima son los reflejados en la Fig.
28:
-Para obtener una adecuada resolución temporal necesitaremos VPS bajas y TE bajo,
y para una adecuada resolución espacial,
un FOV bajo.
-El plano de adquisición debe ser lo más perpendicular posible al vaso (por eso es recomendable planificar la adquisición a partir de dos planos perpendiculares del vaso de interés),
a 1cm de las valvas.
-La velocidad de codificación (velocity encoding) debe ser lo más ajustada posible a la velocidad máxima esperada para ese vaso,
sin que se produzca artefacto de aliasing,
cuya aparición debemos vigilar y corregir,
si lo hay,
en el momento de la adquisición ( Fig.
31).
Cuando la velocidad del flujo es mayor a la velocidad de codificación de la secuencia,
éste “exceso de velocidad” será interpretado como flujo en dirección contraria y nos lo muestra como un área “pixelada” en el centro del vaso,
de color inverso al flujo normal (imagen izquierda en la figura
Fig.
31).
Cuando la velocidad del flujo es mayor a la velocidad de codificación de la secuencia,
éste “exceso de velocidad” será interpretado como flujo en dirección contraria y nos lo muestra como un área “pixelada” en el centro del vaso,
de color inverso al flujo normal (imagen izquierda en la figura  Fig.
31,
con velocidad de codificación de 200 cm/s).
Debe corregirse hasta que desaparezca el artefacto,
lo cual se consiguió,
en el ejemplo de la figura,
con una velocidad de codificación de 300 cm/s.
Esta velocidad no debe ser mucho más alta que la velocidad pico sistólica real,
pues aumentará el ruido y esto nos dará datos erróneos de la medida de velocidad.
Por ello,
es recomendable que las correcciones de la velocidad de codificación,
en caso se aliasing,
de realicen con incrementos de velocidad de 20-30 cm/s.
Fig.
31,
con velocidad de codificación de 200 cm/s).
Debe corregirse hasta que desaparezca el artefacto,
lo cual se consiguió,
en el ejemplo de la figura,
con una velocidad de codificación de 300 cm/s.
Esta velocidad no debe ser mucho más alta que la velocidad pico sistólica real,
pues aumentará el ruido y esto nos dará datos erróneos de la medida de velocidad.
Por ello,
es recomendable que las correcciones de la velocidad de codificación,
en caso se aliasing,
de realicen con incrementos de velocidad de 20-30 cm/s.
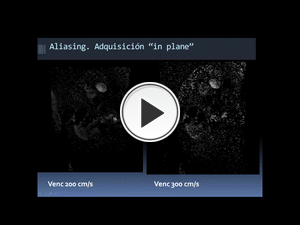
Fig. 31: Artefacto de aliasing con velocidad de codificación de 200 cm/s (vídeo de la izquierda) que se corrige al aumentar la velocidad de codifación, la cual hubo que aumentar hasta 300 cm/s (vídeo de la derecha). Son secuencias tipo contraste de fase con adquisición perpendicular a la dirección del flujo ("in plane").
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
La mayor parte de las secuencias tipo contraste de fase que pueden adquirirse en apnea emplean técnicas de adquisición prospectiva y las que se pueden adquirirse en respiración libre emplean técnicas de adquisición retrospectiva.
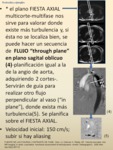
La adquisición puede realizarse "in plane": en un plano perpendicular a la dirección del flujo de interés (Fig.
31) ó “through plane”: en un plano paralelo a la dirección del flujo de interés (Fig.
32),
sirviéndonos esto último para valorar el área de mayor turbulencia y sobre ésta realizar medidas de velocidad o dirigir la adquisición “in plane”,
lo cual nos permitirá obtener datos más exactos de velocidad máxima y de flujo.

Fig. 32: La secuencia contraste de fase se ha planificado sobre la secuencia cine TSVI, cortando al VI y a la Ao, obteniendo un plano 2C VI-Ao, paralelo a la dirección del flujo ("through plane"), en este caso en una paciente con insuficiencia aórtica. Puede realizarse para valorar cualquier flujo turbulento (estenosis valvulares, estenosis vasculares-coartación aórtica, estenosis de arterias pumonares-, etc). Con esta secuencia se pueden realizar medidas de velocidad o servir para dirigir la adquisición “in plane” hacia la zona de mayor turbulencia , lo que nos permitirá obtener datos más exactos de velocidad máxima y, por tanto, de gradiente, importante sobre todo en estenosis.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Las secuencias tipo flujo nos permitiran cuantificar valvulopatías (estenosis,
regurgitación),
valorar estenosis vasculares,
obtener curvas de flujo en cualquier vaso arterial o venoso ( Fig.
33),
curvas de llenado ventricular,
etc.
Fig.
33),
curvas de llenado ventricular,
etc.
3.
Secuencias CONTRASTE DE FASE tipo realce tardío.
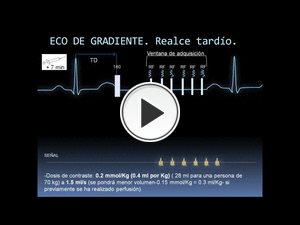
Fig. 34
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Esta secuencia debe adquirirse,
como términos generales,
entre 5 y 25 minutos después de la administración del contraste iv.
El contraste queda acumulado en el espacio extracelular,
el cual está aumentado en el miocardio dañado.
Por ello,
el contraste se acumula en mayor cuantía y tarda más en ser lavado del miocardio dañado que del sano,
y esto es lo que nos permitirá diferenciarlos.
Las secuencias tipo "realce tardío" son secuencias eco de gradiente inversión recuperación potenciadas en T1,
adquiridas con la técnica de segmentación del espacio K. Adquirimos en la fase diastólica del ciclo cardíaco (secuencia monofásica),
lo cual ajustaremos mediante el trigger delay,
que tendremos que variar en función de la FC,
pero que suele estar en torno a 350 ms.
Previamente a los sucesivos pulsos de RF,
daremos un pulso de inversión de 180 grados en el corte de interés,
que invertirá todos los espines.
A partir de este instante,
se irán relajando los protones del miocardio sano (curva azul de la fig.
34) pero a ritmo diferente a los del miocardio dañado (curva amarilla de la fig.
34),
llegando un momento preciso en el que los espines del miocardio sano apenas nos devolverán señal si aplicamos los pulsos de RF.
Adquiriremos la secuencia completa en torno a ese momento,
en el cual serán mayores las diferencias de contraste entre el miocardio sano y dañado.
El tiempo desde el pulso de 180 grados y este momento óptimo de adquisición es el tiempo de inversión (TI),
que suele estar entre 175-250 ms para el miocardio del VI (es menor para el miocardio del VD) y debe ser muy bien seleccionado.
Para ello,
inmediatamente antes de lanzar la secuencia definitiva de realce tardío,
adquiriremos imágenes de prueba,
con las mismas características técnicas que el realce tardío definitivo pero adquiriendo un sólo corte (por ejemplo,
en un plano EC en el tercio medio del corazón),
con diferentes TI,
dentro del intervalo 175-250 ms (Test).
El TI óptimo será el que nos muestre una imagen con el miocardio más “negro” y la cavidad ventricular más “blanca”,
como en la última imagen de TI que aparece en la animación de la Fig.
34.
Inmediatamente tras determinar nuestro TI,
lo aplicaremos a nuestra secuencia definitiva de realce tardío (multicorte) y adquirimos.
El TI va aumentando conforme pasa el tiempo,
por lo que se debe ajustar de nuevo si se realiza una nueva adquisición más tardía.
Generalmente realizamos el realce tardío en plano eje corto ,
copiando la planificación de la secuencia cine RM en EC para tener la correlación entre ambas,
y complementamos adquiriendo otra secuencia realce tardío en otro plano adicional (2C,
4C,
TSVI ó un plano perpendicular al área de realce presente en el plano EC).
El tiempo de adquisición (ventana de adquisición) suele ser menor a 200 ms.
4.
Secuencia PERFUSIÓN DE PRIMER PASO.
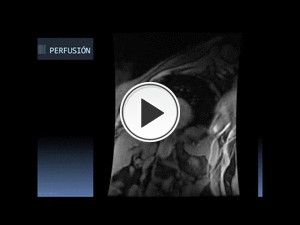
Fig. 35
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Son secuencias muy rápidas,
generalmente de tipo ecoplanar,
que a veces se combinan con técnicas de adquisición eco de gradiente (secuencias híbridas),
potenciadas en T1.
Se aplica un pulso preparatorio saturación-recuperación,
similar a los IR vistos en secuencias anteriores,
pero con un ángulo alfa de 90 grados.
La adquisición es en tiempo real,
durante 40-50 latidos,
adquiriendo 3-4 cortes por latido.
Adquisición:

Fig. 36
La valoración de la perfusión de primer paso debe realizarse en los primeros 20-25 segundos tras la llegada del contraste al corazón; en momentos más tardíos,
estaremos valorando otras características farmacocinéticas del contraste diferentes a la perfusión de primer paso.
Su principal utilidad es para la valoración de defectos de perfusión de origen isquémico,
realizados bajo estrés farmacológico,
aunque no es exclusiva.
5.
Secuencia ANGIOGRAFÍA TORÁCICA.

Fig. 37: Ejemplo de angiografía torácica multifásica: con una misma embolada de contraste podemos obtener múltiples fases para poder valorar así varios lechos vasculares, sin radiación, como supondría un estudio multifásico en el TC, dato importante sobre todo en pacientes con cardiopatías congénitas, susceptibles de llevar a cabo múltiples seguimientos por imagen, como el paciente de la figura, operado de Transposición de grandes arterias mediante la técnica de Mustard.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
Planificación y características de la secuencia:

Fig. 38
- PROTOCOLOS Y EJEMPLOS (CASOS)
El objetivo principal de este trabajo ha sido la creación de un manual de protocolos de adquisición de estudios de cardio-RM.
Tras revisar y unificar la bibliografía acerca de los protocolos de cardioRM,
tanto protocolos de acceso on-line como de artículos,
libros y manuales de protocolos genéricos y específicos de nuestro equipo de RM,
y utilizando nuestra experiencia en distintos equipos de RM (1,5 T) contrastada con la de distintos técnicos de aplicaciones, hemos elaborado un manual para la adquisición de los estudios de cardioRM,
enfocado a nuestro equipo actual (GE Signa®HDx 1,5T),
aunque aplicable a cualquiera.
Pretendemos que el flujo de trabajo sea sencillo y rápido,
con una parte común a la práctica totalidad de los estudios de cardioRM (protocolo estándar),
y una parte más específica según la patología de sospecha o los hallazgos encontrados por el radiólogo en la primera parte (protocolo “específico”).
Hemos conseguido así una mayor independencia del personal técnico,
siendo,
no obstante,
imprescindible el control de calidad por el radiólogo de todas las secuencias adquiridas.
Tras el inicial entrenamiento técnico supervisado,
estamos logrando acortar tiempos totales y tiempo directo de adquisición por el radiólogo,
y estandarizar la adquisición de cara a posibles controles evolutivos,
comparaciones,
elaboración de trabajos,
etc.
PROTOCOLOS ELABORADOS:
-PROTOCOLO ESTÁNDAR

Fig. 40
Ejemplos:
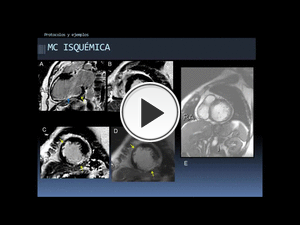
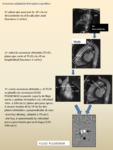
Fig. 41: Ejemplo de aplicación del protocolo estándar. Miocardiopatía isquémica crónica.Realce tardío en plano 2C (A) y EC (B-C) en fase (A-C) y magnitud (D), donde vemos áreas de realce transmural en el segmento inferior del tercio medio (flecha azul) y subendocárdico no transmural en el segmento inferior de la base, anterolateral del tercio medio, e inferior y septal del ápex (flechas amarillas) por necrosis miocárdica isquémica. Se correlacionan, en la secuencia cine EC (vídeo de la derecha) con adelgazamiento y acinesia de la pared del miocardio del VI en las zonas de infarto, dilatación telediastólica y telesistólica y FE VI (fracción de eyección del VI) diminuida (valores no mostrados). También realza el músculo papilar inferior del VI, que está adelgazado.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
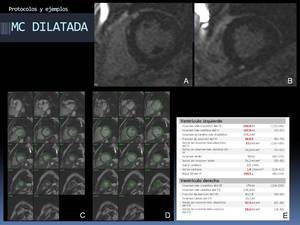
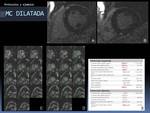
Fig. 42: Ejemplo de aplicación del protocolo estándar. Miocardiopatía dilatada. Post-proceso de la secuencia cine RM en telesístole (C) y telediástole (D) con los trazados de la superficie endocárdica y epicárdica en D y endocárdica en C. Aumento de los volúmenes telediastólicos y telesistólicos absolutos del VI y normalizados del VD (post-proceso no mostrado del VD). Focos centromiocárdicos de realce tardío (realce tardío en EC en imágenes A y B), de características no isquémicas; este hallazgo puede verse asociado a la propia miocardiopatía dilatada, habiendo sido descrito en aproximadamente un 20% de los casos.
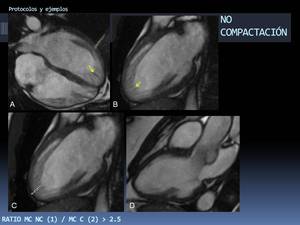
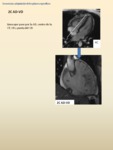
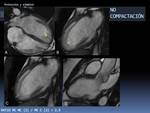
Fig. 43: Ejemplo de aplicación del protocolo estándar. Miocardiopatía no compactada. Varón joven, deportista federado. Padre fallecido de IAM (confirmación en necropsia). FE del 50-55% en eco y BIRD.
Imágenes extraídas de secuencias cine RM 4C (A) y 2C (B y C) donde se aprecia un aumento de la trabeculación del miocardio del tercio medio y apical del VI (flechas) con un ratio entre el miocardio no compactado / compactado > 2.5 en la telediástole (C). Véase la diferencia con otro paciente que muestra una trabeculación normal del VI en esta secuencia (D). El paciente no era hipertenso ni sufría de vavulopatía aórtica ni de miocardiopatía dilatada.
Fig. 44: Ejemplo de aplicación del protocolo estándar. Síndrome de Tako-Tsubo o miocardiopatía de estrés. Mujer de 61 años con antecedentes psiquiátricos. Acude por dolor torácico, elevación de troponinas y cambios ECG sugestivos de IAM anterolateral. Coronarias sanas en angiografía. Ecocardio inicial con FEVI 43% y volumen latido de 55 ml.
La RM muestra una hipocinesia del tercio medio y apical e hipercontractilidad basal (“abalonamiento” en sístole del tercio medio y apical) en las secuencias cine RM 2C (A) hallazgo que es la clave para el diagnóstico. Mínimo edema en el segmento anterior del tercio medio evidente en esta secuencia potenciada en T2 complementaria de la secuencia potenciada en difusión(C), que también puede estar presente en esta entidad; no se manifestó en el doble IR T2 FAT SAT EC habitual(no mostrada). No se apreciaron áreas de realce tardío (B). La ecocardiografía de control,realizada a las pocas semanas, mostró una contractilidad normal.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
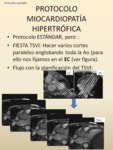
-PROTOCOLO MIOCARDIOPATÍA HIPERTRÓFICA
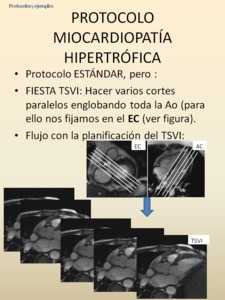
Fig. 45: Con respecto a las modificaciones del protocolo estándar, ampliamos la valoración de la totalidad del TSVI, no limitándonos a un solo corte central, tanto en secuencias cine RM como en secuencias Flujo. Nos permitirán valorar turbulencias en todo el TSVI secundarias a una probable obstrucción por hipertrofia septal y movimiento sisólico anterior de la valva anterior de la mitral (SAM) asociado. Estos hallazgos, importantes en esta entidad, podrían no detectarse en un solo corte central en el TSVI.
-Ejemplos:
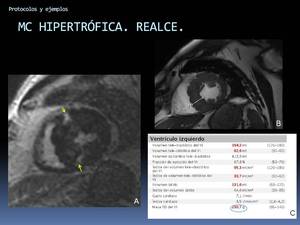
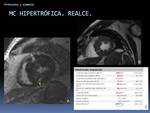
Fig. 46: Ejemplo de aplicación del protocolo miocardiopatía hipertrófica. Miocardiopatía hipetrófica con áreas de realce centromiocárdico (no isquémico) en la zona de unión del VI y VD (flechas) en A. Podemos dar datos de espesor de segmentos cardíacos (B) y de masa del VI (C), aumentada en este paciente.
Fig. 47: Ejemplo de aplicación del protocolo miocardiopatía hipertrófica. Miocardiopatía hipetrófica septal con obstrucción secundaria del TSVI y movimiento sisólico anterior de la valva anterior de la mitral, que dan lugar a las turbulencias sistólicas en el TSVI (flecha azul) y de insuficiencia mitral (flecha amarilla), en las imágenes del TSVI multicorte-multifase. Las imágenes A-D han sido extraídas de las secuencia TSVI (E).
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
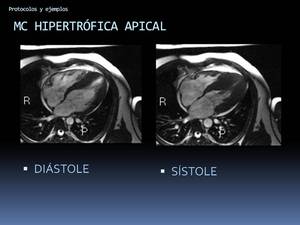
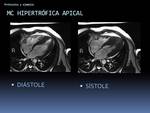
Fig. 48: Ejemplo de aplicación del protocolo miocardiopatía hipertrófica. Miocardiopatía hipertrófica apical.
Fig. 49: Ejemplo de aplicación del protocolo miocardiopatía hipertrófica. Varón joven que debuta con ACV. Coronarias sanas en angio-TC coronario. En ecocardio, trombo en el VI (no presente en el posterior estudio de RM) y aneurisma del VI.
Aneurisma apical del VI visible en las secuencias cine 2C (A) y 4C (B). Continúa en la siguiente figura.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
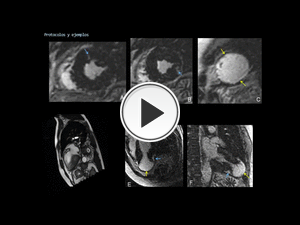
Fig. 50: Continuación de la figura anterior. Secuencias realce tardío en un plano EC (A-C), TSVI (E) y 2C (F): podemos observar el realce centromiocárdico-subepicárdico no isquémico parcheado, en el tercio medio del VI (flechas azules) y el de la pared fibrótica del aneurisma apical del VI (flechas amarillas). Podemos correlacionar la secuencia realce tardío en plano TSVI (E) con la secuencia cine TSVI (D). El desarrollo de aneurismas apicales en el VI se ha descrito en algunos casos de miocardiopatía hipertrófica, a lo cual apoya la distribución del realce y la ausencia de lesión coronaria en el angio-TC.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
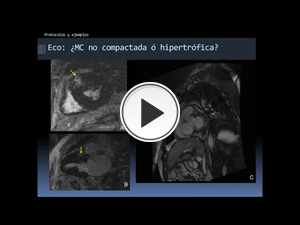
Fig. 51: Ejemplo de aplicación del protocolo miocardiopatía hipertrófica. En este paciente en el que la ecografía ofrecía dudas acerca de si se trataba de una miocardiopatía hipertrófica o no compactada, la RM muestra una severa hipertrofia miocárdica septal con realce centromiocárdico en la zona de mayor hipertrofia, en el tercio basal y medio, a nivel de la unión anterior del VI y VD (flechas en las secuencias tipo realce tardío en EC-A-y 2C-B-). En la imagen cine RM en EC (C) también puede identificarse la presencia del realce (fue adquirida después de las secuencias de realce tardío).
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
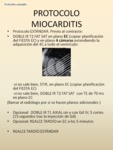
-PROTOCOLO MIOCARDITIS

Fig. 52: Con respecto a las modificaciones del protocolo estándar, añadimos secuencias para valoración de edema, doble IR T2 FAT SAT, en plano EC y 4C (u otro plano adicional).
Puede realizarse un DOBLE IR T1 sin y con GD IV (15 segundos tras la inyección de Gd) y comparar la captación del miocardio con respecto a la del músculo, siendo anormal si ésta es igual o mayor a 4. También puede realizarse una adquisición del realce tardío antes, a los 5 minutos, pues hay trabajos que muestran que el realce tardío en la miocarditis en ese momento es equiparable al adquirido más tarde.
-Ejemplo:
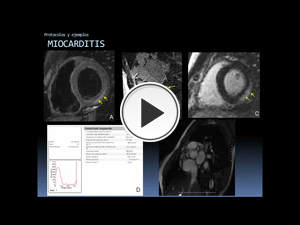
Fig. 53: Ejemplo de aplicación del protocolo miocarditis. Varón joven, consumidor esporádico de cocaína, con clínica sugestiva de miocarditis pero, dados los antecedentes, se requería descartar un IAM.
A. Secuencia Doble IR T2 FAT SAT en EC; B: realce tardío en plano perpendicular al área de realce visible en C; C: realce tardío en EC; D: resultados funcionales del VI; D: cine RM en EC.
La RM muestra edema (flechas amarillas en A) coincidente con áreas de realce tardío (flechas amarillas en B y C) de distribución subepicárdica en la región inferolateral, predominantemente basal, compatibles con miocarditis. Función sistólica y volúmenes del VI, normales.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
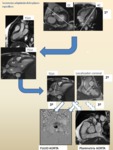
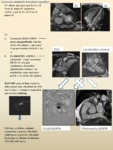
-PROTOCOLO DISPLASIA ARRITMOGÉNICA DEL VD (DAVD)
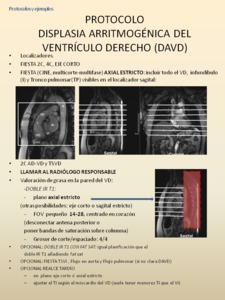
Fig. 54: Lo dirigimos sobre todo a la valoración del VD, mediante secuencias cine RM 4C, EC y axial estricto, siendo más exacta la valoración de los volúmenes del VD cuando la medición se realiza en la secuencia cine axial. Las saculaciones discinéticas, características de la enfermedad, podrán valorarse tanto en el EC como en el plano axial de forma complementaria. El VI podrá valorarse con los planos 4C, EC junto con el 2C AI-VI.
La secuencia doble IR en plano axial estricto nos permitirá valorar depósito graso en la pared del VD y correlacionarlo con la presencia de saculaciones discinéticas en la secuencia cine axial. Opcionalmente se pueden añadir secuencias doble IR axial FAT SAT que ayuden a confirmar la presencia de grasa, aunque no suelen ser necesarias.
La secuencia realce tardío en eje corto, dirigida a la valoración del VD (TI más cortos que para el VI) permitirá valorar áreas de realce por fibrosis. Opcionalmente pueden adquirirse secuencias cine en plano TSVI , Flujo en aorta y Flujo pulmonar si en la primera parte no hay claros datos de DAVD, que nos permitirán valorar globalmente cavidades cardíacas derechas e izquierdas y posibles cortocircuitos, teniendo en conjunto todos los datos posibles para valorar miocardiopatías con afectación de cavidades derechas, izquierdas o ambas.
-Ejemplo DAVD:
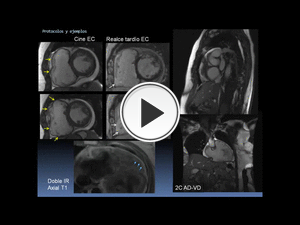
Fig. 55: Ejemplo de aplicación del protocolo DAVD. Mujer de 45 años, que sufre episodio de palpitaciones seguidas de mareo, dolor torácico y diaforesis. Varios episodios similares las últimas semanas, y el último con pérdida de conciencia, sin pulsos, hipotensa. Se objetiva taquicardia ventricular en el ECG.
La RM pone de manifiesto adelgazamiento de la pared del VD y la presencia de saculaciones discinéticas en la pared libre del VD (flechas amarillas) visibles en los vídeos de las secuencias cine en EC y 2C AD-VD (imágenes de la derecha). Probable realce tardío en la pared libre del VD, de difícil valoración por la delgada pared del VD, y en el miocardio del VI (flechas blancas). Depósito de grasa (flechas azules) en la pared libre del VD. Hipocinesia del VD, dilatación de cavidades derechas y disfunción sistólica biventricular.
La RM aporta criterios suficientes para el diagnóstico definitivo de DAVD. A la paciente le fue implantado un DAI.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
-PROTOCOLO MIOCARDIOPATÍA RESTRICTIVA VS PERICARDITIS CONSTRICTIVA

Fig. 56: A las secuencias del protocolo estándar añadimos una secuencia EC centrada en el tercio basal, en inspiración y si es posible, en secuencias en tiempo real, que hará más manifiesta la verticalización del septo interventricular (evidente sobre todo en el primer latido en inspiración mantenida), hallazgo que caracteriza a la pericarditis constrictiva y que permite diferenciarla de la miocardiopatía restrictiva, además del resto de características diferenciadoras pericárdicas y miocárdicas (ver figura 58); la sobrecarga de cavidades derechas o el cor pulmonale también pueden provocar esta alteración septal, pero es patognomónica de la pericarditis constrictiva cuando se modifica con la inspiración.
La secuencia cine axial estricto será útil para valorar:
-Diámetro de Vena Cava Superior e Inferior, no valorados en otras secuencias.
-Complemento para valorar:
-Grosor de pericardio
-Diámetro de aurículas
-Diámetros diastólico y sistólico de ventrículos
-Morfología de los ventrículos, de los surcos A-V y su relación con el pericardio
-Cálculos de volúmenes ventriculares
-Presencia de derrame pleural.
Si se sospecha una miocardiopatía siderótica hemos de añadir secuencias T2* (ver protocolo de miocardiopatía siderótica).
La secuencia doble IR axial sin y con contraste permite valorar la anatomía y grosor del pericardio.
Las secuencias opcionales tipo flujo de la figura 57 sirven para valorar la función diastólica ventricular, que puede estar alterada en ambas patologías.
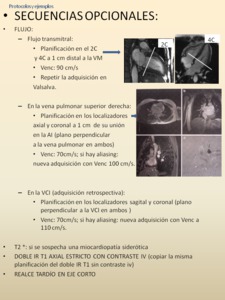
Fig. 57: Ver pie de foto de la figura 56.
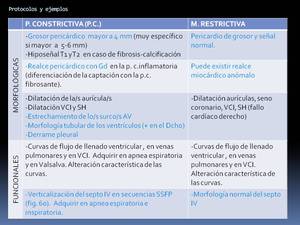
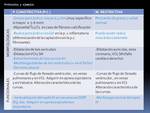
Fig. 58: Características morfológicas y funcionales y diferencias entre la MIOCARDIOPATÍA RESTRICTIVA y la PERICARDITIS CONSTRICTIVA. El texto coloreado en azul representa lo más significativo para su diferenciación.
-Ejemplo:
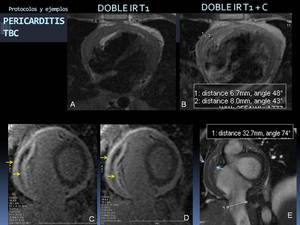
Fig. 59: Ejemplo de aplicación del protocolo miocardiopatía restrictiva vs pericarditis constrictiva. Continúa en la figura siguiente.
Varón de 24 años con febrícula, tos y astenia de 20 días de evolución. Punción de derrame pleural compatible con derrame pleural tuberculoso. Engrosamiento pericárdico marcado de las dos hojas(distancias medidas en B), hipercaptante tras administrar gadolinio, evidente en las secuencias de realce tardío (flechas en C y D) que no puso de manifiesto hipercaptación miocárdica. En la imagen obtenida de la secuencia cine RM en EC (E) se aprecia una dilatación de la VCI (entre cursores), y el engrosamiento de las hojas pericárdicas (flechas azules).
En las secuencias cine RM en plano EC (vídeo de la izquierda en la figura siguiente) se aprecia el marcado engrosamiento pericárdico, la morfología tubular de los ventrículos secundaria a la “coraza” pericárdica y la verticalización del septo interventricular debido al fenómeno de interdependencia ventricular, hallazgo que se hace más manifiesto en inspiración y ayuda a la diferenciación con una miocardiopatía restrictiva. Compárese con un corazón normal (vídeo de la derecha en la figura siguiente).
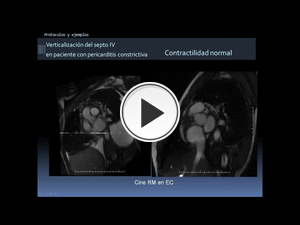
Fig. 60: Ejemplo de aplicación del protocolo miocardiopatía restrictiva vs pericarditis constrictiva. Continuación de la figura anterior.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
-PROTOCOLO MIOCARDIOPATÍA SIDERÓTICA

Fig. 61
-PROTOCOLO MIOCARDIOPATÍA DESCONOCIDA

Fig. 62
-PROTOCOLO IAM

Fig. 63: Al protocolo estándar añadimos secuencias doble IR T2 FAT SAT para valoración de edema miocárdico, perfusión en reposo y realce tardío precoz para la valoración de trombos y obstrucción microvascular.
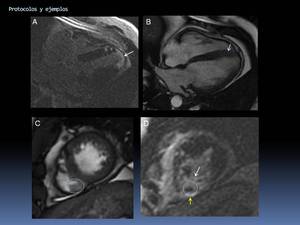
Fig. 64: Ejemplo de aplicación del protocolo IAM. Infarto miocárdico agudo con afectación transmural apical del VI y afectación apical del VD (flechas blancas y amarilla, respectivamente, en las secuencias realce tardío en plano 4C –A- y EC -D-), edema miocárdico (flecha azul) que es valorable en estas secuencias cine RM en plano 4C (B) (doble IR T2 no mostrado) y trombo en el VD en la secuencia cine eje corto (C) y en el realce tardío en EC (D) (círculo azul).
-PROTOCOLO MASA CARDÍACA

Fig. 65: Para valoración de trombos, conviene emplear un TI largo (500-600 ms) con gating cada 3-4 intervalos RR, que permite una valoración mejor de los trombos y ayudará a diferenciar trombo y tumor.
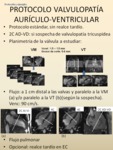
-PROTOCOLO VALVULOPATÍA AURÍCULO-VENTRICULAR
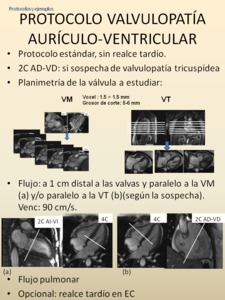
Fig. 66: Además del protocolo estándar, en la valoración valvular mitral y tricuspídea, se recomienda realizar cortes cine RM contiguos de 5-6 mm alineados en la dirección del flujo y que corten la línea principal de coaptación de la válvula, moviéndonos desde la comisura más superior hacia la inferior. La orientación puede ser la del TSVI para la mitral y axial para la tricúspide. También deben realizarse secuencias tipo contraste de fase para valoración de velocidad y flujo, perpendiculares al flujo y distales a las valvas.
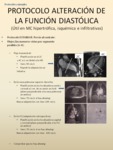
-PROTOCOLO ALTERACIÓN DE LA FUNCIÓN DIASTÓLICA
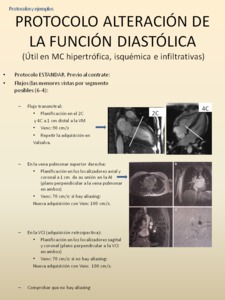
Fig. 67
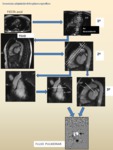
-PROTOCOLO CARDIOPATÍA CONGÉNITA

Fig. 68: Comenzamos con una secuencia cine RM axial estricto, que nos permite tener una primera valoración anatómica y funcional, en una sola secuencia, de este tipo de patología compleja, a partir de la cual dirigiremos la planificación según el tipo de cardiopatía de que se trate. Siempre completaremos con las secuencias necesarias para poder adquirir el flujo en la aorta y en la pulmonar, para valorar posibles cortocircuitos. La mayoría de las veces se asociará a una adquisición angiográfica multifásica.
-Ejemplo:
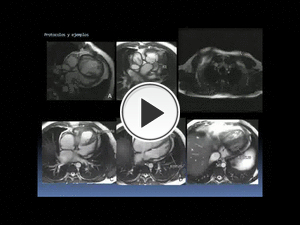
Fig. 69: Ejemplo de aplicación del protocolo Cardiopatía Congénita. Continuación en la siguiente figura.
El cine RM axial estricto (vídeo de la derecha, con imágenes estáticas extraídas del mismo: A-G) nos permite tener una primera valoración anatómica y funcional en una sola secuencia, en este paciente con una TGA tratada con cirugía de Mustard (K). Vemos el origen anómalo de la A. pulmonar desde el VI (A) y el de la Ao desde el VD (B) , dilatado así como que no existe una discordancia A-V ni un situs inversus, gracias a los marcadores anatómicos de cada una de las cámaras cardíacas, evidenciables en esta secuencia (imágenes A-G). Se objetivan también turbulencias correspondientes a una CIA y a una IT.
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
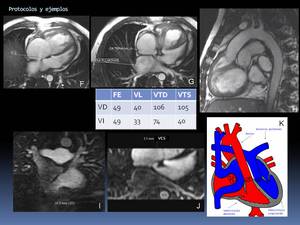
Fig. 70: Ver pie de foto de la figura anterior.
La secuencia cine sagital puro nos permite valorar la anatomía, visualizándose el origen anómalo de la aorta desde el VD.
La valoración funcional puso de manifiesto una insuficiencia tricuspídea, una disfunción sistólica biventricular y un QP/Qs de 27/28: 0,96.
Las secuencias angiográficas adquiridas en coronal, con reconstrucciones multiplanares, nos permiten valorar el diámetro de la comunicación VCI-cavidades izquierdas, de 16 mm (I) y el de la comunicación VCS-cavidades izdas, 5 mm (J) lo que sugiere estenosis de ésta última, siendo, junto con la disfunción del VD, las complicaciones más frecuentes en esta patología, ambas evidenciables mediante RM.
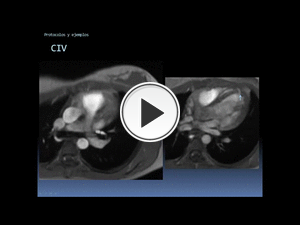
Fig. 71: Ejemplo de aplicación del protocolo Cardiopatías Congénitas. CIV tipo muscular (flecha azul). Véase la diferencia de calidad de esta secuencia eco de gradiente incoherente (spoiled), en el vídeo de la izquierda, más sensible a los artefactos de flujo, que las SSFP de las secuencias cine RM del resto de ejemplos. Se empleó en busca de algún flujo turbulento secundario a la CIV, que la pusiera de manifiesto (no fue demostrado).
 Enlace a vídeo de alta calidad en Youtube
Enlace a vídeo de alta calidad en Youtube
-PROTOCOLO AORTA TORÁCICA

Fig. 72
-PROTOCOLO VALVULOPATÍA AÓRTICA

Fig. 73
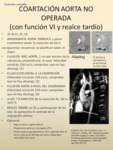
-PROTOCOLO COARTACIÓN AÓRTICA NO OPERADA
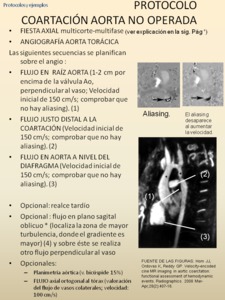
Fig. 74
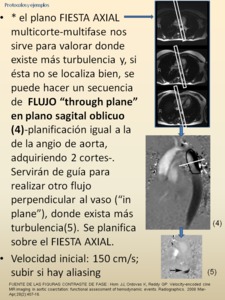
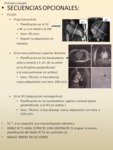
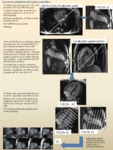
Fig. 75: PROTOCOLO COARTACIÓN AORTA NO OPERADA (continuación).
-PROTOCOLO COARTACIÓN AÓRTICA NO OPERADA (CON FUNCIÓN VI Y REALCE TARDÍO)
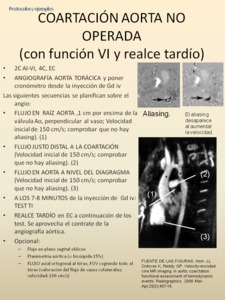
Fig. 76
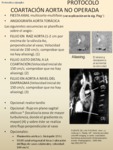
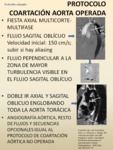
-PROTOCOLO COARTACIÓN AÓRTICA OPERADA
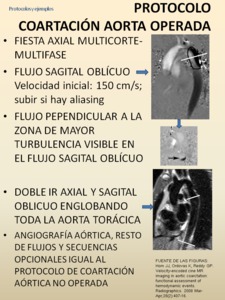
Fig. 77
-PROTOCOLO SOSPECHA AORTITIS

Fig. 78
-PROTOCOLO VENAS PULMONARES PRE Y POST-ABLACIÓN

Fig. 79