El trasplante renal (TR) es el tratamiento de elección para la enfermedad renal en estadios finales y proporciona una mejor supervivencia a largo plazo y una mejor calidad de vida en comparación con la hemodiálisis o diálisis peritoneal. El diagnóstico precoz de las complicaciones mejora el pronóstico general ya que muchas de ellas son potencialmente tratables.
Tenemos varias herramientas de diagnóstico que nos permiten detectarlas como la ecografía (US),
la tomografía computerizada helicoidal (TC),
la resonancia magnética (RM) y la arteriografía.
Las de mayor valor son aquellas que no son invasivas (debido a sus propias complicaciones),
sensibles,
no ionizantes (debido a la necesidad de controles repetidos) y no requieren la administración de contraste intravenoso yodado o gadolinio (debido al riesgo de nefropatía inducida por contraste y la fibrosis sistémica nefrogénica) en pacientes con disfunción renal.
Nuestro objetivo es mostrar las complicaciones,
que agruparemos vasculares,
urológicas,
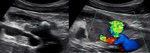
colecciones perirrenales y anormalidades parenquimatosas y mostraremos su cronología gráficamente (una barra azul sobre una amarilla) y describiremos los avances con diferentes técnicas,
tales como ecografía con contraste (CEUS) y RM funcional (RM dinámica,
difusión,
BOLD y ASL).
Complicaciones vasculares
Estenosis de la arteria renal

Fig. 40
Es la complicación vascular más frecuente en el trasplante renal (hasta 10% de los casos y menos frecuente en trasplante pediátrico en bloc) y generalmente es secundaria a la aterosclerosis,
o como complicación de la cirugía. La estenosis ocurre más frecuentemente en el lugar de la anastomosis o arteria proximal y en la anastomosis término-terminal. Se debe sospechar ante hipertensión arterial severa refractaria a tratamiento médico en ausencia de rechazo del injerto,
obstrucción o infección e hipertensión asociada a disfunción del injerto no explicada.
Hallazgos de imagen:
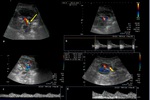
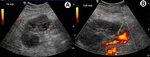
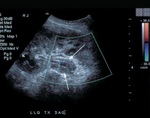
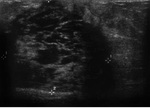
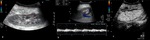
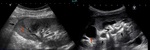
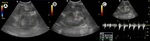
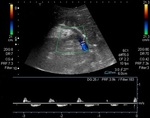
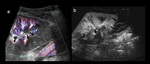
- US ( Fig. 1 )
-
- Doppler Color
-
- Área focal de turbulencias.
- Duplex Doppler
-
- Pico sistólico> 200-250cm/s.
- Ratio post-PS (relación del pico sistólico en la arteria renal con el pico sistólico en arterias interlobares)> 13.
- Índice de resistencia <0.5.
- Ratio de velocidad en la estenosis respecto al segmento preestenótico > 2-4:1.
- Tiempo de aceleración> 0,07 seg.
- Índice de aceleración <300cm/s2.
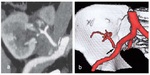
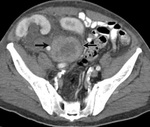
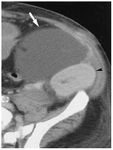
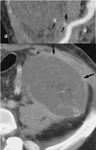
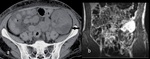
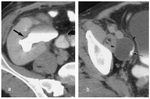
- TC con contraste (TC) ( Fig. 2 )
-
- Muestra la estenosis morfológicamente y permite reconstrucciones multiplanares e interpretación de volumen.
- Menos propenso a artefactos debido a los clips postoperatoris que la RM.
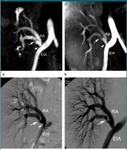
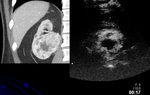
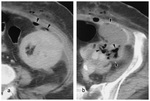
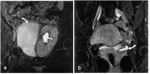
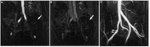
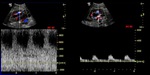
- RM ( Fig. 3 )
-
- Arteriografía con RM (ARM) con gadolinio o con secuencias en estado estacionario con precesión libre (SSFP) sin gadolinio.
- Comparable a la arteriografía diagnóstica.
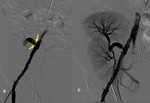
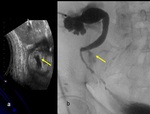
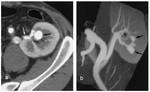
- Arteriografía ( Fig. 4 )
-
- Patrón oro que también permite tratamiento con angioplastia transluminal percutánea (ATP) con o sin stent.
Trombosis de la arteria renal

Fig. 41
Complicación poco frecuente (<1%,
relativamente con más frecuencia en pacientes con trasplante pediátrico en bloc),
que suele ser secundaria a la técnica quirúrgica,
a rechazo hiperagudo,
necrosis tubular aguda (NTA) e hipercoagulabilidad. Clínicamente se presenta como anuria en el período postoperatorio temprano.
Hallazgos de imagen:
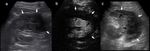
- US ( Fig. 5,
Fig. 6 )
-
- Doppler color y Doppler Duplex.
-
- Ausencia de flujo arterial y venoso.
- CEUS.
-
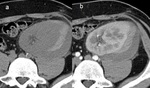
- TC ( Fig. 7 )
-
- Puede demostrar directamente el trombo en la arteria renal en casos que el US no es concluyente.
- El parénquima renal no realza a excepción de la cápsula.
- RM (ARM) ( Fig. 8,
Fig. 9 )
-
- Obstrucción de la arteria renal sin realce parenquimatoso,
también en US no concluyentes.
Trombosis de la vena renal

Fig. 42
Como la trombosis de la arteria renal,
es una complicación poco frecuente (<4%,
relativamente más frecuentes en trasplante pediátrico en bloc) y suele ser consecuencia de complicaciones quirúrgicas,
hipovolemia,
hipercoagulabilidad,
rechazo agudo y compresión venosa (por colecciones perirrenales,
síndrome de compresión por la arteria ilíaca en los injertos colocados en la fosa ilíaca izquierda). Se manifiesta clínicamente con un inicio súbito de distensión en el injerto,
oliguria,
proteinuria y deterioro de la función renal.
Hallazgos de imagen:
- US ( Fig. 10 )
-
- Modo B (inespecífica).
-
- Aumento del tamaño del injerto con seno renal más delgado e hipoecoico.
- Puede visualizarse material ecogénico en la vena renal.
- Doppler color.
-
- Ausencia de flujo en la vena renal.
- Disminución del flujo venoso.
- Duplex Doppler.
-
- Flujo arterial diastólico inverso en las arterias renales o intrarrenales.
- TC. Precisión similar a US.
-
- Defecto de repleción en la vena renal.
- Nefrograma tardío y persistente.
- RM (RM). Precisión similar a US.
-
- Defecto de repleción en la vena renal.
- Nefrograma tardío y persistente.
Infarto segmentario
Los infartos segmentarios se producen debido a trombosis de las arterias intrarrenales.
Hallazgos de imagen:
- US ( Fig. 11 )
-
- Modo B.
-
- Se pueden visualizar áreas hipoecoicas.
- Doppler color.
-
- Defectos de perfusión cuneiformes.
- CEUS (más sensible que el Doppler).
-
- Áreas cuneiformes sin realce.
- TC ( Fig. 12 )
-
- Áreas cuneiformes sin realce.
- RM (con gadolinio) ( Fig. 12 )
-
- Áreas cuneiformes sin realce.
Complicaciones postbiopsia
Estas complicaciones inclueyn las fístulas arteriovenosas y los pseudoaneurismas,
por lo que decidimos incluirlas en el grupo de complicaciones vasculares.
Se observan en menos del 18% de los procedimientos y por lo general tienen un curso autolimitado,
puede tener hematuria macroscópica y con frecuencia se resuelven espontáneamente.
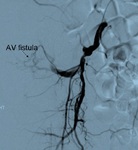
- Fístula arteriovenosa.
-
- Es la comunicación entre los vasos arteriales y venosos debido a una lesión vascular por la aguja.
- Si son lo suficientemente grandes,
pueden causar isquemia renal,
debido a "fenómeno de robo".
- Hallazgos de imagen.
-
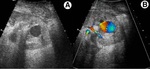
- US ( Fig. 13 )
-
- Doppler Color.
-
- Flujo turbulento con áreas de aliasing.
- Duplex Doppler.
- Pico sistólico elevado con índice de resistencia disminuido (IR <0,50).
- Arterialización de la vena de drenaje.
- TC ( Fig. 14 ): alternativa cuando US no caracteriza a la lesión.
-
- Lesión redondeada parenquimatosa con realce similar a la aorta.
- Drenaje venoso precoz junto a la lesion.
- La angiografía ( Fig. 15 ) permite tratamiento.
- Pseudoaneurismas.
-
- Secundarios a lesión de la pared arterial por la aguja de biopsia.
-
- Hallazgos de imagen:
-
- US ( Fig. 16 )
- Modo B.
-
- Lesión quística intrarrenal simple o mínimanente compleja.
- Doppler color.
-
- Flujo turbulento o con patrón “to-and-fro” en el cuello de la lesión.
- TC ( Fig. 17 ): alternativa cuando US no caracteriza a la lesión.
-
- Lesión parenquimatosa redondeada con realce similar a la aorta sin drenaje venoso precoz.
- La angiografía ( Fig. 18 ) permite tratamiento.
Complicaciones urológicas
Hidronefrosis obstructiva

Fig. 43
La obstrucción ureteral se ha descrito en alrededor del 2-5% de los trasplantes.
Puede observarse ureterohidronefrosis leve a causa de la pérdida de tonicidad secundaria a la denervación. Las causas de la obstrucción ureteral son la isquemia distal ureteral (más frecuente),
edema de la anastomosis (leve ectasia),
infección,
compresión extrínseca por colecciones perirrenales,
o por acodamiento ureteral.
Hallazgos de imagen:
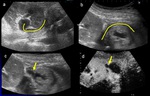
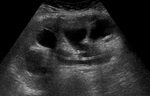
- US ( Fig. 19 ).
-
- Modo B.
-
- Dilatación de pelvis y cálices renales.
- Permite una mejor visualización de la causa de la obstrucción ureteral en comparación con los riñones nativos,
debido a la ubicación anterior del injerto.
- Contenido ecogénico puede corresponder a pionefrosis,
coágulos o tumores (éstos últimos realzan con contraste).
- Duplex Doppler.
-
- Puede mostrar IR aumentado (I> 0,80,
inespecífico).
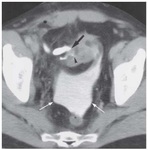
- TC (fase excretora) ( Fig. 20 ).
-
- Permite estudiar todo el curso del uréter para identificar la localización de la obstrucción.
- RM (Uro-RM) ( Fig. 21 ).
-
- Superior a US,
como TC,
en la visualización de la etiología de la obstrucción.
Neoplasias
Existe un riesgo incrementado de neoplasias malignos asociadas con el trasplante renal debido a la inmunosupresión prolongada:
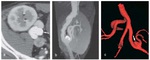
- Adenocarcinoma renal ( Fig. 24 ),
especialmente en los riñones nativos,
donde el 90% de los tumores se presentan,
por lo que es importante valorarlos en los controles periódicos.
-
- No existen diferencias con los adenocarcinomas renales en pacientes no trasplantados.
- Carcinoma de células transicionales,
principalmente en pacientes con tratados con ciclofosfamida.
-
- Se presentan como ocupación de las vías urinarias que realza tras la administración de contraste.
- Trastorno linfoproliferativo postrasplante (TLPT) se produce en el 1% de los trasplantes renales.
-
- Factores de riesgo: pacientes de edad avanzada,
inmunosupresión agresiva,
e infección por CMV y VEB.
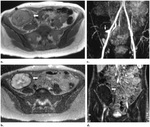
- Hallazgos de imagen ( Fig. 25, Fig. 26 y Fig. 27 ):
-
- Engrosamiento del tejido blando perihiliar.
- Masa perirrenal.
- TLPT puede afectar al hígado,
el cerebro o el tórax.
Otros
- Pielonefritis ( Fig. 22 ).
-
- Se puede visualizar engrosamiento urotelial (inespecífico,
también se puede observar en el rechazo crónico y tras la colocación de catéteres endoluminales o manipulación de la vía excretora).
- Urotelio piélico calcificado en la pielitis incrustada.
- Áreas focales de ecogenicidad anormal o defectos de flujo en el Doppler color.
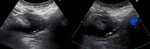
- Litiasis ( Fig. 23 ).
-
- Se puede formar en el riñón trasplantado (por ejemplo en el hiperparatiroidismo) o ser llevada accidentalmente desde el donante.
- Presentación clínica atípica,
debido a la denervación.
- Artefacto del “twinkling” en el Doppler color ayuda a su identificación.
- Gas en el sistema colector.
-
- Por la introducción del catéter o incluso en la biopsia con aguja.
- Pielonefritis enfisematosa (raro).
- Posición o condición anormales de los catéteres ( Fig. 28 ).
Colecciones perirrenales
Las colecciones perirrenales se producen hasta en un 50% en el periodo post-trasplante precoz. Sus hallazgos en imagen se superponen,
por lo que su diagnóstico definitivo se realiza por aspiración,
sin embargo,
su cronología y algunas características de imagen pueden sugerir la etiología.
Urinoma / fuga urinaria

Fig. 44
Los urinomas son colecciones perirrenales de orina que se suelen localizar extraperitonealmente. Son secundarios a fugas de orina,
que frecuentemente ocurren en el uréter distal o en la ureterocistostomía debido a isquemia o la técnica quirúrgica. El líquido presenta una creatinina elevada en el análisis de la aspiración.
Hallazgos de imagen:
- US ( Fig. 29 y Fig. 30).
-
- Colección de líquido anecoica entre el injerto renal y la vejiga que puede crecer rápidamente.
- Mínima o ninguna tabicación.
- TC ( Fig. 31 ) y RM con gadolinio en fase excretora.
-
- Acumulación de contraste en la colección.
Hematoma

Fig. 45
Los hematomas pueden ser secundarios a la cirugía del trasplante o biopsias del injerto.
Las complicaciones incluyen la compresión del parénquima,
la infección o su aumento de tamaño por hemorragia activa.
De esta forma es importante mesurarlos en los controles para asegurar su regresión.
Hallazgos de imagen:
- US ( Fig. 32 )
-
- Modo B.
-
- Colecciones perirrenales complejas (hematomas agudos tienden a ser más complejos y ecogénicos,
mientras que los hematomas crónicos suelen ser más hipoecoicos).
- CEUS.
-
- No realzan.
- Más sensible para su detección.
- Permitir valorar la repercusión en la perfusión renal.
- TC ( Fig. 33 ).
-
- Colecciones hiperdensas sin contraste.
- RM.
-
- Colecciones hiperintensas en T1.
Linfocele

Fig. 46
Los linfoceles son el colección perirenal más frecuente (hasta un 18% de trasplantes renales) y son secundarios a la disrupción de los vasos linfáticos en la cirugía. El diagnóstico definitivo se realiza en el análisis del líquido aspirado,
con niveles de proteínas y creatinina similares al suero.
Por imágenes no son específicos,
siendo colecciones anecoicas o con mínima de tabicación ( Fig. 34 ),
bien definidas e hipodensas en TC,
que no realzan tras administración de contraste ( Fig. 35 ).
Absceso

Fig. 45
Aunque las infecciones del tracto urinario son comunes en los pacientes trasplantados,
los abscesos son relativamente infrecuentes. Las técnicas de imagen son sugestivas,
y es importante que se correlacionen con el cuadro clínico (fiebre y dolor).
Hallazgos de imagen:
- US ( Fig. 36 ).
-
- Colecciones complejas inespecíficas.
- La presencia de gas es sugestiva.
- TC ( Fig. 37 ).
-
- Pueden tener burbujas de gas.
- Colecciones de pared gruesa con realce periférico.
- RM.
-
- Colecciones de paredes gruesas hiperintensas en T2 con realce periférico.
Alteraciones del parénquima
Se pueden clasificar en el focales (como quistes,
tumores,
infartos segmentarios) o anormalidades difusas (rechazo agudo y crónico,
NTA,
toxicidad por fármacos,
necrosis cortical y rotura espontánea) que pueden conducir a disfunción del injerto. Estos últimos,
específicamente el rechazo (agudo y crónico) y la NTA,
que son las alteraciones parenquimatosas difusas más comunes,
son inespecíficas en imagen es necesario realizar biopsia para distinguirlas.
Necrosis tubular aguda

Fig. 47
La NTA es la causa más frecuente de disfunción del injerto en el período postoperatorio temprano. Es más común en los riñones de donante cadavéres (debido a la isquemia fría),
y condiciona un deterioro de la función renal en el postoperatorio inmediato,
que se resuelve generalmente en 1-2 semanas (niveles elevados de creatinina que tienden a disminuir),
pero puede requerir hemodiálisis.
El rechazo agudo

Fig. 48
El rechazo agudo (RA) es el tipo más frecuente de rechazo (hasta el 37% de los trasplantes) y se produce en semanas 1-3 después de la cirugía. Fisiopatológicamente,
el rechazo puede ser mediado por células y/o por anticuerpos (30-35%),
siendo este segundo de alto riesgo de pérdida del injerto. El RA se presenta con disfunción renal (niveles de creatinina que tienden a elevarse a diferencia de la NTA) y puede asociar fiebre,
proteinuria y oliguria. Los episodios repetidos de rechazo agudo empeoran el pronóstico global y aumentar el riesgo de rechazo crónico.
El rechazo crónico

Fig. 49
El rechazo crónico (RC) es la causa más común de fracaso del injerto tardío y ocurre,
por definición,
después de 3 meses del trasplante. En el examen histológico se muestra vasculitis esclerosante y fibrosis intersticial.
Nefrotoxicidad por fármacos
La nefrotoxicidad por fármacos es secundaria al tratamiento inmunosupresor para evitar los episodios de rechazo agudo. Muchos fármacos tienen potencial neurotóxico y de entre ellos la ciclosporina es la más nefrotóxico,
debido a su efecto vasoconstrictor de las arteriolas glomerulares aferentes. El diagnóstico se hace mediante los niveles en suero,
siendo la nefrotoxicidad dosis-dependiente.
Necrosis cortical
La necrosis cortical es una complicación poco frecuente del trasplante renal que se presenta con fallo agudo del injerto. La patogenia sigue siendo poco clara habiéndose descrito en riñones nativos asociada a hemorragia posparto,
shock,
deshidratación severa,
reacciones postransfusionales,
por toxinas,
síndrome hemolítico-urémico,
lupus eritematoso sistémico y síndrome antifosfolípido.
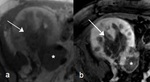
Los hallazgos de imagen ( Fig. 38 ) incluyen un borde periférico de ausencia de realce característico en CEUS y TC que se muestra como una banda periférica hipointensa en T2.
Rotura espontánea del injerto

Fig. 50
La rotura espontánea del injerto es una complicación relativamente frecuente (0,3-3%) y peligrosa que puede conducir a la pérdida del injerto. Se cree que es una consecuencia del aumento de la presión intersticial por rechazo agudo,
y con menor frecuencia por NTA y trombosis de la vena renal.
La ruptura espontánea clínicamente se presenta con la aparición brusca de dolor,
distensión del trasplante y puede producir un shock hipovolémico.
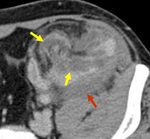
En las imágenes ( Fig. 39 ) se puede mostrar como un injerto desorganizado,
con tractos lineales y colecciones asociadas con componentes hemáticos.
Se han reportado hasta un 86% de supervivencia del injerto en un año con la reparación quirúrgica con aponeurosis del oblicuo externo,
pero la nefrectomía puede ser necesaria.
Avances técnológicos
Como hemos mencionado anteriormente,
todavía se requiere biopsia con aguja para el diagnóstico definitivo de la NTA,
rechazo agudo y crónico,
y los avances en imagen médica se centran precisamente en el diagnóstico de estas patologías. Las modalidades de imágenes que están siendo más utilizadas para tal fin son el US (CEUS) y la resonancia magnética,
con sus muchas aplicaciones funcionales disponibles en la actualidad (perfusión de contraste,
Difusión,
BOLD y técnicas ASL).
Hoy en día la mayoría de las publicaciones en la literatura son estudios con pocos pacientes,
pero se han encontrado diferencias significativas entre las patologías mencionadas. Aunque no hay resultados definitivos,
los informes sugieren que estas técnicas son una buena línea de investigación a seguir. Nuestro propósito en este póster no es explicarlas en detalle,
sino describir brevemente los resultados actuales para ver qué depara el futuro en el diagnóstico de las complicaciones de trasplante renal.
- US.
-
- Power Doppler.
-
- Disminución de la perfusión cortical,
evaluada con un transductor de 12 MHz en el rechazo agudo (Wang et al.
2008).
- CEUS.
-
- Análisis de las curvas tiempo-intensidad en ROIs corticales y medulares (Benozzi et al.
2009).
-
- NTA:
-
- Reducción del pico y el flujo sanguíneo regional.
- La disminución del ratio de volumen sanguíneo renal y del ratio del tiempo de tránsito medio.
- AR:
-
- Reducción del pico y el flujo sanguíneo regional.
- Análisis de las curvas tiempo-intensidad de ROIs en las corticales,
las arterias interlobares,
vena y arteria renal (Fischer et al.
2006).
-
- NTA: Aumento de la diferencia de tiempo para alcanzar el pico máximo en las arterias interlobares respecto a la corteza renal.
- AR: Aumento del cociente de perfusión (PQ).
- Evaluación cuantitativa de la perfusión renal mediante la cinética de reposición de microburbujas para estimar el flujo sanguíneo renal A* β (A =pico de intensidad de la señal,
β = pendiente del aumento de intensidad de la señal) (Schwenger et al.
2006).
-
- Correlación significativa con la creatinina y la tasa de filtración glomerular.
- Utilizando análisis ROC,
se demostró una mayor precisión diagnóstica para la detección de pérdida de la función renal debido a RC en comparación con los IR.
- RM.
-
- Perfusión con gadolinio (Wentland et al.
2009).
-
- NTA: perfusión cortical y medular mantenidas.
- RA: perfusión cortical y medular disminuidas.
- Blood Oxygen Level Dependent (BOLD). R2* es una medida de la tasa de pérdida de señal en T2* debido a la pérdida de fase de los protones a medida que aumenta desoxihemoglobina.
-
- Análisis de las diferencias en la biodisponibilidad de oxígeno y el flujo sanguíneo en los riñones trasplantados (Sadowski et al.
2005,
2010).
-
- NTA: R2* y la perfusión conservada.
- RA: R2* medular y perfusión cortical y medular disminuidos.
- Evaluación de la oxigenación intrarrenal y el estrés oxidativo en pacientes con disfunción crónica del injerto (Djamali et al.
2007).
-
- RC: pérdida de la diferenciación corticomedular en los mapas R2*,
debido a la disminución de los valores R2* de la médula a causa de disminución de la función tubular y el consumo de oxígeno.
- R2* cortical y medular se correlacionaron con marcadores de estrés oxidativo en suero/orina.
- Arterial Spin Labeling (ASL).
-
- Valoración cuantitativa de la perfusión renal con flow-sensitive alternating inversion recovery arterial spin labeling (Lanzman et al.
2010).
-
- RA: disminución de la perfusión cortical (la perfusión medular no se determinó).
- Difusión.
-
- Descomposición de los valores de ADC en RM 3T (en ADC total,
ADC,
el ADC libre de perfusión y la fracción de perfusión) en el trasplante renal precoz (Eisenberg et al.
2010).
-
- RA: reducción de ADC total a expensas de la fracción de perfusión,
que refleja la microcirculación disminuida.
- La fFracción de perfusión que resultó ser directamente proporcional a la tasa de filtración glomerular.
- Comparación del análisis mono y biexponencial de difusión en pacientes con trasplante renal con insuficiencia renal aguda (Blondin et al.
2009).
-
- Análisis monoexponencial de la corteza renal se correlacionó con la función renal.
- El análisis biexponencial mostró una mayor precisión numérica.