ICTUS
- Se trata de una patología de importancia dada su alta frecuencia y elevada morbilidad y mortalidad.
- Supone un elevado coste tanto económico como social y personal.
- El desarrollo de las unidades dedicadas a esta entidad ha supuesto una disminución de su morbi-mortalidad.
- En el caso de los ictus isquémicos,
el tratamiento fibrinolítico tiene sus limitaciones:
- Tiempo ventana limitado.
- Riesgo de hemorragia.
- Contraindicaciones.
La terapia endovascular,
trombectomía o fibrinolisis intraarterial,
puede ser complementaria a la endovenosa,
no obstante existen casos en los que se plantea como primera opción terapeútica.
Existen resultados* que demuestran mayor tasa de recanalización con fibrinolisis intraarterial que con la endovenosa:
- Terapia endovenosa: 43,2%.
- Terapia intraarterial: 63,2%.
- Terapia combinada: 67,,5 %.
*Rha JH,
Shaver JL The impact of recanalization on ischemic stroke outcome: a meta-analysis.
Stroke.
2007;38(3):967.
I) PACIENTE.
Consideremos ciertos aspectos acerca del "campo" en el que vamos a trabajar.
Estos datos deberá aportarlos el clínico.
I.I Antecedentes personales: Edad ( no Tto si >80 años).
Enfermedades neurológica que contraindican terapia ev:
- Infarto cerebral reciente < 3 meses o previo + DMellitus.
- TCE grave < 3 meses.
- Hemorragia cerebral o subaracnoidea previa.
- Patología SNC tipo tumoral,
aneurismático,
cirugía etc...
- Punción lumbar <7 días.
Enfermedades sistémicas que contraindican terapia ev:
- Diátesis hemorrágica conocida.
- Hemorragia grave reciente o activa.
- Biopsia pulmón o hepática < 14 días.
- IAM reciente < 4 semanas.
- Enfermedad gástrica ulcerosa <3 semanas.
- Hepatopatía grave.
- Cirugía mayor < 14 días.
Farmacológicos: Contraindicado.
- Uso de heparina <48h,
TTPA >1,5
- Anticoagulación oral.
Dependencia para las actividades de la vida cotidiana:
- No indicado si paciente presenta un mRS >2.
I.II Clínica del paciente.
- Tienpo de evolución:
- <6-8 horas con mismatch en territorio anterior.
- Se ha descrito hasta 12 horas en el posterior.
- Tratamiento indicado si NIHSS 5-25.
- Si NIHSS >25 peor pronóstico del paciente.
- Si NIHSS <5 mayor riesgo que beneficio.
- Seguir guías clínicas neurológicas.
La contraindicaciones por enfermedad del paciente para la terapia endovenosa pondría ,
si se cumplen el resto de criterios,
a la terapia intervencionista como primera opción.
En cuanto a la Farmacología,
si el paciente anticoagulado presenta INR > 2,7 contraindicaría terapia intervencionista.
Al respecto de dependencia y clínica es igual para las 2 opciones terapeúticas.
II) TIPOS DE ICTUS.
II.I) Hemorrágico:
Aproximadamente el 20% de los ictus.
II.I.1) Tipos:
- Hematoma parenquimatoso: 10-15% de ictus.
- 55% GGBB.
- 25% Lobares
- 7% Cerebelo
- 7% Tronco.
- 4% Masivos.
- 2% Intraventriculares puros.
- Hemorragia subaracnoidea: 5%.
II.II) Isquémico:
II.II.1 Causas:
a) Ateromatosis: Arco aórtico.
ACI.
(segmento cervical e intrapetroso).
A Vertebral : origen y unión con basilar.
A.
Basilar.
Segmentos 1 y 2 de ACA,
ACM y ACP.
Los ACVA de este origen pueden estar ocasionados por diversos mecanismos:
-Inestabilidad de placa con movimiento local de la misma obstruyendo origen de vaso contiguo.
- Ateroembolismo.
- Obstrucción progresiva de vaso.
b) Lacunar: Obstrucción vasos perforantes de CM y PCA.
En Ganglios basales y corona radiada.
Relación directa con HTA y DBT.
c) Cardiogénico:
Situaciones que favorezcan formación de trombos
intracavitarios:
- Arritmias FA
- Infarto miocardio (diskinesias).
- Enfermedad valvular.
- Foramen oval patente (TVP y embolismo para-
dójico).
- Tumores cardíacos ( mixoma).
III) ESTUDIO DE IMAGEN ¿Qué hacer y qué buscar?
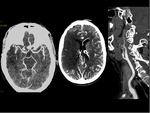
III.I TC Basal:
- Adquisición axial desde agujero magno a vértex con planos
paraleos al plano orbitomeatal inferior.
- Su finalidad es tratar de descartar ictus hemorrágico o la
presencia de LOES,
así como secuelas de infartos previos.
- Este estudio inicial nos permite,
asimismo,
la búsqueda de
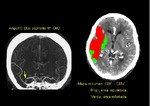
signos de isquemia hiperaguda:
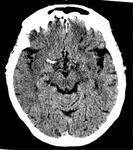
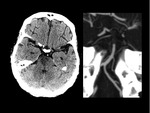
- vaso intracraneal hiperdenso.Fig. 1
- Hipodensidad Ganglios basales.
- Borramiento de ribete insular.
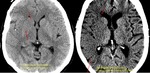
- Hipodensidad/ desdiferenciación cortico-subcortical/
edema cortical.Fig. 2
USAR VENTANA ESTRECHA (MUY CONTRASTADA).
- Con estos hallazgos,
y en el caso de ACVA en el territorio de
de la ACM,
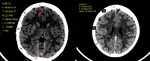
podemos calcular el ASPECTS ( Alberta Stroke
Program Early CT Score):
- Este sistema de evaluación divide el territorio de la CM
en 10 regiones.
- Se valora en 2 planos del estudio:Fig. 3
- En el que coinciden los Ganglios basales e ínsula.
- Un segundo 1cm aproximadamente más craneal que
el anterior,
en el que ya no se visualizan los ganglios
basales.
- Se divide en:
- 6 territorios corticales,
3 en cada plano ,
anterior
medio y posterior .
- ínsula.
- Núcleo caudado.
- Núcleo lentiforme.
- Cápsula interna.
- A cada territorio se le da el valor de 1 si no muestra
hallazgos patológicos,
de modo que una puntuación de
10 es la normalidad.
En el supuesto caso de que en
alguno de ellos se observe anomalía en relación a
cambios isquémicos precoces,
se resta un punto.
A tener en cuenta:
- En el núcleo caudado,
debido a doble sistema de
irrigación,
cuando se aprecia borramiento parcial del
mismo,
basta para considerarlo patológico.
- Para asumir patología isquémica aguda del núcleo
lentiforme,
éste debe encontrarse hipodenso en su
totalidad.
- En el caso de la ínsula si se observan cambios en una
mitad,
se considera patológica.
- En cápsula interna,
con evidenciar cambios agudos
en uno de los brazos es suficiente para restar el
punto.
-En las regiones corticales,
se establece que para
interpretarla como patológica se debe observar al
menos un cambio de los 3 descritos.
- De modo que este estudio,
en el caso de evento
isquémico agudo,
tiene como objetivo:
Detectar área infartada:
Hipodenso = Infarto ya establecido
Si es muy extenso no se fibrinolisa ni se realiza trombectomía.
Además en este estudio es posible poner de manifiesto la prsencia de ateromatosis en vasos intracraneales así como en ACI intrapetrosa y sifones carotídeos que nos harán dirigir especial atención a los mismos en el AngioTC.
III.II TC Perfusión:
a) ¿Qué es?
- Adquisición continua en cine.
- Repetida sobre los mismos 8 cortes de 5mm.
- Durante la admon.
de un bolo de contraste a alta
velocidad (4-5 mL/s).
- Selección plano en ganglios basales.
- Utiliza bajas dosis (100-150 MA).
- Da información sobre el mismatch.
- Contraste 45ml a 4ml/s.
b) Análisis.
Fig. 4
- Selección de una arteria (cerebral anterior en un
corte perpendicular).
- Selección de una vena (seno longitudinal post).
Software analiza el primer paso del contraste en cada píxel
DECONVOLUCION
(cálculo matemático inspirado en un modelo fisiológico)
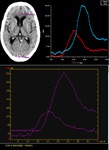
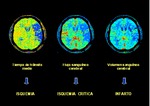
- Obtenemos 3 mapas: Fig. 5
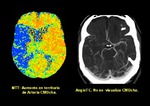
- Tiempo de tránsito medio (MTT)(segundos):
Tiempo medio en el que la sangre circula en el
volumen de cerebro selccionado.
Isquemia.Fig. 6
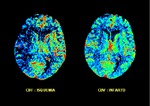
- Flujo sanguíneo cerebral (CBF)(ml sangre/100gr
de tejido cerebral/min).Volumen de sangre
circulante en un volumen dado de cerebro en un
tiempo predeterminado.
Isquemia crítica.
- Volumen sanguíneo cerebral (CBV)(ml sangre/
100grs de tejido cerebral).
Volumen de sangre
circulante en un volumen dado de cerebro.
Infarto.
De modo que CBF=CBV/MTT.
- Se valora el área de estudio infartada.
Teniendo en
cuenta que:
- Infartado si CBV < 2.
-Isquemia si ratio MTT > 145% vs.
contralateral.
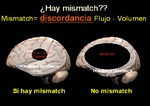
- Con estos mapas y una vez valorado el área de infarto
podemos determinar el posible mismatch (discordancia)
Fig. 7 entre CBF y CBV que se traduce en territorio de
penumbra,
o en otras palabras,
salvable si se inicia
tratamiento.Fig. 8 Fig. 9 .Table 1 .
En este mismo estudio se debe valorar el mapa de superficie de permeabilidad: predictor de riesgo de sangrado tras fibrinolisis.
c ) Limitaciones :
-Limitada cobertura anatómica
-Selección errónea plano adquisición.
- Movimiento del paciente.
- Hay que utilizar el registro automático para corregir
movimientos.
- Selección errónea del ROI arterial.
Resumiendo:
- La mayor parte de los casos el mismatch es claro.
- Casos dudosos entre 4,5 h y 6 h si hay un mismatch de +20% se fibrinolisa o se
realiza trombectomía.
- En mismatch claro o > 20% se debe proceder a tratamiento lo más precozmente
posible,
tanto vía endovenosa o intraarterial.
III.III AngioTC: Troncos supraaórticos y Polígono de Willis.
a) Técnica:
- Contraste 80ml de 350 a 3,5ml/s.
- Lavado con suero 40ml a 5ml/s.
- Scout view amplio.
- Adquisición desde cayado de aorta hasta vértex.
- Se realiza con Smart Prep.
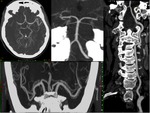
b) Estudio:
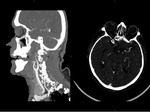
- Reformateo curvo para vasos cervicales.Fig. 10
- MIP de 25mm en Polígono,
con planos básicos.
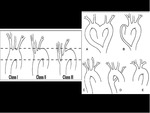
c) Objetivo: Tiene especial importancia.
- Estudiar morfología del cayado y variantes,
con vista
a posible cateterismo.Fig. 11
- Detectar trombosis carotídea.
- Detectar disección en vasos cervicales.
En estos casos existen 2 mecanismos de ictus:
- Embólico.
- Hemodinámico.
En el tratamiento se realiza trombectomía en primer
lugar.
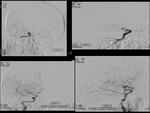
Se realiza control angiográfico.
Si persiste
efecto hemodinámico se coloca Stent.Fig. 12
- Descartar estenosis en bifurcaciones carotídeas.
Se puede realizar trombectomía y ATP+/-Stent de
carótida.
Obliga a antiagregar.
Riesgo hemorrágico.
Valorar beneficio/riesgo.
- Valoración de Polígono de Willis,
estudiando posibles
variantes del mismo.
- Detectar estenosis en vasos que conforman el polí-
gono así como eventuales aneurismas intracraneales
o malformaciones vasculares.
Si existe estenosis primero trombolisis y eventual
ATP+/- Stent intracraneal,
que obliga a antiagrega-
ción.
Valorar riesgo
- Dar información acerca del trombo,
tamaño,
situación
Según situación,
existen estudio de probabilidad de
recanalización con Tto endovenoso:
- Tándem ACI-CMedia: 27%.
- Tronco Basilar: 30%.Fig. 13
- T carotídeo: 6%
- Segmento M1 de CM: 30%.
- Segmento M2 de CM:44%.
- Longitud de trombo: Se considera que si >8mm
existe poca probabilidad de recanalización.
- Con ventana estrecha,
da información acerca del
volumen de la perfusión y sus colaterales.Fig. 12
Especial atención a los hallazgos de AngioTC compatibles con trombosis carotídea.
No siempre es tal,
únicamente existe enlentecimiento de flujo en este vaso por obstrucción distal debido a trombo en T carotídeo intracraneal.
IV) RESUMIENDO:
Debemos pensar en :
- Tiempo de evolución de la clínica.
- Estado del paciente y antecedentes personales.
- Estudio de imagen.
- TC basal: ¿Ha sangrado? ¿Cuánto infarto?.
- TC Perfusión: ¿¿¿Mismatch???
- AngioTC: - Estado de vasos: Ateromatosis,
dolicosidad.
- Variantes.
- Situación de trombo.
- Longitud de trombo.